第十二章 孢子虫
第一节 疟原虫
第二节 刚地弓形虫
第三节 隐孢子虫
第四节 卡氏肺孢子虫
第五节 其它孢子虫
一、肉孢子虫
二、等孢球虫
孢子虫隶属于顶复门(Phylum Apicomplex)的孢子纲(Class Sporozoa)。全为寄生性。细胞内寄生阶段一般无运动细胞器,如有伪足则是摄食作用。生殖方式包括无性和有性两类。无性生殖有裂体增殖(schizogony)产生裂殖子,以及孢子增殖(sporogony)产生具感染性的子孢子(sporozoite);有性生殖是通过雌雄配子结合进行的配子生殖(gametogony)。以上两种生殖方式或可在一个宿主或分别在两个宿主体内完成,有或无宿主更换。
第一节 疟原虫
疟原虫(malaria parasite)寄生于人及多种哺乳动物,少数寄生于鸟类和爬行类动物,目前已知有130余种。疟原虫有严格的宿主选择性,仅极少数的种类可寄生在亲缘相近的宿主。
疟原虫是人体疟疾的病原体。远在公元前10~11世纪的商殷时代,甲骨刻辞中就有了象形“疟”的文字,表明3千多年前,我国已认识疟疾的症状。在隋代《诸病源候论》所述,及以后国内外某些医学家均认为疟疾是由于遇到一种恶浊的气体,称之为“瘴气”所引起的。直至1880年法国人Laveran才在疟疾病人血液中发现疟原虫而认为是其病原体。疟疾是一种严重危害人体健康的寄生虫病,全世界约二分之一人口受威胁。我国建国前疟疾流行狼狈猖獗,建国初期称为五大寄生虫病之一。目前大部分地区疫情被控制或明显下降,但消灭疟疾的任务仍很艰巨。
寄生于人体的疟原虫共有四种,即间日疟原虫[Plasmodium vivax (Grassi and Feletti,1890 Labb'e,1899)],三日疟原虫[P.malariae(Laveran,1881 Grassi and Fetti,1890],恶性疟原虫[P.falciparum(Welch,1897)Schaudinn,1902]和卵形疟原虫[P.Ovale(Graig,1900)Stephens,1922]。在我国主要是间日疟原虫和恶性疟原虫;其他二种少见,近年偶见国外输入的一些病例。
形态与生活史
人体疟原虫的生活史,都需要人和雌性按蚊做宿主,并经历了无性生殖和有性生殖两个世代的交替。
人体四种疟原虫的生活史基本相同。现以间日疟原虫生活史为例(图12-1)叙述如下:
1.在人体内发育 疟原虫在人体内先后经在肝细胞和红细胞内发育。在肝细胞内为裂体增殖,称红细胞外期(红外期);在红细胞内发育包括红细胞内裂体增殖期(红内期)和配子体形成的有性期开始。
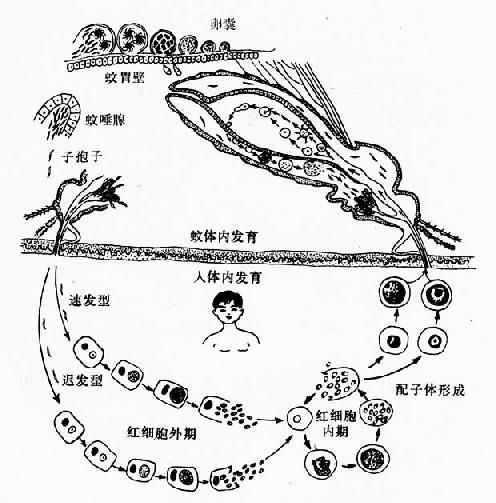
图12-1 间日疟原虫生活史
⑴红细胞外期(exo-erythrocytic,stage):蚊唾腺内含有疟原虫子孢子的雌性按蚊刺吸人血时,子孢子随蚊的唾液进入人体,约30分钟孢子侵入肝细胞。子孢子入侵肝细胞是由于子孢子表面有一种蛋白(环子孢子蛋白,CSP)能与肝细胞表面的疟原虫受体相结合,使两者接触。然后,子孢子释放由棒状体内贮存的分泌物,作用于接触的肝细胞膜,而主动侵入肝细胞。在肝细胞内,虫体中部呈球状突出,前后端收缩,呈圆形,转变为滋养体(trophozoite)。以后,核开始分裂,进行裂体增殖,形成裂殖体(schizont)。裂殖体逐渐长大,反复进行核分裂,至一定程度胞质也分裂,分别包绕核,形成许多裂殖子(merozoite),即为成熟裂殖体(mature schizont)。感染第七天的间日疟原虫的成熟裂殖体,直径约42µm,胞质内有空泡,内含裂殖子约12000个。裂殖子圆形或椭圆形,大小为0.3~0.7µm,由核和少量的胞质组成。当裂殖体发育成熟后,被寄生的肝细胞破裂,裂殖子散出,进入血窦,一部分裂殖子被吞噬细胞吞噬而消失,一部分则侵入红细胞内发育。
Lysenko等援引Moshkovsky(1973)的学说提出,间日疟原虫的子孢子在进入肝细胞后,在发育繁殖的速度上可能是多态的(polymorphism),即有发育快的,称速发型子孢子(tachysporozoites,TS);和发育慢的,称为迟发型子孢子(bradysporozoites,BS)。Krotoski(1980,1982)通过对食蟹猴疟原虫(P.cynomolgi bastianellii)的实验,发现其子孢子接种猴后3~5天,在肝细胞内原虫直径为4µm,第7天达5µm,但此后直至感染后105天其大小仍无改变。提出该种疟原虫子孢子有两个类型,一是进入肝细胞后迅速发育繁殖,产生许多裂殖子,在感染后7~8天侵入血流,进行红细胞内发育;另一型进入肝细胞后发育慢,经不同时间的休眠期,然后被激活,发育为裂殖体并继续分裂为裂殖子,再进入血流。作者将后者,经休眠期的疟原虫称之为休眠子(hypnozoite)。以后进一步证实间日疟原虫也有休眠期,并认为休眠子与疟疾复发有关系。
⑵红细胞内期(erythrocytic stage):由肝细胞释放出的红细胞外期裂殖侵入红细胞内进行裂体增殖,称为红细胞内期(红内期)。包括滋养体和裂殖体两个阶段。疟原虫经Giemsa染剂或Wright染剂染色,光学显微镜观察,核为紫红色或红色,胞质为蓝色,疟色素不着色,仍呈棕褐色(彩图1)。
1)滋养体(trophozoite):是疟原虫在红细胞内摄取营养和发育的阶段。当裂殖子侵入红细胞后,虫体胞质较少,中间出现大空泡,胞质呈环状,细胞核位于虫体一侧,颇似戒指的宝石。因此,早期滋养体又称为环状体(ring form)。环状体继续发育,长大。间日疟原虫和卵形疟原虫约经8~10小时,恶性疟原虫约经10小时,三日疟原虫约经24小时,虫体增大,伸出伪足,为运动细胞器,同时胞质中出现少量疟色素(malarial pigment);随着虫体继续发育,疟色素增多,伪足活动增加,出现多种形态,虫体有1或2~3个空泡。受染的红细胞胀大可达1倍,颜色变淡,并出现能染成淡红色的小点,称薛氏小点(Schüffner's dots)。恶性疟原虫的早期滋养体在外周血液中经十几小时的发育,逐渐隐匿于各种器官组织的毛细血管中,继续发育成滋养体。
2)裂殖体(schizont):约经40小时,间日疟原虫晚期滋养体发育成熟,虫体变圆,胞质内空泡消失,核开始分裂,称未成熟裂殖体(immature schizont)。之后核继续分裂,胞质随之分裂,疟色素渐趋集中。最后,分裂的每一小部分胞质包绕一个胞核,形成裂殖子。这时含有裂殖子的虫体称为成熟裂殖体。间日疟原虫的成熟裂殖体常充满于被寄生的红细胞,最近形成12~24个裂殖子。裂殖子长约1.5µm,宽约1µm。在红细胞受染后48小时左右,形成成熟裂殖体。此时红细胞出现泡状隆起,胀大而失去其双凹面形状。由于裂殖子的运动,导致红细胞破裂,裂殖子逸出进入血浆。从红细胞释出裂殖子的全过程约需1分钟。在血液中的裂殖子,一部分被吞噬细胞吞噬,一部分侵入健康的红细胞,重复裂体增殖过程。
⑶配子体形成:疟原虫经过几次红细胞内裂体增殖,部分裂殖子在红细胞内不再进行裂体增殖,而发育为雌性配子体(female gametocyte,即macrogamete cyte)或雄性配子体(male gametocyte,即microgametocyte),这是疟原虫有性生殖的开始。间日疟原虫配子体呈圆形或椭圆形,疟色素均匀分布于虫体内,核1个。雌性配子体胞质致密,色深蓝,虫体较大,占满胀大的红细胞;核稍小,深红色,多位于虫体一侧。雄性配子体胞质浅蓝而略带红色;核较大,淡红色,多位于虫体的中央。成熟的雌雄配子体如被适宜的按蚊随同血液吸入蚊胃后,即可继续发育。否则经一定时间后即变性,而被吞噬细胞吞噬。
四种疟原虫寄生的红细胞时期不同。间日疟原虫和卵形疟原虫主要寄生于网织红细胞,三日疟原虫多寄生于较衰老的红细胞,而恶性疟原虫可寄生于各时期的红细胞。配子体在人体末梢血液中开始出现的时间也有差别。间日疟原虫在裂体增殖期出现2~3天后可在末梢血液中查见到配子体,而恶性疟原虫则在7~10天之后。
2.在蚊体内发育 疟原虫在蚊体内发育包括在蚊胃腔内进行有性生殖,即配子生殖(gametogony)和在蚊胃壁进行的无性生殖,即孢子增殖(sporogony)两个阶段。
⑴配子生殖:当按蚊刺吸疟疾患者血液时,疟原虫随血液进入蚊胃后,仅雌、雄配子体能存活并继续进行配子生殖,而红细胞内期的各无性发育阶段的疟原虫均被消化。雌配子体逸出红细胞外,发育为不活动的圆形或椭圆形的雌配子(female gamete)或称大配子(macrogamete);与此同时,雄配子体也在几分钟内开始核分裂为4~8块,胞质亦向外伸出成4~8条细丝,然后核分别进入细丝内,称为出丝现象,亦即雄配子形成(exflagellation),不久细丝脱离母体,在蚊胃腔中游动,即雄配子(male gamete)或称小配子(microgamete)。约在1~2小时,雌、雄配子受精,形成圆球形的合子(zygote)。合子最早在数小时后即开始变为长形的香蕉状的能活动的动合子(ookinete)。约在12~24小时,成熟动合子可从蚊胃壁上皮细胞或穿过上皮细胞,停留在蚊胃弹性纤维膜(基底膜)下,在此处虫体变圆并分泌囊壁形成球形的卵囊(oocyst)。
⑵孢子增殖:卵囊形成后即进入孢子增殖阶段,卵囊逐渐长大并向蚊胃壁外突出在卵囊形成2~3天,其核开始分裂。核反复分裂,随后胞质也分裂,部分胞质与部分分裂的核形成了成孢子细胞(sporoblast),子孢子芽从成孢子细胞表面长出(图12-2)。约经8~10天,脱离成孢子细胞体,形成子孢子(sporozoite),并游离于卵囊内。此时为成熟卵囊,其直径约50~60µm。一个卵囊内可含有1000~10000个子孢子。子孢子呈梭形,长约10~15µm,宽约1µm。子孢子可能主动地从卵囊壁钻出或因卵囊破裂后散出而进入蚊血腔。子孢子可随蚊血淋巴钻入蚊体各组织。到达蚊唾腺内的子孢子才具有传染性。在子孢子进入蚊唾腺管后,当雌蚊再度刺吸人血时,便可随唾液进入人体。
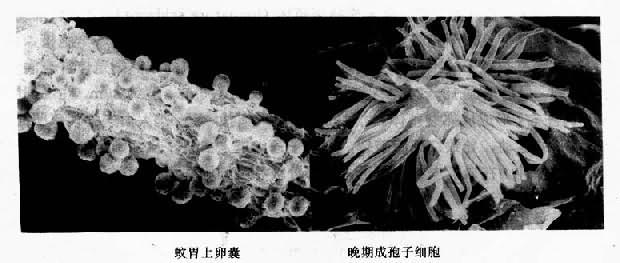
图12-2恶性疟原虫卵囊与成孢子细胞
表12-1 4种疟原虫发育过程比较
| 无性体与配子体出现于周围血液中的相隔时间 | 2~5天 | 7~11 | 10~14天 | 5~6天 |
| 蚊体内发育的温度与时间 | 17.5℃,30天或更长; 20℃,16~17天;25℃,9~10天 | 20℃,22~23天;27℃,10~12天 | 20℃,30~35天; 22~24℃,25~28天 | 25℃,16; 27℃,14天 |
疟原虫在蚊体内发育受多种因素的影响,如配子体的数量和活性,外界的温度、湿度,以及人体的免疫反应对配子体的作用等。此外,蚊媒的易感性也有密切关系,如我国中华按蚊对间日疟原虫的易感性比恶性疟原虫高。
表12-2 4种疟原虫形态的鉴别
| 间日疟 | 恶性疟 | 三日疟 | 卵形疟 | ||
| 环状体 (早期滋养体) |
环较大,约等于红细胞直径的1/3;核1个,偶有2个;胞质淡蓝色;红细胞内多只含1个原虫,偶有2个 | 环纤细,约等于药细胞直径的1/5;核1个,但2个也很常见;红细胞可含2个以上原虫,虫体常位于红细胞的边缘 | 环较粗壮,约等于红细胞直径的1/3;核1个;胞质深蓝色;红细胞很少含有2个原虫 | 似三日疟 | |
| 滋养体 | 虫体由小渐大,活动显著,有伪足伸出,空泡明显,故虫体形状不规则;疟色素黄棕色,小杆状 | 体小结实,不活动;疟色素集中一团。黑褐色,原虫此时开始集中在内脏毛细血管 | 体小圆形或呈带状,空泡小或无;亦可呈大环状,中有一个大空泡,不活动;疟色素棕黑色,颗粒状,常分布于虫体的边缘 | 虫体圆形,似三日疟,但较大;疟色素似间日疟但较细小 | |
| 未成熟裂殖体 | 核开始分裂成2~4个时虫体仍活动,核愈多则虫体渐呈圆形,空泡消失;疟色素开始集中 | 虫体仍似大滋养体,但核分裂成多个 | 虫体圆形或宽带状,核分裂成多个;疟色素集中较迟 | 虫体圆或卵圆形,不活动,核分裂成多个;疟色素数量较少 | |
| 成熟裂殖体 | 裂殖12~24个,通常16个,排列不规则;疟色素集中成堆,虫体占满胀大了的红细胞 | 裂殖子8~36个,通常18~24个,排列不规则;疟色素集中成一团,虫体占红细胞体积的2/3至3/4 | 裂殖子6~12个,通常8个,排成一环;疟色素多集中在中央,虫体占满整个不胀大的红细胞 | 裂殖子6~12个,通常8个,排成一环;疟色素集中在中央或一侧 | |
| 配子体 |
雄 |
圆形,略大于正常红细胞,胞质色蓝而略带红,核疏松,淡红色,常位于中央;疟色素分散 | 腊肠形,两端钝圆,胞质色蓝而略带红,核疏松,淡红色,位于中央;疟色素黄棕色,小杆状,在核周围较多 | 圆形,略小于正常红细胞,包质淡蓝色,核疏松,淡红色,位于中央;疟色素分散 | 似三日疟,但稍大;疟色素似间日疟 |
|
雌 |
圆形占满胀大的红细胞,胞质蓝色,核结实,较小,深红色,偏于一侧;疟色素分散 | 大小正常或略缩小,紫蓝色,边缘常皱缩;常见有几颗粗大紫褐色的茂氏点(Maurer' s dots ) | 圆形,如正常红细胞大,胞质深蓝色,核结实,偏于一侧;疟色素多而分散 | 似三日疟,但稍大;疟色素似间日疟 | |
|
被寄生红细胞的变化 |
胀大。色淡,常呈长圆形或多边形;滋养体期开始出现鲜红色的薛氏点(Schüffner's dots) | 大小正常或略缩小,蓝色,边缘常皱缩;常有几颗粗大紫褐色的茂氏点(Maurer's dots) | 大小正常,有时缩小,颜色无改变;偶可见西门氏点(Zieman' s dots ) | 略胀大,色淡,部分红细胞变长形,边缘呈锯齿状;薛氏点较间日疟的粗大,环状体期即出现 | |
超微结构
迄今疟原虫与其各发育阶段及疟原虫入侵宿主红细胞的全过程,均已作较详细地研究。各种疟原虫的超微结构基本相似,现仅简要介绍疟原虫红细胞内期的裂殖子及其入侵红细胞的过程。
1.裂殖子(图12-3)疟原虫裂殖子通常呈圆形或梨形。虫体前端突出,形似截圆锥体称为顶突(apical prominence),虫体外被表膜复合膜,体内具一个胞核及一些细胞器。
⑴表膜复合膜(pellicular complex):由外膜、内膜和微管(microtube)组成。外膜薄,即质膜。内膜较厚呈网状结构,虫体除顶突和细胞口外,均为内膜所覆盖。内膜的内面紧贴着一层微管,系发自顶突基部的极环,放射状向虫体后方延伸,有些微管止于虫体中部,有些则达虫体后端。内膜和微管的功能,可能是支持虫体,并使虫体有一定形状;微管可能与虫体运动有关。裂殖子的体表尚有一层细胞被或称表被(surface coat),是由“T”形或“丫”形微毛按一定的间隔垂直地排列在虫体外膜上面而成,是外膜的一部分,具有抗原性。
⑵细胞器:包括有顶突及极环(polar rings)、顶凹(apical pit)、棒状体(rhoptry)、微线体(microneme)、线粒体(mitochondrion)、微球体(microspheres)、球形体(spherical body)、核蛋白体(ribosome)、内质网(endoreticulum)、高尔基体(Godgi body)和多膜体(multilamellate body)及细胞口(cytostome)等。极环为外膜皱折增厚而成,有2~3环,可能有助于保持顶突的形状。顶凹由顶突的顶端中央内褶形成,可能在裂殖子入侵时起吸附红细胞的作用。棒状体一对,其前端尖细,似有小孔与顶凹相通,微线体有小管通向前端,当裂殖子侵入红细胞后两者消失,因此认为它们在裂殖子入侵红细胞中起重要作用。在有些疟原虫,如恶性疟原虫的棒状体和微线体中发现大量富含组氨酸的蛋白质,这种物质能使红细胞凝集并增加红细胞渗透性,使红细胞膜内陷,有利于裂殖子进入红细胞。微球体在裂殖子入侵的后期,对含虫空泡(parasitophorous vacuole)起扩展作用。球形体与线粒体的关系密切,可能是能量储藏器。细胞口在裂殖子并无作用,但在滋养体期则为虫体的摄食器官。
⑶胞核:裂殖子的核位于虫体后半部,呈圆形,核膜由双层膜组成,其上有核孔。未见到核仁。
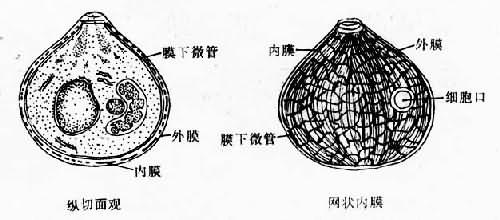
图12-3 鸡疟原虫的裂殖子
(采Aikawa)
2.裂殖子入侵红细胞的过程(图12-4) 裂殖子入侵红细胞的过程按以下顺序进行。
⑴裂殖子粘附红细胞表面:这种粘附是红细胞表面受体与裂殖子表面配体的特异性结合,如间日疟原虫的受体为红细胞膜上的Duffy抗原(糖蛋白)。但裂殖子粘附红, http://www.100md.com(陈佩惠等)