第三节 FCM对外周白细胞的免疫荧光分析
外周血是临床检验中的重要标本。FCM分析外周白细胞的主要目的是了解各种白细胞的数目与分群情况。这些数字的变化与临床的某些疾病有一定的关系。近年来,由于多种识别白细胞膜表面抗原的单克隆抗体的发现,以及对这些单克隆抗体的直接或间接荧光标记物的出现,使得利用FCM的荧光组织化学分析获得被测细胞的多指标的更多、更准确的信息,这无疑对警觉临床和科研有很大帮助。本节 主要讨论有关外周血的白细胞的免疫荧光标记技术、数据分析及临床应用等方面的问题。
一、白细胞的免疫荧光标记技术
1.白细胞抗原下面给出世界卫生组织对白细胞抗原的统一命名,以及它们的分子量、对应的单克隆抗体及反应阳性的细胞(见表10-2)。
表10-2 WHO对白细胞分化抗原的命名
|
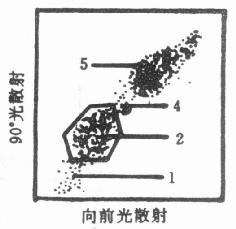
图10-9 人的外周血白细胞分群的二维点图 图中, A、B图的淋巴细胞数大约有6000~9000个;C、D图约有2000~4000个。分群编号依次表示:①红细胞、死细胞和渣滓;②淋巴细胞群;③大颗粒淋巴细胞;④单核细胞;⑤粒细胞。数据是对1000个细胞分析得到的。 若用单指标直方图,对PBMC而言,可以把淋巴细胞和单核细胞分开。见图10-10中的A、B图。但对红细胞溶解后的全血,单指标图分辨率则不够了(图10-10的C、D图),图A、B给出的是经ficoll后的PBMC;图C、D给出的是人外周血白细胞。图中数字编号所代表的组分和图10-9相同。 由上可见,在分析红细胞溶解后的全血时,必须先采用双指标二维点图。从图上也可清楚地看出,粒细胞、未被溶解的红细胞和一些渣滓,由于不同的体积和致密度,明显地区别于淋巴细胞和单核细胞从而能把它们分开。看到清楚的细胞分群以后,可以在计算机的显示屏上将所要分析的细胞画线框出,并通过指令送入存贮器,以后就可只对框出部分做各种数据分析和深入考查。图10-11就是对双指标点图上的淋巴细胞群框定的示意图。数字所表示的意思和图10-9相同。
图10-10 外周血白细胞及PBMC的单指标直方图
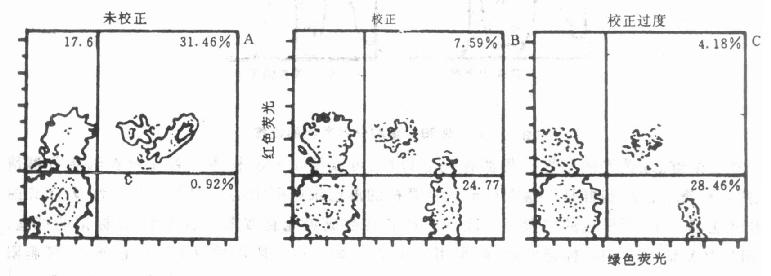
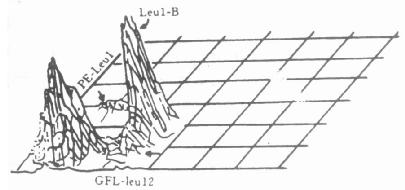
图10-11 双指标点图上细胞的框定 2.单维直方图上阴性分界游标设置前面已经强调,在用FCM分析时,阴性对照是必不可少的。首先用非染色细胞,根据前面介绍的双指标二维点图的办法,将某一细胞群框定;然后分别选用绿色荧光(GFL)和红色荧光(RFL)单指标直方图。在直方图上所出现的细胞均为阳性。可用改变GFL和RFL增益的办法,将细胞恰好调节 到左侧并设立游标(图10-12)。 然后再测试MsIg染色的阴性对照。某些细胞,由于膜上的Fc受体可以与对照抗体鼠Ig非特异性结合,因而有一定的背景染色,不过这种阳性百分率不应超过5%。所以MsIg与非染色细胞的分界游标确立后,以后所测试的标本以此为标准,游标位置基本不变。 图10-12 阴阳性细胞分界游标的设置 MsIg的红、绿荧光阴阳性分界游标确立以后,可以测试实验标本。首先检查细胞分群情况,然后检查淋巴细胞群是否落在已输入计算机的淋巴细胞框定的范围里。若染色及FCM的工作性能都正常,则框定的位置不会改变。然后转换成荧光直方图。若为FITC标记的细胞,则GFL为X轴;若为PE标记的细胞,则用RFL为X轴。由于阴阳性分界游标记已确立,细胞阳性率及图像均显示于计算机荧光屏上;同时也可选用其它指标和图像、打印所需的资料等。 3.双染色分析游标设立和荧光校正 (1)游标的设立:游标设立的原理和单染并无不同,但具体要用二维点图和二维等高图来完成。分别选用GFL和RFL为X和Y轴。先用不染色细胞测试,将阴性细胞集中在左下角(图10-13)。分别为X、Y轴设立游标,再用MsIg的阴性对照测试。可将X、Y轴游标略为移动,使位于窗3内的细胞(阴性)在95%以上。 (2)红、绿荧光的校正:由于红色荧光探测器在最佳测试状态时,会让部分绿色荧光进入红色荧光探测器。这是因为一部分细胞发出的绿色荧光波长较长。若用阻断或滤色的办法消除进入红荧光探测器的这部分GRL,就会大大地降低RFL探测器的灵敏度。因而只好在操作时,通过电子计算机预先进入荧光校正,在RFL中适当扣除GRL的影响。 通常红色荧光进入绿色荧光探测器的情况比较光见,图10-14给出CD11-PE(T细胞、RFL)及CD8-FITC(T抑制细胞,GFL)双染细胞在二维等高图上进行荧光校正的示意图。X轴为GFL,Y轴为RFL,由X轴Y轴游标划分的四个窗的阴阳性和图10-13相同。各窗给出的百分数为该细胞群所占百分比。图A表示未经校正时的情形。窗2内31.46%表示双阳性细胞,即在T细胞中31.46%为抑制细胞毒细胞。经过适当校正,可见有两群阳性双标记细胞出现(B图)。高强度部分为真正的CD8、CD11双标记阳性细胞;低强度部分属于CD8绿色阳性细胞(NK细胞)。此时2窗中细胞份额减为7.59%。需要指出的是校正过度则会使各区的阳性细胞都减少(图C)。
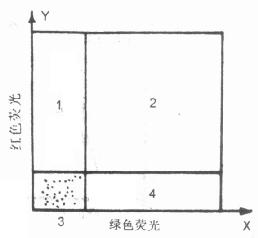
图10-13 双染色二维点图上游标的设置 1区:红色荧光阳性;2区 :红、绿荧光均为阳性;3区:阴性细胞:4区:绿色荧光阳性细胞
图10-14 双染色在二维等高图上荧光校正 双染色的荧光校正是用电子补偿电路来完成的。补偿时先测定一种染料的荧光,此时除了应该接收该荧光的光电倍增管PMT1有信号输出外,另一光电倍增管PMT2也常会有微弱输出。调节 补偿器使PMT2的输出为0;然后再测另一种波长的荧光染料,调PMT1的补偿器使之输出也为0;然后再测另一种波长的荧光的染料,调PMT1的补偿器使之输出也为0:如此反复调节 ,使两种荧光的探测器都获得补偿。实际调节 时用的是一种标准荧光微球,微球上标有已知数量的荧光分子。利用不同的微球可调整、补偿不同荧光的测量通道。需要指出的是:当PMT高压有所改变、激光和滤片系统有所变动时,都要对荧光校正做重新补偿调节 。 三、淋巴细胞亚群的测定及其在临床医学中的实用意义 淋巴细胞由于表面特异性抗原的差异可分为四大类(表10-3),这些不同抗原表现型的亚群执行不同的机能。而且某些疾病会选择性地损伤某些亚群而造成亚群之间的比例失调。根据FCM双荧光分析的结果,现将不同的抗原和不同的机能的淋巴细胞亚群列于表10-4。 表10-13 主要淋巴细胞亚群的表面抗原
| |||||||