治疗药物监测与给药方案个体化
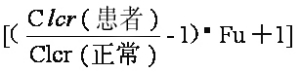 |
治疗药物监测(TDM,Therapeutic Drug Monitoring)是临床药学服务的重要内容之一。它的任务是采用现代的分析测定手段,定量测定血液或其他体液中药物及其代谢物的浓度,并将所测得的数据运用药物动力学原理拟合成各种数学模型,再根据求得的各种动力学参数制定最佳给药方案,从而提高药物疗效,降低药物毒副作用,实现给药方案个体化。做好TDM与给药个体化需要涉及多学科的综合知识,包括药动学、药效学、药物分析化学、临床药理学、毒理学等。
血药浓度
血药浓度与药物疗效
相同药物给予常用剂量范围内的相同剂量,多数人可产生预期的疗效,有些人不产生疗效,而有些人甚至出现毒性反应,这种用药后疗效因人而异的反应就是用药个体差异。临床上,针对不同患者,需要调整适当的给药剂量。如临床常用的抗高血压药物每日所需剂量相差悬殊(见表1),这样给医师确定投药剂量造成困惑,他们希望能有一个指标,通过这一指标的变化来指导用药,而不是盲目地增减剂量。
, http://www.100md.com
表1 抗高血压药的剂量范围
药物治疗作用的强弱与维持时间的长短,理论上取决于受体部位活性药物的浓度。一般说来,药物的体内作用过程是从用药部位进入血液循环,随血液循环分布至病变部位,与受体作用而发挥药理效应。因此,一般血浆中活性药物浓度可间接地作为受体部位活性药物的指标。
早在上世纪40年代末,Brodie等就已经发现药物的药理作用与血药浓度密切相关。药物对不同种属的动物虽然有效剂量差异很大,但产生相同药理作用时的血药浓度却极为相似。例如保泰松对兔和人的抗炎作用剂量相差达几十倍,分别为300毫克/千克和5毫克/千克~10毫克/千克,但有效血药浓度范围很窄,都在100微克/毫升~150微克/毫升之间。以后的研究还发现,随着血药浓度的变化,药物的药理作用及中毒症状也随之发生相应的变化。例如水杨酸的血药浓度为50微克/毫升~100微克/毫升时具有镇痛作用,>250微克/毫升时具有抗风湿作用,350微克/毫升~400微克/毫升时具有抗炎作用,550微克/毫升~850微克/毫升时可产生轻度中毒,1250~1400微克/毫升时即产生中毒,1600微克/毫升~1800微克/毫升时为致死量。又如苯妥英钠的血药浓度为10微克/毫升~20微克/毫升时为有效血药浓度,具有抗惊厥和抗心律失常作用,当血药浓度为20微克/毫升~30微克/毫升时可出现眼球震颤,30微克/毫升~40微克/毫升时出现运动失调,超过40微克/毫升可出现精神异常。
, 百拇医药
从上述的这几个例子可以看出,尽管在用药剂量上相同,但不同的个体间存在很大的差异,而产生相同药理作用时的血药浓度却极为相近。因此将血药浓度作为一个指标来指导临床用药具有重要的意义。
药物动力学的几个重要参数
药物进入机体后在作用部位和体液中的浓度是随时间不断变化的。药物动力学就是用动力学的基本原理,通过数学的方法推导出体内药量与时间的关系式,求出相应的动力学参数来描述药物在体内的吸收、分布、代谢和排泄的过程。常用的药物动力学参数为:
吸收速率常数(Ka):是药物从吸收部位进入体循环的速度,即吸收速度与体内药量之间的比例常数。Ka值的大小可用来衡量药物吸收速度的快慢。
消除速率常数(K):是药物在体内代谢、排泄的速度与体内药量之间的比例常数。K值的大小可用来衡量药物从体内消除速度的快慢。
, 百拇医药
吸收分数(F):是药物进入体循环的量与所给剂量的比值。血管内给药时F=1,表示药物全部进入体循环;其他给药途径F<1,用来衡量血管外给药时进人体循环药物的相对数量,此时又称生物利用度。
表观分布容积(V):是体内药量按血浆中同样浓度分布时所需体液的总体积。表观分布容积是假定药物在体内均匀分布情况下求得的药物分布容积,由于实际上是不存在的,故加‘表观’二字,可用其来表示药物在体内分布的广泛性。表观分布容积小,表明药物主要分布于血浆中,而在组织和器官中的分布有限;表观分布容积大,则表明药物分布广泛,血药浓度很低,药物大多与某些组织和器官有特异性结合或发生了蓄积。
生物半衰期(t1/2):是药物在体内消除一半所需要的时间。其与消除速率常数(K)之间的关系为:t1/2 =0.693/K。也可用来衡量药物消除速度的快慢。
影响血药浓度的因素
, 百拇医药
生理因素
年龄。不同年龄的人群在药物的吸收、分布、代谢和排泄上存在明显的差异(见表2),这是由于各年龄段的生理特点所决定的。
新生儿胃肠道处于发育阶段,口服药物吸收就会较成人慢;皮肤黏膜较薄,且体表面积与体重之比值较成人为大,局部外用药物的吸收就会较成人快;血脑屏障尚未完全形成,药物在脑脊液中分布较多;代谢、排泄机能也不健全,使半衰期延长。
老年人随着年龄的增长,心、肝、肾及胃肠道等主要器官的功能都在不断下降,可引起药物动力学参数的改变。通常可使某些药物的代谢、排泄减慢,半衰期延长,常规剂量连续给药就有可能引起蓄积中毒;与血浆蛋白结合率降低,使游离型药物浓度增高;即使常规剂量也可能出现毒性反应。
表2 不同年龄时磺胺甲口恶唑(SMZ)的t1/2和V
, 百拇医药
性别。通常女性较男性对药物敏感。动物实验表明,雄鼠对药物的代谢较雌鼠要快。再如利眠宁在男性体内的清除也较女性为快,如果女性同时口服固醇类避孕药,对利眠宁的清除会更慢。
肥胖。正常人体中约20%为脂肪组织,而肥胖者脂肪组织在人体的比例会更多,药物在脂肪组织的分布势必影响其他组织的分布,尤其脂溶性药物在脂肪内溶解较多,而脂肪组织中血管分布较少,且血流较慢,因此使药物的分布、代谢、排泄均减慢。肥胖人群与正常人群相比,药物动力学参数表现为V增大,t1/2延长。肥胖者长期使用脂溶性药物,可在脂肪组织中产生蓄积引起中毒反应,应注意调整剂量。
遗传。有研究者对7对单卵性孪生人和7对双卵性孪生人分别给予安替比林、保泰松、双香豆素后,测定药物的半衰期。结果表明,在单卵性孪生人组每对人之间的t1/2十分相似,而双卵性孪生人组每对人之间的t1/2有明显的差异。不同人种、不同民族,甚至不同家族对于药物吸收、分布、代谢、排泄的整个过程均可存在一定的差异。遗传因素对药物体内过程的影响越来越为人们所关注。
, 百拇医药
其他。多种生活和环境因素均可改变药物的体内过程。生活因素包括饮食习惯、食物组成、吸烟、嗜酒、饮茶和咖啡等;环境因素包括经常接触有机溶剂、杀虫剂等。
病理因素
肝功能损害。肝脏是药物代谢的主要器官,肝功能受损,药物的代谢功能则会受到影响,K值、t1/2会发生改变。
肾功能损害。肾脏是药物排泄的主要器官,肾功能受损,药物从体内排出受阻,K值降低,t1/2延长。
心脏疾患。心脏疾患可引起血液分布、流速等血液动力学的改变。如心肌梗死及充血性心衰患者,某些部位或脏器的血流减少,影响药物的消除。
胃肠疾患。胃肠功能的变化可直接改变Ka值和F值。如胃肠道pH、胃排空速率、胃吸收面积、胃壁通透性、胃肠道内的酶等诸多因素的改变,均可引起药物吸收的改变。
, 百拇医药
其他。有些疾病可改变药物与血浆蛋白的结合,这些疾病包括肾病、高胆红素血症、高脂血症等。
药物因素
制剂因素。同一药物的不同剂型,甚至不同厂家、不同批号的相同剂型,虽然测得的药物含量相同,但所产生的临床疗效却不一定相同。这主要是制剂方面的因素,如药物的理化性质、剂型、处方中辅料、制剂的工艺过程等影响了F和时间,使血药浓度发生变化,影响临床疗效。
药物的相互作用。药物相互作用的发生机理十分复杂,通常可用药动学相互作用和药效学相互作用来解释。药动学相互作用是指一个药物的吸收、分布、代谢及排泄为其他药物所改变;药效学相互作用是指一个药物直接改变另一个药物分子的、细胞的或生理的作用。
影响血药浓度的因素很多也很复杂,需要根据具体患者及使用的具体药物进行具体分析。由此可见,开展治疗药物监测工作很有必要,尤其对于一些治疗中个体差异较大的药物和一些具有特殊情况的患者,在治疗过程中随时监测血药浓度,可有效提高治疗效果,减少毒副作用。
, 百拇医药
治疗药物监测的意义
治疗药物监测的主要工作就是应用化学分析的方法,测定血液(或其他体液,如尿液、唾液、组织液等)中的药物浓度,再根据药物动力学的理论拟合成各种数学模型,从而掌握药物在体内随时间变化的规律。
控制药品质量
随着科学技术的不断提高和人们对于用药安全的重视,药品的质量控制已经不局限于体外监测,《药典》和一些厂家已经对很多药物做了生物利用度方面的要求,以提高药品的有效性、安全性和市场竞争力。
新药研制及老药改进
, http://www.100md.com
在新药研制过程中和批准上市前,以及老药改进的研究过程中,均需做药物动力学参数、生物利用度和生物等效性的试验研究。
临床合理用药
在治疗过程当中监测血药浓度,可及时了解药物在体内的变化情况,从而可根据患者的药动学参数,制定针对具体患者的给药方案,减少不良反应及毒副作用的发生,提高疗效,实现“给药方案个体化”,使临床用药更趋于合理。
药物监测的条件
治疗药物监测是一项有意义的工作,要开展这项工作,首先需要建立一个TDM实验室,实验室中需具备满足测定和数据处理所需的各种仪器设备,能保证测定结果及时、准确。另外,关键还需要有一批能建立血药浓度测定方法并能对处理后的结果进行解释的专门人才。最后,领导对开展这项工作的重视和支持也是必不可少的。
需要监测的药物和情况
, http://www.100md.com
需要监测的药物
治疗指数低、安全范围窄、毒副作用强的药物 如地高辛,有效血药浓度范围为0.9~2微克/升,而 > 2.4微克/升即为潜在中毒浓度。再如茶碱,有效血药浓度范围为成人及儿童10~20微克/毫升,新生儿5~10微克/毫升;潜在中毒浓度为成人及儿童> 20微克/毫升,新生儿> 15微克/毫升。有效浓度与中毒浓度十分接近。
具有非线性药物动力学特征的药物 如乙酰水杨酸、苯妥英钠、保泰松等的半衰期均随剂量的增加而延长,当剂量增加到一定程度时,再稍有增加即可引起血药浓度的很大变化(见表1)。
表1 临床常需TDM的药物
注:*表示微克/升,**表示毫摩尔/升
需要监测的情况
, 百拇医药 长期用药 药物长期使用过程中,血药浓度可受各种因素的影响而发生变化,有的可在体内逐渐蓄积而发生毒性反应;也有的血药浓度反而降低,导致无效。另外,环境因素、生活因素的改变均可影响血药浓度,具体问题需具体分析。
合并用药 某些药物合并使用时,药物动力学参数会发生改变,需引起注意。如地高辛与维拉帕米(异搏定)合用时,后者可使地高辛的t1/2显著延长,血药浓度明显升高。
特殊人群用药 患有心、肝、肾、胃肠道疾病者,婴幼儿及老年人的动力学参数与正常人会有较大的差别,用药时需格外注意。
常用药物监测的分析方法
血浆或血清中药物的浓度低,取样量又要尽可能少,且有时患者体内会含有不止一种药物,因此用于血药浓度测定的方法较体外药物测定的方法需要考虑的问题要更复杂,要求也更高。下面将常用的几种方法分类,进行简单介绍并将各种方法的优缺点做比较(见表2),同一种药物可以用多种方法测定,选用时需权衡各方面因素考虑。
, 百拇医药
分光光度法(SP) 包括紫外分光光度法(UV)、荧光分光光度法(Fluor)和原子吸收分光光度法(AA)等,是常用的仪器分析方法。由于其专属性差,容易受血液中其他成分的干扰,在测定前必须进行分离,单独用于血药浓度测定时常常受到限制,在灵敏度、精密度和准确度方面逊于色谱法。但这种方法具有操作简单、价格低廉、速度快等优点,如与层析法结合使用,可提高其专属性。当各单位条件有限时,仍是一个值得推广采用的方法。
气相色谱法(GC) 是将被测样品在一定温度下瞬间气化,由移动相带入固定相,具有速度快、分离效率高等优点。可用于低沸点、易汽化、热稳定性好的化合物。
选择不同的检测器可改善专属性、提高灵敏度。用于治疗药物监测时通常选用以下三种检测器,即氢火焰检测器(FID)、氮磷检测器(NPD)和电子捕获检测器(ECD)。FID灵敏度在10-10克/毫升,且有很宽的线性,适用于治疗浓度范围较宽,灵敏度要求又不很宽的药物的测定;NPD和ECD灵敏度为10-12克/毫升,且有很高的选择性,主要适用于卤素、氮、磷类药物的测定。质谱(MS)作为气相色谱的检测器(即气―质联用)和液相色谱的检测器(即液―质联用),是目前专属性、灵敏度、分离度都较高的方法,特别适用于代谢物的研究,但仪器需要增加许多附加设备,操作条件要求也高,且价格昂贵,普及有困难。
, 百拇医药
高效液相色谱法(HPLC) 是目前使用较普遍的方法,其弥补了气象色谱不能分离不挥发且具有一定溶解性物质的不足。常用的检测器有紫外检测器、荧光检测器和电化学检测器等。紫外检测器最小检出量为5×10-10克/毫升,适用于检测能吸收该波长紫外光的物质;荧光检测器最小检出量10-9克/毫升,适用于某些生物物质及药物代谢物等;电化学检测器最小检出量为20皮摩尔/毫升,适用于检测一些可电离的物质。
免疫学方法(IA) 包括放射免疫法(RIA)、酶免疫法(EIA)和荧光免疫法(FIA)等,本法不需要事先分离,且灵敏度高、取样量少。放射免疫法是应用液体闪烁仪或γ谱仪来测量放射性强度,适用于批量测定,但需要有同位素的防护设备;酶免疫法可以不用放射性同位素,成本低,测定速度快,测定一个样品仅需几分钟,仪器设备也很简单,缺点是必须有大量的样品源,否则会造成试剂盒的浪费,反而使成本提高;荧光免疫法是一种新发展起来的方法,其灵敏度高,稳定性好,具有发展前途。
近年来,药物分析技术发展很快,如用于生物样品分析的简便快捷又灵敏度高的柱切换技术、用于蛋白质组学研究的二维凝胶电泳和质谱结合的分析技术(2D-PAGEMS),以及TIRNA聚合酶增强免疫检测技术(IDTA)等。
, http://www.100md.com
给药方案个体化
给药个体化
药物剂量和所产生的药理强度受很多因素影响,存在很大的个体差异,理想的给药方案应当是根据每个患者的具体情况量身定制,这就是给药个体化。
在临床工作当中,给药个体化主要通过以下两种手段实现:一是凭借临床医生多年的工作经验,根据临床症状,尽可能使用药适合每一个患者的需要。如应用华法林时可根据凝血酶原时间的延长为指标;应用胍乙啶时可根据血压为指标。这就不仅要求药物要有明确的药理反应作为指标,而且要求医生要有丰富的临床经验。当一些药物很难说清疗效、不好由剂量的大小所定时,单凭经验就不具有科学性而具有冒险性。如苯妥英钠常用剂量为每日300毫克,对一部分患者尚不能预防癫痫发作,但对另一部分患者却已引起中枢神经系统的毒性反应。最科学的手段应当是以测定的血药浓度作为指标,计算出具体患者体内的动力学参数,然后再根据这些参数计算出给药方案。
, 百拇医药
给药个体化的步骤
首先,医生对患者要有一个明确的判断,根据诊断结果及患者的身体状况等具体因素,选择认为适合的药物及给药途径,再由临床医师和临床药师一起拟定初始给药方案(包括给药剂量和间隔等),患者按初始方案用药后,随时观察临床效果的同时,按一定时间采取血样标本,测定血药浓度,根据血药浓度―时间的数据,求出患者的药物动力学参数。再一次由临床医师和临床药师共同根据患者的临床表现和动力学数据,结合临床经验和文献资料对初始给药方案做必要的修改,制订出调整后给药方案,用于患者疾病的治疗。根据具体情况,可重复上述过程,反复调整给药方案(见图1)。
给药个体化方法
比例法 比例法所依据的公式为:D1/D2=Ct1/Ct2=Cmax1/Cmax2=Cmin1/Cmin2。
, 百拇医药
首先需要按具体情况设计一个表格,表中包括某一个需监测的药物针对不同半衰期的人群,在某常规给药间隔,给药剂量达到稳态时,各时间的血药浓度。按常规的给药方案(给药间隔、给药剂量)给药,到达稳态后,在某一个给药间隔的某一时间,采集一个血样,测定其药物浓度,通常测定Cmin,即在下一次给药前取血,将测定的结果与表格对比,可初步确定患者的药物动力学参数,并可按比例调整,得到一个较为合理的给药方案。
一点法 只需在给一次初剂量后的某一时间取血,根据测定的结果及规定的稳态时平均血药浓度,推算出维持剂量。此法无需求算动力学参数,允许患者间的半衰期有一定范围的波动。适用于血管外给药时,药物在体内的吸收与分布很快,药物的吸收速率常数与表观分布容积不随浓度的改变而改变,误差的大小由K值或t1/2的波动程度而定,波动范围越大,误差也越大。
重复一点法 是对一点法的改进,需要给两个相同的试验剂量,在每一个试验剂量后同一时间,分别取两次血样,同时求出两个参数K和Vd。此法需要注意的是两次取血的时间间隔应等于两次给药的时间间隔,且两次给药必须是初次给药和第二次给药,不是指在给药过程中的任一连续的两次给药。
, 百拇医药
血清肌酐法 肌酐清除率是评价肾功能的常用指标,通常由血清肌酐计算肌酐清除率,公式为: 。
Clcr为肌酐清除率(毫升/分钟),A为年龄,BW为体重(公斤),Scr为血清肌酐(毫克/100毫升)。
肌酐清除率的正常值:男性为120,女性为108。肌酐清除率如低于正常值,表明患者的肾功能有损害,因此会影响对药物的清除功能,此时药物的清除速率常数需要进行相应的校正,公式为:K患者=K正常 。
Fu为肾排分数,可从常用药物动力学参数表中查到。此公式适用于所有药物,如果能参考各种药物在肾衰时K值变化的资料,经数学处理,找出关系式,结果会更准确。由于本法是通过血清肌酐计算得出K值,因而此法对于主要由肾小球滤过排泄的药物结果较可靠,否则会有较大的误差,不适用本法。
, 百拇医药(赵春杰)