抗癫痫药物研发方式正在转变
在20世纪,大多数抗癫痫药物的开发主要是依靠试误法。加州大学戴维斯分校神经学家罗格・瓦斯基说:“这些药物是在脑内分子靶点被确定前开发和上市的,现在我们仍然不知道其中部分药物的分子靶点。”
20世纪60年代,法国研究人员指出,每一种抗癫痫药物的开发都是在动物身上进行测试的。当时他们把候选化合物溶解在丙戊酸中(这在当时是一种非常常见的做法),却意外地发现溶剂丙戊酸而不是候选药物起着抗惊厥作用。如今,丙戊酸已获批准,是目前世界上应用最广泛的抗癫痫处方药物。
尽管有这样的成就,但人们越来越认识到,旧的方法是远远不够的。现有药物可控制约70%患者的癫痫发作,但对于那些发生耐药性的30%的患者,治疗方法仍然很少。制药公司和研究人员正在寻找方法加以改变。目前的研究有些是从传统的啮齿类动物模型转移到其他模型,进而提升筛选化合物的能力;也有研究者正在探索针对特定分子靶点的新疗法。
模型的转变
, http://www.100md.com
测试抗癫痫药物的传统方法主要是通过对癫痫样惊厥大鼠和小鼠给予电刺激或化学品如戊四唑。例如,如果研究者发现一种化合物可以预防动物癫痫发作,这一化合物随后就可被转移到进行人体临床试验。目前上市的25个左右的抗癫痫药物都是通过这种方式开发的。
为了测试更广泛的靶向性治疗药物,一些研究人员正在转向使用比啮齿类动物操作更容易和价格更便宜、繁殖更快的动物模型,如鱼。加州大学研究员斯科特・巴班一直在研究Dravet综合征(婴儿期严重肌阵挛癫痫),它是最耐药的癫痫类型之一。约70%~80%的Dravet综合征患者携带一个名为SCN1A的基因突变,该基因在激活神经元中发挥着基础性作用。而基因突变似乎是导致癫痫发作的主要原因。
斯科特・巴班使用SCN1A基因突变的斑马鱼――有癫痫样抽搐的鱼为模型,然后筛选可以防止癫痫发作的药物,从“再利用”库(包含已知供人类使用是安全的,但由于种种原因没有足够有效性的化合物库)中检测超过300种化合物。结果发现,一种长期被遗忘的抗组胺药氯咪唑可抑制斑马鱼的癫痫发作。氯咪唑是如何防止癫痫发作的还不清楚,但它可能与组胺的免疫调节分子无关。氯咪唑可能与组胺(或控制其释放的分子)和调节神经兴奋性的离子通道或控制神经递质释放的受体相互作用。
, 百拇医药
靶点的探索
另一种药物开发的新方法是找出导致癫痫发作的分子靶点,然后再确定针对该靶点的药物。研究人员现在已获得了一些此类具有前途的分子,其中许多系通过疾病的遗传形式确定的。例如,普瑞巴林(辉瑞公司,商品名Lyrica)在2004年被美国食品药品管理局(FDA)批准用于治疗神经疼痛,后来批准增加了抗癫痫的适应证。该药物的靶点是钙离子通道的一个组成部分,可以让钙离子进出神经元,并在导致癫痫中起着某些作用。
围绕一个已知靶点开发抗癫痫药物最值得关注的例子是由东京卫材公司生产和销售的吡仑帕奈(Perampanel,商品名为Fycompa),2012年被FDA批准用于治疗12岁及以上的部分性癫痫发作患者。在20世纪90年代,卫材公司在寻找靶向于AMPA受体的药物,该受体是一种存在于神经元细胞膜的蛋白质。神经递质谷氨酸与AMPA受体结合时,神经元会兴奋,并在某些情况下导致癫痫发作。谷氨酸和AMPA受体可引起多种神经系统疾病,包括癫痫。卫材公司的研究人员推测,抑制AMPA受体可用于治疗癫痫。卫材公司从一开始就制定了严格的标准:他们想要一个强有力的口服活性分子,并具有合适的属性,包括能够到达并与受体结合。在经过12年开发后,吡仑帕奈终于成功获得批准上市。
, http://www.100md.com
研究人员还认为,靶向于癫痫相关受体的其他药物也展现出了一定的开发潜力。有研究显示,一种名为γ-氨基丁酸(GABA)的神经递质能抑制癫痫发作中过度兴奋的神经元。所以,通过增加GABA的利用设计出的药物有望能够抑制癫痫,如丙戊酸钠;或者可直接激活GABA受体的药物,也具有类似的抗癫痫效果。
研究人员正在研究神经活性类固醇,可靶向GABA A受体。特定的突变可使该受体失去敏感性进而触发癫痫,而兴奋GABA A受体的药物可能被用来抑制癫痫发作。
老药的改进 研究人员也在试图通过研究现有抗癫痫药物的作用方式来开发新药。1999年,比利时UCB制药公司的左乙拉西坦获得FDA批准用于治疗癫痫。左乙拉西坦可结合到突触小泡糖蛋白2A(SV2A),SV2A广泛存在于神经元囊泡即含有神经递质的球体。左乙拉西坦可抑制癫痫发作时引发中枢神经系统活性失控的神经递质释放,但同时又具有多种副作用,包括头晕、嗜睡和感染,以及普通感冒。UCB的科学家们开始寻找能与SV2A结合的替代化合物,最终发现了布瓦西坦(Brivaracetam)。它与左乙拉西坦的结构类似,但与SV2A结合更强烈。布瓦西坦目前正在进行Ⅲ期临床试验,它的靶点具有更高的亲和力,可以允许布瓦西坦在较低的剂量下发挥疗效,这就意味着其副作用会更少。
尽管在确定药物的分子靶点方面不断取得进步,但改进的或新的抗癫痫药物的数量仍一直很少,而且许多大型制药公司也不再进行抗癫痫药物的开发。这使得大量的发现和开发工作,留给了学者、小型生物技术公司和专业制药公司,结果导致了抗癫痫新药开发领域竞争有限,他们中的一些比如学者,都无法融资进行抗癫痫新药的临床试验,这也是抗癫痫药物试验招募患者人数少的主要原因。不过可以肯定的是,未来的研究必将引导药物开发直达特定分子靶点,副作用也会更少。
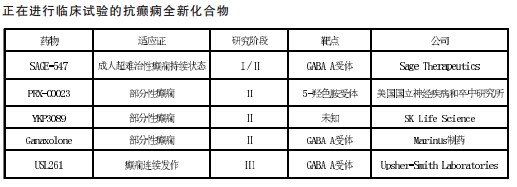
正在进行临床试验的抗癫痫全新化合物如下图
 , 百拇医药(李 勇 编译)
, 百拇医药(李 勇 编译)
20世纪60年代,法国研究人员指出,每一种抗癫痫药物的开发都是在动物身上进行测试的。当时他们把候选化合物溶解在丙戊酸中(这在当时是一种非常常见的做法),却意外地发现溶剂丙戊酸而不是候选药物起着抗惊厥作用。如今,丙戊酸已获批准,是目前世界上应用最广泛的抗癫痫处方药物。
尽管有这样的成就,但人们越来越认识到,旧的方法是远远不够的。现有药物可控制约70%患者的癫痫发作,但对于那些发生耐药性的30%的患者,治疗方法仍然很少。制药公司和研究人员正在寻找方法加以改变。目前的研究有些是从传统的啮齿类动物模型转移到其他模型,进而提升筛选化合物的能力;也有研究者正在探索针对特定分子靶点的新疗法。
模型的转变
, http://www.100md.com
测试抗癫痫药物的传统方法主要是通过对癫痫样惊厥大鼠和小鼠给予电刺激或化学品如戊四唑。例如,如果研究者发现一种化合物可以预防动物癫痫发作,这一化合物随后就可被转移到进行人体临床试验。目前上市的25个左右的抗癫痫药物都是通过这种方式开发的。
为了测试更广泛的靶向性治疗药物,一些研究人员正在转向使用比啮齿类动物操作更容易和价格更便宜、繁殖更快的动物模型,如鱼。加州大学研究员斯科特・巴班一直在研究Dravet综合征(婴儿期严重肌阵挛癫痫),它是最耐药的癫痫类型之一。约70%~80%的Dravet综合征患者携带一个名为SCN1A的基因突变,该基因在激活神经元中发挥着基础性作用。而基因突变似乎是导致癫痫发作的主要原因。
斯科特・巴班使用SCN1A基因突变的斑马鱼――有癫痫样抽搐的鱼为模型,然后筛选可以防止癫痫发作的药物,从“再利用”库(包含已知供人类使用是安全的,但由于种种原因没有足够有效性的化合物库)中检测超过300种化合物。结果发现,一种长期被遗忘的抗组胺药氯咪唑可抑制斑马鱼的癫痫发作。氯咪唑是如何防止癫痫发作的还不清楚,但它可能与组胺的免疫调节分子无关。氯咪唑可能与组胺(或控制其释放的分子)和调节神经兴奋性的离子通道或控制神经递质释放的受体相互作用。
, 百拇医药
靶点的探索
另一种药物开发的新方法是找出导致癫痫发作的分子靶点,然后再确定针对该靶点的药物。研究人员现在已获得了一些此类具有前途的分子,其中许多系通过疾病的遗传形式确定的。例如,普瑞巴林(辉瑞公司,商品名Lyrica)在2004年被美国食品药品管理局(FDA)批准用于治疗神经疼痛,后来批准增加了抗癫痫的适应证。该药物的靶点是钙离子通道的一个组成部分,可以让钙离子进出神经元,并在导致癫痫中起着某些作用。
围绕一个已知靶点开发抗癫痫药物最值得关注的例子是由东京卫材公司生产和销售的吡仑帕奈(Perampanel,商品名为Fycompa),2012年被FDA批准用于治疗12岁及以上的部分性癫痫发作患者。在20世纪90年代,卫材公司在寻找靶向于AMPA受体的药物,该受体是一种存在于神经元细胞膜的蛋白质。神经递质谷氨酸与AMPA受体结合时,神经元会兴奋,并在某些情况下导致癫痫发作。谷氨酸和AMPA受体可引起多种神经系统疾病,包括癫痫。卫材公司的研究人员推测,抑制AMPA受体可用于治疗癫痫。卫材公司从一开始就制定了严格的标准:他们想要一个强有力的口服活性分子,并具有合适的属性,包括能够到达并与受体结合。在经过12年开发后,吡仑帕奈终于成功获得批准上市。
, http://www.100md.com
研究人员还认为,靶向于癫痫相关受体的其他药物也展现出了一定的开发潜力。有研究显示,一种名为γ-氨基丁酸(GABA)的神经递质能抑制癫痫发作中过度兴奋的神经元。所以,通过增加GABA的利用设计出的药物有望能够抑制癫痫,如丙戊酸钠;或者可直接激活GABA受体的药物,也具有类似的抗癫痫效果。
研究人员正在研究神经活性类固醇,可靶向GABA A受体。特定的突变可使该受体失去敏感性进而触发癫痫,而兴奋GABA A受体的药物可能被用来抑制癫痫发作。
老药的改进 研究人员也在试图通过研究现有抗癫痫药物的作用方式来开发新药。1999年,比利时UCB制药公司的左乙拉西坦获得FDA批准用于治疗癫痫。左乙拉西坦可结合到突触小泡糖蛋白2A(SV2A),SV2A广泛存在于神经元囊泡即含有神经递质的球体。左乙拉西坦可抑制癫痫发作时引发中枢神经系统活性失控的神经递质释放,但同时又具有多种副作用,包括头晕、嗜睡和感染,以及普通感冒。UCB的科学家们开始寻找能与SV2A结合的替代化合物,最终发现了布瓦西坦(Brivaracetam)。它与左乙拉西坦的结构类似,但与SV2A结合更强烈。布瓦西坦目前正在进行Ⅲ期临床试验,它的靶点具有更高的亲和力,可以允许布瓦西坦在较低的剂量下发挥疗效,这就意味着其副作用会更少。
尽管在确定药物的分子靶点方面不断取得进步,但改进的或新的抗癫痫药物的数量仍一直很少,而且许多大型制药公司也不再进行抗癫痫药物的开发。这使得大量的发现和开发工作,留给了学者、小型生物技术公司和专业制药公司,结果导致了抗癫痫新药开发领域竞争有限,他们中的一些比如学者,都无法融资进行抗癫痫新药的临床试验,这也是抗癫痫药物试验招募患者人数少的主要原因。不过可以肯定的是,未来的研究必将引导药物开发直达特定分子靶点,副作用也会更少。
正在进行临床试验的抗癫痫全新化合物如下图
 , 百拇医药(李 勇 编译)
, 百拇医药(李 勇 编译)