肿瘤坏死因子在病毒性肝炎肝坏死中的作用及其防护
作者:张定凤 任红 郭树华 潘澄清
单位:(重庆医科大学病毒性肝炎研究所 630010)
关键词:肝炎,病毒性,人;肿瘤坏死因子
中华医学杂志900806
摘要 对47例病毒性肝炎及8名健康供血员测定了血清肿瘤坏死因子(TNF)及外周血细胞诱生的TNF活力。发现重症肝炎及慢性活动性肝炎的TNF活性显著增高,和高血胆红素水平呈正比,有内毒素血症及继发感染者增高更为明显。体外实验,从动物肝脏提取的一种低分子多肽可抑制内毒素对TNF的诱生作用。在动物实验中,低分子多肽可防止内毒素及半乳糖胺引起的肝细胞坏死及TNF活性上升。本研究结果提示TNF和肝细胞坏死有关,低分子多肽对肝脏有保护作用。
乙型肝炎病毒感染引起肝细胞损害的机理系机体免疫应答和病毒相互斗争的结果[1]。近年来,有人提出肝细胞内积聚大量大分子表面抗原可以直接导致肝细胞坏死[2]。但是,上述假说并不能解释所有临床及病理的表现,我们发现某些重症肝炎及严重的慢性活动性肝炎患者,其大片肝细胞坏死区内,不少坏死细胞并无病毒感染的征象,提示尚有非特异性因素介导了肝炎患者的肝细胞坏死。19845年以来,我们对病毒性肝炎的白细胞介素类(IL-2,IL-4,IL-6)及肿瘤坏死因子(TNF)进行了较系统的研究[3,4],发现TNF和病毒性肝炎肝坏死有关。报道如下。
, 百拇医药
材料与方法
一、对象
病毒性肝炎47例,其中包括急性甲型肝炎11例,慢性活动性乙型肝炎27例,亚急性重症乙型肝炎9例。年龄16~47岁。男39例,女8例。另有8名健康供血者作为对照。每个病例均经血清病毒学标志检查,包括HBsAg,抗HBs,HBeAg,抗HBe,抗HBc,抗HBc IgM,抗HAIgA及HBV-DNA斑点杂交。肝功能检查包括胆红素及1分钟胆红素、麝香草酚浊度试验、硫酸锌浊度试验及白蛋白/球蛋白。慢性活动性肝炎及重症肝炎均经肝穿刺活检,诊断标准参照全国病毒性肝炎南宁会议的诊治方案。
二、外周血TNF诱导
取静脉血5ml,肝素抗凝,用Ficoll/Hypaque分离单个核细胞(PBM),用10%小牛血清RPMI1640调整细胞浓度至2×106ml,加入内毒素(Sigma)终末浓度为5μg/ml及0.1%植物血凝素(PHA-P)(Difco)。于5%CO2、37°C孵育48小时后,收获上清液,-30°C保存待测。
, 百拇医药
三、TNF活性检测[5]
将L929细胞以10%小牛血清RPMI1640调整细胞浓度至8×105/ml,取0.1ml加入24孔培养板(Corning),每孔补充营养液至1ml,同时加入2μCi3H-TdR。于5%CO2,37°C孵育48小时,细胞成生长片后弃上清,洗2次,每孔加入待测血清或细胞诱导上清液0.25ml,加营养液至1μg/ml,于37°C、5%CO2继续培养24小时。设置不加测试标本的对照孔。分别收集各孔上清液0.5ml,加入6ml闪烁液(二氯六环、萘、PPO及POPOP),测定已死亡L929细胞释放的3H-TdR的同位素活性(cpm)并计算TNF活性指数。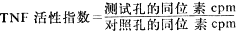
四、半乳糖胺实验性肝损伤
, 百拇医药
2~3月龄纯系Wistar大白鼠24只,雌雄各半,体重130~210g,随机分为4组:A组为对照,B组腹腔一次注入内毒素4000U/ml,C组于腹腔内注入半乳糖胺(GLN)1.2g/kg,并加内毒素4000U/ml,D组腹腔内注射GLN1.2g/kg,内毒素4000U/ml及肝生长素(一种从动物肝脏提取的低分子多肽)0.1ml,36小时后采血测定TNF,并取肝脏进行病理检查。
五、内毒素检测
基质显色法。
六、肝生长素制备
改良LaBreque法[6],本所自行制备。
结 果
一、不同类型病毒性肝炎血清及PBM的TNF活性(表1)
, http://www.100md.com
表1 病毒性肝炎血清及PBM的TNF活性 病例
例数
血清TNFΔ
PBM TNFΔ
健康对照
8
7.1±2.2*
5.9±2.4
慢性活动性乙型肝炎
27
13.8±6.3*
12.6±5.0
, 百拇医药
重症乙型肝炎
6
19.4±3.9**
15.2±4.8
重症乙型肝炎康复期
3
11.9±8.1
7.7±4.9
急性甲型肝炎
11
8.1±2.1
8.3±1.8
, http://www.100md.com Δ δ=0.9273 P〈0.001, *t=7.28,P〈0.001, ** t=13.97 P〈0.001
比较各组病例血清及PBM的TNF活性,两者呈明显相关(γ=0.9273,P〈0.001)。TNF活性以重症乙型肝炎最高(19.4±3.9,P〈0.001),其次为慢性活动性肝炎(13.8±6.3,P〈0.001),重症肝炎恢复期,胆红素已明显下降,则TNF活性也明显下降。急性甲型肝炎TNF活性接近于正常。TNF活性似和病毒性肝炎的病情程度密切相关。
二、血清胆红素水平和TNF活性的关系(表2)
表2 血清胆红素水平和血清及PBM的TNF活性的关系 血清胆红素水平(mg/ml)
例数
血清TNF
, http://www.100md.com
PBM TNF
〉10
12
18.9±8.4*
13.8±5.3
5~9.9
6
16.2±5.0
15.8±6.3
〈4.9
29
10.0±4.2*
9.7±3.5
, http://www.100md.com
* t=13.2 P〈0.001
由于重症肝炎常出现酶胆分离,所以血清胆红素较转氨酶更能反映肝细胞坏死的程度。本组病例血清胆红素高于10mg/ml者其TNF活性显著高于4.9mg/ml以下组(18.9±8.4;10.0±4.2,P〈0.001)。
三、肝炎病人TNF活性和内毒血症及继发感染的关系(表3)
表3 肝炎病人TNF活性和内毒素血症及继发感染的关系
例数
血清TNF
PBM TNF
内毒素血症
11
, 百拇医药
16.8±8.0*
14.6±5.8
无内毒素血症
6
9.3±3.2*
9.2±3.8
合并感染
9
21.7±7.7**
15.0±5.0
未合并感染
37
, http://www.100md.com 11.9±5.2**
10.8±5.4
* t=4.28,P〈0.001,** t=12.3,P〈0.001
内毒素血症阳性者其TNF活性较阴性者显著增高(P〈0.001)。有继发感染。如败血症、原发性腹膜炎、支气管肺炎及病毒感染等,其TNF活性也较无继发感染者为高(P〈0.001),提示内毒素血症及继发感染的毒血症可能激活患者的单核巨噬细胞系统,或为病人高TNF活性的原因。
四、肝生长素对体外诱生TNF的影响
分离病人PBM,分别加内毒素5μg/ml、内毒素5μg/ml及肝生长素10mg/ml,诱生TNF。结果前者TNF活性指数为18.6±0.8,后者为9.5±2.1,提示肝生长素可显著抑制内毒素对TNF的诱生作用(t=5.727,P〈0.001)。
, http://www.100md.com
为判定肝生长素对测定TNF活性的L929细胞有无保护作用,我们于测定血清或细胞诱生上清的TNF活性时,同时加入肝生长素10mg/m1,发现仅血清的TNF活性轻度下降(P〈0.05),对细胞上清的TNF活性无明显影响(表4)。说明肝生长素主要为抑制内毒素诱生TNF的活性,对TNF的细胞毒性靶细胞似无明显保护作用。
表4 肝生长素对体外测定TNF活力的影响 测定标本
TNF活力
血清
21.7±0.6*
血清+肝生长素
17.1±2.3*
(PBM+PHA+内毒素)上清液
, 百拇医药
18.6±0.8
(PBM+PHA+内毒素)上清液+肝生长素
17.8±3.8
(PBM+PHA+肝生长素+内毒素)上清液
9.5±2.1
(PBM+PHA+肝生长素+内毒素)上清液+肝生长素
10.6±2.4
t=2.738 P>0.05
五、实验性肝坏死的TNF活性及肝生长素的保护作用(表5)
表5 大鼠实验性肝坏死和TNF及肝生长素的关系 实验分组
, http://www.100md.com
大鼠数
血清TNF
肝坏死
对照
6
503.8±213.6*
-
半乳糖胺+内毒素
6
1514.3±733.2*
++
内毒素
6
, 百拇医药
1310.7±241.3**
±
半乳糖胺+内毒素+肝生长素
6
522.5±319.2
±
注:“-”正常;“+”小叶性坏死,少于肝小叶的1/3;
“++”亚大块坏死,坏死范围1/3~1/2;
“±”局灶性坏死,肝细胞气球样变
t=5.61,P〈0.001,t=10.6 P〈0.001
大白鼠腹腔注射半乳糖胺及内毒素后,可引起肝细胞大片坏死及血清TNF活性显著升高。单用内毒素也可引起血清TNF活性升高,但肝内病变轻微。注射半乳糖胺及内毒素时同时加人肝生长素,则血清TNF水平无显著上升,肝内病变明显减轻。说明TNF仅当有肝毒性药物或抑制蛋白合成的因素存在时,才引起肝细胞坏死。而肝生长素不仅可以降低TNF水平,早期应用也可以防止肝内严重病变。
, 百拇医药
讨 论
本研究结果表明,慢性活动性肝炎及亚急性重症肝炎患者血清TNF活性及其PBM用内毒素诱生的TNF活性均显著增高,病情恢复时渐下降,与病情轻重呈正比。最近,式藤泰敏也发现暴发性肝功能衰竭患者PBM诱生TNF及IL-1活性憎高[7]。提示TNF和病毒性肝炎肝细胞坏死有一定关系。
慢性活动性肝炎和重症肝炎血清及PBM的TNF活性憎高的机理,可能和内毒素血症及继发感染有关。根据本研究资料及文献报告有关动物实验的结果,均证明内毒素为较强的TNF诱生剂。家兔注射大肠杆菌内毒素,15分钟后血清中出现TNF,高峰见于注射后2小时,5小时后降至基线水平[8]。除内毒素外,其他细菌感染的产物,如化脓性链球菌A的提取物(OK432),金葡菌引起中毒性休克症状群的毒性蛋白(TSST-1),疟原虫裂殖体释出的物质,均可刺激巨噬细胞释放TNF[9,10]。慢性活动性肝炎及重症肝炎由于调理素功能缺陷,抵抗力低下,常易招致继发感染[11]。根据本组病例中合并内毒素血症或继发感染者,血清及PBM TNF活性憎高,病情迅速恶化。TNF可以分为α及β二种: TNFα主要由巨噬细胞产生,有人发现CD4+T细胞也能诱生TNFα[12];TNFβ又称为淋巴毒素,主要由T及B细胞产生[13]。国内有报告严重慢性活动性肝炎患者肝组织内有较多量单核巨噬细胞浸润。井上雅树也发现慢性活动性肝炎患者肝组织内TNF阳性的单核细胞较多见[14]。提示单核巨噬细胞系统产生的TNF在肝炎肝坏死的发病过程中有重要意义。
, 百拇医药
至于TNF引起肝细胞坏死的机理,目前尚不十分清楚。TNF引起微循环障碍及播散性血管内凝血对肝细胞大量坏死可能有一定关系。目前,认为TNF为革兰氏阴性杆菌引起中毒性休克的重要介质[15]。采用多克隆的兔抗TNF血清预先注入小鼠体内,再用内毒素攻击,可以保护小鼠免于死亡[16]。重症肝炙常出现类似内毒素休克的微循环障碍及血液流变学改变,和病情程度及预后有关。其次,TNF也可能直接造成肝损伤,TNF的体内分布以肝脏最多,占31%,TNF的直接细胞毒作用可通过O2及OH-代谢途径,活化cAMP及溶酶体酶。我们从重症肝炎的肝穿刺活检的组织化学检查中,也发现肝细胞坏死区的邻接细胞常有溶酶体酶的激活[17],是否和TNF的作用有关,有待阐明。从本实验中,TNF可加强半乳糖胺的细胞毒。单纯的TNF活性增强并不引起肝细胞大片坏死(表5)。有人报告细胞合成的P36及P42多肽可以抵抗TNF的细胞毒作用,一些抗代谢药物,如放线菌素D,通过干扰上述多肽合成,加强了TNF的细胞毒性作用[18]。重症肝炎由于微循环障碍及病毒感染,也有可能影响P36及P42合成,加重TNF的毒性作用。此外,重症肝炎常有IL-1,IL-6活性憎强,可加强TNF的作用,再通过巨噬细胞的细胞毒作用引起肝损害[19]。
, http://www.100md.com
寻找对抗TNF的细胞毒作用的药物,可能为临床治疗重症肝炎及慢性活动性肝炎开辟一条新途径。从本文资料看来,从动物肝脏提取的低分子多肽,不论在体内或试管中均可对抗内毒素诱生TNF的作用,且可减轻肝脏病变,但对其作用机制有待进一步阐明。有人发现肾上腺皮质激素也可抑制TNF的合成,减轻炎症反应。还有报告在体外试验中,对TNF敏感的细胞预先经上皮生长因子或转化生长因子(TGF-α)短时处理,可抑制对TNF的细胞毒作用。本实验所用低分子多肽的作用部位似乎主要为抑制内毒素对TNF的诱生,对TNF的靶细胞似无保护作用。所以低分子多肽对重症肝炎的治疗,宜早期持续用药,待TNF已造成多器官功能衰竭,则不易奏效,和目前临床初步观察的效果相一致,可供今后临床进一步研究时参考。
参考文献
1.Vento S,Eddlestou ALWF Immunological aspects of chronic active hepatitis Clin Exp Immunol 1987; 68:225.
, 百拇医药
2.Chisari FV, et a1.Intracellular accumulation of the Hepatitis B virus large envelope polypetide induces hepatocellular injury in transgenic mice. J Med Virol 1987;54A.
3.Zhang DF,et a1.In vitro immunoregulation of anti-HBs synthesis by peripheral lymphocytes lymphocytes in HBv infections.Chin Med J l987;100:338.
4.任红,张定凤.乙型肝炎患者B细胞分化因子-白细胞介素6的研究.中华医学杂志 1989;69:264.
5.Flick DA,Comparison of in vitro cell cytotoxic assays for tumour necrosis factor.JImmunl Me-thod l984;68:167.
, http://www.100md.com
6.LaBreque DR,et a1.Purification and physical-chemical characterization of heastic stimulator substance.Heatology l987;7:100.
7.Muto Y, et al. Enhanced tumour necrosis factor and interleukin-1 in fulminant hepatic failure. Lancet 1988;2:72.
8.Beutler BA, et al. Cachectin/tumour necrosis factor production, distribution and metabolic rate in vivo. J Immunol 1985;135:3972.
9. Parant M. Fffects of TNF in bacterial infections. Ann Inst Pasteur/Immunol 1988;139:301.
, 百拇医药
10. Clark LA, et al. The Balance of useful and harmful effects of TNF, with special reference to malaria Ann Inst, Pasteur/Immunol 1988;139:305.
11. Zhang DF, et al. Opsonization activity in subacute hepatic failure and chronic liver diseases. Chin Med J 1987;100:103.
12. Cuturi MC, et al. Independent regulation of tumour necrotic factor and lymphotoxin production by human peripheral blood lymphocytes. J Exp Med 1987;165:1581.
, http://www.100md.com
13. Shalaby MR, et al. An overview of the history and biologic proporties of tumour necrosis factors. Springer Semin Immunopathol 1986:9:33.
14.中上雁树,他,慢性肝疾患いけゐ肝组织内tumour necrosis factor阳性单核球の检对.肝脏 1988;29[suppl]:166.
15.Cerami A, et a1. The role of cachectin/TNF in endotoxic sbock and cachexia. Immunol Today 1988; 9:28.
16.Beutler B,et al.Passive immunization against cachectin/tumour necrotic factor protects mice from lethal effect of endotoxin. Science l985;229:869.
, 百拇医药
17.苗德林,张定凤.酸性磷酸酶及ATP酶对亚急性重型肝炎肝细胞坏死及郁胆的影响.中华病理学杂志 1985;14:176.
18.Rosenblum MG,et a1.Tumor necrosis fecotrα: multifaceted peptide hormone.Crit Rev Immunol 1989;9:21
19. Haeanaka K, et al. Necrotizing activity of tumour necrosis factor and its mechanisms. Ann Inst Pasteur/Immunol 1988;139:288.
(1989年12月27日收稿), 百拇医药
单位:(重庆医科大学病毒性肝炎研究所 630010)
关键词:肝炎,病毒性,人;肿瘤坏死因子
中华医学杂志900806
摘要 对47例病毒性肝炎及8名健康供血员测定了血清肿瘤坏死因子(TNF)及外周血细胞诱生的TNF活力。发现重症肝炎及慢性活动性肝炎的TNF活性显著增高,和高血胆红素水平呈正比,有内毒素血症及继发感染者增高更为明显。体外实验,从动物肝脏提取的一种低分子多肽可抑制内毒素对TNF的诱生作用。在动物实验中,低分子多肽可防止内毒素及半乳糖胺引起的肝细胞坏死及TNF活性上升。本研究结果提示TNF和肝细胞坏死有关,低分子多肽对肝脏有保护作用。
乙型肝炎病毒感染引起肝细胞损害的机理系机体免疫应答和病毒相互斗争的结果[1]。近年来,有人提出肝细胞内积聚大量大分子表面抗原可以直接导致肝细胞坏死[2]。但是,上述假说并不能解释所有临床及病理的表现,我们发现某些重症肝炎及严重的慢性活动性肝炎患者,其大片肝细胞坏死区内,不少坏死细胞并无病毒感染的征象,提示尚有非特异性因素介导了肝炎患者的肝细胞坏死。19845年以来,我们对病毒性肝炎的白细胞介素类(IL-2,IL-4,IL-6)及肿瘤坏死因子(TNF)进行了较系统的研究[3,4],发现TNF和病毒性肝炎肝坏死有关。报道如下。
, 百拇医药
材料与方法
一、对象
病毒性肝炎47例,其中包括急性甲型肝炎11例,慢性活动性乙型肝炎27例,亚急性重症乙型肝炎9例。年龄16~47岁。男39例,女8例。另有8名健康供血者作为对照。每个病例均经血清病毒学标志检查,包括HBsAg,抗HBs,HBeAg,抗HBe,抗HBc,抗HBc IgM,抗HAIgA及HBV-DNA斑点杂交。肝功能检查包括胆红素及1分钟胆红素、麝香草酚浊度试验、硫酸锌浊度试验及白蛋白/球蛋白。慢性活动性肝炎及重症肝炎均经肝穿刺活检,诊断标准参照全国病毒性肝炎南宁会议的诊治方案。
二、外周血TNF诱导
取静脉血5ml,肝素抗凝,用Ficoll/Hypaque分离单个核细胞(PBM),用10%小牛血清RPMI1640调整细胞浓度至2×106ml,加入内毒素(Sigma)终末浓度为5μg/ml及0.1%植物血凝素(PHA-P)(Difco)。于5%CO2、37°C孵育48小时后,收获上清液,-30°C保存待测。
, 百拇医药
三、TNF活性检测[5]
将L929细胞以10%小牛血清RPMI1640调整细胞浓度至8×105/ml,取0.1ml加入24孔培养板(Corning),每孔补充营养液至1ml,同时加入2μCi3H-TdR。于5%CO2,37°C孵育48小时,细胞成生长片后弃上清,洗2次,每孔加入待测血清或细胞诱导上清液0.25ml,加营养液至1μg/ml,于37°C、5%CO2继续培养24小时。设置不加测试标本的对照孔。分别收集各孔上清液0.5ml,加入6ml闪烁液(二氯六环、萘、PPO及POPOP),测定已死亡L929细胞释放的3H-TdR的同位素活性(cpm)并计算TNF活性指数。
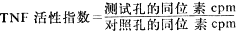
四、半乳糖胺实验性肝损伤
, 百拇医药
2~3月龄纯系Wistar大白鼠24只,雌雄各半,体重130~210g,随机分为4组:A组为对照,B组腹腔一次注入内毒素4000U/ml,C组于腹腔内注入半乳糖胺(GLN)1.2g/kg,并加内毒素4000U/ml,D组腹腔内注射GLN1.2g/kg,内毒素4000U/ml及肝生长素(一种从动物肝脏提取的低分子多肽)0.1ml,36小时后采血测定TNF,并取肝脏进行病理检查。
五、内毒素检测
基质显色法。
六、肝生长素制备
改良LaBreque法[6],本所自行制备。
结 果
一、不同类型病毒性肝炎血清及PBM的TNF活性(表1)
, http://www.100md.com
表1 病毒性肝炎血清及PBM的TNF活性 病例
例数
血清TNFΔ
PBM TNFΔ
健康对照
8
7.1±2.2*
5.9±2.4
慢性活动性乙型肝炎
27
13.8±6.3*
12.6±5.0
, 百拇医药
重症乙型肝炎
6
19.4±3.9**
15.2±4.8
重症乙型肝炎康复期
3
11.9±8.1
7.7±4.9
急性甲型肝炎
11
8.1±2.1
8.3±1.8
, http://www.100md.com Δ δ=0.9273 P〈0.001, *t=7.28,P〈0.001, ** t=13.97 P〈0.001
比较各组病例血清及PBM的TNF活性,两者呈明显相关(γ=0.9273,P〈0.001)。TNF活性以重症乙型肝炎最高(19.4±3.9,P〈0.001),其次为慢性活动性肝炎(13.8±6.3,P〈0.001),重症肝炎恢复期,胆红素已明显下降,则TNF活性也明显下降。急性甲型肝炎TNF活性接近于正常。TNF活性似和病毒性肝炎的病情程度密切相关。
二、血清胆红素水平和TNF活性的关系(表2)
表2 血清胆红素水平和血清及PBM的TNF活性的关系 血清胆红素水平(mg/ml)
例数
血清TNF
, http://www.100md.com
PBM TNF
〉10
12
18.9±8.4*
13.8±5.3
5~9.9
6
16.2±5.0
15.8±6.3
〈4.9
29
10.0±4.2*
9.7±3.5
, http://www.100md.com
* t=13.2 P〈0.001
由于重症肝炎常出现酶胆分离,所以血清胆红素较转氨酶更能反映肝细胞坏死的程度。本组病例血清胆红素高于10mg/ml者其TNF活性显著高于4.9mg/ml以下组(18.9±8.4;10.0±4.2,P〈0.001)。
三、肝炎病人TNF活性和内毒血症及继发感染的关系(表3)
表3 肝炎病人TNF活性和内毒素血症及继发感染的关系
例数
血清TNF
PBM TNF
内毒素血症
11
, 百拇医药
16.8±8.0*
14.6±5.8
无内毒素血症
6
9.3±3.2*
9.2±3.8
合并感染
9
21.7±7.7**
15.0±5.0
未合并感染
37
, http://www.100md.com 11.9±5.2**
10.8±5.4
* t=4.28,P〈0.001,** t=12.3,P〈0.001
内毒素血症阳性者其TNF活性较阴性者显著增高(P〈0.001)。有继发感染。如败血症、原发性腹膜炎、支气管肺炎及病毒感染等,其TNF活性也较无继发感染者为高(P〈0.001),提示内毒素血症及继发感染的毒血症可能激活患者的单核巨噬细胞系统,或为病人高TNF活性的原因。
四、肝生长素对体外诱生TNF的影响
分离病人PBM,分别加内毒素5μg/ml、内毒素5μg/ml及肝生长素10mg/ml,诱生TNF。结果前者TNF活性指数为18.6±0.8,后者为9.5±2.1,提示肝生长素可显著抑制内毒素对TNF的诱生作用(t=5.727,P〈0.001)。
, http://www.100md.com
为判定肝生长素对测定TNF活性的L929细胞有无保护作用,我们于测定血清或细胞诱生上清的TNF活性时,同时加入肝生长素10mg/m1,发现仅血清的TNF活性轻度下降(P〈0.05),对细胞上清的TNF活性无明显影响(表4)。说明肝生长素主要为抑制内毒素诱生TNF的活性,对TNF的细胞毒性靶细胞似无明显保护作用。
表4 肝生长素对体外测定TNF活力的影响 测定标本
TNF活力
血清
21.7±0.6*
血清+肝生长素
17.1±2.3*
(PBM+PHA+内毒素)上清液
, 百拇医药
18.6±0.8
(PBM+PHA+内毒素)上清液+肝生长素
17.8±3.8
(PBM+PHA+肝生长素+内毒素)上清液
9.5±2.1
(PBM+PHA+肝生长素+内毒素)上清液+肝生长素
10.6±2.4
t=2.738 P>0.05
五、实验性肝坏死的TNF活性及肝生长素的保护作用(表5)
表5 大鼠实验性肝坏死和TNF及肝生长素的关系 实验分组
, http://www.100md.com
大鼠数
血清TNF
肝坏死
对照
6
503.8±213.6*
-
半乳糖胺+内毒素
6
1514.3±733.2*
++
内毒素
6
, 百拇医药
1310.7±241.3**
±
半乳糖胺+内毒素+肝生长素
6
522.5±319.2
±
注:“-”正常;“+”小叶性坏死,少于肝小叶的1/3;
“++”亚大块坏死,坏死范围1/3~1/2;
“±”局灶性坏死,肝细胞气球样变
t=5.61,P〈0.001,t=10.6 P〈0.001
大白鼠腹腔注射半乳糖胺及内毒素后,可引起肝细胞大片坏死及血清TNF活性显著升高。单用内毒素也可引起血清TNF活性升高,但肝内病变轻微。注射半乳糖胺及内毒素时同时加人肝生长素,则血清TNF水平无显著上升,肝内病变明显减轻。说明TNF仅当有肝毒性药物或抑制蛋白合成的因素存在时,才引起肝细胞坏死。而肝生长素不仅可以降低TNF水平,早期应用也可以防止肝内严重病变。
, 百拇医药
讨 论
本研究结果表明,慢性活动性肝炎及亚急性重症肝炎患者血清TNF活性及其PBM用内毒素诱生的TNF活性均显著增高,病情恢复时渐下降,与病情轻重呈正比。最近,式藤泰敏也发现暴发性肝功能衰竭患者PBM诱生TNF及IL-1活性憎高[7]。提示TNF和病毒性肝炎肝细胞坏死有一定关系。
慢性活动性肝炎和重症肝炎血清及PBM的TNF活性憎高的机理,可能和内毒素血症及继发感染有关。根据本研究资料及文献报告有关动物实验的结果,均证明内毒素为较强的TNF诱生剂。家兔注射大肠杆菌内毒素,15分钟后血清中出现TNF,高峰见于注射后2小时,5小时后降至基线水平[8]。除内毒素外,其他细菌感染的产物,如化脓性链球菌A的提取物(OK432),金葡菌引起中毒性休克症状群的毒性蛋白(TSST-1),疟原虫裂殖体释出的物质,均可刺激巨噬细胞释放TNF[9,10]。慢性活动性肝炎及重症肝炎由于调理素功能缺陷,抵抗力低下,常易招致继发感染[11]。根据本组病例中合并内毒素血症或继发感染者,血清及PBM TNF活性憎高,病情迅速恶化。TNF可以分为α及β二种: TNFα主要由巨噬细胞产生,有人发现CD4+T细胞也能诱生TNFα[12];TNFβ又称为淋巴毒素,主要由T及B细胞产生[13]。国内有报告严重慢性活动性肝炎患者肝组织内有较多量单核巨噬细胞浸润。井上雅树也发现慢性活动性肝炎患者肝组织内TNF阳性的单核细胞较多见[14]。提示单核巨噬细胞系统产生的TNF在肝炎肝坏死的发病过程中有重要意义。
, 百拇医药
至于TNF引起肝细胞坏死的机理,目前尚不十分清楚。TNF引起微循环障碍及播散性血管内凝血对肝细胞大量坏死可能有一定关系。目前,认为TNF为革兰氏阴性杆菌引起中毒性休克的重要介质[15]。采用多克隆的兔抗TNF血清预先注入小鼠体内,再用内毒素攻击,可以保护小鼠免于死亡[16]。重症肝炙常出现类似内毒素休克的微循环障碍及血液流变学改变,和病情程度及预后有关。其次,TNF也可能直接造成肝损伤,TNF的体内分布以肝脏最多,占31%,TNF的直接细胞毒作用可通过O2及OH-代谢途径,活化cAMP及溶酶体酶。我们从重症肝炎的肝穿刺活检的组织化学检查中,也发现肝细胞坏死区的邻接细胞常有溶酶体酶的激活[17],是否和TNF的作用有关,有待阐明。从本实验中,TNF可加强半乳糖胺的细胞毒。单纯的TNF活性增强并不引起肝细胞大片坏死(表5)。有人报告细胞合成的P36及P42多肽可以抵抗TNF的细胞毒作用,一些抗代谢药物,如放线菌素D,通过干扰上述多肽合成,加强了TNF的细胞毒性作用[18]。重症肝炎由于微循环障碍及病毒感染,也有可能影响P36及P42合成,加重TNF的毒性作用。此外,重症肝炎常有IL-1,IL-6活性憎强,可加强TNF的作用,再通过巨噬细胞的细胞毒作用引起肝损害[19]。
, http://www.100md.com
寻找对抗TNF的细胞毒作用的药物,可能为临床治疗重症肝炎及慢性活动性肝炎开辟一条新途径。从本文资料看来,从动物肝脏提取的低分子多肽,不论在体内或试管中均可对抗内毒素诱生TNF的作用,且可减轻肝脏病变,但对其作用机制有待进一步阐明。有人发现肾上腺皮质激素也可抑制TNF的合成,减轻炎症反应。还有报告在体外试验中,对TNF敏感的细胞预先经上皮生长因子或转化生长因子(TGF-α)短时处理,可抑制对TNF的细胞毒作用。本实验所用低分子多肽的作用部位似乎主要为抑制内毒素对TNF的诱生,对TNF的靶细胞似无保护作用。所以低分子多肽对重症肝炎的治疗,宜早期持续用药,待TNF已造成多器官功能衰竭,则不易奏效,和目前临床初步观察的效果相一致,可供今后临床进一步研究时参考。
参考文献
1.Vento S,Eddlestou ALWF Immunological aspects of chronic active hepatitis Clin Exp Immunol 1987; 68:225.
, 百拇医药
2.Chisari FV, et a1.Intracellular accumulation of the Hepatitis B virus large envelope polypetide induces hepatocellular injury in transgenic mice. J Med Virol 1987;54A.
3.Zhang DF,et a1.In vitro immunoregulation of anti-HBs synthesis by peripheral lymphocytes lymphocytes in HBv infections.Chin Med J l987;100:338.
4.任红,张定凤.乙型肝炎患者B细胞分化因子-白细胞介素6的研究.中华医学杂志 1989;69:264.
5.Flick DA,Comparison of in vitro cell cytotoxic assays for tumour necrosis factor.JImmunl Me-thod l984;68:167.
, http://www.100md.com
6.LaBreque DR,et a1.Purification and physical-chemical characterization of heastic stimulator substance.Heatology l987;7:100.
7.Muto Y, et al. Enhanced tumour necrosis factor and interleukin-1 in fulminant hepatic failure. Lancet 1988;2:72.
8.Beutler BA, et al. Cachectin/tumour necrosis factor production, distribution and metabolic rate in vivo. J Immunol 1985;135:3972.
9. Parant M. Fffects of TNF in bacterial infections. Ann Inst Pasteur/Immunol 1988;139:301.
, 百拇医药
10. Clark LA, et al. The Balance of useful and harmful effects of TNF, with special reference to malaria Ann Inst, Pasteur/Immunol 1988;139:305.
11. Zhang DF, et al. Opsonization activity in subacute hepatic failure and chronic liver diseases. Chin Med J 1987;100:103.
12. Cuturi MC, et al. Independent regulation of tumour necrotic factor and lymphotoxin production by human peripheral blood lymphocytes. J Exp Med 1987;165:1581.
, http://www.100md.com
13. Shalaby MR, et al. An overview of the history and biologic proporties of tumour necrosis factors. Springer Semin Immunopathol 1986:9:33.
14.中上雁树,他,慢性肝疾患いけゐ肝组织内tumour necrosis factor阳性单核球の检对.肝脏 1988;29[suppl]:166.
15.Cerami A, et a1. The role of cachectin/TNF in endotoxic sbock and cachexia. Immunol Today 1988; 9:28.
16.Beutler B,et al.Passive immunization against cachectin/tumour necrotic factor protects mice from lethal effect of endotoxin. Science l985;229:869.
, 百拇医药
17.苗德林,张定凤.酸性磷酸酶及ATP酶对亚急性重型肝炎肝细胞坏死及郁胆的影响.中华病理学杂志 1985;14:176.
18.Rosenblum MG,et a1.Tumor necrosis fecotrα: multifaceted peptide hormone.Crit Rev Immunol 1989;9:21
19. Haeanaka K, et al. Necrotizing activity of tumour necrosis factor and its mechanisms. Ann Inst Pasteur/Immunol 1988;139:288.
(1989年12月27日收稿), 百拇医药