缺血与再灌注时电刺激引起大鼠心去甲肾上腺素释放的变化
作者:冯义柏 Seyfarth M Richardt G Schomig A
单位:430022武汉同济医科大学心血管病研究所(冯义柏),德国海德堡大学内科医院(Seyfarth M, Richardt G, Schmig A)
关键词:心肌再灌流;去甲肾上腺素
中华医学杂志931015 摘要 运用电场刺激(频率6Hz,电压5V,脉宽2ms)研究了离体灌注的鼠心,在缺血早期和再灌注时去甲肾上腺素(NA)释放的变化。经自身前后两次刺激对比(S2/S1),证实电刺激通过兴奋心脏的交感神经,引起NA钙依赖性的出胞释入,并具良好的重复性(S2/S1=1.07,P〉0.05)。而缺血早期(〈10分钟),NA释放受到明显抑制(S2/S1=0.34,)〈0.01),恢复再灌注后,抑制作用逐渐消失。再灌注达5分钟时,电刺激引起的NA释放已达缺血前水平(S2/S1=1.02,P〉0.05)。研究结果表明,缺血早期由于心脏内一系列的代谢改变,对通过突触前调节的NA出胞释放具有抑制作用,恢复再灌注后NA释放的抑制作用也随之消失。
, 百拇医药
心肌缺血时,心脏交感活性增强导致去甲肾上腺素(NA)大量释放,常常是引起心律失常和心肌损伤加剧的重要原因。因此,研究NA在心脏缺血时的释放规律有重要的临床意义。本实验运用电场刺激研究了鼠心在缺血早期(〈10分钟)以及恢复再灌注时。NA释放的变化。
材料与方法
雄性大鼠体重200~250g,使用硫贲妥钠(75~100mg/kg)腹腔内麻醉。经静脉注入500U肝素后,开胸取出心脏。按经典的Langendorr方法[1],由升主动脉插入灌注管,置于主动脉瓣上方,以利冠状动脉灌注。
采用改良Krebs-Henseleit灌注液(成份:单位mmol/L)NaCl125,NaHCO316.9, Na2HPO40.2, kc14.0, CaC11.85, MgC11.2,葡萄糖,11.0,EDTA0.02,灌注速度5ml/分钟。灌注液以氧气氧气充分饱和,并以CO2调节pH到7.4。灌注液进入心脏处的温度保持在37.5℃。整个实验过程中,使用重摄取阻滞剂盐酸脱甲丙咪溱(Ciba-Geigy, Basel, Schweiz)混入灌液液中,浓度为100mmol/L,以阻滞神经末梢对NA的重摄取 ,排除Uptake1的影响[2]。心肌缺血由中断灌注液引起,中断时间即为心肌缺血时间。
, 百拇医药
两个小型靶形电极分别相对与心外膜接触,并与电刺激器相连。刺激脉冲频率为6Hz,脉宽2ms,有效刺激电压5V。心脏经30分钟灌注的平衡后,行第一次电场刺激(S1)为对照,5分钟后加入试验条件,再行第二次刺激(S2)为实验,两次电刺激时间均持续1分钟。分别收集2次电刺激同等时间的心脏流出液,用高压液相色谱仪(Latek, Heidelbeng,FRG)测定其NA的含量,前后比较,即计算S2/S1的比值。
数据处理:数据以X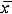 ±S表示,资料用配对t检验处理,计算P值。
±S表示,资料用配对t检验处理,计算P值。
结 果
一、电场刺激引起NA释放的重复性。
本组大鼠10只,不加任何实验条件,仅行前后电场刺激,S1,S2引起的NA释放分别为194±27和209±26mmol/g(每克心脏),S2/S1为1.07(P〉0.05)。示前后两刺激有良好的重复性。
, 百拇医药
二、电场刺激引起NA释放的交感源性
大鼠3组每组6只,分别于S2前10分钟开始加入抗胆碱药阿托品1μmol/L和10μmol/L和拟胆碱药卡巴可(1μmol/L),结果见表1。可见NA释放唯在使用卡巴可后受到明显抑制外,阿托品对其无明显影响。
表1 阿托品、卡巴可对电场刺激引起NA释放的影响(pmol/g,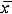 ±S) 组别
±S) 组别
鼠数
S1
S2
S2/S1
, http://www.100md.com
P
阿托品
6
130±20
44±3
0.34
<0.01
(1μmol/L)
阿托品
6
177±25
119±19
0.67
, http://www.100md.com
>0.05
(10μmol/L)
卡巴可
6
210±38
215±41
1.02
>0.05
(1μmol/L)
三、缺血早期(〈10分钟)电刺激引起钙依赖性的NA出胞释放
大鼠两组,于S1后缺血10分钟行S2刺激,随后恢复灌流,并收集心脏灌注液。其中一组于S1后换用无钙灌注液灌注[2],然后缺血并行S2。结果示缺血10分钟电场刺激(S2)引起NA释放减少,而在无钙灌注后缺血10分钟,S2引起的NA释放更进一步减少,表2。
, http://www.100md.com
表2 有钙及无钙灌注下NA释放的变化(pmol/g,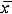 ±S) 组别
±S) 组别
鼠数
S1
S2
S2/S1
P
缺血10分钟
10
136±5
44±6
, 百拇医药
0.31
<0.01
无钙+缺血
6
54±9
8±7
0.15
<0.01
10分钟
四、缺血与再灌注时电场刺激引起NA释放的变化。
大鼠3组,S1后均缺血10分钟。第1组S2仍在缺血的第10分钟开始进行;第2组S2于缺血10分钟完毕后,与再灌注1分钟时同时进行;第3组S2于再灌注后的第五分钟进行。结果可见恢复再灌注后电场刺激S2引起NA释放,已不受明显抑制,表3。
, 百拇医药
表3 再灌注后场刺激引起NA释放的变化(pmol/g,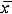 ±S) 组别
±S) 组别
鼠数
S1
S2
S2/S1
P
1组
6
130±20
44±3
, 百拇医药
0.34
<0.01
2组
6
177±25
119±19
0.67
>0.05
3组
6
210±38
215±41
1.02
, 百拇医药
>0.05
讨 论
业已明确,心肌梗塞早期血浆儿茶酚胺浓度增加明显[3~5],但对心肌损伤仅起间接作用,而心肌内局部儿茶酚胺的释放和累积,则起更重要的直接损伤作用。本实验证实,电场刺激引起NA释放具有良好的重复性(S2/S1=1.07,P〉0.05)。阿托品阻滞迷走神经后,但使用拟胆碱药卡巴可后,NA释放显著受抑。由此证实,电场刺激通过兴奋交感神经末梢,产生NA释放,但不伴有乙酰胆碱释出。说明场刺激用于研究心脏缺血时交感神经兴奋NA释放的变化规律,具有类似于通过电刺激左颈胸交感神经节引起NA释放相同的合理性。
缺血10分钟行电场刺激,NA释放受到抑制(S2/S1=0.31P〈0.01),而无钙灌注后,S2/S1进一步下降为0.15,显示出此时NA释放方式仍是一种钙依赖性的出胞释放[3]。Anthomy等[5,6]通过电刺激左颈胸交感神经节,证实鼠心在缺血早期(〈10分钟)交感神经兴奋并不导致NA大量释出。心肌缺血的某些代谢产物,成为NA释放的抑制因素。随再灌注开始缺血代谢产物逐步冲出,NA释放的抑制也逐步减弱直到完全消失。于再灌注开始同时行S2,S2/S1=0.67;于再灌注后5分钟行S2,S2/S1=1.02。
, 百拇医药
现已明确,NA作为分布在心脏交感神经末梢的传递介质,正常时是一种钙依赖性的出胞释放,并需ATP提供能量,受突触前调节。心脏缺血时,随缺血时间长短不同,NA释放释放有3种不同的机制。对此,Schmig[3]通过动物实验证实,长时间缺血(〉40分钟),由于神经细胞膜已有结构上的破坏,造成大量的NA漏出;10~40分钟缺血,ATP消耗歹尽,NA呈一种不依赖钙的非出胞方式释放,累积在细胞间隙的浓度足以导致心肌细胞坏死。缺血早期(〈10分钟),由于糖酵解仍可提供一定能量,NA的出胞释放赖以继续。但NA释放的突触前调节主要是通过A1一腺苷受体而受到有力抑制,与正常时通过ɑ2一受体不同。大量腺苷来自于ATP的代谢。Richardt等[7]的研究指出这种抑制因素实为一种保护机制。此外,笔者通过对缺血单因素如高K+,低pH,缺氧能分别进行研究,也证实某些缺血单因素对缺血早期的NA释放具有不同程度的抑制作用[8]。
, 百拇医药
此外,由本实验结果可见,缺血早期NA释放的掏因素随再灌注恢复而逐步丧失。因此,抑制交感活性的治疗对防止缺血-再灌注损伤是适宜的。
参考文献
1 Langendorff O. Untersuchungen an überlebenden Sugethierherzen. Arch Ges Phusiol, 1985,61:291.
2 Schmig A, Dart AM, Dietz R, et al. Release of endogenous catecholamines in the ischemic myocardium of the rat. Circulation Research, 1984,55:689.
3 Schmig A. Catechoamines in myocardial ischemia. Cir-culation. 1990,82(suppl Ⅱ):Ⅱ-13-Ⅱ-22.
, http://www.100md.com
4 Nadear RA and de Champlain J. Plasma catecholamines in acute myocardial infarction. Am Heart J, 1979,98:548.
5 Karlsberg RP, Cryer PE, Roberts R. Serial plasma catecholamine response early in the course of clinical acute myocardial infarction. Am Heart J, 1981,102:24.
6 Anthomy M, Dart AM, Schmig A, et al. Relese of endogenous catecholamines in the ischemic mycardium of the rat. Circulation Research, 1984, 55:702.
, http://www.100md.com
7 Richardt G, Waas W, Kranzhfer R, et al. Adenosine inhibites exocytotic release of endogenous noradrenaline in rat heart: A protective mechanism in early myocardial ischemia. Circulation Research, 1987, 61:117.
8 Seyfarth M, Feng Yibai, Richardt G, et al. Speziesahngigkeit der exozytotischen Nordiologie, bei Myokardschmie. Kardiologie, 1992,81:306.
(收稿:1992-10-17 修回:1993-07-19), http://www.100md.com
单位:430022武汉同济医科大学心血管病研究所(冯义柏),德国海德堡大学内科医院(Seyfarth M, Richardt G, Schmig A)
关键词:心肌再灌流;去甲肾上腺素
中华医学杂志931015 摘要 运用电场刺激(频率6Hz,电压5V,脉宽2ms)研究了离体灌注的鼠心,在缺血早期和再灌注时去甲肾上腺素(NA)释放的变化。经自身前后两次刺激对比(S2/S1),证实电刺激通过兴奋心脏的交感神经,引起NA钙依赖性的出胞释入,并具良好的重复性(S2/S1=1.07,P〉0.05)。而缺血早期(〈10分钟),NA释放受到明显抑制(S2/S1=0.34,)〈0.01),恢复再灌注后,抑制作用逐渐消失。再灌注达5分钟时,电刺激引起的NA释放已达缺血前水平(S2/S1=1.02,P〉0.05)。研究结果表明,缺血早期由于心脏内一系列的代谢改变,对通过突触前调节的NA出胞释放具有抑制作用,恢复再灌注后NA释放的抑制作用也随之消失。
, 百拇医药
心肌缺血时,心脏交感活性增强导致去甲肾上腺素(NA)大量释放,常常是引起心律失常和心肌损伤加剧的重要原因。因此,研究NA在心脏缺血时的释放规律有重要的临床意义。本实验运用电场刺激研究了鼠心在缺血早期(〈10分钟)以及恢复再灌注时。NA释放的变化。
材料与方法
雄性大鼠体重200~250g,使用硫贲妥钠(75~100mg/kg)腹腔内麻醉。经静脉注入500U肝素后,开胸取出心脏。按经典的Langendorr方法[1],由升主动脉插入灌注管,置于主动脉瓣上方,以利冠状动脉灌注。
采用改良Krebs-Henseleit灌注液(成份:单位mmol/L)NaCl125,NaHCO316.9, Na2HPO40.2, kc14.0, CaC11.85, MgC11.2,葡萄糖,11.0,EDTA0.02,灌注速度5ml/分钟。灌注液以氧气氧气充分饱和,并以CO2调节pH到7.4。灌注液进入心脏处的温度保持在37.5℃。整个实验过程中,使用重摄取阻滞剂盐酸脱甲丙咪溱(Ciba-Geigy, Basel, Schweiz)混入灌液液中,浓度为100mmol/L,以阻滞神经末梢对NA的重摄取 ,排除Uptake1的影响[2]。心肌缺血由中断灌注液引起,中断时间即为心肌缺血时间。
, 百拇医药
两个小型靶形电极分别相对与心外膜接触,并与电刺激器相连。刺激脉冲频率为6Hz,脉宽2ms,有效刺激电压5V。心脏经30分钟灌注的平衡后,行第一次电场刺激(S1)为对照,5分钟后加入试验条件,再行第二次刺激(S2)为实验,两次电刺激时间均持续1分钟。分别收集2次电刺激同等时间的心脏流出液,用高压液相色谱仪(Latek, Heidelbeng,FRG)测定其NA的含量,前后比较,即计算S2/S1的比值。
数据处理:数据以X
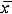 ±S表示,资料用配对t检验处理,计算P值。
±S表示,资料用配对t检验处理,计算P值。结 果
一、电场刺激引起NA释放的重复性。
本组大鼠10只,不加任何实验条件,仅行前后电场刺激,S1,S2引起的NA释放分别为194±27和209±26mmol/g(每克心脏),S2/S1为1.07(P〉0.05)。示前后两刺激有良好的重复性。
, 百拇医药
二、电场刺激引起NA释放的交感源性
大鼠3组每组6只,分别于S2前10分钟开始加入抗胆碱药阿托品1μmol/L和10μmol/L和拟胆碱药卡巴可(1μmol/L),结果见表1。可见NA释放唯在使用卡巴可后受到明显抑制外,阿托品对其无明显影响。
表1 阿托品、卡巴可对电场刺激引起NA释放的影响(pmol/g,
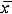 ±S) 组别
±S) 组别鼠数
S1
S2
S2/S1
, http://www.100md.com
P
阿托品
6
130±20
44±3
0.34
<0.01
(1μmol/L)
阿托品
6
177±25
119±19
0.67
, http://www.100md.com
>0.05
(10μmol/L)
卡巴可
6
210±38
215±41
1.02
>0.05
(1μmol/L)
三、缺血早期(〈10分钟)电刺激引起钙依赖性的NA出胞释放
大鼠两组,于S1后缺血10分钟行S2刺激,随后恢复灌流,并收集心脏灌注液。其中一组于S1后换用无钙灌注液灌注[2],然后缺血并行S2。结果示缺血10分钟电场刺激(S2)引起NA释放减少,而在无钙灌注后缺血10分钟,S2引起的NA释放更进一步减少,表2。
, http://www.100md.com
表2 有钙及无钙灌注下NA释放的变化(pmol/g,
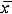 ±S) 组别
±S) 组别鼠数
S1
S2
S2/S1
P
缺血10分钟
10
136±5
44±6
, 百拇医药
0.31
<0.01
无钙+缺血
6
54±9
8±7
0.15
<0.01
10分钟
四、缺血与再灌注时电场刺激引起NA释放的变化。
大鼠3组,S1后均缺血10分钟。第1组S2仍在缺血的第10分钟开始进行;第2组S2于缺血10分钟完毕后,与再灌注1分钟时同时进行;第3组S2于再灌注后的第五分钟进行。结果可见恢复再灌注后电场刺激S2引起NA释放,已不受明显抑制,表3。
, 百拇医药
表3 再灌注后场刺激引起NA释放的变化(pmol/g,
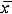 ±S) 组别
±S) 组别鼠数
S1
S2
S2/S1
P
1组
6
130±20
44±3
, 百拇医药
0.34
<0.01
2组
6
177±25
119±19
0.67
>0.05
3组
6
210±38
215±41
1.02
, 百拇医药
>0.05
讨 论
业已明确,心肌梗塞早期血浆儿茶酚胺浓度增加明显[3~5],但对心肌损伤仅起间接作用,而心肌内局部儿茶酚胺的释放和累积,则起更重要的直接损伤作用。本实验证实,电场刺激引起NA释放具有良好的重复性(S2/S1=1.07,P〉0.05)。阿托品阻滞迷走神经后,但使用拟胆碱药卡巴可后,NA释放显著受抑。由此证实,电场刺激通过兴奋交感神经末梢,产生NA释放,但不伴有乙酰胆碱释出。说明场刺激用于研究心脏缺血时交感神经兴奋NA释放的变化规律,具有类似于通过电刺激左颈胸交感神经节引起NA释放相同的合理性。
缺血10分钟行电场刺激,NA释放受到抑制(S2/S1=0.31P〈0.01),而无钙灌注后,S2/S1进一步下降为0.15,显示出此时NA释放方式仍是一种钙依赖性的出胞释放[3]。Anthomy等[5,6]通过电刺激左颈胸交感神经节,证实鼠心在缺血早期(〈10分钟)交感神经兴奋并不导致NA大量释出。心肌缺血的某些代谢产物,成为NA释放的抑制因素。随再灌注开始缺血代谢产物逐步冲出,NA释放的抑制也逐步减弱直到完全消失。于再灌注开始同时行S2,S2/S1=0.67;于再灌注后5分钟行S2,S2/S1=1.02。
, 百拇医药
现已明确,NA作为分布在心脏交感神经末梢的传递介质,正常时是一种钙依赖性的出胞释放,并需ATP提供能量,受突触前调节。心脏缺血时,随缺血时间长短不同,NA释放释放有3种不同的机制。对此,Schmig[3]通过动物实验证实,长时间缺血(〉40分钟),由于神经细胞膜已有结构上的破坏,造成大量的NA漏出;10~40分钟缺血,ATP消耗歹尽,NA呈一种不依赖钙的非出胞方式释放,累积在细胞间隙的浓度足以导致心肌细胞坏死。缺血早期(〈10分钟),由于糖酵解仍可提供一定能量,NA的出胞释放赖以继续。但NA释放的突触前调节主要是通过A1一腺苷受体而受到有力抑制,与正常时通过ɑ2一受体不同。大量腺苷来自于ATP的代谢。Richardt等[7]的研究指出这种抑制因素实为一种保护机制。此外,笔者通过对缺血单因素如高K+,低pH,缺氧能分别进行研究,也证实某些缺血单因素对缺血早期的NA释放具有不同程度的抑制作用[8]。
, 百拇医药
此外,由本实验结果可见,缺血早期NA释放的掏因素随再灌注恢复而逐步丧失。因此,抑制交感活性的治疗对防止缺血-再灌注损伤是适宜的。
参考文献
1 Langendorff O. Untersuchungen an überlebenden Sugethierherzen. Arch Ges Phusiol, 1985,61:291.
2 Schmig A, Dart AM, Dietz R, et al. Release of endogenous catecholamines in the ischemic myocardium of the rat. Circulation Research, 1984,55:689.
3 Schmig A. Catechoamines in myocardial ischemia. Cir-culation. 1990,82(suppl Ⅱ):Ⅱ-13-Ⅱ-22.
, http://www.100md.com
4 Nadear RA and de Champlain J. Plasma catecholamines in acute myocardial infarction. Am Heart J, 1979,98:548.
5 Karlsberg RP, Cryer PE, Roberts R. Serial plasma catecholamine response early in the course of clinical acute myocardial infarction. Am Heart J, 1981,102:24.
6 Anthomy M, Dart AM, Schmig A, et al. Relese of endogenous catecholamines in the ischemic mycardium of the rat. Circulation Research, 1984, 55:702.
, http://www.100md.com
7 Richardt G, Waas W, Kranzhfer R, et al. Adenosine inhibites exocytotic release of endogenous noradrenaline in rat heart: A protective mechanism in early myocardial ischemia. Circulation Research, 1987, 61:117.
8 Seyfarth M, Feng Yibai, Richardt G, et al. Speziesahngigkeit der exozytotischen Nordiologie, bei Myokardschmie. Kardiologie, 1992,81:306.
(收稿:1992-10-17 修回:1993-07-19), http://www.100md.com