全反式维甲酸对人髓母细胞体外生长及分化相关因子表达的抑制作用
作者:刘佳 郭丽 罗阳 江岩 刘宁 李俊伟 李宏
单位:110031 沈阳医学院分子生物学研究室
关键词:
中华医学杂志981128 研究证实维甲酸类物质对某些人类恶性肿瘤有促进分化和诱导凋亡的作用,但它对髓母细胞的生物学效应,却少见报道。为此,我们应用全反式维甲酸(RA)处理体外培养的人髓母细胞系Med-3,观察其对细胞生长和形态的影响,并检测了髓母细胞生长促进因子(LIF)的表达和端粒酶的活性。
一、材料和方法
1.人髓母细胞系Mex-3的培养:由日本神户大学神经外科实验室建立和提供[1]。培养在37℃5%CO2和含10%胎牛血清的伊格尔培养基(Eagle′s MEM)液中。
, http://www.100md.com
2.试剂准备和细胞处理:购自美国Sigma公司,用99%背景对照(DMSO)配制成最终浓度为100 mmol/L的RA储备液,实验分成5组,每组设4~6皿:组1.10 μmol/LRA;组2.8 μmol/LRA;组3.5 μmol/LRA;组4.0.1%.DMSO和组5,正常培养。将10~15张灭菌盖玻片放入各皿后,细胞均匀铺皿。每隔24小时从各皿取盖玻片若干,用于各项指标检测,观察持续5天,每项实验至少重复3次。
3.细胞形态学和细胞动力学观察:采用的主要方法是:HE染色,末端脱氧核苷酰转移酶介导生物素标记(BM)的原位DNA片段化分析(TUNEL),反映细胞增殖和DNA合成情况的MTT比色法以及细胞总数和死/活细胞比值测定。
4.(LIF)表达的RNA和免疫组织化学(ICC)分析:从各组的盖玻片上收集细胞:计数后,用于总RNA提取,逆载录酶(RT)中,同时使用人LIF和小鼠β-actin下游PCR引物合成特定ss-cDNA片段;用同RT产物分别做LIF和β-actin的PCR扩增。扩增产物在1.4%琼脂糖凝胶内分离后,做Southern印迹分析[2]。LIF的ICC染色按文献[3]进行。
, http://www.100md.com
5.端粒酶活性的TRAP分析:从各实验组取2×106细胞,用冰预冷的冲洗缓冲液,洗3遍,离心弃上清;加入100 μl冰预冷细胞裂解缓冲液,制备细胞匀浆;置细胞匀浆于冰水中30分钟;4℃,1 6000 r/min20分钟;取上清,测各蛋白样本的浓度;以6 μg/管分装,-75℃保存。TRAP的实验步骤按[3]进行。
二、结果
1.RA对细胞形态和增殖的影响:正常培养的Med-3细胞呈圆形或类圆形,突起少而短;在RA的作用下,细胞多呈梭形,双极或多级且突起变长。细胞计数和MTT测定结果均显示,RA以剂量相关性方式抑制细胞增殖;其特点是在第48~72小时最明显,而后逐渐减弱,5天后基本消失,TUNEL结果表明,正常和各RA处理组的阳性标记细胞均很少见。
2.RA对LIF基因表达的下调作用:用抗人LIF单克隆抗体对5 μmol/L,8 μmol/L和10 μmol/L和RA处理后,第24、48、72、96和120小时的Med-3细胞所做的ICC染色显示,各浓度RA可不同程度地抑制LIF表达;其特点是以第48~72小时最明显。在第96小时,LIF又趋增多。RT-PCR-Southern分析,除证实ICC染色结果外,与正常培养细胞比较,各RA处理组细胞的b-actin表达水平保持相对稳定(图1)。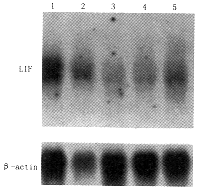
, http://www.100md.com
β-actin用作量性对照:1.正常培养细胞;2~5. 分别是
10μmol RA处理后24、48、72和96小时的Med-3细胞
图1 RT-PCR Southern印记杂交观察RA和Med-3细胞LIF基因表达的影响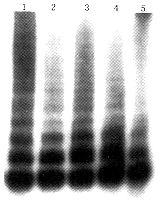
1.正常培养细胞;2.1/2量正常培养细胞;3~5分别是
5μmol/LRA, 8μmol/LRA和10μmol/LRA处理的细胞
图2 不同条件下培养48小时后,Med-3细胞内端酶活性水平的TRAP测定
3.RA使端粒酶活性下降:TRAP分析显示,正常培养组Med-3细胞有较强的端粒酶活性;5 μmol/LRA使细胞内端粒酶活性略有下降;8 μmol/L,则降至正常培养细胞的一增;10 μmol/L时,酶活性明显降低(图2)。为排除DNA污染的可能,先将细胞裂解液在95℃加热处理5分钟,再做TRAP分析,结果未见端粒PCR片段的合成。
, 百拇医药
三、讨论
LIF是髓母细胞瘤的内源性生长因子[2],当用反义寡核苷酸封闭其表达后,髓母细胞Med-3出现明显的生长抑制和形态学改变[4]。但髓母细胞瘤的多向分化特点,使它们缺乏恒定的分化生物标记物,故难以澄清LIF生物学作用的确切机制。为此,本研究我们使用细胞分化诱导剂RA处理体外培养的Med-3细胞,发现,被处理细胞除有生长抑制外,还伴有同阻断LIF表达后相似的形态学改变[4]。说明,这种细胞形态学改变可能和分化有关,与在口腔鳞癌细胞的观察结果相
似[5],RA对Med-3细胞的作用亦有可逆性。表明RA的作用机制可能与调节细胞增殖/分化相关基因的表达有关。
鉴于LIF是迄今发现的唯一髓母细胞瘤内源性生长因子[2,4],故对正常培养和不同浓度RA处理的Med-3细胞内,LIF的表达情况加以分析。结果显示,LIF的表达水平不但与细胞的生长速度正相关,还在有形态改变的Med-3细胞内明显降低。提示RA对LIF表达的下调作用有利于Med-3细胞的再分化。
, 百拇医药
本研究发现,RA以剂量相关性方式,下调靶细胞内端粒酶的活性。由于各组细胞间,β-actin的表达水平无明显差异,且在一定时间范围内未见细胞凋亡之征象,故考虑端粒酶活性降低未必是细胞RNA和蛋白质合成水平整体下降的结果,而是在RA诱导细胞趋于分化过程中,所出现的伴随或同步现象。由于分化程度的提高可增强癌细胞的化疗敏感性[6]而髓母细胞瘤对常规化疗不甚敏感,故本结果提示了改善髓母细胞瘤化疗现状的可能性。
本课题为国家自然科学基金(39670732)和卫生部优秀青年科技人才基金(95-2-50)资助项目
参考文献
1 Kokunai T, Tamaki N, Matsumoto S. Differentiation of a medullablstoma cell line mediated by protein kinase A. In: K. Tabuchi (ed.) Biological Aspects of brain, Tokyo Springer-Verlag, 1991,436-441.
, 百拇医药
2 刘佳,李宏,Moreau JF,等.白血病抑制因子作为内源性生长因子在人脑髓母细胞瘤内的表达.中华病理学杂志,1996,25:24-26.
3 Kim NW, Piatyszek MA, Prowsse KR, et al. Specific association of human telomerase activity with immortal cells and cancer. Science, 1994,266:2011-2015.
4 刘佳,李宏,Hamou MF,等.白血病抑制因子反义寡核苷酸对髓母细胞体外生长的抑制作用.中华病理学杂志,1996,25:132-134.
5 Giannini F, Maestro R, Vukosavljevic T, et al. All-trans, 13-cis and 9-cis retinoic acids induce a fully reversible growth inhibition in HNSCC cell lines: implications for in vivo retinoic acid use. Int J Cancer, 1997,70:194-200.
6 Gunji H, Hass R, Kufe D. Internucleosomal DNA fragmentation during phorbol eater-induced monocytic differentiation and G0/G1 arrest. J Clin Invest, 1992,89:954-960.
(收稿:1998-03-05 修回:1998-07-28), 百拇医药
单位:110031 沈阳医学院分子生物学研究室
关键词:
中华医学杂志981128 研究证实维甲酸类物质对某些人类恶性肿瘤有促进分化和诱导凋亡的作用,但它对髓母细胞的生物学效应,却少见报道。为此,我们应用全反式维甲酸(RA)处理体外培养的人髓母细胞系Med-3,观察其对细胞生长和形态的影响,并检测了髓母细胞生长促进因子(LIF)的表达和端粒酶的活性。
一、材料和方法
1.人髓母细胞系Mex-3的培养:由日本神户大学神经外科实验室建立和提供[1]。培养在37℃5%CO2和含10%胎牛血清的伊格尔培养基(Eagle′s MEM)液中。
, http://www.100md.com
2.试剂准备和细胞处理:购自美国Sigma公司,用99%背景对照(DMSO)配制成最终浓度为100 mmol/L的RA储备液,实验分成5组,每组设4~6皿:组1.10 μmol/LRA;组2.8 μmol/LRA;组3.5 μmol/LRA;组4.0.1%.DMSO和组5,正常培养。将10~15张灭菌盖玻片放入各皿后,细胞均匀铺皿。每隔24小时从各皿取盖玻片若干,用于各项指标检测,观察持续5天,每项实验至少重复3次。
3.细胞形态学和细胞动力学观察:采用的主要方法是:HE染色,末端脱氧核苷酰转移酶介导生物素标记(BM)的原位DNA片段化分析(TUNEL),反映细胞增殖和DNA合成情况的MTT比色法以及细胞总数和死/活细胞比值测定。
4.(LIF)表达的RNA和免疫组织化学(ICC)分析:从各组的盖玻片上收集细胞:计数后,用于总RNA提取,逆载录酶(RT)中,同时使用人LIF和小鼠β-actin下游PCR引物合成特定ss-cDNA片段;用同RT产物分别做LIF和β-actin的PCR扩增。扩增产物在1.4%琼脂糖凝胶内分离后,做Southern印迹分析[2]。LIF的ICC染色按文献[3]进行。
, http://www.100md.com
5.端粒酶活性的TRAP分析:从各实验组取2×106细胞,用冰预冷的冲洗缓冲液,洗3遍,离心弃上清;加入100 μl冰预冷细胞裂解缓冲液,制备细胞匀浆;置细胞匀浆于冰水中30分钟;4℃,1 6000 r/min20分钟;取上清,测各蛋白样本的浓度;以6 μg/管分装,-75℃保存。TRAP的实验步骤按[3]进行。
二、结果
1.RA对细胞形态和增殖的影响:正常培养的Med-3细胞呈圆形或类圆形,突起少而短;在RA的作用下,细胞多呈梭形,双极或多级且突起变长。细胞计数和MTT测定结果均显示,RA以剂量相关性方式抑制细胞增殖;其特点是在第48~72小时最明显,而后逐渐减弱,5天后基本消失,TUNEL结果表明,正常和各RA处理组的阳性标记细胞均很少见。
2.RA对LIF基因表达的下调作用:用抗人LIF单克隆抗体对5 μmol/L,8 μmol/L和10 μmol/L和RA处理后,第24、48、72、96和120小时的Med-3细胞所做的ICC染色显示,各浓度RA可不同程度地抑制LIF表达;其特点是以第48~72小时最明显。在第96小时,LIF又趋增多。RT-PCR-Southern分析,除证实ICC染色结果外,与正常培养细胞比较,各RA处理组细胞的b-actin表达水平保持相对稳定(图1)。

, http://www.100md.com
β-actin用作量性对照:1.正常培养细胞;2~5. 分别是
10μmol RA处理后24、48、72和96小时的Med-3细胞
图1 RT-PCR Southern印记杂交观察RA和Med-3细胞LIF基因表达的影响

1.正常培养细胞;2.1/2量正常培养细胞;3~5分别是
5μmol/LRA, 8μmol/LRA和10μmol/LRA处理的细胞
图2 不同条件下培养48小时后,Med-3细胞内端酶活性水平的TRAP测定
3.RA使端粒酶活性下降:TRAP分析显示,正常培养组Med-3细胞有较强的端粒酶活性;5 μmol/LRA使细胞内端粒酶活性略有下降;8 μmol/L,则降至正常培养细胞的一增;10 μmol/L时,酶活性明显降低(图2)。为排除DNA污染的可能,先将细胞裂解液在95℃加热处理5分钟,再做TRAP分析,结果未见端粒PCR片段的合成。
, 百拇医药
三、讨论
LIF是髓母细胞瘤的内源性生长因子[2],当用反义寡核苷酸封闭其表达后,髓母细胞Med-3出现明显的生长抑制和形态学改变[4]。但髓母细胞瘤的多向分化特点,使它们缺乏恒定的分化生物标记物,故难以澄清LIF生物学作用的确切机制。为此,本研究我们使用细胞分化诱导剂RA处理体外培养的Med-3细胞,发现,被处理细胞除有生长抑制外,还伴有同阻断LIF表达后相似的形态学改变[4]。说明,这种细胞形态学改变可能和分化有关,与在口腔鳞癌细胞的观察结果相
似[5],RA对Med-3细胞的作用亦有可逆性。表明RA的作用机制可能与调节细胞增殖/分化相关基因的表达有关。
鉴于LIF是迄今发现的唯一髓母细胞瘤内源性生长因子[2,4],故对正常培养和不同浓度RA处理的Med-3细胞内,LIF的表达情况加以分析。结果显示,LIF的表达水平不但与细胞的生长速度正相关,还在有形态改变的Med-3细胞内明显降低。提示RA对LIF表达的下调作用有利于Med-3细胞的再分化。
, 百拇医药
本研究发现,RA以剂量相关性方式,下调靶细胞内端粒酶的活性。由于各组细胞间,β-actin的表达水平无明显差异,且在一定时间范围内未见细胞凋亡之征象,故考虑端粒酶活性降低未必是细胞RNA和蛋白质合成水平整体下降的结果,而是在RA诱导细胞趋于分化过程中,所出现的伴随或同步现象。由于分化程度的提高可增强癌细胞的化疗敏感性[6]而髓母细胞瘤对常规化疗不甚敏感,故本结果提示了改善髓母细胞瘤化疗现状的可能性。
本课题为国家自然科学基金(39670732)和卫生部优秀青年科技人才基金(95-2-50)资助项目
参考文献
1 Kokunai T, Tamaki N, Matsumoto S. Differentiation of a medullablstoma cell line mediated by protein kinase A. In: K. Tabuchi (ed.) Biological Aspects of brain, Tokyo Springer-Verlag, 1991,436-441.
, 百拇医药
2 刘佳,李宏,Moreau JF,等.白血病抑制因子作为内源性生长因子在人脑髓母细胞瘤内的表达.中华病理学杂志,1996,25:24-26.
3 Kim NW, Piatyszek MA, Prowsse KR, et al. Specific association of human telomerase activity with immortal cells and cancer. Science, 1994,266:2011-2015.
4 刘佳,李宏,Hamou MF,等.白血病抑制因子反义寡核苷酸对髓母细胞体外生长的抑制作用.中华病理学杂志,1996,25:132-134.
5 Giannini F, Maestro R, Vukosavljevic T, et al. All-trans, 13-cis and 9-cis retinoic acids induce a fully reversible growth inhibition in HNSCC cell lines: implications for in vivo retinoic acid use. Int J Cancer, 1997,70:194-200.
6 Gunji H, Hass R, Kufe D. Internucleosomal DNA fragmentation during phorbol eater-induced monocytic differentiation and G0/G1 arrest. J Clin Invest, 1992,89:954-960.
(收稿:1998-03-05 修回:1998-07-28), 百拇医药