人与大鼠烧伤皮肤及新鲜皮肤提取物的制备及其生物化学研究*
作者:贾晓明 朱兆明 李成文 孔秋华 秦勤 于燕 王亚平
单位:贾晓明 朱兆明 孔秋华 秦勤:解放军304医院烧伤研究所临床部,北京 100037;李成文:解放军军事医学科学院微生物流行病研究所,北京 100071;于燕 王亚平:解放军304医院烧伤研究所基础部
关键词:烧伤皮肤提取物;紫外吸收;凝胶电泳
人与大鼠烧伤皮肤及新鲜皮肤提取物的制备 及其生物化学研究 摘要 目的:改进与研究人与大鼠烧伤皮肤提取物(Human burned skin extracts,hBSE,Rat burned skin extracts,rBSE)制备及其免疫化学分析。方法:对HBSE、HNSE及RBSE与RNSE进行紫外光吸收法蛋白定量及光谱分析;SDS-PAGE蛋白分子量测定;以及小鼠毒性实验。结果:HBSE为 228ku和 138ku的两个毒性蛋白,而HNSE为 148ku和 79ku左右的两条蛋白带,对小鼠不具毒;RBSE为 218ku和 138ku左右的毒性蛋白,而RNSE为 99ku和 79ku左右对小鼠无毒性反应。结论:HBSE与RBSE具有较强的毒性反应,注入小鼠腹腔后,会出现各脏器较严重的病理学改变。
, http://www.100md.com
中国图书资料分类法分类号 R 644
The preparation and biochemical analysis of extracts from burned
andnormal skin of boothhuman andrat
Jia Xiaoming, Zhu Zhaoming, Li Chengwen, Kong Qiuhua, Qin Qin, Yu Yang, Wang Yaping (Burn Institute, 304 thehospital of PLA, Beijing 100853)
Abstract Objective:According to the protocol of Allg wer andhis colleagues, wehave established amodifiedmethod for the preparation of burned andnormal skin extracts of bothhuman andrat.Methods:We performed the SDS-PAGE as well as the ultra-violet chromatographic analysis and total protein quantitation of thenormal and burned skin extracts ofhuman (HNSE andhBSE) andrat (RNSE andrBSE).With the combination ofmice toxic texic tests.Results:Wehave verified thehBSE as a toxic complex of two protein withmolecular weight of 228ku and 138ku.We also verified thehNSE as anon-toxic complex of two proteins withmolecular weight of 148ku and 79ku.TherBSE was proved to be a toxic complex of a 218ku protein and a 138ku protein whereas therNSE was anon-toxic complex of a 99ku protein and a 79ku protein.Conclusion:The burned skin extracts from bothhuman andrat can significantly induce the pathologic changes in certain organs inmice when intra-peritoneally injected.
wer andhis colleagues, wehave established amodifiedmethod for the preparation of burned andnormal skin extracts of bothhuman andrat.Methods:We performed the SDS-PAGE as well as the ultra-violet chromatographic analysis and total protein quantitation of thenormal and burned skin extracts ofhuman (HNSE andhBSE) andrat (RNSE andrBSE).With the combination ofmice toxic texic tests.Results:Wehave verified thehBSE as a toxic complex of two protein withmolecular weight of 228ku and 138ku.We also verified thehNSE as anon-toxic complex of two proteins withmolecular weight of 148ku and 79ku.TherBSE was proved to be a toxic complex of a 218ku protein and a 138ku protein whereas therNSE was anon-toxic complex of a 99ku protein and a 79ku protein.Conclusion:The burned skin extracts from bothhuman andrat can significantly induce the pathologic changes in certain organs inmice when intra-peritoneally injected.
, 百拇医药
Key words burned skin extracts; ultra-violet absorbance;gel electrophoresis
多年来,已有大量的临床观察及动物实验致力于“烧伤皮肤毒素”的研究〔1~6〕,认为确有烧伤后皮肤创面分解出的“毒素”进入血液,形成“烧伤毒血症”。临床中他们也发现,凡早期去除烧伤和创面的痂皮并覆盖创面后,患者全身情况得以好转〔7,8〕,由此推测可能是在细菌入侵前自烧伤部位吸收了某些毒性物质的缘故。本实验旨在对烧伤皮肤提取物的制备及生物毒性实验、免疫化学性质进行系统的研究,为进一步探讨烧伤皮肤提取物抗血清制备及其抗原性质分析提供实验依据。
1 材料和方法
1.1 材料
1.1.1 材料 成年人尸体皮(死后 4h内),260~280g体重Wistar大鼠(处死、剃毛);剥取全层皮肤,分别浸入 1∶1 000新洁尔灭液内 15min,在无菌条件下,用鼓式取皮机修成 0.4mm厚度皮片。分新鲜人皮片组,烧伤人皮片组,新鲜大鼠皮片组及烧伤大鼠皮片组。两组新鲜皮片组立即用剪刀将皮片剪碎,另两组烧伤皮片组置于 100°C水浴锅内 12 s后,将皮片剪碎,分别称重 100mg皮片/ml生理盐水,置于无菌容器内,-80°C保存备用。
, 百拇医药
1.1.2 主要设备 ①YQ-3型电动匀浆机。②日立 557 型双波长、双光束分光光度计。③LKB2130 型多用电泳仪(瑞典)。
1.2 方法 采用本实验室改进的Allg wer等人〔1,9,10〕报告的大鼠皮片烧伤毒素提取物方法,简要步骤如下:
wer等人〔1,9,10〕报告的大鼠皮片烧伤毒素提取物方法,简要步骤如下: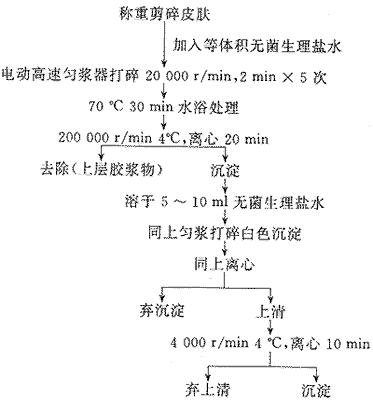
将取沉淀溶于 3~5ml无菌盐水内分装在无菌容器内 -80°C保存备用。
皮肤提取物的蛋白定量及分子量测定:皮肤提取物样品分别用无菌生理盐水作 1∶30 稀释,测出OD280nm及OD260nm的吸收值,计算样品的蛋白浓度、总蛋白量及回收率。四种皮肤提取物的蛋白分子量测定采用SDS(十二烷基硫酸钠)一聚丙烯胺酰酸胺凝胶电脉技术〔11〕。
, 百拇医药
小鼠生物毒性实验:雄性昆明种小鼠体重 15~17g 100 只,分为四组,每组 25 只,每种皮组分为 5 个不同剂量组。腹腔注射提取物,观察注射后动物的反应及 72h内的死亡数,依据寇氏(Karber)法计算出各组注射后的半数致死量(LD50)及LD50的可信限。并将四组小鼠在 72h活杀,或在死后即刻解剖,取心、肺、肝、肾、回肠、脾脏及脑组织,分别进行光镜和电镜病理学检查。
2 结果
2.1 大鼠烧伤后不同时间皮肤提取物的制备分析 结果显示,大鼠烧伤后 1h、3 和 8h 3 个时间点的皮肤提取物与新鲜皮肤相比含量降低,而伤后 12~72h时间点中皮肤提取物含量超过新鲜皮。
采用同一标本室温与 70°C 30min后,大鼠烧伤皮肤 1h、3h、8h、24h、48 和 72h时间点提取物的含量均有显著的提高。经蛋白电泳、光谱定性分析,两种提取方法提取物的化学本质及蛋白质性质没有区别。由于制备过程中操作环节及因素较多,3 批提取物中每种每批含量并不相同。
, 百拇医药
2.2 人与大鼠新鲜、烧伤皮肤提取物的分析
2.2.1 蛋白定量与光谱分析 取相同浓度(1mg/ml)的人与在鼠四种皮提取物匀浆,在 200~500nm的紫外光至蓝紫光光谱扫描中发现,两种新鲜皮均与两种烧伤皮的紫外吸收光谱曲线有显著的不同,其特点均没有典型的蛋白吸收峰,光谱曲线高于两种烧伤皮光谱曲线。人烧伤皮提取物在 258nm处有一个最大吸收峰,说明含苯丙氨酸(257nm最大吸收峰)较多,而烧伤大鼠皮提取物在 276nm处有一最大吸收峰,说明愈靠近 280nm处,其酪氨酸、苯丙氨酸及色氨酸的含量较多。
人皮烧伤与新鲜皮提取物的等电点(PI,柱状等电点聚焦电泳IFE-PAG):人新鲜皮提取物的PI为 11,而人烧伤皮提取物PI=2.0 和 5.2。
2.2.2 四种皮肤提取物的分子量测定(柱状T=7% 的SDS-PAGE不连续系统分离胶)四种皮肤提取物的蛋白分子量,人烧伤提取物为 228ku和 138ku,而人新鲜皮提取物为分子量 148ku和 79ku。大鼠烧伤皮提取物为 218ku和 138ku两条,而大鼠新鲜皮提取物则为 99ku和 79ku。证明烧伤皮肤提取物的蛋白质成份显著不同于新鲜皮的提取物,从上述两种烧伤皮制备出的提取物电泳中均有一条大于 198ku以上的蛋白分子量,与文献中报导关于烧伤毒素的分子量相符〔13,14〕。
, 百拇医药
2.3 四种皮肤提取物的小鼠生物毒性实验结果分析 我们将四种皮肤提取物经过浓缩后,按由小至大的五组不同剂量,依次分别注入小鼠腹腔内,观察注射后 72h内死亡数及其主要脏器的病理改变,根据注射剂量与各组小鼠死亡数计算两种烧伤提取物的LD50及其可信限(附表)。
附表 四组皮肤提取物的LD50观察表
组别(剂量mg/10gBW)
各组LD50及其可信限
(mg/10gBW)
死亡数/例数
1
2
, 百拇医药
3
4
5
新鲜人
皮 组
1.6
0/5
2.52
0/5
3.78
0/5
5.46
0/5
, 百拇医药 6.72
0/5
-
烧伤人
皮 组
1.33
0/5
2.67
0/5
3.99
1/5
5.32
2/5
, http://www.100md.com
6.65
3/5
5.56(4.76~6.51)
新鲜大鼠
皮 组
2.86
0/5
4.29
0/5
5.72
0/5
7.15
0/5
, 百拇医药
8.58
0/5
-
烧伤大鼠
皮 组
1.58
0/5
3.16
0/5
4.74
1/5
6.32
2/5
, 百拇医药
7.90
3/5
6.61(5.65~7.73)
2.4 四种皮肤提取物注射后小鼠体内主要脏器的病理变化 大鼠与人烧伤皮组心肌充血、水肿及小灶性心肌纤维颗粒变性。肺充血及灶状出血,肺泡,Ⅱ型上皮增生伴板层体排空,肺泡毛细血管内皮细胞胞浆水肿,形成较大水肿疱。肝充血,肝细胞浊肿、轻度脂肪变性,肝细胞灶性坏死伴中性白细胞浸润;大部肝细胞胞核异染色质边移,胞浆基质水肿,线粒体肿胀、絮状变性,核糖体减少,滑面内质网层状排列伴扩张。枯否细胞线粒体变性,溶酶体与核糖体减少。肾小管上皮浊肿,髓质明显充血;肾小球毛细血管表面微绒毛样突起明显增多,足细胞轻微水肿。小肠粘膜上皮细胞粒体肿胀空化,核糖体增多,胞核染色质凝集边移。脾窦明显充血,局部白髓脾小体消散,巨噬细胞增生;脾窦内皮细胞水肿,白髓淋巴细胞多呈核质凝集变性及核破碎,呈现细胞调亡现象。脑实质轻度水肿。
, http://www.100md.com
3 讨论
文献报道〔6〕将皮肤烧伤毒素(CBT)与内毒素一同作为体内免疫抑制因素的比较研究发现,两种毒素对免疫抑制作用为 50% 时,大肠杆菌内毒素剂量显著高于CBT的 1000倍,即CBT是远比内毒素更有效应用的免疫抑制剂。作者认为,CBT来自热力引起的皮肤脂蛋白聚合,为烧伤所特有,在治疗严重烧伤时予以重视。
本实验结果也验证了两种烧伤皮肤提取物的理化特性和生物学活性均与新鲜皮肤提取物存在着异同的观点,这也为深入探讨烧伤皮肤毒素的研究,以及烧伤皮肤提取物抗原特性的分析提供了实验数据及奠定了实验基础。
*国家自然科学基金资助项目,批准号39290700-03
参考文献
[1]Allg werm,grafm,hasler P et al.Evidence of possible basic involvement of a cutanoeous burn toxin in the late burn disease/mortality.Bull Clinrev Burn Inj, 1984,1∶27
werm,grafm,hasler P et al.Evidence of possible basic involvement of a cutanoeous burn toxin in the late burn disease/mortality.Bull Clinrev Burn Inj, 1984,1∶27
, 百拇医药
[2]Kremer B, Allg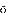 werm,grafm et al.The present status ofresearch in burn toxins, Intensive Caremed, 1981,7∶77
werm,grafm et al.The present status ofresearch in burn toxins, Intensive Caremed, 1981,7∶77
[3]SchoenenbergergA.Burn toxins isolated frommouse andhuman skin.Monogr Allergy,1975,9∶72
[4]Ninneman JA,SteinmD.Suppressin of in vitro lymphocyteresponse by burn boxin isolates from thermally injure skin.Immunol Lett, 1981,2∶339
, 百拇医药
[5]Sparkes BG,mongeg,marshall SL et al.Plasma levels of Cutaneous burn toxin and Lipid peroxides in thermal injury.Burns, 1990,16(2)∶118
[6]Sparkes BG,gyorkos JW,gorczynskirM et al.Comparison of endotoxins and cutaneous burn toxin as immunosuppressants.Burns, 1990,16(2)∶123
[7]DobkemK, Simoni J,ninnemann JL et al.Endotoxemia after burn injury:effect of early excision on circulating endotoxin levels.J Burn Carerehabil, 1989,10(2)∶107
, http://www.100md.com
[8]Guo ZR.Sheng CY, Diao L et al.Extensive wound excision in the acute shock stage in patients withmajor burns.Burns, 1995,21(2)∶139
[9]Allg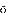 werm,Burri C, cueni F et al.study of burns toxins.Annn Y Acad Sci, 1968,150∶807
werm,Burri C, cueni F et al.study of burns toxins.Annn Y Acad Sci, 1968,150∶807
[10]Allg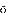 werm, Cueni LB, Stadtler K et al.Burn toxin inmouse skin.J Trauma, 1973,13∶95
werm, Cueni LB, Stadtler K et al.Burn toxin inmouse skin.J Trauma, 1973,13∶95
, 百拇医药
[11]李成文编.电泳技术.现代免疫化学技术.上海:上海科学技术出版社,1992.62~75
[12]章元沛主编,药理学实验.北京:人民卫生出版社,1985.163~165
[13]FedorovnA,movshev BE,nedoshivinarV et al.Immunotherapy as a pathogenetic treatmentmethod in burns.pathophysiol.Exper Ther, 1982,6∶30
[14]SchoenenbergergA, Bauer U, Cueni L et al.Physical, Chemical and biological properties of a specific toxic lipid-Protein complex formed in thermally alteredmouse skin.Biochem Biophys Acta, 1972,263(2)∶140
(1998―10―23收稿,1998―12―02修回), 百拇医药
单位:贾晓明 朱兆明 孔秋华 秦勤:解放军304医院烧伤研究所临床部,北京 100037;李成文:解放军军事医学科学院微生物流行病研究所,北京 100071;于燕 王亚平:解放军304医院烧伤研究所基础部
关键词:烧伤皮肤提取物;紫外吸收;凝胶电泳
人与大鼠烧伤皮肤及新鲜皮肤提取物的制备 及其生物化学研究 摘要 目的:改进与研究人与大鼠烧伤皮肤提取物(Human burned skin extracts,hBSE,Rat burned skin extracts,rBSE)制备及其免疫化学分析。方法:对HBSE、HNSE及RBSE与RNSE进行紫外光吸收法蛋白定量及光谱分析;SDS-PAGE蛋白分子量测定;以及小鼠毒性实验。结果:HBSE为 228ku和 138ku的两个毒性蛋白,而HNSE为 148ku和 79ku左右的两条蛋白带,对小鼠不具毒;RBSE为 218ku和 138ku左右的毒性蛋白,而RNSE为 99ku和 79ku左右对小鼠无毒性反应。结论:HBSE与RBSE具有较强的毒性反应,注入小鼠腹腔后,会出现各脏器较严重的病理学改变。
, http://www.100md.com
中国图书资料分类法分类号 R 644
The preparation and biochemical analysis of extracts from burned
andnormal skin of boothhuman andrat
Jia Xiaoming, Zhu Zhaoming, Li Chengwen, Kong Qiuhua, Qin Qin, Yu Yang, Wang Yaping (Burn Institute, 304 thehospital of PLA, Beijing 100853)
Abstract Objective:According to the protocol of Allg
, 百拇医药
Key words burned skin extracts; ultra-violet absorbance;gel electrophoresis
多年来,已有大量的临床观察及动物实验致力于“烧伤皮肤毒素”的研究〔1~6〕,认为确有烧伤后皮肤创面分解出的“毒素”进入血液,形成“烧伤毒血症”。临床中他们也发现,凡早期去除烧伤和创面的痂皮并覆盖创面后,患者全身情况得以好转〔7,8〕,由此推测可能是在细菌入侵前自烧伤部位吸收了某些毒性物质的缘故。本实验旨在对烧伤皮肤提取物的制备及生物毒性实验、免疫化学性质进行系统的研究,为进一步探讨烧伤皮肤提取物抗血清制备及其抗原性质分析提供实验依据。
1 材料和方法
1.1 材料
1.1.1 材料 成年人尸体皮(死后 4h内),260~280g体重Wistar大鼠(处死、剃毛);剥取全层皮肤,分别浸入 1∶1 000新洁尔灭液内 15min,在无菌条件下,用鼓式取皮机修成 0.4mm厚度皮片。分新鲜人皮片组,烧伤人皮片组,新鲜大鼠皮片组及烧伤大鼠皮片组。两组新鲜皮片组立即用剪刀将皮片剪碎,另两组烧伤皮片组置于 100°C水浴锅内 12 s后,将皮片剪碎,分别称重 100mg皮片/ml生理盐水,置于无菌容器内,-80°C保存备用。
, 百拇医药
1.1.2 主要设备 ①YQ-3型电动匀浆机。②日立 557 型双波长、双光束分光光度计。③LKB2130 型多用电泳仪(瑞典)。
1.2 方法 采用本实验室改进的Allg

将取沉淀溶于 3~5ml无菌盐水内分装在无菌容器内 -80°C保存备用。
皮肤提取物的蛋白定量及分子量测定:皮肤提取物样品分别用无菌生理盐水作 1∶30 稀释,测出OD280nm及OD260nm的吸收值,计算样品的蛋白浓度、总蛋白量及回收率。四种皮肤提取物的蛋白分子量测定采用SDS(十二烷基硫酸钠)一聚丙烯胺酰酸胺凝胶电脉技术〔11〕。
, 百拇医药
小鼠生物毒性实验:雄性昆明种小鼠体重 15~17g 100 只,分为四组,每组 25 只,每种皮组分为 5 个不同剂量组。腹腔注射提取物,观察注射后动物的反应及 72h内的死亡数,依据寇氏(Karber)法计算出各组注射后的半数致死量(LD50)及LD50的可信限。并将四组小鼠在 72h活杀,或在死后即刻解剖,取心、肺、肝、肾、回肠、脾脏及脑组织,分别进行光镜和电镜病理学检查。
2 结果
2.1 大鼠烧伤后不同时间皮肤提取物的制备分析 结果显示,大鼠烧伤后 1h、3 和 8h 3 个时间点的皮肤提取物与新鲜皮肤相比含量降低,而伤后 12~72h时间点中皮肤提取物含量超过新鲜皮。
采用同一标本室温与 70°C 30min后,大鼠烧伤皮肤 1h、3h、8h、24h、48 和 72h时间点提取物的含量均有显著的提高。经蛋白电泳、光谱定性分析,两种提取方法提取物的化学本质及蛋白质性质没有区别。由于制备过程中操作环节及因素较多,3 批提取物中每种每批含量并不相同。
, 百拇医药
2.2 人与大鼠新鲜、烧伤皮肤提取物的分析
2.2.1 蛋白定量与光谱分析 取相同浓度(1mg/ml)的人与在鼠四种皮提取物匀浆,在 200~500nm的紫外光至蓝紫光光谱扫描中发现,两种新鲜皮均与两种烧伤皮的紫外吸收光谱曲线有显著的不同,其特点均没有典型的蛋白吸收峰,光谱曲线高于两种烧伤皮光谱曲线。人烧伤皮提取物在 258nm处有一个最大吸收峰,说明含苯丙氨酸(257nm最大吸收峰)较多,而烧伤大鼠皮提取物在 276nm处有一最大吸收峰,说明愈靠近 280nm处,其酪氨酸、苯丙氨酸及色氨酸的含量较多。
人皮烧伤与新鲜皮提取物的等电点(PI,柱状等电点聚焦电泳IFE-PAG):人新鲜皮提取物的PI为 11,而人烧伤皮提取物PI=2.0 和 5.2。
2.2.2 四种皮肤提取物的分子量测定(柱状T=7% 的SDS-PAGE不连续系统分离胶)四种皮肤提取物的蛋白分子量,人烧伤提取物为 228ku和 138ku,而人新鲜皮提取物为分子量 148ku和 79ku。大鼠烧伤皮提取物为 218ku和 138ku两条,而大鼠新鲜皮提取物则为 99ku和 79ku。证明烧伤皮肤提取物的蛋白质成份显著不同于新鲜皮的提取物,从上述两种烧伤皮制备出的提取物电泳中均有一条大于 198ku以上的蛋白分子量,与文献中报导关于烧伤毒素的分子量相符〔13,14〕。
, 百拇医药
2.3 四种皮肤提取物的小鼠生物毒性实验结果分析 我们将四种皮肤提取物经过浓缩后,按由小至大的五组不同剂量,依次分别注入小鼠腹腔内,观察注射后 72h内死亡数及其主要脏器的病理改变,根据注射剂量与各组小鼠死亡数计算两种烧伤提取物的LD50及其可信限(附表)。
附表 四组皮肤提取物的LD50观察表
组别(剂量mg/10gBW)
各组LD50及其可信限
(mg/10gBW)
死亡数/例数
1
2
, 百拇医药
3
4
5
新鲜人
皮 组
1.6
0/5
2.52
0/5
3.78
0/5
5.46
0/5
, 百拇医药 6.72
0/5
-
烧伤人
皮 组
1.33
0/5
2.67
0/5
3.99
1/5
5.32
2/5
, http://www.100md.com
6.65
3/5
5.56(4.76~6.51)
新鲜大鼠
皮 组
2.86
0/5
4.29
0/5
5.72
0/5
7.15
0/5
, 百拇医药
8.58
0/5
-
烧伤大鼠
皮 组
1.58
0/5
3.16
0/5
4.74
1/5
6.32
2/5
, 百拇医药
7.90
3/5
6.61(5.65~7.73)
2.4 四种皮肤提取物注射后小鼠体内主要脏器的病理变化 大鼠与人烧伤皮组心肌充血、水肿及小灶性心肌纤维颗粒变性。肺充血及灶状出血,肺泡,Ⅱ型上皮增生伴板层体排空,肺泡毛细血管内皮细胞胞浆水肿,形成较大水肿疱。肝充血,肝细胞浊肿、轻度脂肪变性,肝细胞灶性坏死伴中性白细胞浸润;大部肝细胞胞核异染色质边移,胞浆基质水肿,线粒体肿胀、絮状变性,核糖体减少,滑面内质网层状排列伴扩张。枯否细胞线粒体变性,溶酶体与核糖体减少。肾小管上皮浊肿,髓质明显充血;肾小球毛细血管表面微绒毛样突起明显增多,足细胞轻微水肿。小肠粘膜上皮细胞粒体肿胀空化,核糖体增多,胞核染色质凝集边移。脾窦明显充血,局部白髓脾小体消散,巨噬细胞增生;脾窦内皮细胞水肿,白髓淋巴细胞多呈核质凝集变性及核破碎,呈现细胞调亡现象。脑实质轻度水肿。
, http://www.100md.com
3 讨论
文献报道〔6〕将皮肤烧伤毒素(CBT)与内毒素一同作为体内免疫抑制因素的比较研究发现,两种毒素对免疫抑制作用为 50% 时,大肠杆菌内毒素剂量显著高于CBT的 1000倍,即CBT是远比内毒素更有效应用的免疫抑制剂。作者认为,CBT来自热力引起的皮肤脂蛋白聚合,为烧伤所特有,在治疗严重烧伤时予以重视。
本实验结果也验证了两种烧伤皮肤提取物的理化特性和生物学活性均与新鲜皮肤提取物存在着异同的观点,这也为深入探讨烧伤皮肤毒素的研究,以及烧伤皮肤提取物抗原特性的分析提供了实验数据及奠定了实验基础。
*国家自然科学基金资助项目,批准号39290700-03
参考文献
[1]Allg
, 百拇医药
[2]Kremer B, Allg
[3]SchoenenbergergA.Burn toxins isolated frommouse andhuman skin.Monogr Allergy,1975,9∶72
[4]Ninneman JA,SteinmD.Suppressin of in vitro lymphocyteresponse by burn boxin isolates from thermally injure skin.Immunol Lett, 1981,2∶339
, 百拇医药
[5]Sparkes BG,mongeg,marshall SL et al.Plasma levels of Cutaneous burn toxin and Lipid peroxides in thermal injury.Burns, 1990,16(2)∶118
[6]Sparkes BG,gyorkos JW,gorczynskirM et al.Comparison of endotoxins and cutaneous burn toxin as immunosuppressants.Burns, 1990,16(2)∶123
[7]DobkemK, Simoni J,ninnemann JL et al.Endotoxemia after burn injury:effect of early excision on circulating endotoxin levels.J Burn Carerehabil, 1989,10(2)∶107
, http://www.100md.com
[8]Guo ZR.Sheng CY, Diao L et al.Extensive wound excision in the acute shock stage in patients withmajor burns.Burns, 1995,21(2)∶139
[9]Allg
[10]Allg
, 百拇医药
[11]李成文编.电泳技术.现代免疫化学技术.上海:上海科学技术出版社,1992.62~75
[12]章元沛主编,药理学实验.北京:人民卫生出版社,1985.163~165
[13]FedorovnA,movshev BE,nedoshivinarV et al.Immunotherapy as a pathogenetic treatmentmethod in burns.pathophysiol.Exper Ther, 1982,6∶30
[14]SchoenenbergergA, Bauer U, Cueni L et al.Physical, Chemical and biological properties of a specific toxic lipid-Protein complex formed in thermally alteredmouse skin.Biochem Biophys Acta, 1972,263(2)∶140
(1998―10―23收稿,1998―12―02修回), 百拇医药