HBV基因疫苗联合抗原蛋白免疫小鼠的研究*
作者:李文波 姚志强 周永兴 冯志华
单位:第四军医大学唐都医院感染病科 陕西省西安市 710038
关键词:乙型肝炎病毒;基因,病毒;肝炎疫苗,乙型;乙型肝炎表面抗原
世界化人消化杂志990302
中国图书资料分类号 R512.6
摘 要
目的 构建乙肝病毒(HBV)基因疫苗,观察其与HBV表面抗原蛋白(HBsAg)联合免疫小鼠诱导的免疫应答.
方法 构建重组真核表达质粒pCR3.1-S作为HBV基因疫苗,联合应用纯HBsAg蛋白免疫Balb/c小鼠,以单用基因疫苗pCR3.1-S或纯蛋白HBsAg免疫小鼠作为对照组. 采用ELISA法检测免疫小鼠血清抗HBs,另取免疫小鼠脾细胞,用3H-TdR掺入法测定各组免疫小鼠的淋巴细胞增殖活性.
, http://www.100md.com
结果 2,4wk时联合免疫组抗HBs效价低于纯蛋白免疫组,高于基因疫苗免疫组;6wk后基因疫苗免疫组抗HBs效价升至最高,联合免疫组次之. 3H-TdR掺入法测定显示,各组免疫小鼠的淋巴细胞增殖反应差异不显著.
结论 乙肝病毒基因疫苗与表面抗原蛋白联合免疫无优势.
Studies on immunization with HBV
gene vaccine plus HBsAg protein in
mice*
LI Wen-Bo, YAO Zhi-Qiang, ZHOU Yong-Xing and FENG Zhi-Hua
Department of Infectious Diseases, Tangdu Hospital, The Fourth Military Medical University, Xi'an 710038, Shanxi Province, China
, 百拇医药
Subject headings hepatitis B virus; gene, viral; hepatitis B vaccines; HBsAg
Abstract
AIM To investigate the immune responses in mice immunized with gene vaccines of hepatitis B virus (HBV) in combination with hepatitis B surface protein (HBsAg).
METHODS Eukaryotic expression plasmids of pCR3.1-S were constructed as HBV gene vaccines. Balb/c mice were immunized with HBV gene vaccines plus HBsAg protein, and control groups of mice were immunized with HBV gene vaccines or HBsAg protein. Anti-HBs antibodies in vaccinated mice were measured by ELISA, and lymphocyte proliferation activity of immunized mice was detected through 3H-TdR incorporation.
, 百拇医药
RESULTS At the 2nd and 4th week, mice in combination group had lower anti-HBs titer titers than mice in HBsAg protein group and higher anti-HBs titer than mice in gene vaccines group. But at the sixth week, mice in gene vaccines group had the highest anti-HBs titers and mice in combination group had the second highest titers. In addition, it appeared that lymphocyte proliferation activity among each group had no significant differences detected through 3H-TdR incorporation.
, 百拇医药
CONCLUSION Immunization with HBV gene vaccines plus HBsAg protein produces no better immune responses.
0 引言
基因工程重组的乙型肝炎疫苗早在1986年获准广泛使用,为预防、控制HBV的感染和流行发挥了重要作用. 然而,15%~20%的人群对其呈现无应答或应答低下. 研究更有效的乙肝疫苗很有必要. Davis et al[1,2]应用新兴的基因疫苗技术诱导小鼠产生HBV特异的体液和细胞免疫应答. 目前,有关基因疫苗和重组蛋白联合应用对免疫应答影响的研究报道不多. 我们构建了编码HBV S蛋白的重组真核表达质粒pCR3.1-S作为基因疫苗,联合应用纯HBsAg蛋白免疫小鼠,研究HBV基因疫苗和重组蛋白诱导免疫应答单用与联用的异同.
1 材料和方法
, 百拇医药
1.1 重组质粒的构建与细胞表达 重组质粒的构建工作由姚志强教授在比利时鲁汶大学完成. 主要步骤是:以计算机设计PCR引物,从HBV患者血清(adw型)中获得HBV S基因序列;再以T-A克隆法,插入真核表达载体pCR3.1(Invitrogen公司);酶切、电泳鉴定正向插入片段,即得重组质粒pCR3.1-S. 细胞HCC(人肝癌细胞系)为本室保存. Lipofectamine转染试剂购自Gibco公司). 具体转染方法参照lipofectamine产品说明书. 以G418(华美生物工程公司)筛选转染细胞. 不同时间点制作细胞爬片并以40g/L多聚甲醛液固定15min. 应用SABC免疫组织化学染色法检测HBsAg的表达. SABC试剂盒、DAB显色试剂盒及小鼠抗HBsAg抗体购自武汉博士德生物工程有限公司. 具体检测方法依照有关文献及试剂盒说明书进行.
1.2 免疫接种与检测 选用♀ Balb/c小鼠,6wk~8wk龄(本校实验动物中心),随机分组,每组5只. 以5g/L盐酸布比卡因、1g/L对羧基苯甲酸甲酯(生理盐水为溶剂)处理小鼠股四头肌[3]. 24h后,于上述注射部位,多点注射100μg的重组质粒和4μg的纯HBsAg蛋白(北京原平生物技术公司),间隔2wk加强注射,共3次. 同时以100μg重组质粒免疫小鼠、4μg HBsAg蛋白免疫小鼠作为对照. 不同时间间隔剪小鼠尾巴取血. ①抗HBs的检测:采用间接ELISA法. 包被抗原为纯化的HBsAg(包被浓度5mg/L),HRP标记的羊抗鼠IgG为二抗,TMB为底物,结果以P/N>2.1为阳性. ②淋巴细胞增殖的测定:采用3H-TdR掺入法. 取小鼠脾细胞(浓度调至5×109/L),按100μL/孔加入96孔培养板中. 培养4h~6h后,分别加入20mg/L的纯化HBsAg至总体积达200μL/孔. 培养72h后,每孔再加入8.5kBq3H-TdR,继续培养12h~18h,以β液闪计数仪(Beckman公司)计数cpm值. 增殖水平以刺激指数(SI)表示,SI=(实验组cpm值-仪器本底)/(对照组cpm值-仪器本底).
, 百拇医药
2 结果
2.1 转染细胞的免疫组化染色 应用SABC法检测重组质粒pCR3.1-S转染的HCC细胞,发现大部分细胞呈HBsAg染色阳性(图1),而未转染细胞呈阴性.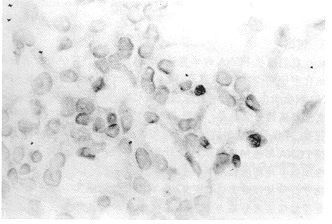
图1 SABC染色法检测转染细胞,大部分细胞呈HBsAg阳性.
2.2 免疫小鼠的抗HBs应答 100μg重组质粒,4μg纯HBsAg蛋白,联合免疫3组小鼠血清抗HBs动力学有差异(图2).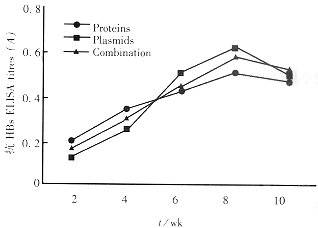
图2 三组免疫小鼠的抗HBs动力学比较
2.3 免疫小鼠淋巴细胞增殖的测定 各组3次免疫接种后约1wk测定免疫小鼠的淋巴细胞增殖活性,结果见图3.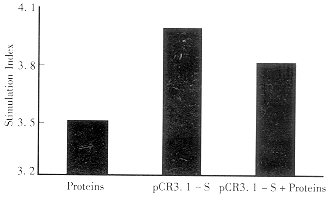
, 百拇医药
图3 三组免疫小鼠的淋巴细胞增殖反应.
3 讨论
我们构建了HBV重组真核表达质粒pCR3.1-S作为基因疫苗,联合应用纯HBsAg蛋白免疫小鼠,与单用基因疫苗pCR3.1-S或纯蛋白HBsAg免疫小鼠组相比较,免疫小鼠的血清抗HBs有差异. 2wk,4wk时联合免疫组抗HBs效价低于纯蛋白免疫组,高于基因免疫组;6wk后基因免疫组抗HBs效价升至最高,联合免疫组次之. 结果提示:①100μg重组质粒pCR3.1-S初次免疫效果差于4μg纯HBsAg蛋白,但加强接种后重组质粒免疫小鼠抗HBs升高较快;②重组质粒pCR3.1-S和纯HBsAg蛋白联合免疫的协同作用不明显,可能相互间有些负效应.
Barnett et al[5]研究发现,若以HIV重组蛋白gP120加强接种HIV-1gP120DNA免疫接种猴子,抗HIV的免疫应答可增强;Letvin et al[4]以HIV-1 env DNA加env蛋白作加强注射也取得了类似效果. 这可能与外源蛋白和基因疫苗分别经不同的途径加工提呈有关. 抗原加工提呈途径分胞质途径(cytosolic pathway)和胞内体途径(endosomal pathway)两条. 基因疫苗等经胞质途径可诱导CD8+T细胞活化、增殖,并激活TH中的TH1亚群;外源蛋白则经胞内体途径,诱导CD4+T细胞活化增殖和抗体的产生. 故基因疫苗和外源蛋白同时或顺序应用,诱导免疫应答可能产生协同作用. 然而,本实验联合应用HBV基因疫苗和重组蛋白免疫小鼠,免疫小鼠的免疫应答无增强. 其原因不清,分析可能有:①Schirmbeck et al[6]学者研究发现,HBV表面蛋白可经胞质途径加工提呈. 基因疫苗和重组蛋白联合应用,其中基因疫苗有可能发挥DNA佐剂效应,调控免疫小鼠产生THⅠ型应答,抗HBs的产生因而不增强. ②重组蛋白诱发免疫应答较早,有可能杀伤基因疫苗进入或附着的细胞,从而使基因疫苗的免疫效应减弱.
, 百拇医药
尽管本实验结果显示,HBV基因疫苗和重组蛋白HBsAg联合免疫无优势,但类似的试验应进一步进行,以为今后疫苗的合理应用奠定一定的基础.
作者简介:
李文波,男,1974-04-15生,山西省洪洞县人,汉族. 1996年第四军医大学本科毕业,1996年第四军医大学硕士研究生,住院医师.
*国家自然科学基金资助项目,No.39770665.
通讯作者 李文波,710038,第四军医大学唐都医院感染病科,陕西省西安市新寺路1号.
*Supported by the National Natural Science Foundation of China, No.39770665.
, http://www.100md.com
Correspondence to:LI Wen-Bo, Department of Infectious Diseases, Tangdu Hospital, The Fourth Military Medical University, 1 Xinsilu, Xi'an 710038, Shanxi Province, China
Tel. +86.29.3510595 Ext. 77595(O)
4 参考文献
[1] Davis HL, Mancini M, Michel ML, Whalen RG. DNA-mediated immunization to hepatitis B surface antigen: longevity of primary response and effect of boost. Vaccine, 1996;14:910-915
, http://www.100md.com
[2] Geissler M, Tokushige K, Chante CC, Zurawski VR, Wands JR. Cellular and humor immune response to hepatitis B virus structure proteins in mice after DNA-based immunization. Gastroenterology, 1997;112:1307-1320
[3] Wang B, Ugen KE, Srikantan V, Agadjanyan MG, Dang K, Refaeli Y. Gene inoculation generates immune responses against human immunodeficiency virus type 1. Proc Natl Acad Sci USA, 1993;90:4156-4160
[4] Letvin NL, Montetiri DL, Yasutomi Y, Perry HC, Davies ME, Leuktis L. Potent protective anti-HIV immune responses generated by bimodal HIV envelope DNA plus protein vaccination. Proc Natl Acad Sci USA, 1997;94:9378-9383
, http://www.100md.com
[5] Barnett SW, Rajasekar S, Legg H, Doe B, Fuller DH, Haynes JR. Vaccination with HIV-1 gp120 DNA induces immune responses that one boosted by a recombinant gp120 protein subunit. Vaccine, 1997;15:869-873
[6] Schirmbeck R, Melber K, Reimann J. Hepatitis B virus small surface antgen particles are processed in a novel endosomal pathway for major histocompatibility complex class Ⅰ-restricted epitope presentation. Eur J Immunol, 1995;25:1063-1070
收稿日期 1998-10-04, 百拇医药
单位:第四军医大学唐都医院感染病科 陕西省西安市 710038
关键词:乙型肝炎病毒;基因,病毒;肝炎疫苗,乙型;乙型肝炎表面抗原
世界化人消化杂志990302
中国图书资料分类号 R512.6
摘 要
目的 构建乙肝病毒(HBV)基因疫苗,观察其与HBV表面抗原蛋白(HBsAg)联合免疫小鼠诱导的免疫应答.
方法 构建重组真核表达质粒pCR3.1-S作为HBV基因疫苗,联合应用纯HBsAg蛋白免疫Balb/c小鼠,以单用基因疫苗pCR3.1-S或纯蛋白HBsAg免疫小鼠作为对照组. 采用ELISA法检测免疫小鼠血清抗HBs,另取免疫小鼠脾细胞,用3H-TdR掺入法测定各组免疫小鼠的淋巴细胞增殖活性.
, http://www.100md.com
结果 2,4wk时联合免疫组抗HBs效价低于纯蛋白免疫组,高于基因疫苗免疫组;6wk后基因疫苗免疫组抗HBs效价升至最高,联合免疫组次之. 3H-TdR掺入法测定显示,各组免疫小鼠的淋巴细胞增殖反应差异不显著.
结论 乙肝病毒基因疫苗与表面抗原蛋白联合免疫无优势.
Studies on immunization with HBV
gene vaccine plus HBsAg protein in
mice*
LI Wen-Bo, YAO Zhi-Qiang, ZHOU Yong-Xing and FENG Zhi-Hua
Department of Infectious Diseases, Tangdu Hospital, The Fourth Military Medical University, Xi'an 710038, Shanxi Province, China
, 百拇医药
Subject headings hepatitis B virus; gene, viral; hepatitis B vaccines; HBsAg
Abstract
AIM To investigate the immune responses in mice immunized with gene vaccines of hepatitis B virus (HBV) in combination with hepatitis B surface protein (HBsAg).
METHODS Eukaryotic expression plasmids of pCR3.1-S were constructed as HBV gene vaccines. Balb/c mice were immunized with HBV gene vaccines plus HBsAg protein, and control groups of mice were immunized with HBV gene vaccines or HBsAg protein. Anti-HBs antibodies in vaccinated mice were measured by ELISA, and lymphocyte proliferation activity of immunized mice was detected through 3H-TdR incorporation.
, 百拇医药
RESULTS At the 2nd and 4th week, mice in combination group had lower anti-HBs titer titers than mice in HBsAg protein group and higher anti-HBs titer than mice in gene vaccines group. But at the sixth week, mice in gene vaccines group had the highest anti-HBs titers and mice in combination group had the second highest titers. In addition, it appeared that lymphocyte proliferation activity among each group had no significant differences detected through 3H-TdR incorporation.
, 百拇医药
CONCLUSION Immunization with HBV gene vaccines plus HBsAg protein produces no better immune responses.
0 引言
基因工程重组的乙型肝炎疫苗早在1986年获准广泛使用,为预防、控制HBV的感染和流行发挥了重要作用. 然而,15%~20%的人群对其呈现无应答或应答低下. 研究更有效的乙肝疫苗很有必要. Davis et al[1,2]应用新兴的基因疫苗技术诱导小鼠产生HBV特异的体液和细胞免疫应答. 目前,有关基因疫苗和重组蛋白联合应用对免疫应答影响的研究报道不多. 我们构建了编码HBV S蛋白的重组真核表达质粒pCR3.1-S作为基因疫苗,联合应用纯HBsAg蛋白免疫小鼠,研究HBV基因疫苗和重组蛋白诱导免疫应答单用与联用的异同.
1 材料和方法
, 百拇医药
1.1 重组质粒的构建与细胞表达 重组质粒的构建工作由姚志强教授在比利时鲁汶大学完成. 主要步骤是:以计算机设计PCR引物,从HBV患者血清(adw型)中获得HBV S基因序列;再以T-A克隆法,插入真核表达载体pCR3.1(Invitrogen公司);酶切、电泳鉴定正向插入片段,即得重组质粒pCR3.1-S. 细胞HCC(人肝癌细胞系)为本室保存. Lipofectamine转染试剂购自Gibco公司). 具体转染方法参照lipofectamine产品说明书. 以G418(华美生物工程公司)筛选转染细胞. 不同时间点制作细胞爬片并以40g/L多聚甲醛液固定15min. 应用SABC免疫组织化学染色法检测HBsAg的表达. SABC试剂盒、DAB显色试剂盒及小鼠抗HBsAg抗体购自武汉博士德生物工程有限公司. 具体检测方法依照有关文献及试剂盒说明书进行.
1.2 免疫接种与检测 选用♀ Balb/c小鼠,6wk~8wk龄(本校实验动物中心),随机分组,每组5只. 以5g/L盐酸布比卡因、1g/L对羧基苯甲酸甲酯(生理盐水为溶剂)处理小鼠股四头肌[3]. 24h后,于上述注射部位,多点注射100μg的重组质粒和4μg的纯HBsAg蛋白(北京原平生物技术公司),间隔2wk加强注射,共3次. 同时以100μg重组质粒免疫小鼠、4μg HBsAg蛋白免疫小鼠作为对照. 不同时间间隔剪小鼠尾巴取血. ①抗HBs的检测:采用间接ELISA法. 包被抗原为纯化的HBsAg(包被浓度5mg/L),HRP标记的羊抗鼠IgG为二抗,TMB为底物,结果以P/N>2.1为阳性. ②淋巴细胞增殖的测定:采用3H-TdR掺入法. 取小鼠脾细胞(浓度调至5×109/L),按100μL/孔加入96孔培养板中. 培养4h~6h后,分别加入20mg/L的纯化HBsAg至总体积达200μL/孔. 培养72h后,每孔再加入8.5kBq3H-TdR,继续培养12h~18h,以β液闪计数仪(Beckman公司)计数cpm值. 增殖水平以刺激指数(SI)表示,SI=(实验组cpm值-仪器本底)/(对照组cpm值-仪器本底).
, 百拇医药
2 结果
2.1 转染细胞的免疫组化染色 应用SABC法检测重组质粒pCR3.1-S转染的HCC细胞,发现大部分细胞呈HBsAg染色阳性(图1),而未转染细胞呈阴性.

图1 SABC染色法检测转染细胞,大部分细胞呈HBsAg阳性.
2.2 免疫小鼠的抗HBs应答 100μg重组质粒,4μg纯HBsAg蛋白,联合免疫3组小鼠血清抗HBs动力学有差异(图2).

图2 三组免疫小鼠的抗HBs动力学比较
2.3 免疫小鼠淋巴细胞增殖的测定 各组3次免疫接种后约1wk测定免疫小鼠的淋巴细胞增殖活性,结果见图3.

, 百拇医药
图3 三组免疫小鼠的淋巴细胞增殖反应.
3 讨论
我们构建了HBV重组真核表达质粒pCR3.1-S作为基因疫苗,联合应用纯HBsAg蛋白免疫小鼠,与单用基因疫苗pCR3.1-S或纯蛋白HBsAg免疫小鼠组相比较,免疫小鼠的血清抗HBs有差异. 2wk,4wk时联合免疫组抗HBs效价低于纯蛋白免疫组,高于基因免疫组;6wk后基因免疫组抗HBs效价升至最高,联合免疫组次之. 结果提示:①100μg重组质粒pCR3.1-S初次免疫效果差于4μg纯HBsAg蛋白,但加强接种后重组质粒免疫小鼠抗HBs升高较快;②重组质粒pCR3.1-S和纯HBsAg蛋白联合免疫的协同作用不明显,可能相互间有些负效应.
Barnett et al[5]研究发现,若以HIV重组蛋白gP120加强接种HIV-1gP120DNA免疫接种猴子,抗HIV的免疫应答可增强;Letvin et al[4]以HIV-1 env DNA加env蛋白作加强注射也取得了类似效果. 这可能与外源蛋白和基因疫苗分别经不同的途径加工提呈有关. 抗原加工提呈途径分胞质途径(cytosolic pathway)和胞内体途径(endosomal pathway)两条. 基因疫苗等经胞质途径可诱导CD8+T细胞活化、增殖,并激活TH中的TH1亚群;外源蛋白则经胞内体途径,诱导CD4+T细胞活化增殖和抗体的产生. 故基因疫苗和外源蛋白同时或顺序应用,诱导免疫应答可能产生协同作用. 然而,本实验联合应用HBV基因疫苗和重组蛋白免疫小鼠,免疫小鼠的免疫应答无增强. 其原因不清,分析可能有:①Schirmbeck et al[6]学者研究发现,HBV表面蛋白可经胞质途径加工提呈. 基因疫苗和重组蛋白联合应用,其中基因疫苗有可能发挥DNA佐剂效应,调控免疫小鼠产生THⅠ型应答,抗HBs的产生因而不增强. ②重组蛋白诱发免疫应答较早,有可能杀伤基因疫苗进入或附着的细胞,从而使基因疫苗的免疫效应减弱.
, 百拇医药
尽管本实验结果显示,HBV基因疫苗和重组蛋白HBsAg联合免疫无优势,但类似的试验应进一步进行,以为今后疫苗的合理应用奠定一定的基础.
作者简介:
李文波,男,1974-04-15生,山西省洪洞县人,汉族. 1996年第四军医大学本科毕业,1996年第四军医大学硕士研究生,住院医师.
*国家自然科学基金资助项目,No.39770665.
通讯作者 李文波,710038,第四军医大学唐都医院感染病科,陕西省西安市新寺路1号.
*Supported by the National Natural Science Foundation of China, No.39770665.
, http://www.100md.com
Correspondence to:LI Wen-Bo, Department of Infectious Diseases, Tangdu Hospital, The Fourth Military Medical University, 1 Xinsilu, Xi'an 710038, Shanxi Province, China
Tel. +86.29.3510595 Ext. 77595(O)
4 参考文献
[1] Davis HL, Mancini M, Michel ML, Whalen RG. DNA-mediated immunization to hepatitis B surface antigen: longevity of primary response and effect of boost. Vaccine, 1996;14:910-915
, http://www.100md.com
[2] Geissler M, Tokushige K, Chante CC, Zurawski VR, Wands JR. Cellular and humor immune response to hepatitis B virus structure proteins in mice after DNA-based immunization. Gastroenterology, 1997;112:1307-1320
[3] Wang B, Ugen KE, Srikantan V, Agadjanyan MG, Dang K, Refaeli Y. Gene inoculation generates immune responses against human immunodeficiency virus type 1. Proc Natl Acad Sci USA, 1993;90:4156-4160
[4] Letvin NL, Montetiri DL, Yasutomi Y, Perry HC, Davies ME, Leuktis L. Potent protective anti-HIV immune responses generated by bimodal HIV envelope DNA plus protein vaccination. Proc Natl Acad Sci USA, 1997;94:9378-9383
, http://www.100md.com
[5] Barnett SW, Rajasekar S, Legg H, Doe B, Fuller DH, Haynes JR. Vaccination with HIV-1 gp120 DNA induces immune responses that one boosted by a recombinant gp120 protein subunit. Vaccine, 1997;15:869-873
[6] Schirmbeck R, Melber K, Reimann J. Hepatitis B virus small surface antgen particles are processed in a novel endosomal pathway for major histocompatibility complex class Ⅰ-restricted epitope presentation. Eur J Immunol, 1995;25:1063-1070
收稿日期 1998-10-04, 百拇医药