聚乳酸和骨生长因子复合植入块修复骨缺损的实验研究
作者:许建辉 孟昭业 杨震 张森林 梁河清
单位:210002 南京军区南京总医院口腔科(许建辉、孟昭业、杨震、张森林);第一军医大学珠江医院口腔科(梁河清)
关键词:重组蛋白质类;成纤维细胞生长因子,碱性;骨基质
中华口腔医学杂志/990313 【摘要】 目的 探讨碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)对重组人骨形成蛋白2(recombinant human bone morphogenetic protein-2,rhBMP-2)诱导骨形成的影响,评价多孔聚乳酸(polylactic acid ,PLA)复合人工骨修复骨缺损的作用。方法 在56例下颌骨缺损的兔模型中分别植入PLA/rhBMP-2/bFGF、PLA/rhBMP-2、 PLA/bFGF、PLA,并设空白对照。植入后2、4、8周行X线摄片和组织学观察骨缺损区骨形成的情况。结果 3种材料复合物较两种材料复合物成骨更好,而后者又较单一的PLA成骨好,所有含骨生长因子的植入组成骨量与对照组比较差异均有显著性(P<0.05)。结论 PLA具有良好的生物相容性和可吸收性,有骨传导性能;bFGF可促进rhBMP-2在骨缺损愈合过程中的骨诱导作用;PLA/rhBMP-2/bFGF复合材料是一种有临床应用前景的骨移植材料。
, http://www.100md.com
Polylactic acid combined with recombinant human bone morphogenetic protein and basic fibroblast growth factor to repair the mandibular defects in rabbits XU Jianhui, MENG Zhaoye, YANG Zhen, et al. Department of Stomatology, Nanjing General Hospital of PLA, Nanjing 210002
【Abstract】 Objective To study the effect of basic fibroblast growth factor(bFGF) on bone formation induced by recombinant human bone morphogenetic protein-2(rhBMP-2) in repair of mandibular defects in rabbits. Methods 56 adult domestic rabbits were classified into five groups. The mandiblar three-wall defects(1.5 cm×0.5 cm ,full thick) were created in right sides. The defects were implanted with various grafts: PLA/rhBMP-2/bFGF, PLA/rhBMP-2, PLA/bFGF, PLA and no implant as control group. At 2, 4 and 8 weeks after operation, the effectivenesses of defect repaire were observed by histological and roentgenographic analysis. Results The composite consisting of three materials stimulated more bone formation than of two materials, and the latter was more than single PLA(at 4 weeks postoperation, P<0.05). All experimental groups,which had one or two growth factors, were significantly higher compared with control group in every stage of postimplantation. Conclusion PLA has good biocompatibility, absorbability and osteoconductibility, rhBMP-2 and bFGF are cooperated in bone healing process, and PLA/rhBMP-2/bFGF is a promising bone substitute in clinical uses.
, 百拇医药
【Key words】 Recombinant proteins Fibroblast growth factor,basic Bone matrix
骨基质中含有多种生长因子,它们通过促进成骨细胞的增殖和分化来调节骨形成过程。脱钙骨基质植入试验表明:一旦骨诱导过程被骨形成蛋白(bone morphogenetic protein, BMP)启动,则其他生长因子均可参与骨诱导的调节[1]。碱性成纤维细胞生长因子(basic fibroblast growth factor, bFGF)是其中的一种,它也参与了骨诱导过程,并对新骨形成产生影响。我们将人工合成、可被生物降解、吸收的多孔聚乳酸(polylactic acid, PLA)与重组人骨形成蛋白2(recombinant human bone morphogenetic protein-2,rhBMP-2)和bFGF组合修复兔大面积骨缺损,以期探讨bFGF对rhBMP-2的诱导骨形成作用,并评价多孔PLA复合人工骨的生物学性能。
, http://www.100md.com
材料与方法
一、材料的制备
1.PLA:广州中山大学高分子研究所提供,平均相对分子质量为48 000,为固体块状。
2.bFGF:广州暨南大学生物工程研究所提供,为 bFGF的PBS液,2.5 g/L。
3.rhBMP-2:军事医学科学院基础医学研究所研制,异位成骨试验示活性良好。
4.PLA植入块的制作:通过注模方式将配制成的10% PLA二氧六环[2]溶液倒入预先用石膏制成的模具内,在-70℃下冻干24小时,4℃风干6小时后取出。成形后为1.5 cm×0.5 cm×0.3 cm的长方体,常温下保存。扫描电镜观察其内部结构(图1),内部微孔直径为150~200 μm,微孔相互串联。
, 百拇医药
图1 扫描电镜观察PLA的内部结构,呈珊瑚状,微孔相互串联,孔率达50%以上,孔径约150~200 μm(×400)
5.PLA/rhBMP-2、PLA/bFGF、PLA/rhBMP-2/bFGF的复合:用电子天秤称取1.5 mg定量的rhBMP-2干冻粉或(和)10 μl浓度为50 mg/L bFGF的PBS液(含bFGF 500 ng),加入阴模内,充分搅匀、干冻、风干,4℃低温保存备用。
6.植入块的消毒:所有植入块在植入术前,用2.5×104 Gy的γ射线照射1小时,杀灭表面可能粘附的病菌[3]。
二、动物模型
健康家兔56只,雌雄不限,体重2.5~3.5 kg,随机分成5组,详见表1。用2%戊巴比妥钠按30~40 mg/kg行耳缘静脉注射麻醉,沿右下颌骨下缘作切口,暴露下颌骨体部,用牙钻作1.5 cm × 0.5cm的三壁全厚缺损,术中切断了下牙槽神经血管束,形成血供不足的较大缺损模型。置入各种植入块,并用钢丝结扎固定。
, 百拇医药
表1 实验动物分组及处理(n=56,只) 组别
植入块
术后时间(周)
2
4
8
A
PLA/rhBMP-2/bFGF
2
5
5
B
PLA/rhBMP-2
, http://www.100md.com
2
5
5
C
PLA/bFGF
2
5
5
D
PLA
2
5
5
对照
, http://www.100md.com
无
2
3
3
注:PLA:多孔聚乳酸;rhBMP-2:重组人骨形成蛋白2;bFGF:碱性成纤维细胞生长因子
三、观察方法
于术后2、4、8周分别处死动物,取兔右侧(手术侧)下颌骨。
1.X线摄片:兔下颌骨平放在胶片盒上,100 mA X线机垂直照射,48 kV条件下0.02 s,预实验X线片反应兔下颌骨结构清晰,对比度良好,PLA材料为非阻射。通过3人盲法估计骨形成和塑形,标准采用5分制[4]:0:缺损区无新骨;1:1%~25% 被新骨充填;2:26%~50% 被新骨充填;3:51%~75% 被新骨充填;4:76%~100% 被新骨充填。
, http://www.100md.com
2.组织学检查:甲酸、硝酸脱钙、脱水、石蜡包埋,制成5 μm 厚的切片,HE 染色,光镜下观察新生骨的形成、PLA的吸收情况以及缺损区内的组织及细胞构成。
结果
一、X线片检查
各组动物缺损区均有不同程度的成骨反应,其中A组最明显,达75%以上(图2)。图3描述了各种植入组的骨形成,A组与D组、对照组相比差异均有显著性;而B、C2组仅和对照组间差异有显著性,此2组与D组相比成骨量较高(4周,P<0.05),但在第8周它们之间差异无显著性。A、B、C 3组之间两两比较差异无显著性。
图2 术后8周,PLA/rhBMP-2/bFGF植入组新骨形成占缺损区
, http://www.100md.com 面积的75%以上,见小梁结构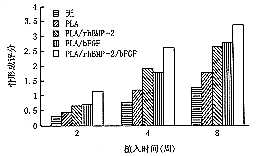
PLA:多孔聚乳酸; rhBMP-2:重组人骨形成蛋白2; bFGF:碱性成纤维细胞生长因子
图3 植入组及对照组在2、4、8周的骨形成评分
二、组织学观察
术后2周,各组骨缺损边缘均有少量新生骨痂覆盖。A组和B组,伴随着新生骨痂有大量成纤维细胞、成骨母细胞和成骨细胞增殖,与植床紧密接触的修复块部分开始降解,少量纤维结缔组织和骨髓来源的细胞组织进入表面的微孔内,部分骨样小岛在植入块周缘形成(图4)。C组可见大量的梭形细胞和肥大的间充质细胞增殖,成骨细胞和成纤维样细胞的数量较多,许多血管向缺损区方向长入,植入块内偶见一些成骨样组织。
, http://www.100md.com
图4 术后2周,PLA/rhBMP-2/bFGF和PLA/rhBMP-2组植入块周缘见骨样小岛(HE 3.3×20)
术后4周,A、B、C 3组缺损区均可见散在的类骨组织和新骨形成,成骨细胞数量较多,一些纤维组织长入缺损区,此3组组织类型已无明显差别,大量编织骨形成,亦见少量板层结构和髓腔形成(图5),PLA大片降解吸收,微孔增大形成空隙,结构显现不规则的松散状态,见一些吞噬细胞和多核巨细胞以及少许的白细胞浸润,部分PLA残片被新生骨包围,成骨活跃。在A、B两组的部分标本中可在新生骨痂周围见软骨细胞增生、肥大、软骨形成及软骨内化骨这一过程(图6)。D组,骨缺损边缘的新生骨组织通过PLA裂解形成的间隙侵入植入块内,同时较多的纤维结缔组织也长入缺损区,编织骨形成缓慢,成骨细胞数量较少。对照组呈现部分纤维性成骨,纤维组织继续增生,较多瘢痕组织形成。
图5 术后4周,PLA/rhBMP-2/bFGF组见大量编织骨、部分板层结构和骨髓,PLA大片降解吸收,结构松散(HE 3.3×10)
, 百拇医药
图6 术后4周,rhBMP-2组可见软骨内骨化形成(HE 3.3×10)
术后8周,A、B、C 3组缺损区50% 以上被新生骨占据,虽然编织骨成份占大多数,但板层骨数量有所增加,髓腔亦增大,新生骨周围可见破骨细胞存在。同时,一定量的纤维组织及纤维性骨痂形成,PLA结构大部分破裂被新骨充填,部分新骨组织50% 以上被新生骨融合成蜿蜒迂曲的骨小梁,板层结构及哈佛系统明显(图7)。D组,成骨亦活跃,但PLA吸收并被新骨替代较前3组少。对照组仍为缺损边缘少量新生骨痂新生覆盖和纤维组织的形成,缺损区大部分被瘢痕组织充填,部分标本见肌肉组织长入缺损区。
图7 术后8周,PLA/rhBMP-2/bFGF植入组显示骨改建和塑形,板层结构和哈佛系统明显,可见梁状结构(HE 3.3×20)
讨论
, 百拇医药
现已从骨基质、骨器官及骨系细胞培养液中分离了多种骨生长因子,包括BMP、β-转化生长因子(TGF-β)、骨骼生长因子或胰岛素样生长因子(IGFs)、FGFs和血小板衍生性生长因子(PDGF)等。在众多生长因子中,BMP被证明是正常胚胎时期骨、牙组织和成年骨修复中最主要的诱导分化因子,但其他生长因子都对BMP的骨诱导过程产生影响[5]。本实验使用PLA/rhBMP-2/bFGF复合植入块对兔下颌骨缺损进行修复,术后4周、8周,PLA/rhBMP-2/bFGF组的新骨形成高于PLA/rhBMP-2和PLA/bFGF 2组,统计学上组间差异无显著性,作者认为这是由于样本含量较小所致。但PLA/rhBMP-2/bFGF与单独PLA组相比差异有显著性,PLA/rhBMP-2和PLA/bFGF与PLA组比较,仅在4周差异有显著性,表明bFGF对rhBMP-2诱导骨形成的影响。
体外实验发现,bFGF能促进软骨细胞前质的分化及软骨细胞的增殖和成熟[6]。而在体内,Aspenberg和Lohmander[7]在DBM中加入外源性的bFGF可增加诱导成骨的数量;此外,它是一种毛细血管增殖刺激剂,能促进毛细血管向断端及骨移植物中长入,使骨修复早期的组织中软骨岛数量增多并使断端骨痂和骨移植物提前血管重建时限[8]。bFGF不仅有利于多种细胞包括软骨细胞的增殖和分化作用,而且有明显的血管形成作用。在BMP诱导新骨形成过程中,血管大量形成、长入,随之带来大量的血管内皮细胞和管外周细胞(未分化间充质细胞),从而为BMP提供了大量的靶细胞,使骨量增多。本实验结果显示,含有bFGF的复合植入材料置入缺损区后,bFGF加速了新骨形成的过程,作用于骨诱导成骨的早期阶段(至4周),未分化间充质细胞、成纤维细胞、骨髓来源的基质细胞、成骨细胞以及毛细血管侵入数量的明显增多(与PLA组相比)。由于BMP主要起形态原(morphogeny)的作用,它是一种微弱丝裂原,而bFGF是一种较强的丝裂原,通过二者的协同作用,将加速骨诱导的进程。PLA/rhBMP-2/bFGF组在X线片和组织学观察方面均表明新骨形成活跃,成骨量较多。
, http://www.100md.com
PLA具有骨传导性,实验已显示其有良好的生物相容性和可吸收性,没有严重的急性和亚急性组织反应及清理反应[9]。本研究中各实验组通过组织学观察,术后2周仅有一层微薄的结缔组织膜包绕,术后4周见少量的巨噬细胞和多核巨细胞浸润,但随着纤维结缔组织和新骨的形成并侵入到PLA内,这些轻微的异物反应随着植入物的降解和新骨组织的逐渐融合而消失,并不影响骨缺损的修复进程。术后8周,PLA/rhBMP-2/bFGF 组缺损区新骨形成达75%以上,PLA组的成骨量亦明显高于对照组。
PLA/rhBMP-2/bFGF复合材料将骨传导性与诱导性结合起来,较大限度地促进了新骨的形成。结果表明:多孔状PLA具有较好的生物相容性和骨传导性。微孔孔径在150~200 μm(内部),与人体骨组织的微孔道结构相似,起到类似松质骨的支架作用,术后8周,PLA仅有小部分残留,无炎症反应。rhBMP-2和bFGF共同作用于骨诱导过程,成骨量明显增加,出现大量松质骨,部分已出现板层骨及骨髓并可见骨改建和塑形组织群。PLA/rhBMP-2/bFGF复合材料是一种有应用前景的骨移植替代品。
, 百拇医药
参考文献
[1] Urist MR, Delange RJ, Finerman GA. Bone cell differentiation and growth factors. Science,1983,220:680-686.
[2] Miki T, Harada K, Imai Y, et al. Effect of freeze-dried poly-L-lactic acid discs mixed with bone morphogenetic protein on the healing of rat skull defects. J Oral Maxillofac Surg,1994, 52:387-391.
[3] Ijiri S, Yamamuro T, Nakamura T, et al. Effect of sterilization on bone morphogenetic protein. J Orthop Res, 1994, 12: 628-636.
, 百拇医药
[4] Bostrom M, Lane JM, Tomin E, et al. Use of bone morphogenetic protein-2 in the rabbit ulnar nonunion model.Clin Orthop,1996,327: 272-282.
[5] 胡蕴玉. 骨生长因子与骨愈合的研究和展望. 中华骨科杂志, 1996,16:39.
[6] Cuevas P, Burgos J, Baird A. Basic fibroblast growth factor(FGF) promotes cartilage repair in vivo. Biochem Biophys Res Commun,1988,156:611-618.
[7] Aspenberg P, Lohmander LS. Fibroblast growth factor stimulates bone formation. Bone induction studied in rats. Acta Orthop Scand,1989,60: 473-476.
, 百拇医药
[8] Eppley BL, Doucet M, Connolly DT,et al.Enhancement of angiogenesis by bFGF in mandibular bone graft healing in the rabbit. J Oral Maxillofac Surg,1988,46:391-398.
[9] Miyamoto S, Takaoka K, Okada T, et al. Evaluation of polylactic acid homopolymers as carriers for bone morphogenetic protein. Clin Orthop,1992,(278):274-285.
(收稿:1998-07-28 修回:1999-02-24), http://www.100md.com
单位:210002 南京军区南京总医院口腔科(许建辉、孟昭业、杨震、张森林);第一军医大学珠江医院口腔科(梁河清)
关键词:重组蛋白质类;成纤维细胞生长因子,碱性;骨基质
中华口腔医学杂志/990313 【摘要】 目的 探讨碱性成纤维细胞生长因子(basic fibroblast growth factor,bFGF)对重组人骨形成蛋白2(recombinant human bone morphogenetic protein-2,rhBMP-2)诱导骨形成的影响,评价多孔聚乳酸(polylactic acid ,PLA)复合人工骨修复骨缺损的作用。方法 在56例下颌骨缺损的兔模型中分别植入PLA/rhBMP-2/bFGF、PLA/rhBMP-2、 PLA/bFGF、PLA,并设空白对照。植入后2、4、8周行X线摄片和组织学观察骨缺损区骨形成的情况。结果 3种材料复合物较两种材料复合物成骨更好,而后者又较单一的PLA成骨好,所有含骨生长因子的植入组成骨量与对照组比较差异均有显著性(P<0.05)。结论 PLA具有良好的生物相容性和可吸收性,有骨传导性能;bFGF可促进rhBMP-2在骨缺损愈合过程中的骨诱导作用;PLA/rhBMP-2/bFGF复合材料是一种有临床应用前景的骨移植材料。
, http://www.100md.com
Polylactic acid combined with recombinant human bone morphogenetic protein and basic fibroblast growth factor to repair the mandibular defects in rabbits XU Jianhui, MENG Zhaoye, YANG Zhen, et al. Department of Stomatology, Nanjing General Hospital of PLA, Nanjing 210002
【Abstract】 Objective To study the effect of basic fibroblast growth factor(bFGF) on bone formation induced by recombinant human bone morphogenetic protein-2(rhBMP-2) in repair of mandibular defects in rabbits. Methods 56 adult domestic rabbits were classified into five groups. The mandiblar three-wall defects(1.5 cm×0.5 cm ,full thick) were created in right sides. The defects were implanted with various grafts: PLA/rhBMP-2/bFGF, PLA/rhBMP-2, PLA/bFGF, PLA and no implant as control group. At 2, 4 and 8 weeks after operation, the effectivenesses of defect repaire were observed by histological and roentgenographic analysis. Results The composite consisting of three materials stimulated more bone formation than of two materials, and the latter was more than single PLA(at 4 weeks postoperation, P<0.05). All experimental groups,which had one or two growth factors, were significantly higher compared with control group in every stage of postimplantation. Conclusion PLA has good biocompatibility, absorbability and osteoconductibility, rhBMP-2 and bFGF are cooperated in bone healing process, and PLA/rhBMP-2/bFGF is a promising bone substitute in clinical uses.
, 百拇医药
【Key words】 Recombinant proteins Fibroblast growth factor,basic Bone matrix
骨基质中含有多种生长因子,它们通过促进成骨细胞的增殖和分化来调节骨形成过程。脱钙骨基质植入试验表明:一旦骨诱导过程被骨形成蛋白(bone morphogenetic protein, BMP)启动,则其他生长因子均可参与骨诱导的调节[1]。碱性成纤维细胞生长因子(basic fibroblast growth factor, bFGF)是其中的一种,它也参与了骨诱导过程,并对新骨形成产生影响。我们将人工合成、可被生物降解、吸收的多孔聚乳酸(polylactic acid, PLA)与重组人骨形成蛋白2(recombinant human bone morphogenetic protein-2,rhBMP-2)和bFGF组合修复兔大面积骨缺损,以期探讨bFGF对rhBMP-2的诱导骨形成作用,并评价多孔PLA复合人工骨的生物学性能。
, http://www.100md.com
材料与方法
一、材料的制备
1.PLA:广州中山大学高分子研究所提供,平均相对分子质量为48 000,为固体块状。
2.bFGF:广州暨南大学生物工程研究所提供,为 bFGF的PBS液,2.5 g/L。
3.rhBMP-2:军事医学科学院基础医学研究所研制,异位成骨试验示活性良好。
4.PLA植入块的制作:通过注模方式将配制成的10% PLA二氧六环[2]溶液倒入预先用石膏制成的模具内,在-70℃下冻干24小时,4℃风干6小时后取出。成形后为1.5 cm×0.5 cm×0.3 cm的长方体,常温下保存。扫描电镜观察其内部结构(图1),内部微孔直径为150~200 μm,微孔相互串联。

, 百拇医药
图1 扫描电镜观察PLA的内部结构,呈珊瑚状,微孔相互串联,孔率达50%以上,孔径约150~200 μm(×400)
5.PLA/rhBMP-2、PLA/bFGF、PLA/rhBMP-2/bFGF的复合:用电子天秤称取1.5 mg定量的rhBMP-2干冻粉或(和)10 μl浓度为50 mg/L bFGF的PBS液(含bFGF 500 ng),加入阴模内,充分搅匀、干冻、风干,4℃低温保存备用。
6.植入块的消毒:所有植入块在植入术前,用2.5×104 Gy的γ射线照射1小时,杀灭表面可能粘附的病菌[3]。
二、动物模型
健康家兔56只,雌雄不限,体重2.5~3.5 kg,随机分成5组,详见表1。用2%戊巴比妥钠按30~40 mg/kg行耳缘静脉注射麻醉,沿右下颌骨下缘作切口,暴露下颌骨体部,用牙钻作1.5 cm × 0.5cm的三壁全厚缺损,术中切断了下牙槽神经血管束,形成血供不足的较大缺损模型。置入各种植入块,并用钢丝结扎固定。
, 百拇医药
表1 实验动物分组及处理(n=56,只) 组别
植入块
术后时间(周)
2
4
8
A
PLA/rhBMP-2/bFGF
2
5
5
B
PLA/rhBMP-2
, http://www.100md.com
2
5
5
C
PLA/bFGF
2
5
5
D
PLA
2
5
5
对照
, http://www.100md.com
无
2
3
3
注:PLA:多孔聚乳酸;rhBMP-2:重组人骨形成蛋白2;bFGF:碱性成纤维细胞生长因子
三、观察方法
于术后2、4、8周分别处死动物,取兔右侧(手术侧)下颌骨。
1.X线摄片:兔下颌骨平放在胶片盒上,100 mA X线机垂直照射,48 kV条件下0.02 s,预实验X线片反应兔下颌骨结构清晰,对比度良好,PLA材料为非阻射。通过3人盲法估计骨形成和塑形,标准采用5分制[4]:0:缺损区无新骨;1:1%~25% 被新骨充填;2:26%~50% 被新骨充填;3:51%~75% 被新骨充填;4:76%~100% 被新骨充填。
, http://www.100md.com
2.组织学检查:甲酸、硝酸脱钙、脱水、石蜡包埋,制成5 μm 厚的切片,HE 染色,光镜下观察新生骨的形成、PLA的吸收情况以及缺损区内的组织及细胞构成。
结果
一、X线片检查
各组动物缺损区均有不同程度的成骨反应,其中A组最明显,达75%以上(图2)。图3描述了各种植入组的骨形成,A组与D组、对照组相比差异均有显著性;而B、C2组仅和对照组间差异有显著性,此2组与D组相比成骨量较高(4周,P<0.05),但在第8周它们之间差异无显著性。A、B、C 3组之间两两比较差异无显著性。

图2 术后8周,PLA/rhBMP-2/bFGF植入组新骨形成占缺损区
, http://www.100md.com 面积的75%以上,见小梁结构

PLA:多孔聚乳酸; rhBMP-2:重组人骨形成蛋白2; bFGF:碱性成纤维细胞生长因子
图3 植入组及对照组在2、4、8周的骨形成评分
二、组织学观察
术后2周,各组骨缺损边缘均有少量新生骨痂覆盖。A组和B组,伴随着新生骨痂有大量成纤维细胞、成骨母细胞和成骨细胞增殖,与植床紧密接触的修复块部分开始降解,少量纤维结缔组织和骨髓来源的细胞组织进入表面的微孔内,部分骨样小岛在植入块周缘形成(图4)。C组可见大量的梭形细胞和肥大的间充质细胞增殖,成骨细胞和成纤维样细胞的数量较多,许多血管向缺损区方向长入,植入块内偶见一些成骨样组织。

, http://www.100md.com
图4 术后2周,PLA/rhBMP-2/bFGF和PLA/rhBMP-2组植入块周缘见骨样小岛(HE 3.3×20)
术后4周,A、B、C 3组缺损区均可见散在的类骨组织和新骨形成,成骨细胞数量较多,一些纤维组织长入缺损区,此3组组织类型已无明显差别,大量编织骨形成,亦见少量板层结构和髓腔形成(图5),PLA大片降解吸收,微孔增大形成空隙,结构显现不规则的松散状态,见一些吞噬细胞和多核巨细胞以及少许的白细胞浸润,部分PLA残片被新生骨包围,成骨活跃。在A、B两组的部分标本中可在新生骨痂周围见软骨细胞增生、肥大、软骨形成及软骨内化骨这一过程(图6)。D组,骨缺损边缘的新生骨组织通过PLA裂解形成的间隙侵入植入块内,同时较多的纤维结缔组织也长入缺损区,编织骨形成缓慢,成骨细胞数量较少。对照组呈现部分纤维性成骨,纤维组织继续增生,较多瘢痕组织形成。

图5 术后4周,PLA/rhBMP-2/bFGF组见大量编织骨、部分板层结构和骨髓,PLA大片降解吸收,结构松散(HE 3.3×10)

, 百拇医药
图6 术后4周,rhBMP-2组可见软骨内骨化形成(HE 3.3×10)
术后8周,A、B、C 3组缺损区50% 以上被新生骨占据,虽然编织骨成份占大多数,但板层骨数量有所增加,髓腔亦增大,新生骨周围可见破骨细胞存在。同时,一定量的纤维组织及纤维性骨痂形成,PLA结构大部分破裂被新骨充填,部分新骨组织50% 以上被新生骨融合成蜿蜒迂曲的骨小梁,板层结构及哈佛系统明显(图7)。D组,成骨亦活跃,但PLA吸收并被新骨替代较前3组少。对照组仍为缺损边缘少量新生骨痂新生覆盖和纤维组织的形成,缺损区大部分被瘢痕组织充填,部分标本见肌肉组织长入缺损区。

图7 术后8周,PLA/rhBMP-2/bFGF植入组显示骨改建和塑形,板层结构和哈佛系统明显,可见梁状结构(HE 3.3×20)
讨论
, 百拇医药
现已从骨基质、骨器官及骨系细胞培养液中分离了多种骨生长因子,包括BMP、β-转化生长因子(TGF-β)、骨骼生长因子或胰岛素样生长因子(IGFs)、FGFs和血小板衍生性生长因子(PDGF)等。在众多生长因子中,BMP被证明是正常胚胎时期骨、牙组织和成年骨修复中最主要的诱导分化因子,但其他生长因子都对BMP的骨诱导过程产生影响[5]。本实验使用PLA/rhBMP-2/bFGF复合植入块对兔下颌骨缺损进行修复,术后4周、8周,PLA/rhBMP-2/bFGF组的新骨形成高于PLA/rhBMP-2和PLA/bFGF 2组,统计学上组间差异无显著性,作者认为这是由于样本含量较小所致。但PLA/rhBMP-2/bFGF与单独PLA组相比差异有显著性,PLA/rhBMP-2和PLA/bFGF与PLA组比较,仅在4周差异有显著性,表明bFGF对rhBMP-2诱导骨形成的影响。
体外实验发现,bFGF能促进软骨细胞前质的分化及软骨细胞的增殖和成熟[6]。而在体内,Aspenberg和Lohmander[7]在DBM中加入外源性的bFGF可增加诱导成骨的数量;此外,它是一种毛细血管增殖刺激剂,能促进毛细血管向断端及骨移植物中长入,使骨修复早期的组织中软骨岛数量增多并使断端骨痂和骨移植物提前血管重建时限[8]。bFGF不仅有利于多种细胞包括软骨细胞的增殖和分化作用,而且有明显的血管形成作用。在BMP诱导新骨形成过程中,血管大量形成、长入,随之带来大量的血管内皮细胞和管外周细胞(未分化间充质细胞),从而为BMP提供了大量的靶细胞,使骨量增多。本实验结果显示,含有bFGF的复合植入材料置入缺损区后,bFGF加速了新骨形成的过程,作用于骨诱导成骨的早期阶段(至4周),未分化间充质细胞、成纤维细胞、骨髓来源的基质细胞、成骨细胞以及毛细血管侵入数量的明显增多(与PLA组相比)。由于BMP主要起形态原(morphogeny)的作用,它是一种微弱丝裂原,而bFGF是一种较强的丝裂原,通过二者的协同作用,将加速骨诱导的进程。PLA/rhBMP-2/bFGF组在X线片和组织学观察方面均表明新骨形成活跃,成骨量较多。
, http://www.100md.com
PLA具有骨传导性,实验已显示其有良好的生物相容性和可吸收性,没有严重的急性和亚急性组织反应及清理反应[9]。本研究中各实验组通过组织学观察,术后2周仅有一层微薄的结缔组织膜包绕,术后4周见少量的巨噬细胞和多核巨细胞浸润,但随着纤维结缔组织和新骨的形成并侵入到PLA内,这些轻微的异物反应随着植入物的降解和新骨组织的逐渐融合而消失,并不影响骨缺损的修复进程。术后8周,PLA/rhBMP-2/bFGF 组缺损区新骨形成达75%以上,PLA组的成骨量亦明显高于对照组。
PLA/rhBMP-2/bFGF复合材料将骨传导性与诱导性结合起来,较大限度地促进了新骨的形成。结果表明:多孔状PLA具有较好的生物相容性和骨传导性。微孔孔径在150~200 μm(内部),与人体骨组织的微孔道结构相似,起到类似松质骨的支架作用,术后8周,PLA仅有小部分残留,无炎症反应。rhBMP-2和bFGF共同作用于骨诱导过程,成骨量明显增加,出现大量松质骨,部分已出现板层骨及骨髓并可见骨改建和塑形组织群。PLA/rhBMP-2/bFGF复合材料是一种有应用前景的骨移植替代品。
, 百拇医药
参考文献
[1] Urist MR, Delange RJ, Finerman GA. Bone cell differentiation and growth factors. Science,1983,220:680-686.
[2] Miki T, Harada K, Imai Y, et al. Effect of freeze-dried poly-L-lactic acid discs mixed with bone morphogenetic protein on the healing of rat skull defects. J Oral Maxillofac Surg,1994, 52:387-391.
[3] Ijiri S, Yamamuro T, Nakamura T, et al. Effect of sterilization on bone morphogenetic protein. J Orthop Res, 1994, 12: 628-636.
, 百拇医药
[4] Bostrom M, Lane JM, Tomin E, et al. Use of bone morphogenetic protein-2 in the rabbit ulnar nonunion model.Clin Orthop,1996,327: 272-282.
[5] 胡蕴玉. 骨生长因子与骨愈合的研究和展望. 中华骨科杂志, 1996,16:39.
[6] Cuevas P, Burgos J, Baird A. Basic fibroblast growth factor(FGF) promotes cartilage repair in vivo. Biochem Biophys Res Commun,1988,156:611-618.
[7] Aspenberg P, Lohmander LS. Fibroblast growth factor stimulates bone formation. Bone induction studied in rats. Acta Orthop Scand,1989,60: 473-476.
, 百拇医药
[8] Eppley BL, Doucet M, Connolly DT,et al.Enhancement of angiogenesis by bFGF in mandibular bone graft healing in the rabbit. J Oral Maxillofac Surg,1988,46:391-398.
[9] Miyamoto S, Takaoka K, Okada T, et al. Evaluation of polylactic acid homopolymers as carriers for bone morphogenetic protein. Clin Orthop,1992,(278):274-285.
(收稿:1998-07-28 修回:1999-02-24), http://www.100md.com