增殖细胞核抗原在星形细胞瘤中的表达及与病理分级关系
作者:王 勇 王桂松 罗其中
单位:上海第二医科大学附属仁济医院神经外科(上海200001)
关键词:脑肿瘤;增殖细胞核抗原
肿瘤990311 星形细胞瘤作为颅内原发性恶性肿瘤,现代诊治技术尚未能对其治疗取得突破性进展,绝大多数病人预后险恶。肿瘤组织病理学分级虽与其生物学行为有一定关系,但由于较多因素的影响,不能准确、客观反映肿瘤细胞的增殖程度以及病人的预后。近十年来,各种细胞动力学研究已用于脑肿瘤的增殖研究,尤其是免疫组织化学技术的日趋成熟,用这种方法研究脑肿瘤细胞增殖,具有可保留细胞和组织结构的完整,方法易行,获得结果快,可用于石蜡切片等优点,因而临床研究者乐于采用。
本研究采用ABC免疫组化方法,对我院手术切除的颅内幕上星形细胞瘤石蜡包埋标本的PCNA检测,结合临床资料进行回顾性研究,以探讨PCNA表达与组织病理分级及术后生存的关系。
, 百拇医药
材料与方法
一、病例选择
1993年1月~1995年12月,上海第二医科大学附属仁济医院神经外科共手术切除颅内幕上星形细胞瘤79例,其中38例因下列原因未进入本研究:(1)临床资料不完整;(2)术后1月内死亡;(3)因肿瘤复发而再次手术;(4)初访即失访。其余41例临床资料完整并获随访,随访截止期为1996年12月31日,各年度病例数分别为,1993年14例,1994年14例,1995年13例。病例中包括男性27例,年龄45.0±15.0岁,女性14例,年龄42.4±12.0岁,男女之比为1.93∶1。
二、组织病理学分类
根据WHO中枢神经系统肿瘤分类法(1993年)[1]的原则进行分类。资料中包括毛细胞型星形细胞瘤(Pilocytic Astrocytoma)13例(WHO Grade I),纤维型星形细胞瘤(Fibrillar Astrocytoma)16例(WHO Grade II),分化不良型星形细胞瘤(Anaplastic Astrocytoma)9例(WHO Grade Ⅲ),多形性胶质母细胞瘤(Glioblastoma Multiforme)3例(WHO Grade Ⅳ)。肿瘤组织病理学分类及有关临床资料总结见表1。
, 百拇医药
表1 41例幕上星形细胞瘤临床资料
肿瘤类型
病例数(例)
年龄范围(岁)
平均年龄(岁)
各级总数
41
10~72
44.1
男
27
10~72
45.0
, http://www.100md.com
女
14
15~62
42.4
I级
13
10~57
39.7
男
7
10~57
43.1
女
, http://www.100md.com
6
15~44
35.7
II级
16
11~72
44.5
男
12
11~72
44.1
女
4
, http://www.100md.com
34~62
45.8
Ⅲ级
9
15~61
47.2
男
6
15~61
48.0
女
3
33~55
, 百拇医药
45.7
Ⅳ级
3
48~59
52.0
男
2
58~49
48.5
女
1
59
59.0
, 百拇医药 三、标本准备
标本系本院病理科存档保存的石蜡包埋组织块,重新作4 μm切片,备染。
四、免疫组织化学染色
PCNA单克隆抗体PC10为DM公司产品,SAB药盒为Vector公司产品。主要步骤:石蜡切片常规脱蜡,加用1∶40 PC10作为一抗,按ABC法作免疫组化反应[5],光镜下控制DAB显色,苏木素复染、常规脱水、透明、封片。
每次实验均设阴性对照,以PBS代替一抗,结果显示阴性。
五、判断标准
染色后切片在100~400倍光镜下观察,选择5个细胞较丰富的高倍视野作为计数单位,观察的细胞数一般在400~1200间,计数阳性细胞数及阳性细胞数占细胞总数的百分比。视野中坏死细胞、血管内皮细胞以及无法辨认细胞核的细胞不包括在计数范围。
, http://www.100md.com
阳性反应为细胞核内呈现棕黄色颗粒,阴性反应为细胞核内无棕黄色颗粒。
阳性测定以细胞阳性率和细胞阳性强度两个指标相加而定。根据阳性率评分,分别为0分(0%)、1分(<20%)、2分(20%~50%)、3分(50%~80%)和4分(>80%);根据阳性强度即染色深浅评分,分别为0分(无显色)、1分(显浅色)、2分(中等显色)和3分(显深色)。两个得分相加,0分为阴性“-”、2分为“+”、3~4分为“++”、5~7分为“+++”。
六、统计方法
PCNA表达与不同组织病理分级间关系作Ridit检验,不同组织病理分级及PCNA表达与病人术后生存间关系作Log rank检验。
结果
一、PCNA表达与组织病理分级的关系
, 百拇医药
PCNA阳性呈现为核内棕色颗粒或均一棕色。各级星形细胞瘤PCNA表达情况见表2。Ridit分析表明,I级与II级间有显著差别(P<0.05),I级与Ⅲ级、Ⅳ级间有极显著差别(P<0.001),II级与Ⅲ级、Ⅳ级间有显著差别(P<0.05),Ⅲ级与Ⅳ级间差别无显著性(P>0.05)。PCNA表达最高为Ⅳ级,其次为Ⅲ级、II级和I级(见图1)。等级相关分析表明,星形细胞瘤PCNA表达与组织病理分级呈正相关(rs=0.74053,P<0.001)。
二、生存期评估
41例星形细胞瘤术后中位生存期(Median Survival Time)为19.5月,一年生存率为61.0%,生存曲线见图2。不同组织病理分级和不同PCNA表达水平的生存曲线见图3、4。两种因素对生存期影响的Log rank检验结果见表3。
表2 PCNA在各级星形细胞瘤中表达
, 百拇医药
组别
-例数(%)
+例数(%)
++例数(%)
+++例数(%)
总阳性率%
I级
4(30.8)
8(61.5)
1(7.7)
0(0)
69.2
II级
, 百拇医药
1(6.3)
7(43.8)
5(33.9)
3(18.8)
93.4
III级
0(0)
0(0)
4(44.4)
5(55.6)
100.0
IV级
0(0)
, http://www.100md.com
0(0)
0(0)
3(100.0)
100.0
图1 各级星形细胞瘤PCNA表达Ridit值比较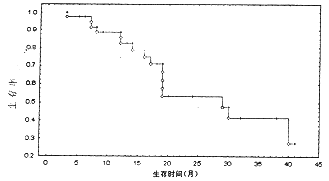
图2 41例星形细胞瘤生存曲线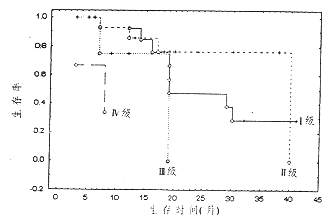
图3 各级星形细胞瘤生存曲线
, http://www.100md.com
图4 不同PCNA表达水平生存曲线
表3 两种因素Log rank检验结果
预后因素
分组
例数
死亡数
χ2值
df值
P值
组织病理分级
I级
13
, http://www.100md.com
5
8.01
3
0.04579
II级
16
12
Ⅲ级
9
7
Ⅳ级
3
1
PCNA表达
, http://www.100md.com
-
5
3
11.61
3
0.00884
+
15
4
++
10
9
+++
11
, http://www.100md.com
9
讨论
从系统性红斑狼疮(SLE)病人体内发现的一种自身抗体能识别存在于增殖细胞中的核抗原,该抗原已被用来作为增殖细胞的标记。所谓自身抗体所识别的抗原即增殖细胞核抗原(Proliferating Cell Nuclear Antigen,PCNA)。PCNA是一种生物进化中高度保守的分子量为36 kD的酸性蛋白质,它直接参与DNA的合成[2]。
PCNA也称为周期素(cyclin),它是DNA多聚酶的辅助蛋白[3]。有资料提示,在整个细胞周期中,PCNA总体水平变化很小(约2~3倍),这种变化主要出现在S期细胞中与DNA复制部位有关部分[4]。PCNA蛋白的半衰期为20小时,因此刚离开细胞周期的细胞仍可用免疫法测出PCNA的存在[3]。
, http://www.100md.com
有研究显示,用各种针对核抗原的抗体所获得标记指数来反映肿瘤细胞的增殖状态,对于预测胶质瘤复发与否有很大价值,如溴脱氧尿核苷(BUdR)标记指数>1%往往提示预后不良或高复发率[5]。Kim等[6]认为,Ki-67反映的是除G0期外整个细胞周期,而PCNA仅为特异性S期的标记,因此在反映胶质瘤恶性程度上,可靠性不如Ki-67甚至BUdR。单纯用Ki-67或结合BUdR评估胶质瘤恶性程度以及病人预后状态,结果与临床较为吻合,两种标记指数升高,提示不良临床结局。然而从技术方面考虑,PCNA更为简便并可用于石蜡切片研究,而BUdR需用新鲜组织标本或需术前用药,目前虽已有可用于石蜡标本的Ki-67单抗MIB-1[9],但价格较为昂贵,而常用的单抗仅适用于新鲜组织标本。作者采用PCNA研究星形细胞瘤石蜡标本的结果显示,除Ⅲ级与Ⅳ级间PCNA表达差别无显著性外,余各级间均有显著差别。这也提示I、II级与Ⅲ、Ⅳ级间的增殖程度有很大差别,而Ⅲ、Ⅳ级间的增殖程度则无不同。故有学者建议将Ⅲ、Ⅳ级肿瘤归于高度恶性星形细胞瘤(high gradeastrocytoma)[7],本组结果与其他学者用不同核抗体研究脑肿瘤的结果颇为一致。
, 百拇医药
颅内星形细胞瘤组织病理学分级的标准并不完全一致,许多学者倡导各自分级法。North[8]等采用Kernohan四级分类法对77例星形细胞瘤进行分析,结果提示肿瘤分级并不影响病人的生存状态。而本组研究却显示肿瘤分级与病人生存密切相关(P<0.01),I~Ⅳ级的术后生存期分别为19.0月、17.5月、6.0月和8.0月。本文的结果与Burger[7]等对1440例星形细胞瘤生存研究的结果较为一致。
PCNA在反映肿瘤细胞增殖上虽然很有价值,但同所有形态学观察一样,受观察者、观察视野和标本均一性等条件的限制。但PCNA作为一种半定量指标,理论上比单纯的组织病理学分级要准确,而PCNA与肿瘤组织病理分级之间的不完全一致,往往是由于不同研究所采用标本和方法学上的差别所造成,但绝大多数研究结果提示两者之间总的趋势是一致的。分化良好低度恶性肿瘤,PCNA的表达水平较低(-~++),而分化不良高度恶性的肿瘤,PCNA表达水平往往较高(++~+++)。本组研究首次将PCNA表达用于脑星形细胞瘤的术后生存期研究,结果显示不同PCNA表达对生存期的影响有显著差异(P<0.0088),各水平的中位生存期分别为“-”,30月;“+”,18月;“++”,12月和“+++”,5月。该结果表明了PCNA对术后生存评估具有一定意义,同时也表明PCNA检测在判断星形细胞瘤生物学行为方面比组织病理学更为准确,且实施也颇为简便,可作为评估预后指标之一,是一种反映预后的良好指标,至于能否作为临床病理的常规检测手段,有待于更进一步的深入研究。
, http://www.100md.com
第一作者简介 王勇,男,博士,副主任医师,副教授。
参 考 文 献
1 Burger PC.Classification and biology of brain tumors.In:Youmans JR,ed. Neurological Surgery,Vol5,Philadelphia,USA:WB Saunders Co,1990,2947
2 Mathews MB,Bernstein KM,Franza BR, et al. Identity of the proliferating cell nuclear antigen and cyclin.Nature,1984,303:374
3 Ottavio L,Chang CD,Rizzo MG, et al. Importance of introns in the growth regulation of mRNA levels of the proliferating cell nuclear antigen gene.Mol Cell Biol,1990,10:303
, 百拇医药
4 Morris GF,Mathews MB.Regulation of proliferating cell nuclear antigen during the cell cycle.J Cell Biol,1989,264:13856
5 Garcia RL,Coltrera MD,Gown AM.Analysis of proliferative grade using anti-PCNA/cyclin monoclonal antibodies in fixed embedded tissue:Comparison with flow cytometric analysis.Am J Pathol,149,134:733
6 Kim DK,Hoyt J,Bacchi C, et al.Detection of proliferating cell nuclear antigenin gliomas and adjacent resection margins.Neurosurgery,1993,33:619
, http://www.100md.com
7 Burger PC,Vogel FS,Green SB, et al. Glioblastoma multiforme and anaplastic as trocytoma:pathologic criteria and prognostic implications.Cancer,1985,56,1106
8 North CA,North RB,Epstein JA, et al. Low grade cerebral astrocytomas.Survival
and quality of life after radiation therapy.Cancer,1990,66:6
9 Julie MC,David WK,Bernd WS,et al. Analysis of proliferation markers and p53 expression in gliomas of astrocytic origin:relationships and prognostic value.J Neurosurg,1997,86:121
(收稿:1997-12-04 修回:1998-03-28), 百拇医药
单位:上海第二医科大学附属仁济医院神经外科(上海200001)
关键词:脑肿瘤;增殖细胞核抗原
肿瘤990311 星形细胞瘤作为颅内原发性恶性肿瘤,现代诊治技术尚未能对其治疗取得突破性进展,绝大多数病人预后险恶。肿瘤组织病理学分级虽与其生物学行为有一定关系,但由于较多因素的影响,不能准确、客观反映肿瘤细胞的增殖程度以及病人的预后。近十年来,各种细胞动力学研究已用于脑肿瘤的增殖研究,尤其是免疫组织化学技术的日趋成熟,用这种方法研究脑肿瘤细胞增殖,具有可保留细胞和组织结构的完整,方法易行,获得结果快,可用于石蜡切片等优点,因而临床研究者乐于采用。
本研究采用ABC免疫组化方法,对我院手术切除的颅内幕上星形细胞瘤石蜡包埋标本的PCNA检测,结合临床资料进行回顾性研究,以探讨PCNA表达与组织病理分级及术后生存的关系。
, 百拇医药
材料与方法
一、病例选择
1993年1月~1995年12月,上海第二医科大学附属仁济医院神经外科共手术切除颅内幕上星形细胞瘤79例,其中38例因下列原因未进入本研究:(1)临床资料不完整;(2)术后1月内死亡;(3)因肿瘤复发而再次手术;(4)初访即失访。其余41例临床资料完整并获随访,随访截止期为1996年12月31日,各年度病例数分别为,1993年14例,1994年14例,1995年13例。病例中包括男性27例,年龄45.0±15.0岁,女性14例,年龄42.4±12.0岁,男女之比为1.93∶1。
二、组织病理学分类
根据WHO中枢神经系统肿瘤分类法(1993年)[1]的原则进行分类。资料中包括毛细胞型星形细胞瘤(Pilocytic Astrocytoma)13例(WHO Grade I),纤维型星形细胞瘤(Fibrillar Astrocytoma)16例(WHO Grade II),分化不良型星形细胞瘤(Anaplastic Astrocytoma)9例(WHO Grade Ⅲ),多形性胶质母细胞瘤(Glioblastoma Multiforme)3例(WHO Grade Ⅳ)。肿瘤组织病理学分类及有关临床资料总结见表1。
, 百拇医药
表1 41例幕上星形细胞瘤临床资料
肿瘤类型
病例数(例)
年龄范围(岁)
平均年龄(岁)
各级总数
41
10~72
44.1
男
27
10~72
45.0
, http://www.100md.com
女
14
15~62
42.4
I级
13
10~57
39.7
男
7
10~57
43.1
女
, http://www.100md.com
6
15~44
35.7
II级
16
11~72
44.5
男
12
11~72
44.1
女
4
, http://www.100md.com
34~62
45.8
Ⅲ级
9
15~61
47.2
男
6
15~61
48.0
女
3
33~55
, 百拇医药
45.7
Ⅳ级
3
48~59
52.0
男
2
58~49
48.5
女
1
59
59.0
, 百拇医药 三、标本准备
标本系本院病理科存档保存的石蜡包埋组织块,重新作4 μm切片,备染。
四、免疫组织化学染色
PCNA单克隆抗体PC10为DM公司产品,SAB药盒为Vector公司产品。主要步骤:石蜡切片常规脱蜡,加用1∶40 PC10作为一抗,按ABC法作免疫组化反应[5],光镜下控制DAB显色,苏木素复染、常规脱水、透明、封片。
每次实验均设阴性对照,以PBS代替一抗,结果显示阴性。
五、判断标准
染色后切片在100~400倍光镜下观察,选择5个细胞较丰富的高倍视野作为计数单位,观察的细胞数一般在400~1200间,计数阳性细胞数及阳性细胞数占细胞总数的百分比。视野中坏死细胞、血管内皮细胞以及无法辨认细胞核的细胞不包括在计数范围。
, http://www.100md.com
阳性反应为细胞核内呈现棕黄色颗粒,阴性反应为细胞核内无棕黄色颗粒。
阳性测定以细胞阳性率和细胞阳性强度两个指标相加而定。根据阳性率评分,分别为0分(0%)、1分(<20%)、2分(20%~50%)、3分(50%~80%)和4分(>80%);根据阳性强度即染色深浅评分,分别为0分(无显色)、1分(显浅色)、2分(中等显色)和3分(显深色)。两个得分相加,0分为阴性“-”、2分为“+”、3~4分为“++”、5~7分为“+++”。
六、统计方法
PCNA表达与不同组织病理分级间关系作Ridit检验,不同组织病理分级及PCNA表达与病人术后生存间关系作Log rank检验。
结果
一、PCNA表达与组织病理分级的关系
, 百拇医药
PCNA阳性呈现为核内棕色颗粒或均一棕色。各级星形细胞瘤PCNA表达情况见表2。Ridit分析表明,I级与II级间有显著差别(P<0.05),I级与Ⅲ级、Ⅳ级间有极显著差别(P<0.001),II级与Ⅲ级、Ⅳ级间有显著差别(P<0.05),Ⅲ级与Ⅳ级间差别无显著性(P>0.05)。PCNA表达最高为Ⅳ级,其次为Ⅲ级、II级和I级(见图1)。等级相关分析表明,星形细胞瘤PCNA表达与组织病理分级呈正相关(rs=0.74053,P<0.001)。
二、生存期评估
41例星形细胞瘤术后中位生存期(Median Survival Time)为19.5月,一年生存率为61.0%,生存曲线见图2。不同组织病理分级和不同PCNA表达水平的生存曲线见图3、4。两种因素对生存期影响的Log rank检验结果见表3。
表2 PCNA在各级星形细胞瘤中表达
, 百拇医药
组别
-例数(%)
+例数(%)
++例数(%)
+++例数(%)
总阳性率%
I级
4(30.8)
8(61.5)
1(7.7)
0(0)
69.2
II级
, 百拇医药
1(6.3)
7(43.8)
5(33.9)
3(18.8)
93.4
III级
0(0)
0(0)
4(44.4)
5(55.6)
100.0
IV级
0(0)
, http://www.100md.com
0(0)
0(0)
3(100.0)
100.0

图1 各级星形细胞瘤PCNA表达Ridit值比较

图2 41例星形细胞瘤生存曲线

图3 各级星形细胞瘤生存曲线

, http://www.100md.com
图4 不同PCNA表达水平生存曲线
表3 两种因素Log rank检验结果
预后因素
分组
例数
死亡数
χ2值
df值
P值
组织病理分级
I级
13
, http://www.100md.com
5
8.01
3
0.04579
II级
16
12
Ⅲ级
9
7
Ⅳ级
3
1
PCNA表达
, http://www.100md.com
-
5
3
11.61
3
0.00884
+
15
4
++
10
9
+++
11
, http://www.100md.com
9
讨论
从系统性红斑狼疮(SLE)病人体内发现的一种自身抗体能识别存在于增殖细胞中的核抗原,该抗原已被用来作为增殖细胞的标记。所谓自身抗体所识别的抗原即增殖细胞核抗原(Proliferating Cell Nuclear Antigen,PCNA)。PCNA是一种生物进化中高度保守的分子量为36 kD的酸性蛋白质,它直接参与DNA的合成[2]。
PCNA也称为周期素(cyclin),它是DNA多聚酶的辅助蛋白[3]。有资料提示,在整个细胞周期中,PCNA总体水平变化很小(约2~3倍),这种变化主要出现在S期细胞中与DNA复制部位有关部分[4]。PCNA蛋白的半衰期为20小时,因此刚离开细胞周期的细胞仍可用免疫法测出PCNA的存在[3]。
, http://www.100md.com
有研究显示,用各种针对核抗原的抗体所获得标记指数来反映肿瘤细胞的增殖状态,对于预测胶质瘤复发与否有很大价值,如溴脱氧尿核苷(BUdR)标记指数>1%往往提示预后不良或高复发率[5]。Kim等[6]认为,Ki-67反映的是除G0期外整个细胞周期,而PCNA仅为特异性S期的标记,因此在反映胶质瘤恶性程度上,可靠性不如Ki-67甚至BUdR。单纯用Ki-67或结合BUdR评估胶质瘤恶性程度以及病人预后状态,结果与临床较为吻合,两种标记指数升高,提示不良临床结局。然而从技术方面考虑,PCNA更为简便并可用于石蜡切片研究,而BUdR需用新鲜组织标本或需术前用药,目前虽已有可用于石蜡标本的Ki-67单抗MIB-1[9],但价格较为昂贵,而常用的单抗仅适用于新鲜组织标本。作者采用PCNA研究星形细胞瘤石蜡标本的结果显示,除Ⅲ级与Ⅳ级间PCNA表达差别无显著性外,余各级间均有显著差别。这也提示I、II级与Ⅲ、Ⅳ级间的增殖程度有很大差别,而Ⅲ、Ⅳ级间的增殖程度则无不同。故有学者建议将Ⅲ、Ⅳ级肿瘤归于高度恶性星形细胞瘤(high gradeastrocytoma)[7],本组结果与其他学者用不同核抗体研究脑肿瘤的结果颇为一致。
, 百拇医药
颅内星形细胞瘤组织病理学分级的标准并不完全一致,许多学者倡导各自分级法。North[8]等采用Kernohan四级分类法对77例星形细胞瘤进行分析,结果提示肿瘤分级并不影响病人的生存状态。而本组研究却显示肿瘤分级与病人生存密切相关(P<0.01),I~Ⅳ级的术后生存期分别为19.0月、17.5月、6.0月和8.0月。本文的结果与Burger[7]等对1440例星形细胞瘤生存研究的结果较为一致。
PCNA在反映肿瘤细胞增殖上虽然很有价值,但同所有形态学观察一样,受观察者、观察视野和标本均一性等条件的限制。但PCNA作为一种半定量指标,理论上比单纯的组织病理学分级要准确,而PCNA与肿瘤组织病理分级之间的不完全一致,往往是由于不同研究所采用标本和方法学上的差别所造成,但绝大多数研究结果提示两者之间总的趋势是一致的。分化良好低度恶性肿瘤,PCNA的表达水平较低(-~++),而分化不良高度恶性的肿瘤,PCNA表达水平往往较高(++~+++)。本组研究首次将PCNA表达用于脑星形细胞瘤的术后生存期研究,结果显示不同PCNA表达对生存期的影响有显著差异(P<0.0088),各水平的中位生存期分别为“-”,30月;“+”,18月;“++”,12月和“+++”,5月。该结果表明了PCNA对术后生存评估具有一定意义,同时也表明PCNA检测在判断星形细胞瘤生物学行为方面比组织病理学更为准确,且实施也颇为简便,可作为评估预后指标之一,是一种反映预后的良好指标,至于能否作为临床病理的常规检测手段,有待于更进一步的深入研究。
, http://www.100md.com
第一作者简介 王勇,男,博士,副主任医师,副教授。
参 考 文 献
1 Burger PC.Classification and biology of brain tumors.In:Youmans JR,ed. Neurological Surgery,Vol5,Philadelphia,USA:WB Saunders Co,1990,2947
2 Mathews MB,Bernstein KM,Franza BR, et al. Identity of the proliferating cell nuclear antigen and cyclin.Nature,1984,303:374
3 Ottavio L,Chang CD,Rizzo MG, et al. Importance of introns in the growth regulation of mRNA levels of the proliferating cell nuclear antigen gene.Mol Cell Biol,1990,10:303
, 百拇医药
4 Morris GF,Mathews MB.Regulation of proliferating cell nuclear antigen during the cell cycle.J Cell Biol,1989,264:13856
5 Garcia RL,Coltrera MD,Gown AM.Analysis of proliferative grade using anti-PCNA/cyclin monoclonal antibodies in fixed embedded tissue:Comparison with flow cytometric analysis.Am J Pathol,149,134:733
6 Kim DK,Hoyt J,Bacchi C, et al.Detection of proliferating cell nuclear antigenin gliomas and adjacent resection margins.Neurosurgery,1993,33:619
, http://www.100md.com
7 Burger PC,Vogel FS,Green SB, et al. Glioblastoma multiforme and anaplastic as trocytoma:pathologic criteria and prognostic implications.Cancer,1985,56,1106
8 North CA,North RB,Epstein JA, et al. Low grade cerebral astrocytomas.Survival
and quality of life after radiation therapy.Cancer,1990,66:6
9 Julie MC,David WK,Bernd WS,et al. Analysis of proliferation markers and p53 expression in gliomas of astrocytic origin:relationships and prognostic value.J Neurosurg,1997,86:121
(收稿:1997-12-04 修回:1998-03-28), 百拇医药