����L-�Ŷ�����ø��ǰ��֬��������Ƽ�������ʵIJⶨ
���ߣ����� ����ͩ ��ѧ��
��λ���й�ҩ�ƴ�ѧ������ҩѧԺ(����ͩ)������ҩ�ƴ�ѧҩѧϵ(��ѧ��)
�ؼ��ʣ�ǰ��֬���壻����L-�Ŷ�����ø֬���壻������
����ҩ�ƴ�ѧѧ��990401 ժ Ҫ �����黯-��ѹ-������������ɿ�ǰ��֬������Ʊ�.��ǰ��֬������L-�Ŷ�����øΪʵ����ⶨ�˰�����.�Ƶõ�ǰ��֬����ˮ���γɵ�L-�Ŷ�����ø֬������̬Բ����������(0.662��0.079 2) ��m ��Χ��.3��ǰ��֬�����L-�Ŷ�����ø�İ����ʷֱ�Ϊ(48.2��0.99)%��(51.0��1.21)%��(52.2��1.25)%.3�����ŵİ����ʱ���ϵ��(RSD%)��С��3%.���˵���Ʊ��Ŀ�ǰ��֬����ˮ���γɵ�L-�Ŷ�����ø֬�����������ˣ�������L-�Ŷ�����ø�İ���.
����� R94
, ��Ĵҽҩ
Preparation of Proliposomes and the Determination of Encapsulation
of Recombinant-L-asparaginase
Wang Hong,Wu Wutong,Gu Xueqiu
College of Biopharmaceutics,China Pharmaceutical University,Nanjing 210009
Abstract Proliposomes were prepared by the emulsification,extrusion and lyophilization methods.The experiments revealed that the L-asparaginase liposomes were regular in their morphology within diameters of (0.662��0.079 2) ��m.The three batches of entrapment efficiency were(48.2��0.99)%��(51.0��1.21)%��(52.2��1625)% respectively.
, ��Ĵҽҩ
Key words proliposomes;L-asparaginase liposomes;entrapment efficiency
L-�Ŷ�����ø(L-asparaginase,L-ASNase)�����Ƽ����ܰ�ϸ����Ѫ������Чҩ�������ע��L-�Ŷ�����ø������ijЩ�����ã��������Ӧ�����ա�Ƥ��������ݿˡ�Ѫ˨��Ѫ֢��.����֬�������Һ��ˮ��ɢ�崢�棬��ˮ���ҩ���ȶ����ܵ��ܴ�Ӱ��.������֬�ױ����������ӳ������ۼ����ںϵ��°���ҩ��й©�ȣ���Щ����ʹ֬���岻�ܳ��ڴ��.��Ȼ�����ѱ���L-�Ŷ�����ø֬����������о���1��������������Ʊ��м���Ļ���ҩ��L-�Ŷ�����ø���ڲ���Ҫ����ʧ�������֬�������Һ�йص��������.Ϊ���֬������ȶ��ԣ���Һ̬��֬�����Ʊ��ɹ�̬�����֬���壬ʹ��ǰ��ˮˮ���γ�֬�������Ӧ��.ǰ��֬����(proliposome)Ϊһ�ָ���IJ�Ʒ���ڼ���ˮ��ҩ��ˮ��Һ��ɢ���ܽ��γ�һ������֬�������Һ���������ھ���������;����ҩ����������Ʒ.���Ʊ�����������֬������Ȼ�����2�������ϼ��ԸĽ����ƳɵĿ�ǰ��֬���壬����һ���̶��ϱ���ע���õ�֬�������������̾������������˫���ӽṹ�����ƻ������ⱻ��������\����Ʒ�Ȳ��ȶ����л���ҩ���ʧ����L-�Ŷ�����ø���ȶ����ܡ���Ч�ؽ�L-�Ŷ�����øת�˵�����ϸ��.������L-�Ŷ�����øΪģ��ҩ��о��˿�ǰ��֬������Ʊ����ռ���������.
, ��Ĵҽҩ
1 ʵ�鲿��
1.1 ������ҩƷ
ɨ���������(SX-40�ͣ��ձ���ʯ��˾)�����������(H-7000�ͣ��ձ�������˾)���ֹ��ȼ�(DU640�ͣ�����Beckman��˾)������ؼ�����(Multisizer AccuComp�R.119�ͣ�����)���䶳�����(LYOLAB B11��)��722-��դ�ֹ��ȼ�(�Ϻ���������������)��������֯�Ƚ���(DS-1�ͣ��Ϻ��걾ģ�ͳ�).
ע���ô���֬(soyabean lecithin������951001���Ϻ���֬һ��)�����̴�(cholesterol����������Holland���ڷ�װ)��L-�Ŷ�����ø(�й�ҩ�ƴ�ѧ�������ṩ)��Sephadex G 200(����930514�����ڷ�װ).
1.2 ��ǰ��֬������Ʊ�
, ��Ĵҽҩ
֬������Ʊ��з�������������ת����-��Ĥˮ����������-��ѹ���������黯���廯������3��4��.�����ڴ˻����ϼ��ԸĽ��������黯����ѹ��������������ɿ�ǰ��֬������Ʊ�.������������֬�͵��̴����������������������λ���Һ�����������¾���������֯�Ƚ����Ȼ����Ƴ���Һ.�ٽ�������֬��Һ��ѹ������Ĥ���ÿ�ǰ��֬������Һ���ڵ��������¹�⣬��ͨ�������.�����֬������Һ�����������·�װ�ڰ���У����䶳����۷⣬���ð�ɫ��ǰ��֬����.
1.3 ǰ��֬����ˮ�Ϻ��γ�L-�Ŷ�����ø֬�������̬�۲�
��������������۲��ǰ��֬�������L-�Ŷ�����ø��Һˮ�Ϻ��γɵ�L-�Ŷ�����ø֬���徭2%������Ⱦɫ��������̬����ͼ1��2.�����ʾL-�Ŷ�����ø֬���������Բ���Σ����ɼ����Ϊ�����.
, http://www.100md.com
Fig.1 Transmission electron micrograph of L-ASNase liposomes derived from proliposomes (��250 000)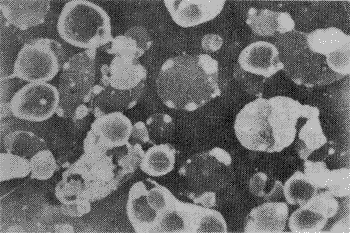
Fig.2 Transmission electron micrograph of L-ASNase liposomes derived from proliposomes (��20 000)
1.4 L-�Ŷ�����ø֬��������ȷ�Χ�������ڶ����ȷ�Χ��Ӱ��
��ǰ��֬�������L-�Ŷ�����ø��Һˮ���γɵ�L-�Ŷ�����ø֬���壬�ÿ���ؼ����Ǽ�����Ӵ�С�ֲ����������֬����������(0.662��0.0792)��m��Χ������ϵ��Ϊ12%(ͳ��������Ŀ66 141����95%�����ޣ�0.661��0.662 ��m).L-�Ŷ�����ø֬�������Һ����4�洢��2���º�������(0.684��0.1)��m��Χ������ϵ��Ϊ14.6%(ͳ��������Ŀ42 508����95%�����ޣ�0.683��0.685 ��m).L-�Ŷ�����ø֬���徭4�洢��3���º�������(0.745��0.179)��m��Χ�ڣ�(ͳ��������Ŀ��55 277����95%�����ޣ�0.744��0.747 ��m)������ϵ��Ϊ24.1%.
, ��Ĵҽҩ
1.5 L-�Ŷ�����ø�IJⶨ������L-�Ŷ�����ø�Ļ���������
1.5.1 ����������
��������һϵ��L-ASNase��ˮ��Һ��Ũ�ȷֱ�Ϊ0.01��0.02��0.04��0.06��0.08 mg/mL.
������ȡpH 8.5���Ỻ��Һ0.5 mL��L-�Ŷ�����ø��Һ(0.04 mol/L)1.0 mL���ȣ���37��ˮԡԤ�ȣ����ܼ��빩��L-�Ŷ�����ø����Һ0.5 mL��37��ˮԡ15 min����15%����������Һ0.5 mL�����ȣ�������ȡ��ӦҺ1.0 mL����ˮ7 mL����Ե⻯������Һ2 mL�����ȣ�����15 min���հ�ͬ�����������ȼ�15%����������Һ�����L-�Ŷ�����ø��Һ����500 nm���ⶨ���ն�.���ݹ������߶�������Ʒ�ж�Ӧ����������ø������λ(������Ӧ�����£�ÿ�����ܴ�L-�Ŷ������ͷ�1Ħ������ø��Ϊһ��������λ)���������1.�ֱ��Ի�����λAΪ�����꣬Ũ��CΪ��������ͼ���ñ����߷��̣�A=4.708 5+155.770 5 C,Y=0.999 9.
, ��Ĵҽҩ
1.5.2 �����ʺ;��ܶ�����
��������һϵ��L-ASNaseˮ��Һ��3�ݣ�Ũ�ȷֱ�Ϊ��4.0��8.0��12.0��16.0��20.0��24.0 ��g/��L.������������6��Ũ��ˮƽ�ϲⶨ��L-�Ŷ�ø��ø�Ļ������ɱ�������û����ʺ;��ܶ�(RSD)���������1.
Tab.1 Recoveries of the spectrophotometry for the
assay of L-asparaginase (n=3) Add/��g.��L-1
Found/��g.��L-1
Recovery/%
, ��Ĵҽҩ RSD/%
4.0
4.006��0.121
100.1
0.520
8.0
8.003��0.025
100.0
0.314
12.0
12.003��0.031
100.0
, http://www.100md.com 0.254
16.0
15.987��0.035
99.9
0.220
20.0
19.980��0.035
99.9
0.175
24.0
23.963��0.051
99.8
, http://www.100md.com 0.213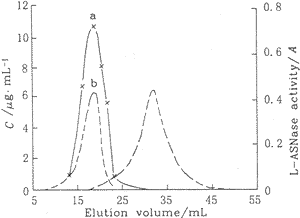
Fig.3 Gel filtration patterns of L-ASNase liposomes
a��Liposome concentration of phosphorus;
b��L-ASNase activity
1.6 L-�Ŷ�����ø֬����İ���������
1.6.1 �����ʲⶨ��
���ܳ�ȡ��ǰ��֬����500 mg,��L-�Ŷ�����øҺ(2 mg/mL)10 mLˮ���ܽ⣬�γ�L-�Ŷ�����ø֬�������Һ.������ȡ�û���Һ1 mL������10 mL����ƿ�У���ˮ���ݣ��پ�����ȡ0.1 mL������Sephadex G 200���������룬���ö������Ʒ���������5������ͼ3.
, ��Ĵҽҩ
������ѷ��������ռ�L-ASNase֬����ij�ϴ��Һ25 mL������50 mL����ƿ�ռ�����L-ASNase����ϴ��Һ���̶ȣ��ⶨ��500 nm������L-ASNase�ĺ���(Cf)������ʽ���������.������=(C\-0-C\-f)/C\-0��100%.C0ΪL-ASNase֬�������Ũ��.
1.6.2 �����ʲⶨ�Ļ���������
��L-ASNase����Һ��Sephadex G 200������������1.6.1��֬����İ����ʲⶨ����ϴ�ѣ��ռ�ϴ��Һ75 mL���ⶨ����L-ASNase����.���ƽ��������Ϊ99.72%��RSDΪ0.51%��n=6.
�ڿ�ǰ��֬�����м���L-�Ŷ�����øҺ1.0 mL����֬����İ����ʲⶨ����ϴ�ѣ��ռ���ϴ��Һ50 mL���ⶨ����L-ASNase����.���ƽ��������Ϊ99.47%��RSDΪ0.77%��n=6.
, http://www.100md.com
1.6.3 ��ǰ��֬�����L-�Ŷ�����ø�İ����ʲⶨ
��ǰ��֬����500 mg���ֱ����L-�Ŷ�����øҺ(2 mg/mL)10 mL����ˮ�ϰ��⣬�γ�L-�Ŷ�����ø֬�������Һ�����Ʊ������L-�Ŷ�����ø��֬�������Բⶨ�����ʣ�����2.
�Ʊ���ǰ��֬�����L-�Ŷ�����ø�İ�������(48.2��0.99)%��(52.2��1.25)%֮��.3�����ŵı���ϵ��(RSD%)��С��3%������ʵ��Ҫ��.
2 ����
����ҩ�ô���֬�Ʊ���������ҩ��Ŀ�ǰ��֬���壬����������ҩ���֬����ɵij���ǰ��֬���壬�˷������ҩ���ȶ�������(ҩ�ﱾ�����������)���������ڳ���֬�������Һ���˷��������Һ�ȶ�������(��֬����صı�������֬����ۼ���ҩ���֬������й©)���ʺϰ������ҩ���ǰ��֬����.
, ��Ĵҽҩ
ͨ����ǰ��֬�������L-�Ŷ�����øҺ����ˮ�ϰ��⣬�γ�L-�Ŷ�����ø֬�������Һ�������˽ϸߵ�ø���Բ����ȶ��İ�����.
������3��4��Ŀǰ�����Ʊ���ǰ��֬�����Ϊ����ij��ҩ���֬����Ԥ��Ʒ����Ȼ��ˮ�����γ�֬���壬�����Ʊ������м���ҩ������Ʊ���Щ���ȶ��Ļ���ҩ��֬���岻��.���⣬���ڴ�������\����Ʒ�����ȣ������Ʊ��������������Ʒ�ƻ�ʧЧ.��ˣ�����һ�ֲ�����ҩ�������棬����ǰ����Ŀ�ǰ��֬���������Ҫ�����ʵ�ü�ֵ.
Tab.2 The entrapment efficiency of L-ASNase
liposomes derived from proliposomes Lot No.
n=6
Entrapment
, ��Ĵҽҩ
efficiency/%
Mean entrapment
efficiency/%��s
RSD/%
96072701
50.8
49.5
53.2
51.0��1.21
2.37
50.6
50.9
, http://www.100md.com
51.0
96072702
49.2
48.4
47.2
48.2��0.99
2.06
48.2
49.3
46.4
96072903
52.3
53.5
, ��Ĵҽҩ
53.2
52.2��1.25
2.39
50.2
52.9
51.4
���о��н���ǰ��֬���嶳��Ʒ��L-�Ŷ�����ø����Ʒ�ֱ��װ��Ȼ����L-�Ŷ�����ø�ܽ�Һ��ǰ��֬����ˮ���Ƴ�L-�Ŷ�����ø֬�������Һ�����Ʊ����ǿ��еģ����䡢���淽��.����ǰ���䣬�ȶ��Ե������.
����飺�� �룬����ҩ�ƴ�ѧ1993��ҩ��ѧ��ʿ������Ϊ��������ҽѧ�о�����ʿ��
�����
1 Gurz MEM,Gaspar M M,Lopes F.Liposomal L-asparaginese:in virto evaluation.Int J Pharm,1993��96��67��77
, http://www.100md.com
2 ��ѧ������.�й�����֬�����о�.�������й�ҽҩ�Ƽ������磬1991.1��10
3 Ahn BN,Kim SK,Shim CK.Preparation and evaluation of proliposomes containing propranolol hydrochloride.J Microencapsulation,1995��12(4)��363��375
4 Katare OP,Vras SP,VK Dixit VK,et al. Enhanced in vivo performance of liposomal indomethacin derived from effervescent granule based proliposomes.J Microencapsutation,1995��12(5)��487��493
5 ��֮�裬������������ţ���.֬��������֬�ĺ������ⶨ.ҩѧͨ����1987��22��77��79
�ո�����:1998-12-17, ��Ĵҽҩ
��λ���й�ҩ�ƴ�ѧ������ҩѧԺ(����ͩ)������ҩ�ƴ�ѧҩѧϵ(��ѧ��)
�ؼ��ʣ�ǰ��֬���壻����L-�Ŷ�����ø֬���壻������
����ҩ�ƴ�ѧѧ��990401 ժ Ҫ �����黯-��ѹ-������������ɿ�ǰ��֬������Ʊ�.��ǰ��֬������L-�Ŷ�����øΪʵ����ⶨ�˰�����.�Ƶõ�ǰ��֬����ˮ���γɵ�L-�Ŷ�����ø֬������̬Բ����������(0.662��0.079 2) ��m ��Χ��.3��ǰ��֬�����L-�Ŷ�����ø�İ����ʷֱ�Ϊ(48.2��0.99)%��(51.0��1.21)%��(52.2��1.25)%.3�����ŵİ����ʱ���ϵ��(RSD%)��С��3%.���˵���Ʊ��Ŀ�ǰ��֬����ˮ���γɵ�L-�Ŷ�����ø֬�����������ˣ�������L-�Ŷ�����ø�İ���.
����� R94
, ��Ĵҽҩ
Preparation of Proliposomes and the Determination of Encapsulation
of Recombinant-L-asparaginase
Wang Hong,Wu Wutong,Gu Xueqiu
College of Biopharmaceutics,China Pharmaceutical University,Nanjing 210009
Abstract Proliposomes were prepared by the emulsification,extrusion and lyophilization methods.The experiments revealed that the L-asparaginase liposomes were regular in their morphology within diameters of (0.662��0.079 2) ��m.The three batches of entrapment efficiency were(48.2��0.99)%��(51.0��1.21)%��(52.2��1625)% respectively.
, ��Ĵҽҩ
Key words proliposomes;L-asparaginase liposomes;entrapment efficiency
L-�Ŷ�����ø(L-asparaginase,L-ASNase)�����Ƽ����ܰ�ϸ����Ѫ������Чҩ�������ע��L-�Ŷ�����ø������ijЩ�����ã��������Ӧ�����ա�Ƥ��������ݿˡ�Ѫ˨��Ѫ֢��.����֬�������Һ��ˮ��ɢ�崢�棬��ˮ���ҩ���ȶ����ܵ��ܴ�Ӱ��.������֬�ױ����������ӳ������ۼ����ںϵ��°���ҩ��й©�ȣ���Щ����ʹ֬���岻�ܳ��ڴ��.��Ȼ�����ѱ���L-�Ŷ�����ø֬����������о���1��������������Ʊ��м���Ļ���ҩ��L-�Ŷ�����ø���ڲ���Ҫ����ʧ�������֬�������Һ�йص��������.Ϊ���֬������ȶ��ԣ���Һ̬��֬�����Ʊ��ɹ�̬�����֬���壬ʹ��ǰ��ˮˮ���γ�֬�������Ӧ��.ǰ��֬����(proliposome)Ϊһ�ָ���IJ�Ʒ���ڼ���ˮ��ҩ��ˮ��Һ��ɢ���ܽ��γ�һ������֬�������Һ���������ھ���������;����ҩ����������Ʒ.���Ʊ�����������֬������Ȼ�����2�������ϼ��ԸĽ����ƳɵĿ�ǰ��֬���壬����һ���̶��ϱ���ע���õ�֬�������������̾������������˫���ӽṹ�����ƻ������ⱻ��������\����Ʒ�Ȳ��ȶ����л���ҩ���ʧ����L-�Ŷ�����ø���ȶ����ܡ���Ч�ؽ�L-�Ŷ�����øת�˵�����ϸ��.������L-�Ŷ�����øΪģ��ҩ��о��˿�ǰ��֬������Ʊ����ռ���������.
, ��Ĵҽҩ
1 ʵ�鲿��
1.1 ������ҩƷ
ɨ���������(SX-40�ͣ��ձ���ʯ��˾)�����������(H-7000�ͣ��ձ�������˾)���ֹ��ȼ�(DU640�ͣ�����Beckman��˾)������ؼ�����(Multisizer AccuComp�R.119�ͣ�����)���䶳�����(LYOLAB B11��)��722-��դ�ֹ��ȼ�(�Ϻ���������������)��������֯�Ƚ���(DS-1�ͣ��Ϻ��걾ģ�ͳ�).
ע���ô���֬(soyabean lecithin������951001���Ϻ���֬һ��)�����̴�(cholesterol����������Holland���ڷ�װ)��L-�Ŷ�����ø(�й�ҩ�ƴ�ѧ�������ṩ)��Sephadex G 200(����930514�����ڷ�װ).
1.2 ��ǰ��֬������Ʊ�
, ��Ĵҽҩ
֬������Ʊ��з�������������ת����-��Ĥˮ����������-��ѹ���������黯���廯������3��4��.�����ڴ˻����ϼ��ԸĽ��������黯����ѹ��������������ɿ�ǰ��֬������Ʊ�.������������֬�͵��̴����������������������λ���Һ�����������¾���������֯�Ƚ����Ȼ����Ƴ���Һ.�ٽ�������֬��Һ��ѹ������Ĥ���ÿ�ǰ��֬������Һ���ڵ��������¹�⣬��ͨ�������.�����֬������Һ�����������·�װ�ڰ���У����䶳����۷⣬���ð�ɫ��ǰ��֬����.
1.3 ǰ��֬����ˮ�Ϻ��γ�L-�Ŷ�����ø֬�������̬�۲�
��������������۲��ǰ��֬�������L-�Ŷ�����ø��Һˮ�Ϻ��γɵ�L-�Ŷ�����ø֬���徭2%������Ⱦɫ��������̬����ͼ1��2.�����ʾL-�Ŷ�����ø֬���������Բ���Σ����ɼ����Ϊ�����.

, http://www.100md.com
Fig.1 Transmission electron micrograph of L-ASNase liposomes derived from proliposomes (��250 000)

Fig.2 Transmission electron micrograph of L-ASNase liposomes derived from proliposomes (��20 000)
1.4 L-�Ŷ�����ø֬��������ȷ�Χ�������ڶ����ȷ�Χ��Ӱ��
��ǰ��֬�������L-�Ŷ�����ø��Һˮ���γɵ�L-�Ŷ�����ø֬���壬�ÿ���ؼ����Ǽ�����Ӵ�С�ֲ����������֬����������(0.662��0.0792)��m��Χ������ϵ��Ϊ12%(ͳ��������Ŀ66 141����95%�����ޣ�0.661��0.662 ��m).L-�Ŷ�����ø֬�������Һ����4�洢��2���º�������(0.684��0.1)��m��Χ������ϵ��Ϊ14.6%(ͳ��������Ŀ42 508����95%�����ޣ�0.683��0.685 ��m).L-�Ŷ�����ø֬���徭4�洢��3���º�������(0.745��0.179)��m��Χ�ڣ�(ͳ��������Ŀ��55 277����95%�����ޣ�0.744��0.747 ��m)������ϵ��Ϊ24.1%.
, ��Ĵҽҩ
1.5 L-�Ŷ�����ø�IJⶨ������L-�Ŷ�����ø�Ļ���������
1.5.1 ����������
��������һϵ��L-ASNase��ˮ��Һ��Ũ�ȷֱ�Ϊ0.01��0.02��0.04��0.06��0.08 mg/mL.
������ȡpH 8.5���Ỻ��Һ0.5 mL��L-�Ŷ�����ø��Һ(0.04 mol/L)1.0 mL���ȣ���37��ˮԡԤ�ȣ����ܼ��빩��L-�Ŷ�����ø����Һ0.5 mL��37��ˮԡ15 min����15%����������Һ0.5 mL�����ȣ�������ȡ��ӦҺ1.0 mL����ˮ7 mL����Ե⻯������Һ2 mL�����ȣ�����15 min���հ�ͬ�����������ȼ�15%����������Һ�����L-�Ŷ�����ø��Һ����500 nm���ⶨ���ն�.���ݹ������߶�������Ʒ�ж�Ӧ����������ø������λ(������Ӧ�����£�ÿ�����ܴ�L-�Ŷ������ͷ�1Ħ������ø��Ϊһ��������λ)���������1.�ֱ��Ի�����λAΪ�����꣬Ũ��CΪ��������ͼ���ñ����߷��̣�A=4.708 5+155.770 5 C,Y=0.999 9.
, ��Ĵҽҩ
1.5.2 �����ʺ;��ܶ�����
��������һϵ��L-ASNaseˮ��Һ��3�ݣ�Ũ�ȷֱ�Ϊ��4.0��8.0��12.0��16.0��20.0��24.0 ��g/��L.������������6��Ũ��ˮƽ�ϲⶨ��L-�Ŷ�ø��ø�Ļ������ɱ�������û����ʺ;��ܶ�(RSD)���������1.
Tab.1 Recoveries of the spectrophotometry for the
assay of L-asparaginase (n=3) Add/��g.��L-1
Found/��g.��L-1
Recovery/%
, ��Ĵҽҩ RSD/%
4.0
4.006��0.121
100.1
0.520
8.0
8.003��0.025
100.0
0.314
12.0
12.003��0.031
100.0
, http://www.100md.com 0.254
16.0
15.987��0.035
99.9
0.220
20.0
19.980��0.035
99.9
0.175
24.0
23.963��0.051
99.8
, http://www.100md.com 0.213

Fig.3 Gel filtration patterns of L-ASNase liposomes
a��Liposome concentration of phosphorus;
b��L-ASNase activity
1.6 L-�Ŷ�����ø֬����İ���������
1.6.1 �����ʲⶨ��
���ܳ�ȡ��ǰ��֬����500 mg,��L-�Ŷ�����øҺ(2 mg/mL)10 mLˮ���ܽ⣬�γ�L-�Ŷ�����ø֬�������Һ.������ȡ�û���Һ1 mL������10 mL����ƿ�У���ˮ���ݣ��پ�����ȡ0.1 mL������Sephadex G 200���������룬���ö������Ʒ���������5������ͼ3.
, ��Ĵҽҩ
������ѷ��������ռ�L-ASNase֬����ij�ϴ��Һ25 mL������50 mL����ƿ�ռ�����L-ASNase����ϴ��Һ���̶ȣ��ⶨ��500 nm������L-ASNase�ĺ���(Cf)������ʽ���������.������=(C\-0-C\-f)/C\-0��100%.C0ΪL-ASNase֬�������Ũ��.
1.6.2 �����ʲⶨ�Ļ���������
��L-ASNase����Һ��Sephadex G 200������������1.6.1��֬����İ����ʲⶨ����ϴ�ѣ��ռ�ϴ��Һ75 mL���ⶨ����L-ASNase����.���ƽ��������Ϊ99.72%��RSDΪ0.51%��n=6.
�ڿ�ǰ��֬�����м���L-�Ŷ�����øҺ1.0 mL����֬����İ����ʲⶨ����ϴ�ѣ��ռ���ϴ��Һ50 mL���ⶨ����L-ASNase����.���ƽ��������Ϊ99.47%��RSDΪ0.77%��n=6.
, http://www.100md.com
1.6.3 ��ǰ��֬�����L-�Ŷ�����ø�İ����ʲⶨ
��ǰ��֬����500 mg���ֱ����L-�Ŷ�����øҺ(2 mg/mL)10 mL����ˮ�ϰ��⣬�γ�L-�Ŷ�����ø֬�������Һ�����Ʊ������L-�Ŷ�����ø��֬�������Բⶨ�����ʣ�����2.
�Ʊ���ǰ��֬�����L-�Ŷ�����ø�İ�������(48.2��0.99)%��(52.2��1.25)%֮��.3�����ŵı���ϵ��(RSD%)��С��3%������ʵ��Ҫ��.
2 ����
����ҩ�ô���֬�Ʊ���������ҩ��Ŀ�ǰ��֬���壬����������ҩ���֬����ɵij���ǰ��֬���壬�˷������ҩ���ȶ�������(ҩ�ﱾ�����������)���������ڳ���֬�������Һ���˷��������Һ�ȶ�������(��֬����صı�������֬����ۼ���ҩ���֬������й©)���ʺϰ������ҩ���ǰ��֬����.
, ��Ĵҽҩ
ͨ����ǰ��֬�������L-�Ŷ�����øҺ����ˮ�ϰ��⣬�γ�L-�Ŷ�����ø֬�������Һ�������˽ϸߵ�ø���Բ����ȶ��İ�����.
������3��4��Ŀǰ�����Ʊ���ǰ��֬�����Ϊ����ij��ҩ���֬����Ԥ��Ʒ����Ȼ��ˮ�����γ�֬���壬�����Ʊ������м���ҩ������Ʊ���Щ���ȶ��Ļ���ҩ��֬���岻��.���⣬���ڴ�������\����Ʒ�����ȣ������Ʊ��������������Ʒ�ƻ�ʧЧ.��ˣ�����һ�ֲ�����ҩ�������棬����ǰ����Ŀ�ǰ��֬���������Ҫ�����ʵ�ü�ֵ.
Tab.2 The entrapment efficiency of L-ASNase
liposomes derived from proliposomes Lot No.
n=6
Entrapment
, ��Ĵҽҩ
efficiency/%
Mean entrapment
efficiency/%��s
RSD/%
96072701
50.8
49.5
53.2
51.0��1.21
2.37
50.6
50.9
, http://www.100md.com
51.0
96072702
49.2
48.4
47.2
48.2��0.99
2.06
48.2
49.3
46.4
96072903
52.3
53.5
, ��Ĵҽҩ
53.2
52.2��1.25
2.39
50.2
52.9
51.4
���о��н���ǰ��֬���嶳��Ʒ��L-�Ŷ�����ø����Ʒ�ֱ��װ��Ȼ����L-�Ŷ�����ø�ܽ�Һ��ǰ��֬����ˮ���Ƴ�L-�Ŷ�����ø֬�������Һ�����Ʊ����ǿ��еģ����䡢���淽��.����ǰ���䣬�ȶ��Ե������.
����飺�� �룬����ҩ�ƴ�ѧ1993��ҩ��ѧ��ʿ������Ϊ��������ҽѧ�о�����ʿ��
�����
1 Gurz MEM,Gaspar M M,Lopes F.Liposomal L-asparaginese:in virto evaluation.Int J Pharm,1993��96��67��77
, http://www.100md.com
2 ��ѧ������.�й�����֬�����о�.�������й�ҽҩ�Ƽ������磬1991.1��10
3 Ahn BN,Kim SK,Shim CK.Preparation and evaluation of proliposomes containing propranolol hydrochloride.J Microencapsulation,1995��12(4)��363��375
4 Katare OP,Vras SP,VK Dixit VK,et al. Enhanced in vivo performance of liposomal indomethacin derived from effervescent granule based proliposomes.J Microencapsutation,1995��12(5)��487��493
5 ��֮�裬������������ţ���.֬��������֬�ĺ������ⶨ.ҩѧͨ����1987��22��77��79
�ո�����:1998-12-17, ��Ĵҽҩ