星形细胞瘤及其瘤细胞凋亡的研究:透射电镜与原位细胞凋亡检测
作者:郝卓芳 罗欣鸣 黄世章 陆光明 林英 廖德贵
单位:广州医学院第二附属医院病理科,广州 510260
关键词:星形细胞瘤;凋亡;原位标记
广州医学院学报990401
提要 目的:探讨星形细胞瘤瘤细胞及其凋亡的超微结构变化,为阐述肿瘤内在的生物学行为寻找形态学依据,分析瘤细胞凋亡与肿瘤恶性转化的关系。方法:收集本院神经外科手术标本, 应用透射电镜及原位细胞凋亡试剂盒对星形细胞瘤进行观察和检测。结果:电镜下发现瘤细胞胞浆内胶质丝与发育不良/幼稚的细胞器并存;瘤细胞核核内假性包涵体;瘤细胞间缺乏细胞连接。原位细胞凋亡检测显示,星形细胞瘤中低分级组瘤细胞凋亡的细胞密度明显高于高分级组(P<0.01)。结论:瘤细胞凋亡的细胞密度随着肿瘤级数的增高而降低,提示星形细胞瘤瘤细胞的增殖和凋亡失衡,即瘤细胞无限制性增生和/或瘤细胞不能进入凋亡。这可能是星形细胞瘤发生发展的重要因素。
, http://www.100md.com
中图分类号 R739.4
A Study of Astrocytoma and the Apoptosis of its Tumor Cells by the methods of Electron Microscopy and in Situ End-labeling of DNA Breaks
Hao Zhuofang,Luo Xinming,Huang Shizhang,et al
(Department of Pathology,the Second Affiliated Hospital,Guangzhou Medical College,Guangzhou 510182)
Objective: To explore the ultrastructural features of the tumor cells of astrocytoma and their apoptosis,so as to discover morphological clue to the biological behavior of the tumor,and elucidate the relationship between the apoptosis of the tumor cells and the malignant transformation of the tumor. Methods: The specimens of astrocytoma from operations in Neurosurgery Department in our hospital were collected,and were observed and detected with transmission electron microscopy and in situ end-labeling of DNA breaks. Results: With electron microscopy,glial filaments and dysplasia/immature cell organs were observed in the cytoplasm of the tumor cells;Moreover,intranuclear pseuonucleus inclusions and deficiency of cellular junction among tumor cells were found. The assay with in situ end-labeling of DNA breaks showed that the density of the apoptotic cells in low pathological grade group was greater than that in high grade group (P<0.01). Conclusion:The density of apoptotic cells decreased with the increasing of the pathological grade,suggesting the imbalance of the proliferation and apoptosis in tumor cells of astrocytoma,i.e.,the tumor cells unlimitedly proliferate and never enter into apoptosis,which may be an important factor leading to the formation and progress of a strocytoma.
, 百拇医药
Key words Astrocytoma;Apoptosis;In situ end-labeling
细胞凋亡在肿瘤发生发展及治疗中的作用已成为当今医学研究领域的热点。肿瘤的生长有赖于细胞分裂、分化和细胞死亡。肿瘤中的细胞凋亡现象很可能是机体对抗肿瘤的主动努力[1-3]。星形细胞瘤是最为常见的一种胶质瘤,手术切除后复发是其固有的趋向,且恶性程度进行性增高,对人类的危害极大[4-6]。本研究试图(1)从亚细胞水平观察星形细胞瘤瘤细胞及其凋亡的超微结构变化,为阐述肿瘤细胞内在的生物学行为寻找形态学依据;(2)以原位细胞凋亡检测试剂盒原位显示凋亡,进一步探讨瘤细胞凋亡在星形细胞瘤发生发展及其恶性转化过程中所起的作用。
1 材料与方法
1.1 星形细胞瘤的分级:星形细胞瘤按WHO(1993)分级方法进行数字分级。依组织处理方法及观察目的不同,详见下面。
, http://www.100md.com
1.2 电镜技术:共收集15例星形细胞瘤标本,其中Ⅰ级1例,Ⅱ级7例,Ⅲ级4例,多形性胶质母细胞瘤3例。男性10例,女性5例。发病年龄3~66岁,平均37.3岁。标本从手术中取出后迅速放入2.5%戊二醛冷固定,1%锇酸后固定,经环氧树脂包埋,超薄切片,常规铀铅染色后观察。
1.3 原位细胞凋亡的检测:随机选出40例星形细胞瘤,其中Ⅰ级3例,Ⅱ级15例,Ⅲ级11例,多形性胶质母细胞瘤11例。男性29例,女性11例,发病年龄2~67岁,平均37.5岁。采用石蜡包埋组织,切片常规脱蜡入水,蛋白酶K消化,利用末端转移酶(TdT)作为催化酶(美国Promega公司产品),在适当条件下,用地高辛标记的dUTP作为底物(Dig-dUTP为德国B.M公司产品),接合于DNA双链钝端,再用免疫组化(SABC)法( 博士德公司原位细胞凋亡检测试剂盒)放大标记信号,然后 DAB显色,苏木素染色,能结构完好地原位显示凋亡细胞。用装有目镜网格测微尺的400倍视野计数凋亡细胞(个/0.05mm2),每张切片计数两个视野。
, 百拇医药
1.4 统计学分析:F分析和Q检验。
2 结果
2.1 电镜下观察
2.1.1 星形细胞瘤的一般形态学:星形细胞瘤瘤细胞单一,但细胞形态大小不规则,宽距离分布于树突状胞突之中;胞突与胞突之间的疏松网眼中有絮状无结构物或空白-微囊形成;胞浆内含大量胶质丝,缺乏细胞器;胞核外形极不规则,表面锯齿状,有的可见假性核内包涵体(图1),核染色质常贴近核膜;核分裂少。随着肿瘤分级的级数增高,瘤细胞更加密集,异型性更加突出:多形/怪异形核或多核,核分裂易见;胞浆内细胞器明显增多,有的出现发育不良的细胞器(图2),但仍可见胶质丝。无论星形细胞瘤分化程度高低,或是瘤细胞密度的高低,瘤细胞多弥漫排列,瘤细胞之间及其与瘤细胞突起间未见明显的细胞连接。一些瘤组织中尚可见神经元、神经轴突、树突及髓鞘等结构。
, 百拇医药
图1 显示核内假包涵体及核周胶质丝。
原放大为×13000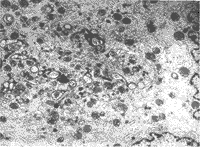
图2 显示瘤细胞浆内发育不良细胞器区。
原放大为×8300
2.1.2 细胞凋亡的形态学特征:凋亡细胞呈单个散在于瘤细胞之中。我们观察到凋亡的演变过程:凋亡早期,核染色质边集浓缩,细致均一,呈半月形或花环状;以后胞浆皱缩,胞浆内细胞器正常或空泡化;凋亡小体形成并与邻近细胞接触变圆(图3);凋亡小体很快被邻近细胞吞噬;周围无炎症反应。
图3 显示凋亡细胞,其核染色质呈半月形。
, 百拇医药
原放大为×13000
2.2.2 细胞凋亡的原位检测
凋亡细胞核呈深棕黄色,染色不均,阳性细胞分布不均匀,散在于瘤组织中。星形细胞瘤中,无论分化程度高低均可见标记的凋亡细胞(阳性率为100%)。未凋亡细胞非特异染色较浅。坏死区弥漫着染,细胞轮廓不清,呈均一棕黄色片状,核无苏木素着染。本实验统计结果表明(表1),星形细胞瘤Ⅱ级的凋亡细胞密度明显高于Ⅲ级及多形性胶质母细胞瘤(P<0.01)。Ⅰ级例数少,放入Ⅱ级中一并讨论。
表1 不同分级星形细胞瘤凋亡细胞密度的比较 分 级
例 数
凋亡细胞
Ⅰ级
3
, 百拇医药
14.1208±3.7082
Ⅱ级
15
12.5000±3.5847
Ⅲ级
11
5.1538±2.3970
胶母
11
4.3000±2.0025
3 讨论
自70年代电镜逐渐应用于病理诊断中,超微结构的研究开拓了认识肿瘤更深层次的视野。瘤细胞超微结构特征取决于组织学类型、分化和功能状态。国内外文献对星形细胞瘤已作了详细的描述[6,7],本研究的观察与文献相似,同时发现有些瘤细胞胞浆内发育不良的细胞器明显增多(图2),但仍可见少量胶质丝,这种瘤细胞的不协调性生长,是细胞分化与分裂失控在形态上的表达。有的可见假性核内包涵体(图1),这是由于细胞核表面积增大,核膜内折凹陷所致,反映瘤细胞代谢水平较高及生长活跃。关于细胞连接结构问题,据部分文献记载及个别作者观察仍可发现发育不良的粘着小体,而本观察中未找到明确的细胞连接,有待进一步探讨。观察中发现瘤组织中有神经元、神经轴突、树突及髓鞘等结构,可能与所取的样本有关,如取到肿瘤与脑组织交界处,就可以观察到神经的结构,表明肿瘤向脑组织内浸润性生长。
, 百拇医药
细胞凋亡的概念与细胞坏死截然不同,其区别主要体现在发生机制、形态学和生物化学等诸方面。Kerr(1972)发现电镜下凋亡的细胞具有共同的形态学特征[8],核的变化发生较早,核染色质凝集,常附着于核内膜处呈半月状或环状,核仁消失;继而发生细胞皱缩,细胞核及胞质均十分致密,伴有胞质空泡形成,核碎裂成膜包团块,细胞膜表面伸出突起(起泡),突起脱落形成凋亡小体。凋亡小体很快被邻近的细胞吞噬,周围不发生炎症反应。我们在电镜下观察到星形细胞瘤的瘤细胞凋亡及其凋亡不同阶段的演变,与Kerr等描述的相符合。由于电镜取材的局限性(组织太小),观察范围太小难与病理形态学紧密结合;由于整个凋亡过程所花的时间很短,且很快消失,组织切片中凋亡就不那么引人注目。况且,并非所有的凋亡细胞都显示其形态特征,故难于进行计数定量分析。
Gavrieli(1992)首次报道原位DNA片段末端标记(In Situ End-Labeling,ISEL)法,能原位显示凋亡细胞。这是一种较好的研究细胞凋亡的方法,其操作简便,敏感性高,重复性好。它不仅能显示光镜下典型的凋亡细胞,且能显示形态学改变尚不明显的早期凋亡细胞,并能进行计数。事实上,细胞发生凋亡的生化改变要比形态结构的变化更早发生。生化研究的细胞凋亡变化主要是指核小体间DNA规则性断裂[1~3,9],而这些大分子的改变,是不能从形态上观察得到的;病理学研究的细胞凋亡,则是寻找具有诊断性的形态特征,表明凋亡的细胞发生不可逆反应。从某种意义上讲,原位凋亡细胞检测可标记更早期的凋亡细胞[10]。本实验对40例不同分化程度的星形细胞瘤进行了凋亡细胞的原位检测(表1),结果显示:随着肿瘤恶性程度的增加(级数增高),凋亡细胞密度减少(图4,5),表明星形细胞瘤生长失调与细胞生存增加相关,提示瘤细胞的增殖和凋亡失衡,即瘤细胞无限制性增生和/或瘤细胞不能进入凋亡[2]。这可能是星形细胞瘤发生发展的重要因素。
, 百拇医药
图4 显示星形细胞瘤Ⅱ级凋亡细胞,呈深棕黄色。
(ISEL)法。×400
本实验在对凋亡细胞的原位检测中发现,瘤组织中有弥漫性着染(图5),有的呈浅棕黄色,见蓝染核,易于与凋亡细胞区别,有文献报道可能是由于固定不够及时或固定不够充分,导致细胞自溶,核内DNA 在内切酶作用下裂解;有的呈深棕色,无蓝染核存在,难于与凋亡细胞区别,文献指出可能是由于组织坏死、严重自溶或染色前蛋白酶K过消化所致。这种现象目前尚不能合理解释[9~11],有待进一步探讨分析。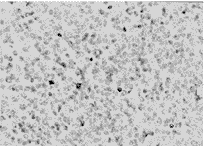
图5 显示星形细胞瘤Ⅲ级凋亡细胞,呈深棕黄色。
伴弥漫性染色显浅棕黄色。 (ISEL)法。×400
, 百拇医药
参考文献:
[1]Hermann Steller. Mechanisms and genes of cellular suicide.Science, 1995;267 :1445~47
[2]Craig B. Thompson.Apoptosis in the pathogenesis and treatment ofdisease,Science, 1995;267:1456~58
[3]Claire M. Payne, Harris Bernstein, et al. Role of apoptosis in biology and pathology: Resistance to apoptosis in colon carcinogenesis. Ultrastruct Pathol,1995;19:221~25
, 百拇医药
[4]Schiffer D, Migheli A, Chio A, et al. Apoptosis and cell proliferation in human neuroepithelial tumors. Neuro- sci Lett,1995;195:81~85
[5]Chozick BS, Weicker ME, Pezzllo JC,et al. Pattern of mutant p53 expression in human astrocytomas suggests the exsistence of alternate pathways of tumorigenesis. Cancer,1994;73:406~10
[6]Pawel P, Liberski, Radzislaw Kordek. Ultrastructural pathology of glial brain tumors revisited:A review. Ultrastruct Pathol, 1997;21: 1~4
, 百拇医药
[7]黄文清. 神经系统的肿瘤,肿瘤电子显微镜诊断学.上海科学技术出版社. 1993:104~12
[8]Kerr JFR, Wyllie AH, Currie AR. Apoptosis: a basis biological phenomenon with wide-ranging implica- tions in tissue kinetics. Br J Cancer,1972;26:239~42
[9]Ricardo H Bardales, Su-su Xie, Su-ming HSU. In situ fragmentation assay for detection of apoptosis in paraffin-embedded tissue sections. Am J Pathol,1997;107:332~35
[10]Korsek R,Hironshi M, Yanagihara R, et al. Apoptosis in glialtumors as determined by in situ nonradioactive labeling of DNA breaks.Acta Neuro- pathol Berl,1996;91:112~113
[11]Henrik B. Hellquist, kaarina Sundelin, Alessandra Di Bacco, et al.Tumor growth fraction and apoptosis in salivary gland acinic cellcarcinomas. Prognostic implications of Ki-67 and bcl-2 expression and of in situ end labeling. J Pathol,1997;181:323~26
(收稿:1999-05-15), 百拇医药
单位:广州医学院第二附属医院病理科,广州 510260
关键词:星形细胞瘤;凋亡;原位标记
广州医学院学报990401
提要 目的:探讨星形细胞瘤瘤细胞及其凋亡的超微结构变化,为阐述肿瘤内在的生物学行为寻找形态学依据,分析瘤细胞凋亡与肿瘤恶性转化的关系。方法:收集本院神经外科手术标本, 应用透射电镜及原位细胞凋亡试剂盒对星形细胞瘤进行观察和检测。结果:电镜下发现瘤细胞胞浆内胶质丝与发育不良/幼稚的细胞器并存;瘤细胞核核内假性包涵体;瘤细胞间缺乏细胞连接。原位细胞凋亡检测显示,星形细胞瘤中低分级组瘤细胞凋亡的细胞密度明显高于高分级组(P<0.01)。结论:瘤细胞凋亡的细胞密度随着肿瘤级数的增高而降低,提示星形细胞瘤瘤细胞的增殖和凋亡失衡,即瘤细胞无限制性增生和/或瘤细胞不能进入凋亡。这可能是星形细胞瘤发生发展的重要因素。
, http://www.100md.com
中图分类号 R739.4
A Study of Astrocytoma and the Apoptosis of its Tumor Cells by the methods of Electron Microscopy and in Situ End-labeling of DNA Breaks
Hao Zhuofang,Luo Xinming,Huang Shizhang,et al
(Department of Pathology,the Second Affiliated Hospital,Guangzhou Medical College,Guangzhou 510182)
Objective: To explore the ultrastructural features of the tumor cells of astrocytoma and their apoptosis,so as to discover morphological clue to the biological behavior of the tumor,and elucidate the relationship between the apoptosis of the tumor cells and the malignant transformation of the tumor. Methods: The specimens of astrocytoma from operations in Neurosurgery Department in our hospital were collected,and were observed and detected with transmission electron microscopy and in situ end-labeling of DNA breaks. Results: With electron microscopy,glial filaments and dysplasia/immature cell organs were observed in the cytoplasm of the tumor cells;Moreover,intranuclear pseuonucleus inclusions and deficiency of cellular junction among tumor cells were found. The assay with in situ end-labeling of DNA breaks showed that the density of the apoptotic cells in low pathological grade group was greater than that in high grade group (P<0.01). Conclusion:The density of apoptotic cells decreased with the increasing of the pathological grade,suggesting the imbalance of the proliferation and apoptosis in tumor cells of astrocytoma,i.e.,the tumor cells unlimitedly proliferate and never enter into apoptosis,which may be an important factor leading to the formation and progress of a strocytoma.
, 百拇医药
Key words Astrocytoma;Apoptosis;In situ end-labeling
细胞凋亡在肿瘤发生发展及治疗中的作用已成为当今医学研究领域的热点。肿瘤的生长有赖于细胞分裂、分化和细胞死亡。肿瘤中的细胞凋亡现象很可能是机体对抗肿瘤的主动努力[1-3]。星形细胞瘤是最为常见的一种胶质瘤,手术切除后复发是其固有的趋向,且恶性程度进行性增高,对人类的危害极大[4-6]。本研究试图(1)从亚细胞水平观察星形细胞瘤瘤细胞及其凋亡的超微结构变化,为阐述肿瘤细胞内在的生物学行为寻找形态学依据;(2)以原位细胞凋亡检测试剂盒原位显示凋亡,进一步探讨瘤细胞凋亡在星形细胞瘤发生发展及其恶性转化过程中所起的作用。
1 材料与方法
1.1 星形细胞瘤的分级:星形细胞瘤按WHO(1993)分级方法进行数字分级。依组织处理方法及观察目的不同,详见下面。
, http://www.100md.com
1.2 电镜技术:共收集15例星形细胞瘤标本,其中Ⅰ级1例,Ⅱ级7例,Ⅲ级4例,多形性胶质母细胞瘤3例。男性10例,女性5例。发病年龄3~66岁,平均37.3岁。标本从手术中取出后迅速放入2.5%戊二醛冷固定,1%锇酸后固定,经环氧树脂包埋,超薄切片,常规铀铅染色后观察。
1.3 原位细胞凋亡的检测:随机选出40例星形细胞瘤,其中Ⅰ级3例,Ⅱ级15例,Ⅲ级11例,多形性胶质母细胞瘤11例。男性29例,女性11例,发病年龄2~67岁,平均37.5岁。采用石蜡包埋组织,切片常规脱蜡入水,蛋白酶K消化,利用末端转移酶(TdT)作为催化酶(美国Promega公司产品),在适当条件下,用地高辛标记的dUTP作为底物(Dig-dUTP为德国B.M公司产品),接合于DNA双链钝端,再用免疫组化(SABC)法( 博士德公司原位细胞凋亡检测试剂盒)放大标记信号,然后 DAB显色,苏木素染色,能结构完好地原位显示凋亡细胞。用装有目镜网格测微尺的400倍视野计数凋亡细胞(个/0.05mm2),每张切片计数两个视野。
, 百拇医药
1.4 统计学分析:F分析和Q检验。
2 结果
2.1 电镜下观察
2.1.1 星形细胞瘤的一般形态学:星形细胞瘤瘤细胞单一,但细胞形态大小不规则,宽距离分布于树突状胞突之中;胞突与胞突之间的疏松网眼中有絮状无结构物或空白-微囊形成;胞浆内含大量胶质丝,缺乏细胞器;胞核外形极不规则,表面锯齿状,有的可见假性核内包涵体(图1),核染色质常贴近核膜;核分裂少。随着肿瘤分级的级数增高,瘤细胞更加密集,异型性更加突出:多形/怪异形核或多核,核分裂易见;胞浆内细胞器明显增多,有的出现发育不良的细胞器(图2),但仍可见胶质丝。无论星形细胞瘤分化程度高低,或是瘤细胞密度的高低,瘤细胞多弥漫排列,瘤细胞之间及其与瘤细胞突起间未见明显的细胞连接。一些瘤组织中尚可见神经元、神经轴突、树突及髓鞘等结构。

, 百拇医药
图1 显示核内假包涵体及核周胶质丝。
原放大为×13000

图2 显示瘤细胞浆内发育不良细胞器区。
原放大为×8300
2.1.2 细胞凋亡的形态学特征:凋亡细胞呈单个散在于瘤细胞之中。我们观察到凋亡的演变过程:凋亡早期,核染色质边集浓缩,细致均一,呈半月形或花环状;以后胞浆皱缩,胞浆内细胞器正常或空泡化;凋亡小体形成并与邻近细胞接触变圆(图3);凋亡小体很快被邻近细胞吞噬;周围无炎症反应。

图3 显示凋亡细胞,其核染色质呈半月形。
, 百拇医药
原放大为×13000
2.2.2 细胞凋亡的原位检测
凋亡细胞核呈深棕黄色,染色不均,阳性细胞分布不均匀,散在于瘤组织中。星形细胞瘤中,无论分化程度高低均可见标记的凋亡细胞(阳性率为100%)。未凋亡细胞非特异染色较浅。坏死区弥漫着染,细胞轮廓不清,呈均一棕黄色片状,核无苏木素着染。本实验统计结果表明(表1),星形细胞瘤Ⅱ级的凋亡细胞密度明显高于Ⅲ级及多形性胶质母细胞瘤(P<0.01)。Ⅰ级例数少,放入Ⅱ级中一并讨论。
表1 不同分级星形细胞瘤凋亡细胞密度的比较 分 级
例 数
凋亡细胞
Ⅰ级
3
, 百拇医药
14.1208±3.7082
Ⅱ级
15
12.5000±3.5847
Ⅲ级
11
5.1538±2.3970
胶母
11
4.3000±2.0025
3 讨论
自70年代电镜逐渐应用于病理诊断中,超微结构的研究开拓了认识肿瘤更深层次的视野。瘤细胞超微结构特征取决于组织学类型、分化和功能状态。国内外文献对星形细胞瘤已作了详细的描述[6,7],本研究的观察与文献相似,同时发现有些瘤细胞胞浆内发育不良的细胞器明显增多(图2),但仍可见少量胶质丝,这种瘤细胞的不协调性生长,是细胞分化与分裂失控在形态上的表达。有的可见假性核内包涵体(图1),这是由于细胞核表面积增大,核膜内折凹陷所致,反映瘤细胞代谢水平较高及生长活跃。关于细胞连接结构问题,据部分文献记载及个别作者观察仍可发现发育不良的粘着小体,而本观察中未找到明确的细胞连接,有待进一步探讨。观察中发现瘤组织中有神经元、神经轴突、树突及髓鞘等结构,可能与所取的样本有关,如取到肿瘤与脑组织交界处,就可以观察到神经的结构,表明肿瘤向脑组织内浸润性生长。
, 百拇医药
细胞凋亡的概念与细胞坏死截然不同,其区别主要体现在发生机制、形态学和生物化学等诸方面。Kerr(1972)发现电镜下凋亡的细胞具有共同的形态学特征[8],核的变化发生较早,核染色质凝集,常附着于核内膜处呈半月状或环状,核仁消失;继而发生细胞皱缩,细胞核及胞质均十分致密,伴有胞质空泡形成,核碎裂成膜包团块,细胞膜表面伸出突起(起泡),突起脱落形成凋亡小体。凋亡小体很快被邻近的细胞吞噬,周围不发生炎症反应。我们在电镜下观察到星形细胞瘤的瘤细胞凋亡及其凋亡不同阶段的演变,与Kerr等描述的相符合。由于电镜取材的局限性(组织太小),观察范围太小难与病理形态学紧密结合;由于整个凋亡过程所花的时间很短,且很快消失,组织切片中凋亡就不那么引人注目。况且,并非所有的凋亡细胞都显示其形态特征,故难于进行计数定量分析。
Gavrieli(1992)首次报道原位DNA片段末端标记(In Situ End-Labeling,ISEL)法,能原位显示凋亡细胞。这是一种较好的研究细胞凋亡的方法,其操作简便,敏感性高,重复性好。它不仅能显示光镜下典型的凋亡细胞,且能显示形态学改变尚不明显的早期凋亡细胞,并能进行计数。事实上,细胞发生凋亡的生化改变要比形态结构的变化更早发生。生化研究的细胞凋亡变化主要是指核小体间DNA规则性断裂[1~3,9],而这些大分子的改变,是不能从形态上观察得到的;病理学研究的细胞凋亡,则是寻找具有诊断性的形态特征,表明凋亡的细胞发生不可逆反应。从某种意义上讲,原位凋亡细胞检测可标记更早期的凋亡细胞[10]。本实验对40例不同分化程度的星形细胞瘤进行了凋亡细胞的原位检测(表1),结果显示:随着肿瘤恶性程度的增加(级数增高),凋亡细胞密度减少(图4,5),表明星形细胞瘤生长失调与细胞生存增加相关,提示瘤细胞的增殖和凋亡失衡,即瘤细胞无限制性增生和/或瘤细胞不能进入凋亡[2]。这可能是星形细胞瘤发生发展的重要因素。

, 百拇医药
图4 显示星形细胞瘤Ⅱ级凋亡细胞,呈深棕黄色。
(ISEL)法。×400
本实验在对凋亡细胞的原位检测中发现,瘤组织中有弥漫性着染(图5),有的呈浅棕黄色,见蓝染核,易于与凋亡细胞区别,有文献报道可能是由于固定不够及时或固定不够充分,导致细胞自溶,核内DNA 在内切酶作用下裂解;有的呈深棕色,无蓝染核存在,难于与凋亡细胞区别,文献指出可能是由于组织坏死、严重自溶或染色前蛋白酶K过消化所致。这种现象目前尚不能合理解释[9~11],有待进一步探讨分析。

图5 显示星形细胞瘤Ⅲ级凋亡细胞,呈深棕黄色。
伴弥漫性染色显浅棕黄色。 (ISEL)法。×400
, 百拇医药
参考文献:
[1]Hermann Steller. Mechanisms and genes of cellular suicide.Science, 1995;267 :1445~47
[2]Craig B. Thompson.Apoptosis in the pathogenesis and treatment ofdisease,Science, 1995;267:1456~58
[3]Claire M. Payne, Harris Bernstein, et al. Role of apoptosis in biology and pathology: Resistance to apoptosis in colon carcinogenesis. Ultrastruct Pathol,1995;19:221~25
, 百拇医药
[4]Schiffer D, Migheli A, Chio A, et al. Apoptosis and cell proliferation in human neuroepithelial tumors. Neuro- sci Lett,1995;195:81~85
[5]Chozick BS, Weicker ME, Pezzllo JC,et al. Pattern of mutant p53 expression in human astrocytomas suggests the exsistence of alternate pathways of tumorigenesis. Cancer,1994;73:406~10
[6]Pawel P, Liberski, Radzislaw Kordek. Ultrastructural pathology of glial brain tumors revisited:A review. Ultrastruct Pathol, 1997;21: 1~4
, 百拇医药
[7]黄文清. 神经系统的肿瘤,肿瘤电子显微镜诊断学.上海科学技术出版社. 1993:104~12
[8]Kerr JFR, Wyllie AH, Currie AR. Apoptosis: a basis biological phenomenon with wide-ranging implica- tions in tissue kinetics. Br J Cancer,1972;26:239~42
[9]Ricardo H Bardales, Su-su Xie, Su-ming HSU. In situ fragmentation assay for detection of apoptosis in paraffin-embedded tissue sections. Am J Pathol,1997;107:332~35
[10]Korsek R,Hironshi M, Yanagihara R, et al. Apoptosis in glialtumors as determined by in situ nonradioactive labeling of DNA breaks.Acta Neuro- pathol Berl,1996;91:112~113
[11]Henrik B. Hellquist, kaarina Sundelin, Alessandra Di Bacco, et al.Tumor growth fraction and apoptosis in salivary gland acinic cellcarcinomas. Prognostic implications of Ki-67 and bcl-2 expression and of in situ end labeling. J Pathol,1997;181:323~26
(收稿:1999-05-15), 百拇医药