重组反义c-myc 腺病毒对人胃癌细胞的体内及体外分子治疗*
作者:陈洁平*1 林 晨* 徐采朴 张雪艳 付明 邓 友平 隗月 吴旻
单位:陈洁平 徐采朴 第三军医大学西南医院消化科 重庆市 400038; 林 晨 张雪艳 付 明 邓 友平 隗 月 吴 旻 中国医学科学院肿瘤研究所细胞生物室 北京市 100021
关键词:胃肿瘤;腺病毒;反义c- myc;细胞凋亡;肿瘤移植
世界华人消化杂志990608 摘 要
目的 研究重组反义c-myc腺病毒对胃癌细胞的体内外生物学 作用.
方法 采用LacZ基因X-gal染色、MTT,DNA梯度降解试验、原位末 端标记、流式细胞仪、PCR分析、裸鼠致瘤性、裸鼠皮下移植瘤模型实验等方法,对反义c -myc重组腺病毒在人胃癌SGC7901细胞系中的作用进行体内外研究.
, 百拇医药
结果 Ad-AS c-myc对SGC7901细胞能产生明显的生长抑制作用,MT T显示生长抑制率为44.1%. DNA梯度降解试验、原位末端标记、流式细胞仪显示Ad-AS c -myc诱导了SGC7901细胞凋亡. 经Ad-AS c-myc处理的SGC7901细胞裸鼠致瘤性消失 . Ad-AS c-myc对裸鼠皮下移植瘤模型瘤内注射能有效降低肿瘤的生长速度,生长抑 制率为68.9%.
结论 Ad-AS c-myc对胃癌细胞具有显著的体内外生长抑制及凋亡 诱导作用.
中国图书馆分类号 R735.2
In vitro and in vivo molecular therapy with ASc-myc adenovirus for human gastric carcinoma cell line*
, 百拇医药 CHEN Jie-Ping*1,LIN Chen*2,XU Cai-Pu1,ZHANG Xue-Y an2,FU Ming2,DENG You-Ping2,KUI Yue2 and WU Min2
1Department of Gastroenterology, Southwest Hospital, Third Mil itary Medical University, Chongqing 400038, China
2National Laboratory of Molecular, Department of Cell Biology, Cancer Insi titute, Peking Union Medical College(PUMC) & Chinese Academy of Medical Sciencer s(CAMS), Beijing 100021,China
, http://www.100md.com
Subject headings adenovirus; antisense c-myc; apoptosis; neoplasm transplantation
Abstract
AIM To study the biological effects of recombinant antisen se c-myc adenovirus on human gastric cancer cell line in vitro and in vivo.
METHODS Human gastric cell line SGC7901 was treated with Ad-AS c-myc or Ad-LacZ X-gal stain, MTT, DNA ladder, Tunel, FCM, PCR, the tumo rigenicity in nude mice and experimental therapy on the nude mice model were stu died.
, 百拇医药
RESULTS Ad-AS c-myc could strongly inhibit cell growth an d induce apoptosis of SGC7901 cells. The inhibitory rate of the Ad-AS c-myc -infected SGC7901 cells was 44.1%. The tumorigenicity in nude mice using Ad-AS c-myc showed that all three mice failed to form tumors from 7 to 30 days as compared with Ad-LacZ and parent SGC7901 cells. Experimental therapy on the nude mice model bearing subcutaneous tumor of SGC7901 cells showed that intratumor instill ation of Ad-AS c-myc inhibited the growth of the tumors. Ad-AS c-myc -treated tumors were inhibited by 68.9%,compared with the tumors injec ted with Ad-LacZ and mock.
, 百拇医药
CONCLUSION The expression of Ad-AS c-myc can inhibit grow th and induce apoptosis of gastric cancer cells in vitro and in vivo.
0 引言
目前肿瘤发生的分子机制还不十分清楚,但越来越多的证据表明,它与多个癌基因的激活、 扩增及抑癌基因的失活有关[1]. 抑制癌基因表达,重建抑癌基因的功能是目前基 因治疗所追求的基本目标. 胃癌为常见恶性肿瘤,发病率及死亡率均居我国各种恶性肿瘤 的前列. 寻找有效的针对肿瘤细胞的目的基因,无疑对临床胃癌的防治具有重要意义. 序列 特异的DNA结合蛋白c-myc在细胞的增殖与分化过程中起着十分重要的调节作用. 反义 c-myc采用c-myc基因含有起始密码子的第2外显子及其两侧部分内含子序列共1.53kb片段构建而成,具有抑制c-myc表达的作用[2]. 本课题以胃癌细 胞系作为 靶细胞,腺病毒介导,研究反义c-myc对人胃癌细胞的体内外生物学作用. 探索腺病 毒介导反义c-myc治疗胃癌的可行性,为胃癌的基因治疗提供候选基因,并为胃癌基 因治疗的临床前研究提供实验依据.
, http://www.100md.com
1 材料和方法
1.1 细胞系 293细胞为腺 病毒E1基因转化的人胚肾细胞系. 培养条件为高糖DMEM培养基,含100mL/L胎牛血 清,37℃,5% CO2. SGC7901细胞为人胃腺癌细胞系. 培养条件为M199培养基,含100mL/L胎牛血清,37℃,5% CO2.
1.2 重组体腺病毒的制备 为E1和E3区缺失的复制缺陷型 5型腺病毒载体. 重组反义myc及LacZ腺病毒(Ad-AS c-myc及Ad-LacZ)均为中国医学 科学院肿瘤研究所细胞生物室构建,为E1和E3区缺失的复制缺陷型腺病毒载体构建而成. 采 用 Ad-AS c-myc及Ad-LacZ经鉴定为阳性的重组体腺病毒,在293细胞中繁殖. 稀释后 ,以293细胞进行滴度测定. 提取腺病毒DNA,用一对反义c-myc基因引物及一对腺病 毒基因组引物进行PCR扩增鉴定.
, http://www.100md.com
1.3 病毒感染 接种细胞于培养皿中,24h以内在 细胞贴壁后感染病毒,以一定的感染强度(multiplicity of infection, MOI)计算所需病毒 量. 置3°CO2孵箱中1h后加入完全培养基培养.
1.4 腺病毒转导效率测定 用重组腺病毒Ad-LacZ(含报 告基因LacZ),按25,50,100,200MOI感染细胞. 37℃孵箱中培养. 多聚甲醛固定. 加 入X-gal染液置37℃孵箱中2h. 用PBS清洗. 显微镜下观察,蓝染的细胞即LacZ 基因表达的阳性细胞. 分别计算蓝染细胞的百分率.
1.5 细胞生长曲线(MTT法) 采用96孔板,每孔接种细胞 ,孵箱中培养12h~24h后按上述方法4步骤用病毒感染细胞. 取不同时间点, 每孔加入150μLMTT溶液. 孵育3h~4h后每孔加入150μL DMSD. 以酶标仪测定每孔A(OD值). 计算细胞存活率.
, http://www.100md.com
1.6 细胞DNA梯度降解(DNA ladder)的检测[1,6] 取病毒感染组及对照组细胞,PBS洗后加裂解液400μL,离心收集上清. SDS及 RN A酶56℃作用1h. 蛋白酶K 37℃1h. 用乙醇沉淀DNA. 干燥后加TE20μL 溶解DNA沉淀. 琼脂糖凝胶电泳,长波紫外灯下观察并照相.
1.7 细胞凋亡原位检测(TUNEL试验)收集细胞用PBS洗后 将细胞悬液滴玻片上,4%多聚甲醇固定10min,干燥后PBS洗,穿透液冰上2min. 加10μLTunel反应混合液,用封口膜覆盖,置湿盒中,37℃,1h. 荧光显微镜下观察,摄 片. PBS洗,AP覆盖液10μL,37℃ 1h,封口膜覆盖. PBS洗,底物缓冲液50 μL,室温下10min~15min,苏木素复染,树脂封片.
1.8 流式细胞仪检测细胞周期及细胞凋亡 PI染色法:病毒感染细胞后收集细胞,注入予冷的700mL/L乙醇,固定15h以 上. 离心弃乙醇后用PBS洗少许PBS重悬转入Eppendorf管中. 加入RNA酶37℃作用1h. 加入PI 100μL混匀置冰上,流式细胞仪检测.
, http://www.100md.com
1.9 PCR分析 PCR条件:25μL反应体系中含DNA 2μL,10×PCR buffer,15mmol/L MgCl2,4种dNTPs各25μmol/L ,加目的基因引物50pmol/L及1UTaq DNA多聚酶,反应在PCR仪中进行. 95℃预变性5min,95℃ 1min,56℃ 1min,72℃ 1min,28~30个循环后72℃延伸7min. PCR产物鉴定及定量分析:PCR产物用琼脂糖凝胶电泳检测,在长波紫外灯下观测并照相.
1.10 裸鼠皮下致瘤实验裸小鼠,品系为Balb/c,5周龄~6周龄,雌雄随机,由中国医学科学院肿瘤研究所动物室提供. 接种SGC7901 细胞于60mm培养皿中,贴壁后弃培养液,按MOI100分别感染Ad-AS c-myc,Ad -LacZ及PBS(Mock),于37℃孵箱中作用后加入培养液,24h内消化细胞,制成10×10 9细胞/L的细胞悬液. 5周龄♂裸鼠12只,随机分为4组,每组3只,分别注射Ad-ASc-m yc, Ad-LacZ及PBS各0.1mL. 连续观察肿瘤出现时间和体积,时间为1mo.
, 百拇医药
1.11 裸鼠皮下移植瘤模型治疗实验 收集对数生长期SGC 79 01细胞,PBS(Mock)清洗后制成1×1010细胞/L的细胞悬液,按100μL/ 只量接 种于裸鼠皮下. 裸鼠均为5周龄鼠,共23只. 雌雄各半. 待肿瘤长至5mm左右时,取其 中20只肿瘤体积较为均一的裸鼠,随机分为4组,每组5只, 瘤体内注射腺病毒液或PBS 0.1mL,病毒液含量为109pfu/只,隔日注射1次,共 3次,连续观察肿瘤大小,持续1mo.
统计学处理 采用计算机统计程序进行χ2检验及t检验.
2 结果
2.1 重组体腺病毒的制备 Ad-AS c-myc及Ad-LacZ重组体腺病毒,经293细胞繁殖后制备成病毒贮存液. 各重组 体腺病毒滴度测定为Ad-AS c-myc3.0×109pfu/mL,Ad-LacZ 3.0×1 011pfu/mL提取各重组体腺病毒DNA,分别以腺病毒及反义c-myc的 引物进 行PCR鉴定,结果Ad-LacZ可见腺病毒阳性扩增条带,Ad-AS c-myc可见腺病毒及AS c-myc阳性扩增条带.
, http://www.100md.com
2.2 重组体腺病毒的转导效率 采用插入LacZ报告基因的 重组体腺病毒,进行重组体腺病毒对不同细胞转导效率的检测. 以Ad-LacZ按感染强度(Mul tiplicity of Infection, MOI)25,50,100,200的量分别感染SGC7901细胞,48h后 进行X-gal染色显示转染效率分别为90,100,100,100.
2.3 腺病毒介导反义c-myc对胃癌细胞的生物学作 用
2.3.1 Ad-AS c-myc感染后胃癌细胞的形态学变化 以Ad-AS c-myc,Ad-LacZ及PBS处理SGC7901细胞,在倒置显微镜下观察细胞 形态. SGC7901细胞在Ad-AS c-myc持续作用1d~3d开始发生细胞形态变 化,表现为细胞聚集、细胞间隙增大、胞体变圆,部分细胞体积变大,细胞内出现空泡,持 续4d~5d后大部分细胞脱落死亡,而Ad-LacZ及PBS处理组细胞形态无明显变 化.
, 百拇医药
2.3.2 Ad-AS c-myc对胃癌细胞生长的抑制作用 采用MTT法,对Ad-AS c-myc,Ad-LacZ,PBS作用的SGC7901细胞进行检测,时间点为 2,4,6,8d. Ad-AS c-myc对SGC7901细胞生长抑制率可达44.1%. 与Ad-Lac Z比P<0.01(表1).
表1 Ad-AS c-myc对SGC7901细胞生长的抑制作用 ( ±s) MOI
±s) MOI
Ad-AS c-myc
Ad-LacZ
A
Survival (%)
A
, 百拇医药
Survival (%)
25
1.26±0.04
98.4±2.8
1.28±0.09
100±7.0
50
1.24±0.06
97.1±5.0
1.27±0.08
99±5.9
100
, 百拇医药
1.05±0.07
81.6±5.7a
1.25±0.04
97.6±2.7
200
0.72±0.07
55.9±5.5b
1.21±0.08
94.1±6.3
aP<0.05 vs Ad-LacZ bP<0.01 vs Ad-LacZ.
, http://www.100md.com
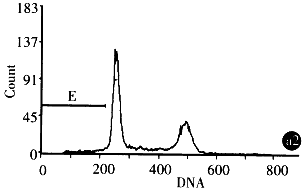
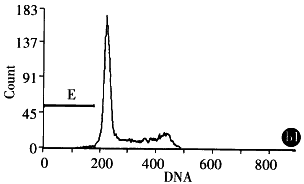
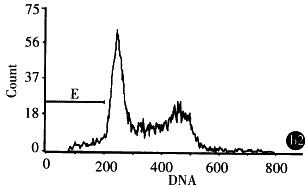
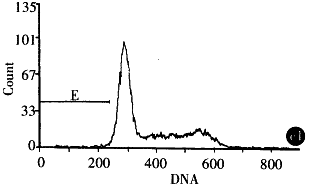
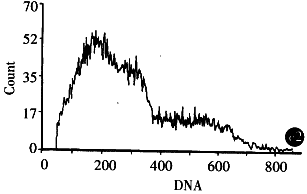
2.3.3 Ad-AS c-myc对SGC7901细胞的凋亡诱导作用 ①DNA梯度降解试验:提取细胞染色体DNA进行琼脂糖凝胶电泳结果发现,SGC7901细胞经A d-AS c-myc处理2后染色体DNA发生断裂,2,4,6d电泳可见180bp~200 bp 不同倍体梯状DNA(DNA Ladder),DNA Ladder的出现有一定的时间效应,以6d时明显 ,Ad-LacZ处理组染色体DNA未见明显的DNA Ladder. ②细胞凋亡原位末端标记:细胞发生 凋亡时,染色体DNA在核小体之间发生断裂,形成以核小体为单位的不同长度的DNA片断,同 时产生多个3-OH末端,使用末端转移酶可将标记的dUTP连接在DNA片段的3-OH末端上,显 色显示凋亡细胞,经Ad-AS c-myc处理的SGC7901细胞Tunel试验可见明显的细胞凋亡现象. ③流式细胞仪检测:将SGC7901细胞分为Ad-AS c-myc,Ad-LacZ 及细胞对照组, 以MOI 100感染细胞,不同时间点收获细胞,PI染色处理后于FCM上检测,结果显示Ad-AS c-myc处理组48h内细胞周期无明显改变,4,6d可见S、G2M期阻滞. 2 d开始出现凋亡,凋亡高峰在6d,2,4,6d凋亡率分别为1.6%,2.9%,50 .7%(图1).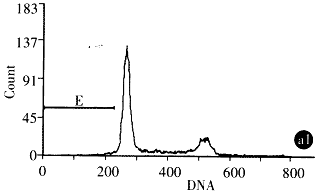
, 百拇医药
图1 经Ad-AS C-myc感染的SGC7901的流式细胞仪检测(A,B,C:Ad-Lac Z or Ad-AS c-myc 2,4,6d).
2.4 腺病毒介导反义c-myc对体内胃癌细胞生长的抑制作用
2.4.1 裸鼠皮下致瘤实验 将经Ad-AS c-myc及Ad -LacZ以MOI100的感染强度处理的SGC7901细胞,分别注射于3组裸鼠皮下,每组3只,每只 注射1010细胞/L的细胞悬液100μL,另1组3只各注射PBS100μL,结 果显示,1mo后Ad-AS c-myc处理的SGC7901细胞裸鼠成瘤率为零,而Ad-LacZ 及PBS处理组成瘤为100%(表2).
表2 Ad-AS c-myc处理后裸鼠致瘤检测 Infected
virus
, 百拇医药
cell number
tumorigenic-
ity/mice
Tumorigenic-
it y(%)
tumor
weight(g)
Ad-AS c-myc
106
0/3
0
0
, 百拇医药
Ad-LacZ
106
3/3
100
0.947
Mock
106
3/3
100
0.580
2.4.2 裸鼠皮下移植瘤模型的治疗实验 将SGC/7901细胞制成1010细胞/L的细胞悬液,每只0.1mL的量分别注射于裸鼠皮下. 待肿瘤 长至5mm左右时取肿体较为均一的20只裸鼠. 随机分为4组,每组5只. 分别瘤体内注射 100μLAd-AS c-myc,Ad-LacZ及PBS(Mock). 每4d测量1次肿瘤大小, 持续1mo,根据公式计算肿瘤体积. Ad-ASc-myc对裸鼠皮下移植瘤模型的治疗结果显示,1mo后肿瘤小于对照组,Ad-ASc-myc对肿瘤生长的抑制率为68.9% (表3).表3 Ad-AS c-myc对裸鼠SGC7901肿瘤的体内治疗
, 百拇医药
Infected
virus
Tumor Size(cm3) on different days
0
4
8
12
16
20
24
28
Ad-AS c-myc
, 百拇医药
0.36
0.44
0.81a
1.80b
2.88b
3.28b
6.49b
7.78b
Ad-HacZ
0.39
0.95
, 百拇医药
2.76
5.89
9.73
14.25
17.65
20.60
Mock
0.36
0.86
2.12
5.87
10.25
14.89
, 百拇医药
17.90
25.01
aP<0.05 vs Ad-LacZ or Mock;bP<0.01 vs Ad-LacZ or Mock.
3 讨论
腺病毒载体是继逆转录病毒载体后,发展得较快的载体系统. 它以遗传毒性低,致病性小, 宿主范围广,滴度高,装载容量大等优势已广泛用于基因治疗[3]. 1993年美国NIH 的RAC通过了首例腺病毒载体进行基因治疗的临床方案. 目前腺病毒载体已成为最有应用前 景的 病毒载体. 在肿瘤的基因治疗中,基因的转移主要采取将目的基因直接转移至宿主体内的 in vivo方式. 要求选择的载体高效转导,只有这样才能满足临床肿瘤基因治疗的需要. 为此,我们选择了腺病毒作为反义c-myc基因的载体系统. 在研究中发现,腺病毒转导效 率高,能将目的基因转移到几乎100%的肿瘤细胞,通过使用LacZ重组腺病毒转导SGC7901细 胞显示MOI 25时,培养细胞的转导效率即高达90%以上. Ad-ASc-myc对SGC7901细胞有明显 的生长抑制及凋亡诱导作用,可能与Ad-AS c-myc为SGC7901细胞的高效转导有关.
, 百拇医药
胃癌的发生是多因素、多阶段及多基因变异的综合病变过程. 多种癌基因及抑癌基因的异常 累积是 癌变过程的重要机制[1]. 从慢性胃粘膜疾病逐渐演化成胃癌需要较长的时间,在这一病变过程中有多少基因参与病变过程,哪些是重要的肿瘤相关性基因,它们以何种方式发生变异,这是肿瘤基因治疗的前提. 据此重建抑癌基因功能及抑制癌基因表达的反义RNA或DNA技术,成为目前胃癌基因治疗所追求的基本目标. 基因治疗不同于单基因遗传病,除基因载体, 导入手段外,目的基因的选择较为复杂,由于肿瘤的个体差异较大,不同的肿瘤及同一肿瘤的不同阶段,可能起作用的基因也不一样,因此,目的基因的确定极为关键. c-myc基因不仅在细胞转化、增殖、分化和细胞周期进程中起着重要的作用,而且还参与了凋亡[4,5]. 刺激 c-myc蛋白出现和c-myc表达水平提高,均可诱导细 胞凋亡,而间接导致c-myc蛋白产生一个急剧由高浓度到低浓度的浓度差,也会诱导 细胞凋亡[4,5]. 用反义RNA技术人为降低肿瘤细胞中c-myc的过量表达,有可能阻止肿瘤的异常增殖[6]. 针对胃癌中存在癌基因c-myc扩增[7] ,我们选用癌基因 c-myc高表达的人胃癌细胞系SGC7901,以c-myc第二外显 子和其两侧部分内含子序列共1.53Kb的反义RNA片断,构建反义c-myc重组腺 病毒. 实验结果显示,反义c-myc重组腺病毒in vitro及in vivo对肿瘤细胞 生长均有显著的抑制作用. 体外对胃癌细胞的生长抑制率为44.1%. 对裸鼠体内致瘤性为 零,裸鼠皮下移植瘤生长抑制率为68.9%. 表明反义c-myc重组腺病毒具有显著的抑制 胃癌细胞生长的作用. 从理论上讲,其在体内的作用方式可能有3种:首先,与mRNA互补, 阻断c-mycmRNA前体,同时阻断c-myc蛋白的翻译. 其次反义RNA链与c-myc DNA双链形成三股螺旋,从而干预c-myc基因的表达. 第三反义RNA翻 译成新的蛋白质,与myc蛋白竞争靶位或相互作用. 细胞DNA梯度降解试验、细胞凋 亡原位检测及流式细胞仪检测均显示反义c-myc腺病毒在抑制胃癌细胞生长的同时诱 导了凋亡. 产生这种作用的解释是在myc蛋白上促进增殖、引起共转化和诱导分化并起动凋亡的功能域紧密相连、部分重叠,因而它能驱动两个截然相反的生命过程. 文献也报道了应用反义c-mycRNA(与我们不同的c-myc基因序列部分)及反义c-myc寡核苷 酸有效抑制肿瘤细胞的增殖,并诱导分化和凋亡[6-8]. 但这些实验均未采用c-myc的大片段反义序列,也无系统的体内研究. 采用反义c-myc RNA进行胃癌 的基因治疗未见文献报告. 还有作者报告采用反义C-Ha-ras DNA,H-ras反义RNA逆转录病毒、PCNA特异性反义寡核苷酸可以部分逆转胃癌细胞的恶性表型[9,10]. 与我 们用反义c-myc腺病毒得到的研究结果一致. 这些结果表明:针对不同的癌基因高表达 及扩增,利用反义RNA或DNA技术,可部分阻断肿瘤细胞的恶性增殖.
, http://www.100md.com
本结果表明,Ad-AS c-myc对c-myc基因高表达的SGC7901细胞具有很强的体内外生长抑制及凋亡诱导作用. 我们的实验结果证实Ad-AS c-myc在用于胃癌基因治疗的方面具有良好的应用价值.
作者简介:*陈洁平 林晨均为第一作者
陈洁平,女,1963-05-10生,贵州省贵阳市人,汉族. 1988年遵义医学院本 科毕业,1995年第三军医大学西南医院消化科硕士,1998年博士,讲师. 主治医师,主要从 事幽门螺杆菌及胃癌研究,发表论文30篇.
*国家863高科技发展基金,No.Z20-01-02
通讯作者 陈洁平,400038,第三军医大学西南医院消化科.
*Supported by the National 863 High Science and Technology Foundat ion of China, No. Z20-01-02
, http://www.100md.com
Correspondence to:Dr. CHEN Jie-Ping, Department of Gastroentero logy, Southwest Hospital, Third Military Medical University, Chongqing 400038, China
Tel. +86.23.65318301. Ext 73094
E-mail jpchen@public.cta.cq.cn
4 参考文献
1 Anderson WF Gene therapy of cance Ther. Hum Gene Ther, 1994;5:1-2
, 百拇医药
2 Feng L, Wang XQ, Fu M,Wang ZH, Tian Y, Cai Y, WuM A strategy for isolating di fferentiation-inducing complementary DNAs from human esophageal cancer cell lin e treated with retinoic acid, ZHONG GUO KE TUE(B), 1992;35:445-454
3 Brody SL, Crystal RG. Adenovirus-mediated in vivo gene transfer. Ann NY Acad Sci, 1994;716:90-101
4 Ryan KM, Birnie GD. myc oncogens: the enigmatic family. Biochem J, 1996;314:713-721
, 百拇医药
5 Xu Y, Nguyen Q, Lo DC, Czaja MJ. C-myc-dependent hepatoma cell apoptosi s results from oxidative stress and not a deficiency of growth factors. J Cel l Physiol, 1997;170:192-199
6 VanWaardenburg RC, Meijer C, Burger H, Nooter K, De Vries EG, Mulder NH, De J o ng S. Effects of an inducible antisense c-myc gene transfer in a drug-resis tant human small-cell-carcinoma cell line. Int J Cancer, 1997;14:73:544-550
7 Onoda N, Maeda K, Chung YS, Yano Y, Matsui Yuasa I, Otani S, Sowa M. Overexpr ession of c-myc messenger RNA in primary and metastatic Lesions of carcinom a of the stomach. J Am Coll Surg, 1996;182:55-59
, http://www.100md.com
8 Leonetti C, D'Agnano I, Lozupone F, Valentini A, Geiser T, Zon G, Calabretta B, Citro G C, Zupi G. Antitumor effect of c-myc antisense phosphoothioate o ligocdeoxynuleotide on human melanoma cells in vitro and in mice. J Natl Cancer Inst, 1996;88:419-429
9 李文梅,吕有勇. 导入Rb,P53,P16和H-ras反义RNA对人胃癌细胞恶性增 殖的影响,中国肿瘤生物治疗杂志,1997;4:90-94
10 Sakakura C, A, Hagjwara A, Tsujimoto H, Ozaki K Sakakibara T, Oyama T, Ogaki T, Ogaki M, Takahashi T. The anti-proliferative effect of proliferatin g cell nuclear antigenspecific antisence oligonucleotides on human gastric cance r cell lines. Surg Today, 1995;25:184-186
收稿日期 1998-12-22 修回日期 1999-03-06, 百拇医药(陈洁平*1 林 晨* 徐采朴 张雪艳 付明 邓 友平 隗月 吴旻)
单位:陈洁平 徐采朴 第三军医大学西南医院消化科 重庆市 400038; 林 晨 张雪艳 付 明 邓 友平 隗 月 吴 旻 中国医学科学院肿瘤研究所细胞生物室 北京市 100021
关键词:胃肿瘤;腺病毒;反义c- myc;细胞凋亡;肿瘤移植
世界华人消化杂志990608 摘 要
目的 研究重组反义c-myc腺病毒对胃癌细胞的体内外生物学 作用.
方法 采用LacZ基因X-gal染色、MTT,DNA梯度降解试验、原位末 端标记、流式细胞仪、PCR分析、裸鼠致瘤性、裸鼠皮下移植瘤模型实验等方法,对反义c -myc重组腺病毒在人胃癌SGC7901细胞系中的作用进行体内外研究.
, 百拇医药
结果 Ad-AS c-myc对SGC7901细胞能产生明显的生长抑制作用,MT T显示生长抑制率为44.1%. DNA梯度降解试验、原位末端标记、流式细胞仪显示Ad-AS c -myc诱导了SGC7901细胞凋亡. 经Ad-AS c-myc处理的SGC7901细胞裸鼠致瘤性消失 . Ad-AS c-myc对裸鼠皮下移植瘤模型瘤内注射能有效降低肿瘤的生长速度,生长抑 制率为68.9%.
结论 Ad-AS c-myc对胃癌细胞具有显著的体内外生长抑制及凋亡 诱导作用.
中国图书馆分类号 R735.2
In vitro and in vivo molecular therapy with ASc-myc adenovirus for human gastric carcinoma cell line*
, 百拇医药 CHEN Jie-Ping*1,LIN Chen*2,XU Cai-Pu1,ZHANG Xue-Y an2,FU Ming2,DENG You-Ping2,KUI Yue2 and WU Min2
1Department of Gastroenterology, Southwest Hospital, Third Mil itary Medical University, Chongqing 400038, China
2National Laboratory of Molecular, Department of Cell Biology, Cancer Insi titute, Peking Union Medical College(PUMC) & Chinese Academy of Medical Sciencer s(CAMS), Beijing 100021,China
, http://www.100md.com
Subject headings adenovirus; antisense c-myc; apoptosis; neoplasm transplantation
Abstract
AIM To study the biological effects of recombinant antisen se c-myc adenovirus on human gastric cancer cell line in vitro and in vivo.
METHODS Human gastric cell line SGC7901 was treated with Ad-AS c-myc or Ad-LacZ X-gal stain, MTT, DNA ladder, Tunel, FCM, PCR, the tumo rigenicity in nude mice and experimental therapy on the nude mice model were stu died.
, 百拇医药
RESULTS Ad-AS c-myc could strongly inhibit cell growth an d induce apoptosis of SGC7901 cells. The inhibitory rate of the Ad-AS c-myc -infected SGC7901 cells was 44.1%. The tumorigenicity in nude mice using Ad-AS c-myc showed that all three mice failed to form tumors from 7 to 30 days as compared with Ad-LacZ and parent SGC7901 cells. Experimental therapy on the nude mice model bearing subcutaneous tumor of SGC7901 cells showed that intratumor instill ation of Ad-AS c-myc inhibited the growth of the tumors. Ad-AS c-myc -treated tumors were inhibited by 68.9%,compared with the tumors injec ted with Ad-LacZ and mock.
, 百拇医药
CONCLUSION The expression of Ad-AS c-myc can inhibit grow th and induce apoptosis of gastric cancer cells in vitro and in vivo.
0 引言
目前肿瘤发生的分子机制还不十分清楚,但越来越多的证据表明,它与多个癌基因的激活、 扩增及抑癌基因的失活有关[1]. 抑制癌基因表达,重建抑癌基因的功能是目前基 因治疗所追求的基本目标. 胃癌为常见恶性肿瘤,发病率及死亡率均居我国各种恶性肿瘤 的前列. 寻找有效的针对肿瘤细胞的目的基因,无疑对临床胃癌的防治具有重要意义. 序列 特异的DNA结合蛋白c-myc在细胞的增殖与分化过程中起着十分重要的调节作用. 反义 c-myc采用c-myc基因含有起始密码子的第2外显子及其两侧部分内含子序列共1.53kb片段构建而成,具有抑制c-myc表达的作用[2]. 本课题以胃癌细 胞系作为 靶细胞,腺病毒介导,研究反义c-myc对人胃癌细胞的体内外生物学作用. 探索腺病 毒介导反义c-myc治疗胃癌的可行性,为胃癌的基因治疗提供候选基因,并为胃癌基 因治疗的临床前研究提供实验依据.
, http://www.100md.com
1 材料和方法
1.1 细胞系 293细胞为腺 病毒E1基因转化的人胚肾细胞系. 培养条件为高糖DMEM培养基,含100mL/L胎牛血 清,37℃,5% CO2. SGC7901细胞为人胃腺癌细胞系. 培养条件为M199培养基,含100mL/L胎牛血清,37℃,5% CO2.
1.2 重组体腺病毒的制备 为E1和E3区缺失的复制缺陷型 5型腺病毒载体. 重组反义myc及LacZ腺病毒(Ad-AS c-myc及Ad-LacZ)均为中国医学 科学院肿瘤研究所细胞生物室构建,为E1和E3区缺失的复制缺陷型腺病毒载体构建而成. 采 用 Ad-AS c-myc及Ad-LacZ经鉴定为阳性的重组体腺病毒,在293细胞中繁殖. 稀释后 ,以293细胞进行滴度测定. 提取腺病毒DNA,用一对反义c-myc基因引物及一对腺病 毒基因组引物进行PCR扩增鉴定.
, http://www.100md.com
1.3 病毒感染 接种细胞于培养皿中,24h以内在 细胞贴壁后感染病毒,以一定的感染强度(multiplicity of infection, MOI)计算所需病毒 量. 置3°CO2孵箱中1h后加入完全培养基培养.
1.4 腺病毒转导效率测定 用重组腺病毒Ad-LacZ(含报 告基因LacZ),按25,50,100,200MOI感染细胞. 37℃孵箱中培养. 多聚甲醛固定. 加 入X-gal染液置37℃孵箱中2h. 用PBS清洗. 显微镜下观察,蓝染的细胞即LacZ 基因表达的阳性细胞. 分别计算蓝染细胞的百分率.
1.5 细胞生长曲线(MTT法) 采用96孔板,每孔接种细胞 ,孵箱中培养12h~24h后按上述方法4步骤用病毒感染细胞. 取不同时间点, 每孔加入150μLMTT溶液. 孵育3h~4h后每孔加入150μL DMSD. 以酶标仪测定每孔A(OD值). 计算细胞存活率.
, http://www.100md.com
1.6 细胞DNA梯度降解(DNA ladder)的检测[1,6] 取病毒感染组及对照组细胞,PBS洗后加裂解液400μL,离心收集上清. SDS及 RN A酶56℃作用1h. 蛋白酶K 37℃1h. 用乙醇沉淀DNA. 干燥后加TE20μL 溶解DNA沉淀. 琼脂糖凝胶电泳,长波紫外灯下观察并照相.
1.7 细胞凋亡原位检测(TUNEL试验)收集细胞用PBS洗后 将细胞悬液滴玻片上,4%多聚甲醇固定10min,干燥后PBS洗,穿透液冰上2min. 加10μLTunel反应混合液,用封口膜覆盖,置湿盒中,37℃,1h. 荧光显微镜下观察,摄 片. PBS洗,AP覆盖液10μL,37℃ 1h,封口膜覆盖. PBS洗,底物缓冲液50 μL,室温下10min~15min,苏木素复染,树脂封片.
1.8 流式细胞仪检测细胞周期及细胞凋亡 PI染色法:病毒感染细胞后收集细胞,注入予冷的700mL/L乙醇,固定15h以 上. 离心弃乙醇后用PBS洗少许PBS重悬转入Eppendorf管中. 加入RNA酶37℃作用1h. 加入PI 100μL混匀置冰上,流式细胞仪检测.
, http://www.100md.com
1.9 PCR分析 PCR条件:25μL反应体系中含DNA 2μL,10×PCR buffer,15mmol/L MgCl2,4种dNTPs各25μmol/L ,加目的基因引物50pmol/L及1UTaq DNA多聚酶,反应在PCR仪中进行. 95℃预变性5min,95℃ 1min,56℃ 1min,72℃ 1min,28~30个循环后72℃延伸7min. PCR产物鉴定及定量分析:PCR产物用琼脂糖凝胶电泳检测,在长波紫外灯下观测并照相.
1.10 裸鼠皮下致瘤实验裸小鼠,品系为Balb/c,5周龄~6周龄,雌雄随机,由中国医学科学院肿瘤研究所动物室提供. 接种SGC7901 细胞于60mm培养皿中,贴壁后弃培养液,按MOI100分别感染Ad-AS c-myc,Ad -LacZ及PBS(Mock),于37℃孵箱中作用后加入培养液,24h内消化细胞,制成10×10 9细胞/L的细胞悬液. 5周龄♂裸鼠12只,随机分为4组,每组3只,分别注射Ad-ASc-m yc, Ad-LacZ及PBS各0.1mL. 连续观察肿瘤出现时间和体积,时间为1mo.
, 百拇医药
1.11 裸鼠皮下移植瘤模型治疗实验 收集对数生长期SGC 79 01细胞,PBS(Mock)清洗后制成1×1010细胞/L的细胞悬液,按100μL/ 只量接 种于裸鼠皮下. 裸鼠均为5周龄鼠,共23只. 雌雄各半. 待肿瘤长至5mm左右时,取其 中20只肿瘤体积较为均一的裸鼠,随机分为4组,每组5只, 瘤体内注射腺病毒液或PBS 0.1mL,病毒液含量为109pfu/只,隔日注射1次,共 3次,连续观察肿瘤大小,持续1mo.
统计学处理 采用计算机统计程序进行χ2检验及t检验.
2 结果
2.1 重组体腺病毒的制备 Ad-AS c-myc及Ad-LacZ重组体腺病毒,经293细胞繁殖后制备成病毒贮存液. 各重组 体腺病毒滴度测定为Ad-AS c-myc3.0×109pfu/mL,Ad-LacZ 3.0×1 011pfu/mL提取各重组体腺病毒DNA,分别以腺病毒及反义c-myc的 引物进 行PCR鉴定,结果Ad-LacZ可见腺病毒阳性扩增条带,Ad-AS c-myc可见腺病毒及AS c-myc阳性扩增条带.
, http://www.100md.com
2.2 重组体腺病毒的转导效率 采用插入LacZ报告基因的 重组体腺病毒,进行重组体腺病毒对不同细胞转导效率的检测. 以Ad-LacZ按感染强度(Mul tiplicity of Infection, MOI)25,50,100,200的量分别感染SGC7901细胞,48h后 进行X-gal染色显示转染效率分别为90,100,100,100.
2.3 腺病毒介导反义c-myc对胃癌细胞的生物学作 用
2.3.1 Ad-AS c-myc感染后胃癌细胞的形态学变化 以Ad-AS c-myc,Ad-LacZ及PBS处理SGC7901细胞,在倒置显微镜下观察细胞 形态. SGC7901细胞在Ad-AS c-myc持续作用1d~3d开始发生细胞形态变 化,表现为细胞聚集、细胞间隙增大、胞体变圆,部分细胞体积变大,细胞内出现空泡,持 续4d~5d后大部分细胞脱落死亡,而Ad-LacZ及PBS处理组细胞形态无明显变 化.
, 百拇医药
2.3.2 Ad-AS c-myc对胃癌细胞生长的抑制作用 采用MTT法,对Ad-AS c-myc,Ad-LacZ,PBS作用的SGC7901细胞进行检测,时间点为 2,4,6,8d. Ad-AS c-myc对SGC7901细胞生长抑制率可达44.1%. 与Ad-Lac Z比P<0.01(表1).
表1 Ad-AS c-myc对SGC7901细胞生长的抑制作用 (
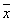 ±s) MOI
±s) MOIAd-AS c-myc
Ad-LacZ
A
Survival (%)
A
, 百拇医药
Survival (%)
25
1.26±0.04
98.4±2.8
1.28±0.09
100±7.0
50
1.24±0.06
97.1±5.0
1.27±0.08
99±5.9
100
, 百拇医药
1.05±0.07
81.6±5.7a
1.25±0.04
97.6±2.7
200
0.72±0.07
55.9±5.5b
1.21±0.08
94.1±6.3
aP<0.05 vs Ad-LacZ bP<0.01 vs Ad-LacZ.
, http://www.100md.com
2.3.3 Ad-AS c-myc对SGC7901细胞的凋亡诱导作用 ①DNA梯度降解试验:提取细胞染色体DNA进行琼脂糖凝胶电泳结果发现,SGC7901细胞经A d-AS c-myc处理2后染色体DNA发生断裂,2,4,6d电泳可见180bp~200 bp 不同倍体梯状DNA(DNA Ladder),DNA Ladder的出现有一定的时间效应,以6d时明显 ,Ad-LacZ处理组染色体DNA未见明显的DNA Ladder. ②细胞凋亡原位末端标记:细胞发生 凋亡时,染色体DNA在核小体之间发生断裂,形成以核小体为单位的不同长度的DNA片断,同 时产生多个3-OH末端,使用末端转移酶可将标记的dUTP连接在DNA片段的3-OH末端上,显 色显示凋亡细胞,经Ad-AS c-myc处理的SGC7901细胞Tunel试验可见明显的细胞凋亡现象. ③流式细胞仪检测:将SGC7901细胞分为Ad-AS c-myc,Ad-LacZ 及细胞对照组, 以MOI 100感染细胞,不同时间点收获细胞,PI染色处理后于FCM上检测,结果显示Ad-AS c-myc处理组48h内细胞周期无明显改变,4,6d可见S、G2M期阻滞. 2 d开始出现凋亡,凋亡高峰在6d,2,4,6d凋亡率分别为1.6%,2.9%,50 .7%(图1).






, 百拇医药
图1 经Ad-AS C-myc感染的SGC7901的流式细胞仪检测(A,B,C:Ad-Lac Z or Ad-AS c-myc 2,4,6d).
2.4 腺病毒介导反义c-myc对体内胃癌细胞生长的抑制作用
2.4.1 裸鼠皮下致瘤实验 将经Ad-AS c-myc及Ad -LacZ以MOI100的感染强度处理的SGC7901细胞,分别注射于3组裸鼠皮下,每组3只,每只 注射1010细胞/L的细胞悬液100μL,另1组3只各注射PBS100μL,结 果显示,1mo后Ad-AS c-myc处理的SGC7901细胞裸鼠成瘤率为零,而Ad-LacZ 及PBS处理组成瘤为100%(表2).
表2 Ad-AS c-myc处理后裸鼠致瘤检测 Infected
virus
, 百拇医药
cell number
tumorigenic-
ity/mice
Tumorigenic-
it y(%)
tumor
weight(g)
Ad-AS c-myc
106
0/3
0
0
, 百拇医药
Ad-LacZ
106
3/3
100
0.947
Mock
106
3/3
100
0.580
2.4.2 裸鼠皮下移植瘤模型的治疗实验 将SGC/7901细胞制成1010细胞/L的细胞悬液,每只0.1mL的量分别注射于裸鼠皮下. 待肿瘤 长至5mm左右时取肿体较为均一的20只裸鼠. 随机分为4组,每组5只. 分别瘤体内注射 100μLAd-AS c-myc,Ad-LacZ及PBS(Mock). 每4d测量1次肿瘤大小, 持续1mo,根据公式计算肿瘤体积. Ad-ASc-myc对裸鼠皮下移植瘤模型的治疗结果显示,1mo后肿瘤小于对照组,Ad-ASc-myc对肿瘤生长的抑制率为68.9% (表3).表3 Ad-AS c-myc对裸鼠SGC7901肿瘤的体内治疗
, 百拇医药
Infected
virus
Tumor Size(cm3) on different days
0
4
8
12
16
20
24
28
Ad-AS c-myc
, 百拇医药
0.36
0.44
0.81a
1.80b
2.88b
3.28b
6.49b
7.78b
Ad-HacZ
0.39
0.95
, 百拇医药
2.76
5.89
9.73
14.25
17.65
20.60
Mock
0.36
0.86
2.12
5.87
10.25
14.89
, 百拇医药
17.90
25.01
aP<0.05 vs Ad-LacZ or Mock;bP<0.01 vs Ad-LacZ or Mock.
3 讨论
腺病毒载体是继逆转录病毒载体后,发展得较快的载体系统. 它以遗传毒性低,致病性小, 宿主范围广,滴度高,装载容量大等优势已广泛用于基因治疗[3]. 1993年美国NIH 的RAC通过了首例腺病毒载体进行基因治疗的临床方案. 目前腺病毒载体已成为最有应用前 景的 病毒载体. 在肿瘤的基因治疗中,基因的转移主要采取将目的基因直接转移至宿主体内的 in vivo方式. 要求选择的载体高效转导,只有这样才能满足临床肿瘤基因治疗的需要. 为此,我们选择了腺病毒作为反义c-myc基因的载体系统. 在研究中发现,腺病毒转导效 率高,能将目的基因转移到几乎100%的肿瘤细胞,通过使用LacZ重组腺病毒转导SGC7901细 胞显示MOI 25时,培养细胞的转导效率即高达90%以上. Ad-ASc-myc对SGC7901细胞有明显 的生长抑制及凋亡诱导作用,可能与Ad-AS c-myc为SGC7901细胞的高效转导有关.
, 百拇医药
胃癌的发生是多因素、多阶段及多基因变异的综合病变过程. 多种癌基因及抑癌基因的异常 累积是 癌变过程的重要机制[1]. 从慢性胃粘膜疾病逐渐演化成胃癌需要较长的时间,在这一病变过程中有多少基因参与病变过程,哪些是重要的肿瘤相关性基因,它们以何种方式发生变异,这是肿瘤基因治疗的前提. 据此重建抑癌基因功能及抑制癌基因表达的反义RNA或DNA技术,成为目前胃癌基因治疗所追求的基本目标. 基因治疗不同于单基因遗传病,除基因载体, 导入手段外,目的基因的选择较为复杂,由于肿瘤的个体差异较大,不同的肿瘤及同一肿瘤的不同阶段,可能起作用的基因也不一样,因此,目的基因的确定极为关键. c-myc基因不仅在细胞转化、增殖、分化和细胞周期进程中起着重要的作用,而且还参与了凋亡[4,5]. 刺激 c-myc蛋白出现和c-myc表达水平提高,均可诱导细 胞凋亡,而间接导致c-myc蛋白产生一个急剧由高浓度到低浓度的浓度差,也会诱导 细胞凋亡[4,5]. 用反义RNA技术人为降低肿瘤细胞中c-myc的过量表达,有可能阻止肿瘤的异常增殖[6]. 针对胃癌中存在癌基因c-myc扩增[7] ,我们选用癌基因 c-myc高表达的人胃癌细胞系SGC7901,以c-myc第二外显 子和其两侧部分内含子序列共1.53Kb的反义RNA片断,构建反义c-myc重组腺 病毒. 实验结果显示,反义c-myc重组腺病毒in vitro及in vivo对肿瘤细胞 生长均有显著的抑制作用. 体外对胃癌细胞的生长抑制率为44.1%. 对裸鼠体内致瘤性为 零,裸鼠皮下移植瘤生长抑制率为68.9%. 表明反义c-myc重组腺病毒具有显著的抑制 胃癌细胞生长的作用. 从理论上讲,其在体内的作用方式可能有3种:首先,与mRNA互补, 阻断c-mycmRNA前体,同时阻断c-myc蛋白的翻译. 其次反义RNA链与c-myc DNA双链形成三股螺旋,从而干预c-myc基因的表达. 第三反义RNA翻 译成新的蛋白质,与myc蛋白竞争靶位或相互作用. 细胞DNA梯度降解试验、细胞凋 亡原位检测及流式细胞仪检测均显示反义c-myc腺病毒在抑制胃癌细胞生长的同时诱 导了凋亡. 产生这种作用的解释是在myc蛋白上促进增殖、引起共转化和诱导分化并起动凋亡的功能域紧密相连、部分重叠,因而它能驱动两个截然相反的生命过程. 文献也报道了应用反义c-mycRNA(与我们不同的c-myc基因序列部分)及反义c-myc寡核苷 酸有效抑制肿瘤细胞的增殖,并诱导分化和凋亡[6-8]. 但这些实验均未采用c-myc的大片段反义序列,也无系统的体内研究. 采用反义c-myc RNA进行胃癌 的基因治疗未见文献报告. 还有作者报告采用反义C-Ha-ras DNA,H-ras反义RNA逆转录病毒、PCNA特异性反义寡核苷酸可以部分逆转胃癌细胞的恶性表型[9,10]. 与我 们用反义c-myc腺病毒得到的研究结果一致. 这些结果表明:针对不同的癌基因高表达 及扩增,利用反义RNA或DNA技术,可部分阻断肿瘤细胞的恶性增殖.
, http://www.100md.com
本结果表明,Ad-AS c-myc对c-myc基因高表达的SGC7901细胞具有很强的体内外生长抑制及凋亡诱导作用. 我们的实验结果证实Ad-AS c-myc在用于胃癌基因治疗的方面具有良好的应用价值.
作者简介:*陈洁平 林晨均为第一作者
陈洁平,女,1963-05-10生,贵州省贵阳市人,汉族. 1988年遵义医学院本 科毕业,1995年第三军医大学西南医院消化科硕士,1998年博士,讲师. 主治医师,主要从 事幽门螺杆菌及胃癌研究,发表论文30篇.
*国家863高科技发展基金,No.Z20-01-02
通讯作者 陈洁平,400038,第三军医大学西南医院消化科.
*Supported by the National 863 High Science and Technology Foundat ion of China, No. Z20-01-02
, http://www.100md.com
Correspondence to:Dr. CHEN Jie-Ping, Department of Gastroentero logy, Southwest Hospital, Third Military Medical University, Chongqing 400038, China
Tel. +86.23.65318301. Ext 73094
E-mail jpchen@public.cta.cq.cn
4 参考文献
1 Anderson WF Gene therapy of cance Ther. Hum Gene Ther, 1994;5:1-2
, 百拇医药
2 Feng L, Wang XQ, Fu M,Wang ZH, Tian Y, Cai Y, WuM A strategy for isolating di fferentiation-inducing complementary DNAs from human esophageal cancer cell lin e treated with retinoic acid, ZHONG GUO KE TUE(B), 1992;35:445-454
3 Brody SL, Crystal RG. Adenovirus-mediated in vivo gene transfer. Ann NY Acad Sci, 1994;716:90-101
4 Ryan KM, Birnie GD. myc oncogens: the enigmatic family. Biochem J, 1996;314:713-721
, 百拇医药
5 Xu Y, Nguyen Q, Lo DC, Czaja MJ. C-myc-dependent hepatoma cell apoptosi s results from oxidative stress and not a deficiency of growth factors. J Cel l Physiol, 1997;170:192-199
6 VanWaardenburg RC, Meijer C, Burger H, Nooter K, De Vries EG, Mulder NH, De J o ng S. Effects of an inducible antisense c-myc gene transfer in a drug-resis tant human small-cell-carcinoma cell line. Int J Cancer, 1997;14:73:544-550
7 Onoda N, Maeda K, Chung YS, Yano Y, Matsui Yuasa I, Otani S, Sowa M. Overexpr ession of c-myc messenger RNA in primary and metastatic Lesions of carcinom a of the stomach. J Am Coll Surg, 1996;182:55-59
, http://www.100md.com
8 Leonetti C, D'Agnano I, Lozupone F, Valentini A, Geiser T, Zon G, Calabretta B, Citro G C, Zupi G. Antitumor effect of c-myc antisense phosphoothioate o ligocdeoxynuleotide on human melanoma cells in vitro and in mice. J Natl Cancer Inst, 1996;88:419-429
9 李文梅,吕有勇. 导入Rb,P53,P16和H-ras反义RNA对人胃癌细胞恶性增 殖的影响,中国肿瘤生物治疗杂志,1997;4:90-94
10 Sakakura C, A, Hagjwara A, Tsujimoto H, Ozaki K Sakakibara T, Oyama T, Ogaki T, Ogaki M, Takahashi T. The anti-proliferative effect of proliferatin g cell nuclear antigenspecific antisence oligonucleotides on human gastric cance r cell lines. Surg Today, 1995;25:184-186
收稿日期 1998-12-22 修回日期 1999-03-06, 百拇医药(陈洁平*1 林 晨* 徐采朴 张雪艳 付明 邓 友平 隗月 吴旻)