监测FasL表达评估异基因造血干细胞移植后T细胞免疫功能状态
作者:冯晓勤 周淑芸 冯茹 张建军 王随照 伍伯松 朱为国 杨艺
单位:冯晓勤(第一军医大学南方医院血液科,广东 广州 510515);周淑芸(第一军医大学南方医院血液科,广东 广州 510515);冯茹(第一军医大学南方医院血液科,广东 广州 510515);张建军(广东省人民医院流式细胞室,广东 广州 510080);王随照(广东省人民医院流式血液科,广东 广州 510080);伍伯松(第一军医大学南方医院血液科,广东 广州 510515)
关键词:流式细胞术;异基因造血干细胞移植;FasL;细胞免疫;移植物抗宿主病
第一军医大学学报000218 摘要: 目的 评估异基因造血干细胞移植后T淋巴细胞免疫功能状态。 方法 采用三色荧光标记的流式细胞术,对4例异基因造血干细胞移植、2例自体干细胞移植患者移植前后的T淋巴细胞及其亚群的FasL表达进行监测。结果 移植前T细胞的FasL表达率仅(2.13±2.02)%,与正常对照组无显著差异(P>0.05),移植后异基因造血干细胞移植患者FasL表达水平升高,尤以急性GVHD患者表达升高显著(P<0.05),而自体干细胞移植患者的FasL表达未见明显改变。结论 异基因造血干细胞移植术后部分T淋巴细胞处于激活状态;FasL表达可能与aGVHD相关;对FasL表达的监测可从细胞、免疫分子两个层次对T细胞免疫功能状态进行评估,该体系的完善对临床判断预后、指导治疗可能有较直接的参考价值。
, http://www.100md.com
中图分类号: R392.4;R457.7 文献标识码:A
文章编号:1000-2588(2000)02-0109-04
Investigation of the FasL expression to evaluate the immunoactivity of T lymphocytes in patients undergoing allogeneic hemopoietic stem cells transplantation
FENG Xiao-qin,ZHOU Shu-yun,FENG Ru,WU Bo-song,YANG Yi
(Department of Hemotology , Nanfang Hospital, Guangzhou 510515, China)
, http://www.100md.com
ZHANG Jian-jun
(Lab of Flow Cytometry, Guangdong People’s Hospital, Guangzhou 510008, China)
WANG Sui-zhao
(Department of Hemotology, Guangdong People’s Hospital, Guangzhou 510008, China)
ZHU Wei-guo
(Department of Pediatrics, Nanfang Hospital, Guangzhou 510515, China)
Abstract: objective To evaluate the immunoactivity of T lymphocytes in patients after allogeneic hemopoietic stem cells transplantation (allo-HSCT). Methods Four patients undergoing allo-HSCT and 2 patients undergoing autogenous hemopoietic stem cells transplantation (auto-HSCT) were investigated for the expression of FasL among lymphocyte subsets before and after transplantation using three-color flow cytometry. Results The expression of FasL in T cells was very low before transplantation (2.13%±2.02%), which showed no significant difference from that in normal controls (P>0.05). The expression of FasL increased after allo-HSCT, which was most obviously demonstrated in 2 patients with acute graft versus host disease (aGVHD) (P<0.05). Significant increase of FasL in T cells was not observed in patients undergoing auto-HSCT. Conclusions A proportion of T lymphocytes were activated after allo-HSCT and the expression of FasL may be related with aGVHD. The expression of FasL in T cells serves as a parameter in the cytological and immunomolecular evaluation of the immunoactivity of T cells. This method may be of value in judging the clinical prognosis and provides experimental information for clinical treatment.
, http://www.100md.com
Key words: flow cytometry; allo-HSCT; FasL; cellular immunity; GVHD
异基因造血干细胞移植(allo-HSCT)后免疫功能重建过程中的T淋巴细胞是影响移植物存活、产生移植物抗宿主(Graft versus host, GVH)及移植物抗白血病(Graft versus leukemia, GVL)作用的主要细胞功能群,因此,了解其免疫功能状态对判断预后、指导临床治疗具有十分重要的意义。本研究以 T 淋巴细胞的 FasL 表达水平作为监测指标,对患者allo-HSCT后的T淋巴细胞免疫功能状态进行评估。
1 病例和方法
1.1 病例
正常献血员6例作为正常对照组,造血干细胞移植组共6例(包括自体移植2例、异基因移植4例),详细临床资料见表1。
, http://www.100md.com
1.2 标本采集
分别采集正常献血员、患者移植前及移植后1、3月等不同时间点的肝素抗凝血1 ml,室温放置,6 h内用单克隆抗体标记。
1.3 单克隆抗体标记
每份样本均设立空白对照及阴性对照,各管加入(0.5~1.0)×106个白细胞。用三色荧光标记,其中CD3、CD8分别采用FITC和PE直接标记 (CD3 FITC/CD8 PE,DAKO),FasL通过生物素间接标记CY-5(Biotin-FasL及SAV-CY-5,Pharmingen)。样本经单克隆抗体标记后,用1%甲醛PBS液固定,48 h内用流式细胞仪检测。
1.4 流式细胞仪检测
使用 Becton Dickinson FACS Calibur流式细胞仪,CELLQuest软件检测CD3+FasL+及CD3+CD8+FasL+细胞的阳性率。
, 百拇医药
表 1 接受HSCT患者的临床资料
Tab.1 Clinical data of patients undergoing allogeneic or autogenous HSCT
auto-HSCT1
auto-HSCT2
allo-HSCT1
allo-HSCT2
allo-HSCT3
allo-HSCT4
Patient gender
M
, 百拇医药
M
M
M
M
F
Age
40
12
25
5
19
35
Diagnosis
NHL
, 百拇医药
AML-M5
CML
β-thalassemia
ALL
AML- M3
Donor gender
M
M
F
M
HLA
Matched
, 百拇医药
1 site mismatched
Matched
Matched
Method of transplantation
auto-PBSCT
auto-PBSCT
allo-PBSCT
allo-BMT
allo-PBSCT
allo-PBSCT
Conditioning therapy
, 百拇医药
TBI+Cy+Vp16
MAC
TBI+Cy
Bu+Cy
TBI+Cy
TBI+Cy
Infusion of CD3、4+ cells (×106/kg)
3.65
4.18
8.6
7.80
, 百拇医药 10.50
4.18
Prevention of GVHD
CSA+MTX
ATG+CSA
CSA+MTX
CSA+MTX
Evidence of engraft
Blood
Thalassemia gene
Chromosome
Chromosome
, http://www.100md.com
GVHD
Ⅱ
Ⅱ
No
No
2 结果
2.1 患者T淋巴细胞及其亚群的FasL表达水平检测
本研究结果显示,患者移植前T淋巴细胞的FasL表达率低,与正常对照组无显著差异;自体干细胞移植患者的FasL表达水平在移植前后未见明显改变,而异基因移植后患者FasL表达水平升高,尤以急性GVHD患者表达升高显著(P<0.05),且主要表现为CD3+CD8+细胞群的FasL表达,详见表2及图1、2。
, 百拇医药 表 2 移植前患者T淋巴细胞及其亚群的FasL表达水平检测
Tab.2 The expression of FasL in T cells and its subsets in patients before allogeneic or autogenous transplantation (%)
CD3+FasL+
CD3+ CD8+FasL+
Normal control
0.98±0.56
0.88±0.50
, http://www.100md.com
Patients before transplantation
2.13±2.03*
1.98±1.96*
*P>0.05 vs normal control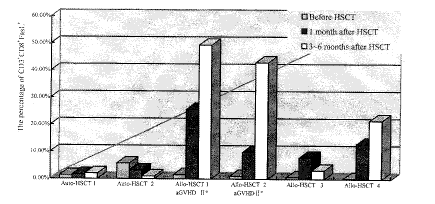
图 1 HSCT前后CD3+CD8+细胞的 FasL表达比较
Fig. 1 The percentage of CD3+CD8+FasL+ cells before and after transplantation
, http://www.100md.com 2.2 移植前后T淋巴细胞亚群变化6例患者中5例在移植后出现明显CD3+CD8+/CD3+CD8-比例升高,该比值在自体移植组与异基因移植组未见明显差异(P>0.05),详见图3。
3 讨论
FasL是一种能特异性结合靶细胞上的Fas抗原,诱导Fas+细胞发生凋亡的免疫活性分子[1]。目前已发现它表达于激活的人淋巴细胞、角膜上皮细胞及睾丸滋养层细胞[2~3],前者在免疫失衡中起重要作用。近年来的研究从一个侧面揭示了T淋巴细胞与靶细胞之间相互作用的分子免疫机制,即CD4+、CD8+细胞均可通过Fas/ FasL途径显示CTL的杀伤活性[4]。
在异基因造血干细胞移植中, 即使HLA全相合,也有40%左右的病例发生不同程度的移植物抗宿主病(GVHD),直接影响着患者移植后的生存质量,甚至危及生命;而GVL作用则是保证患者长期无病存活的重要因素,作为产生这两种免疫作用的主要细胞功能群T淋巴细胞,由于造血微环境的改变及异体抗原的刺激,其亚群的分布及功能均会发生不同程度的变化,这些变化在GVH及GVL的发生、发展中起着极其重要的作用。我们采用流式细胞术检测FasL在T淋巴细胞上的功能性表达,从细胞、免疫分子两个层次监测这些变化,并评估移植后的T细胞免疫功能状态,结果显示,异基因移植后T细胞表达一定数量的FasL,说明这些细胞处于免疫激活状态,而这种激活状态是破坏机体免疫自稳及清除残存白血病细胞的潜在因素,当这些细胞与Fas+的细胞发生作用时,则可导致Fas+细胞的损伤和破坏,至于FasL在这两种作用中有何异同,尚有待于进一步的研究;在FasL+的T细胞中,以CD8+细胞占主导,结合异基因移植后多数出现CD3+CD8+的比例升高,在理论上说明CD3+CD8+细胞群在移植后通过功能的增强及相对数量的增加而具有发挥主要免疫杀伤作用的能力。而自体造血干细胞移植后仅出现CD3+CD8+比例的改变,其功能状态并未见增强,推测这亦是自体移植后缺乏GVL作用的原因之一。本研究中2例自体干细胞移植病例移植前、后FasL的表达均未见明显改变,符合机体免疫自稳的状态。而2例发生Ⅱ度aGVHD的患者,其移植后FasL的表达均高于另2例无GVHD患者,提示FasL的功能性表达可能与GVHD的免疫损伤成正相关,这与Lee[5]的研究结果一致。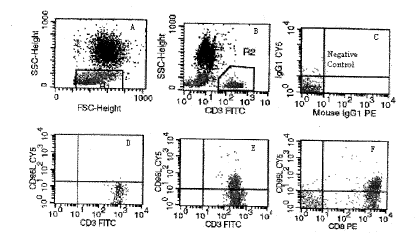
, 百拇医药
图 2 T细胞主要以CD3+CD8+的亚群表达FasL
Fig.2 The expresson of FasL increased, observed mainly in CD3+CD8+ cells after HSCT
These figures were derived from the examination result of patient 2 with allo-HSCT using three-color flow cytometry and processed by CELLQuest software. A. Cells in the area of R1 were lymphocytes. B. The CD3+ cells in the area of R2 was 30.40% of total lymphocytes. C. The negative control. D. CD3+ FasL+ cells was about 2.45% before HSCT. E and F. CD3+ FasL+ cells was 46.71% (E) in the 3rd month after HSCT including 0.99% of CD8- FasL+ cells and 42.89% of CD8+FasL+ cells (F).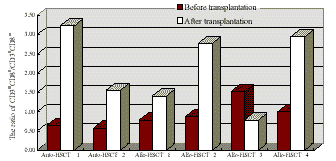
, 百拇医药
图 3 移植前后的CD3+CD8+/CD3+CD8 比例变化
Fig.3 The change of the ratio of CD3+CD8+/CD3+CD8
在技术方法上,本研究采用流式细胞术一次性从细胞及免疫分子两个层次评价T细胞免疫功能状态,数据客观,方法简便,能对临床产生比较直接、广泛的指导意义。
致谢:衷心感谢本科刘启发副教授、孙竟副教授、儿科李夏新副教授给予的大力支持和帮助。
基金项目:广东省自然科学基金资助项目(980222)
作者简介:冯晓勤(1967-),女,1994年毕业于第一军医大学,硕士,主治医师,现为97级博士生。电话:85141617
, http://www.100md.com
作者单位:朱为国(第一军医大学南方医院儿科,广东 广州 510515)
杨艺(第一军医大学南方医院血液科,广东 广州 510515)
参考文献
1,Ju ST, Panka DJ, Cui H et al. Fas(CD95)/FasL interactions required for programmed cell death after T-cell activation[J]. Nature, 1995, 373 (6513):444~8.
2,Stuart PM, Griffith TS, Usui N et al. CD95 ligand (FasL)-induced apoptosis is necessary for corneal allograft survival[J]. J Clin Inves, 1997, 99 (3):396~402.
, 百拇医药
3,Bellgrau D, Gold D, Selawry H et al. A role for CD95 ligand in preventing graft rejection[J]. Nature, 1995, 377 (6550):630~2.
4,Hanabuchi S, Koyanagi M, Kawasaki A et al. Fas and its ligand in a general mechanism of T-cell-mediated cytotoxicity[J]. Proc Natl Acad Sci USA, 1994, 91 (11):4930~4.
5,Lee S, Chong SY, Lee JW et al. Difference in the expression of Fas/Fas-ligand and the lymphocyte subset reconstitution according to the occurrence of acute GVHD[J]. Bone Marrow Transplant, 1997, 20 (10):883~8.
收稿日期:1999-06-20, 百拇医药
单位:冯晓勤(第一军医大学南方医院血液科,广东 广州 510515);周淑芸(第一军医大学南方医院血液科,广东 广州 510515);冯茹(第一军医大学南方医院血液科,广东 广州 510515);张建军(广东省人民医院流式细胞室,广东 广州 510080);王随照(广东省人民医院流式血液科,广东 广州 510080);伍伯松(第一军医大学南方医院血液科,广东 广州 510515)
关键词:流式细胞术;异基因造血干细胞移植;FasL;细胞免疫;移植物抗宿主病
第一军医大学学报000218 摘要: 目的 评估异基因造血干细胞移植后T淋巴细胞免疫功能状态。 方法 采用三色荧光标记的流式细胞术,对4例异基因造血干细胞移植、2例自体干细胞移植患者移植前后的T淋巴细胞及其亚群的FasL表达进行监测。结果 移植前T细胞的FasL表达率仅(2.13±2.02)%,与正常对照组无显著差异(P>0.05),移植后异基因造血干细胞移植患者FasL表达水平升高,尤以急性GVHD患者表达升高显著(P<0.05),而自体干细胞移植患者的FasL表达未见明显改变。结论 异基因造血干细胞移植术后部分T淋巴细胞处于激活状态;FasL表达可能与aGVHD相关;对FasL表达的监测可从细胞、免疫分子两个层次对T细胞免疫功能状态进行评估,该体系的完善对临床判断预后、指导治疗可能有较直接的参考价值。
, http://www.100md.com
中图分类号: R392.4;R457.7 文献标识码:A
文章编号:1000-2588(2000)02-0109-04
Investigation of the FasL expression to evaluate the immunoactivity of T lymphocytes in patients undergoing allogeneic hemopoietic stem cells transplantation
FENG Xiao-qin,ZHOU Shu-yun,FENG Ru,WU Bo-song,YANG Yi
(Department of Hemotology , Nanfang Hospital, Guangzhou 510515, China)
, http://www.100md.com
ZHANG Jian-jun
(Lab of Flow Cytometry, Guangdong People’s Hospital, Guangzhou 510008, China)
WANG Sui-zhao
(Department of Hemotology, Guangdong People’s Hospital, Guangzhou 510008, China)
ZHU Wei-guo
(Department of Pediatrics, Nanfang Hospital, Guangzhou 510515, China)
Abstract: objective To evaluate the immunoactivity of T lymphocytes in patients after allogeneic hemopoietic stem cells transplantation (allo-HSCT). Methods Four patients undergoing allo-HSCT and 2 patients undergoing autogenous hemopoietic stem cells transplantation (auto-HSCT) were investigated for the expression of FasL among lymphocyte subsets before and after transplantation using three-color flow cytometry. Results The expression of FasL in T cells was very low before transplantation (2.13%±2.02%), which showed no significant difference from that in normal controls (P>0.05). The expression of FasL increased after allo-HSCT, which was most obviously demonstrated in 2 patients with acute graft versus host disease (aGVHD) (P<0.05). Significant increase of FasL in T cells was not observed in patients undergoing auto-HSCT. Conclusions A proportion of T lymphocytes were activated after allo-HSCT and the expression of FasL may be related with aGVHD. The expression of FasL in T cells serves as a parameter in the cytological and immunomolecular evaluation of the immunoactivity of T cells. This method may be of value in judging the clinical prognosis and provides experimental information for clinical treatment.
, http://www.100md.com
Key words: flow cytometry; allo-HSCT; FasL; cellular immunity; GVHD
异基因造血干细胞移植(allo-HSCT)后免疫功能重建过程中的T淋巴细胞是影响移植物存活、产生移植物抗宿主(Graft versus host, GVH)及移植物抗白血病(Graft versus leukemia, GVL)作用的主要细胞功能群,因此,了解其免疫功能状态对判断预后、指导临床治疗具有十分重要的意义。本研究以 T 淋巴细胞的 FasL 表达水平作为监测指标,对患者allo-HSCT后的T淋巴细胞免疫功能状态进行评估。
1 病例和方法
1.1 病例
正常献血员6例作为正常对照组,造血干细胞移植组共6例(包括自体移植2例、异基因移植4例),详细临床资料见表1。
, http://www.100md.com
1.2 标本采集
分别采集正常献血员、患者移植前及移植后1、3月等不同时间点的肝素抗凝血1 ml,室温放置,6 h内用单克隆抗体标记。
1.3 单克隆抗体标记
每份样本均设立空白对照及阴性对照,各管加入(0.5~1.0)×106个白细胞。用三色荧光标记,其中CD3、CD8分别采用FITC和PE直接标记 (CD3 FITC/CD8 PE,DAKO),FasL通过生物素间接标记CY-5(Biotin-FasL及SAV-CY-5,Pharmingen)。样本经单克隆抗体标记后,用1%甲醛PBS液固定,48 h内用流式细胞仪检测。
1.4 流式细胞仪检测
使用 Becton Dickinson FACS Calibur流式细胞仪,CELLQuest软件检测CD3+FasL+及CD3+CD8+FasL+细胞的阳性率。
, 百拇医药
表 1 接受HSCT患者的临床资料
Tab.1 Clinical data of patients undergoing allogeneic or autogenous HSCT
auto-HSCT1
auto-HSCT2
allo-HSCT1
allo-HSCT2
allo-HSCT3
allo-HSCT4
Patient gender
M
, 百拇医药
M
M
M
M
F
Age
40
12
25
5
19
35
Diagnosis
NHL
, 百拇医药
AML-M5
CML
β-thalassemia
ALL
AML- M3
Donor gender
M
M
F
M
HLA
Matched
, 百拇医药
1 site mismatched
Matched
Matched
Method of transplantation
auto-PBSCT
auto-PBSCT
allo-PBSCT
allo-BMT
allo-PBSCT
allo-PBSCT
Conditioning therapy
, 百拇医药
TBI+Cy+Vp16
MAC
TBI+Cy
Bu+Cy
TBI+Cy
TBI+Cy
Infusion of CD3、4+ cells (×106/kg)
3.65
4.18
8.6
7.80
, 百拇医药 10.50
4.18
Prevention of GVHD
CSA+MTX
ATG+CSA
CSA+MTX
CSA+MTX
Evidence of engraft
Blood
Thalassemia gene
Chromosome
Chromosome
, http://www.100md.com
GVHD
Ⅱ
Ⅱ
No
No
2 结果
2.1 患者T淋巴细胞及其亚群的FasL表达水平检测
本研究结果显示,患者移植前T淋巴细胞的FasL表达率低,与正常对照组无显著差异;自体干细胞移植患者的FasL表达水平在移植前后未见明显改变,而异基因移植后患者FasL表达水平升高,尤以急性GVHD患者表达升高显著(P<0.05),且主要表现为CD3+CD8+细胞群的FasL表达,详见表2及图1、2。
, 百拇医药 表 2 移植前患者T淋巴细胞及其亚群的FasL表达水平检测
Tab.2 The expression of FasL in T cells and its subsets in patients before allogeneic or autogenous transplantation (%)
CD3+FasL+
CD3+ CD8+FasL+
Normal control
0.98±0.56
0.88±0.50
, http://www.100md.com
Patients before transplantation
2.13±2.03*
1.98±1.96*
*P>0.05 vs normal control

图 1 HSCT前后CD3+CD8+细胞的 FasL表达比较
Fig. 1 The percentage of CD3+CD8+FasL+ cells before and after transplantation
, http://www.100md.com 2.2 移植前后T淋巴细胞亚群变化6例患者中5例在移植后出现明显CD3+CD8+/CD3+CD8-比例升高,该比值在自体移植组与异基因移植组未见明显差异(P>0.05),详见图3。
3 讨论
FasL是一种能特异性结合靶细胞上的Fas抗原,诱导Fas+细胞发生凋亡的免疫活性分子[1]。目前已发现它表达于激活的人淋巴细胞、角膜上皮细胞及睾丸滋养层细胞[2~3],前者在免疫失衡中起重要作用。近年来的研究从一个侧面揭示了T淋巴细胞与靶细胞之间相互作用的分子免疫机制,即CD4+、CD8+细胞均可通过Fas/ FasL途径显示CTL的杀伤活性[4]。
在异基因造血干细胞移植中, 即使HLA全相合,也有40%左右的病例发生不同程度的移植物抗宿主病(GVHD),直接影响着患者移植后的生存质量,甚至危及生命;而GVL作用则是保证患者长期无病存活的重要因素,作为产生这两种免疫作用的主要细胞功能群T淋巴细胞,由于造血微环境的改变及异体抗原的刺激,其亚群的分布及功能均会发生不同程度的变化,这些变化在GVH及GVL的发生、发展中起着极其重要的作用。我们采用流式细胞术检测FasL在T淋巴细胞上的功能性表达,从细胞、免疫分子两个层次监测这些变化,并评估移植后的T细胞免疫功能状态,结果显示,异基因移植后T细胞表达一定数量的FasL,说明这些细胞处于免疫激活状态,而这种激活状态是破坏机体免疫自稳及清除残存白血病细胞的潜在因素,当这些细胞与Fas+的细胞发生作用时,则可导致Fas+细胞的损伤和破坏,至于FasL在这两种作用中有何异同,尚有待于进一步的研究;在FasL+的T细胞中,以CD8+细胞占主导,结合异基因移植后多数出现CD3+CD8+的比例升高,在理论上说明CD3+CD8+细胞群在移植后通过功能的增强及相对数量的增加而具有发挥主要免疫杀伤作用的能力。而自体造血干细胞移植后仅出现CD3+CD8+比例的改变,其功能状态并未见增强,推测这亦是自体移植后缺乏GVL作用的原因之一。本研究中2例自体干细胞移植病例移植前、后FasL的表达均未见明显改变,符合机体免疫自稳的状态。而2例发生Ⅱ度aGVHD的患者,其移植后FasL的表达均高于另2例无GVHD患者,提示FasL的功能性表达可能与GVHD的免疫损伤成正相关,这与Lee[5]的研究结果一致。

, 百拇医药
图 2 T细胞主要以CD3+CD8+的亚群表达FasL
Fig.2 The expresson of FasL increased, observed mainly in CD3+CD8+ cells after HSCT
These figures were derived from the examination result of patient 2 with allo-HSCT using three-color flow cytometry and processed by CELLQuest software. A. Cells in the area of R1 were lymphocytes. B. The CD3+ cells in the area of R2 was 30.40% of total lymphocytes. C. The negative control. D. CD3+ FasL+ cells was about 2.45% before HSCT. E and F. CD3+ FasL+ cells was 46.71% (E) in the 3rd month after HSCT including 0.99% of CD8- FasL+ cells and 42.89% of CD8+FasL+ cells (F).

, 百拇医药
图 3 移植前后的CD3+CD8+/CD3+CD8 比例变化
Fig.3 The change of the ratio of CD3+CD8+/CD3+CD8
在技术方法上,本研究采用流式细胞术一次性从细胞及免疫分子两个层次评价T细胞免疫功能状态,数据客观,方法简便,能对临床产生比较直接、广泛的指导意义。
致谢:衷心感谢本科刘启发副教授、孙竟副教授、儿科李夏新副教授给予的大力支持和帮助。
基金项目:广东省自然科学基金资助项目(980222)
作者简介:冯晓勤(1967-),女,1994年毕业于第一军医大学,硕士,主治医师,现为97级博士生。电话:85141617
, http://www.100md.com
作者单位:朱为国(第一军医大学南方医院儿科,广东 广州 510515)
杨艺(第一军医大学南方医院血液科,广东 广州 510515)
参考文献
1,Ju ST, Panka DJ, Cui H et al. Fas(CD95)/FasL interactions required for programmed cell death after T-cell activation[J]. Nature, 1995, 373 (6513):444~8.
2,Stuart PM, Griffith TS, Usui N et al. CD95 ligand (FasL)-induced apoptosis is necessary for corneal allograft survival[J]. J Clin Inves, 1997, 99 (3):396~402.
, 百拇医药
3,Bellgrau D, Gold D, Selawry H et al. A role for CD95 ligand in preventing graft rejection[J]. Nature, 1995, 377 (6550):630~2.
4,Hanabuchi S, Koyanagi M, Kawasaki A et al. Fas and its ligand in a general mechanism of T-cell-mediated cytotoxicity[J]. Proc Natl Acad Sci USA, 1994, 91 (11):4930~4.
5,Lee S, Chong SY, Lee JW et al. Difference in the expression of Fas/Fas-ligand and the lymphocyte subset reconstitution according to the occurrence of acute GVHD[J]. Bone Marrow Transplant, 1997, 20 (10):883~8.
收稿日期:1999-06-20, 百拇医药