5-HT3受体拮抗剂阿扎西隆的合成
作者:张雅芳 赵冬梅 杨淑敏 徐冰珠
单位:张雅芳 赵冬梅(沈阳药科大学药物合成室,沈阳 110015);杨淑敏(河南华利制药厂,平顶山 467001);徐冰珠(广昌动物保健品公司,番禺 511442)
关键词:5-HT3受体拮抗剂;阿扎西隆;合成
中国药物化学杂志000218 摘要 以水杨酸甲酯为起始原料,经氯代、硝化等8步反应合成5-HT3受体拮抗剂阿扎西隆,以化合物(2)计总收率为45%(文献〔6〕收率为34%),其结构经IR,1H-NMR和MS确证.
Synthesis of the 5-HT3 Receptor Antagonist Azasetron
, http://www.100md.com
Zhang Yafang Zhao Dongmei Yang Shumin Xu Bingzhu
(The Lab.of Drug Synthesis,Shenyang Pharmaceutical University,Shenyang 110015)
Abstract The 5-HT3 receptor antagonist azasetron was synthesized from methyl salicylate through an eight-step synthetic route with chlorination,nitration,etc.The total yield was 45%(calculated on 2).The yield reported in literature〔6〕 was 34%.It was characterized by IR,1H-NMR and MS.
, 百拇医药
Key words 5-HT3 receptor antagonist;azasetron;synthesis
阿扎西隆(azasetron,Y-25130,1)〔1,2〕,商品名为Serotone,化学名:(±)-N-(1-氮杂双环〔2.2.2〕辛-3-基)-6-氯-4-甲基-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-甲酰胺盐酸盐.由吉富制药(Yoshitomi pharm.Ind.Ltd.)和日本烟草(Japan Tobacco)公司共同研究开发,于1994年在日本首次上市.阿扎西隆为强效、高选择性、使用安全、副作用低的5-HT3受体拮抗剂,用于预防和治疗肿瘤化疗、放疗和手术后引起的恶心和呕吐.该药的特点是不仅能有效抑制急性恶心和呕吐,而且对延迟性恶心和呕吐的疗效更佳〔3~5〕.
阿扎西隆的合成主要有两条路线〔6,7〕,文献〔6〕是以5-氯-2-羟基苯甲酸甲酯(2)为起始原料,经硝化、还原得中间体(4),(4)与氯乙酰氯发生缩合、环合反应得共同中间体(5),再经甲基化、水解、氯化、胺解和成盐制得产物.文献〔7〕是以5-氯-2-乙氧羰基甲氧基苯甲酸甲酯为起始原料,经硝化、还原,同时发生分子内的亲核取代(酯的胺解)反应,环合得中间体(5).两种起始原料均无商品供应,都需自行合成.本文作者主要参考文献〔6〕设计了如图1所示的合成路线.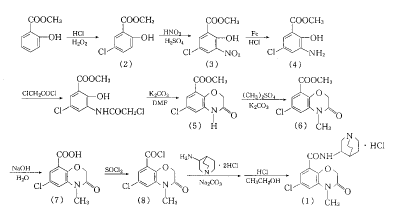
, 百拇医药
Fig.1 The synthetic route
化合物(2)的合成文献多用氯气氯化,本文改用浓盐酸和过氧化氢为氯代试剂,操作方便,产物较纯.化合物(4)的合成文献使用铁粉和氯化胺水溶液,本文改用铁酸还原法.化合物(6)的合成文献使用碘甲烷,本文改用硫酸二甲酯,收率较高.化合物(1)的合成文献使用3-氨基喹宁环(游离碱),本文直接使用其二盐酸盐,产物经IR,1H-NMR,MS确证其结构.
1 实验部分
熔点用毛细管法测定,温度未经校正.IR用Bruker IFS-55型红外光谱仪测定.1H-NMR用ARX-300核磁共振波谱仪测定.MS用Finnigan公司LCQ型液相色-质联用仪测定.
1.1 5-氯-2-羟基苯甲酸甲酯(2)的制备
, 百拇医药
于500 mL三颈瓶中依次加入15.2 g(0.1 mol)水杨酸甲酯、160 mL冰乙酸、17 mL(约0.2 mol)浓盐酸,搅拌溶解,在室温下滴加12.5 mL(约0.12 mol)30%过氧化氢,反应2 h,倾入冰水中,析出白色固体,抽滤,水洗,真空干燥,得白色粉末15.4 g,收率:83%,mp 44~47℃(文献〔8〕mp 48℃).
1.2 5-氯-2-羟基-3-硝基苯甲酸甲酯(3)的制备
将化合物(2)37.4 g(0.2 mol)溶于100 mL浓硫酸中,搅拌,冰水浴冷却,于0~5℃缓慢滴加9.2 mL(约0.27 mol)硝酸和9.2 mL硫酸组成的混酸,加毕,继续反应1 h,倾入碎冰中,析出黄色固体,抽滤,水洗,醇洗,得浅黄色粉末43 g,收率:93%,mp 159~162℃(文献〔6〕mp 164℃,收率:86%).
, http://www.100md.com 1.3 3-氨基-5-氯-2-羟基苯甲酸甲酯(4)的制备
将500 mL四颈瓶分别安装机械搅拌器、回流冷凝器、温度计和恒压滴液漏斗,加入9.8 g(0.04 mol)化合物(3)、200 mL甲苯及9.5 g(0.17 mol)铁粉,快速搅拌,加热,约20 min滴加盐酸水溶液(V∶V=1∶10)40 mL,维持微回流状态至反应完全(1~2 h),通过温热硅藻土抽滤,分出甲苯层,无水硫酸钠干燥,过滤,旋转蒸发至干,得浅灰色粉末8 g,收率:94%,mp 86~89℃.乙醇重结晶得灰白色小片晶,mp 89~91℃(文献〔6〕mp 92~93℃,收率:79%).
1.4 6-氯-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-羧酸甲酯(5)的制备
将8.9 g(44 mmol)化合物(4)溶于200 mL氯仿中,加入100 mL饱和碳酸氢钠,搅拌,冷却至10℃以下缓慢滴加6.0 g(53 mmol)氯乙酰氯的10 mL氯仿的溶液,继续反应2 h,分出氯仿层,水洗,无水硫酸钠干燥,过滤,旋转蒸发至干得中间体5-氯-3-氯乙酰氨基-2-羟基苯甲酸甲酯,用70 mL DMF溶解,加入6.0 g无水碳酸钾,在70℃搅拌反应2 h,冷后倾入冰水中,抽滤,水洗,乙醇洗,得白色粉末(5)10 g,收率:93%,mp 237~240℃(文献〔6〕收率:90%,mp 239~241℃).
, http://www.100md.com
1.5 6-氯-4-甲基-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-羧酸甲酯(6)的制备
于250 mL三颈瓶中依次加入9.7 g(40 mmol)化合物(5)和50 mL DMF,搅拌使溶,再加入8.3 g(60 mmol)无水碳酸钾,滴加7.6 g(60 mmol)硫酸二甲酯,室温反应2 h,然后缓慢升温至50℃,再反应1 h,将反应混合物倾入冰水中,抽滤,水洗,醇洗.得白色粉末(6)9.6 g,收率:93%,mp 148~150℃(文献〔6〕 mp 150~152℃,收率:82%).
1.6 6-氯-4-甲基-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-羧酸(7)的制备
于250 mL三颈瓶中加10.2 g(40 mmol)化合物(6)、60 mL乙醇及100 mL 5%氢氧化钠,搅拌过夜,旋转蒸发回收大部分乙醇,剩余物冷却,用1∶1盐酸酸化,抽滤,水洗,干燥,得白色粉末(7)8.9 g,收率:92%,mp 237~238℃,乙醇重结晶得白色针状结晶,mp 237~239℃(文献〔6〕 mp 236~238℃,收率:81.5%).1H-NMR(DMSO-d6)δ:3.287(s,3H,—CH3),4.730(s,2H,—CH2CO),7.355,7.410(dd,2H,Ar-H),Ca.13.4(s,1H,—COOH).IR(KBr)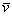 cm-1:3441,3100~3005,1733,1657,1582,1469,1439,1192,1088.
cm-1:3441,3100~3005,1733,1657,1582,1469,1439,1192,1088.
, 百拇医药
1.7 6-氯-4-甲基-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-甲酰氯(8)的制备
于500 mL三颈瓶中依次加入7.3 g(30 mmol)化合物(7)、100 mL 1,2-二氯乙烷、4.5 mL(约60 mmol)二氯亚砜和2滴DMF,搅拌,60℃反应2 h,降温,驱除系统中的氯化氢和二氧化硫等刺激性气体后,充分旋转蒸发至干,得微黄色疏松固体(8),直接用于下步反应.
1.8 阿扎西隆盐酸盐(1)的合成
将上步得到的化合物(8)加入250 mL氯仿中,振摇溶解,再加5.0 g(0.025 mol)3-氨基喹宁环二盐酸盐及13 g(0.125 mol)无水碳酸钠,室温搅拌2 d,加水100 mL,分出氯仿层,再用氯仿(100 mL×3)提取水层,合并有机相,水洗,无水硫酸镁干燥,回收氯仿,乙醇-异丙醚重结晶,无水乙醇溶解,加浓盐酸成盐,抽滤,醇洗,干燥,得白色粉末晶(1)6.3 g,收率:65%〔文献〔6〕mp 305℃(分解),收率:82%;文献〔7〕 mp 281℃(分解)〕.1H-NMR(D2O)δ:1.99(m),2.27(d),3.10~3.29(m),3.72(q),4.29(t)(共12H为喹宁环氢),3.18(s,3H,—CH3),4.65(s,2H,—O—CH2),7.22(s,2H,Ar-H).IR(KBr)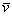 cm-1:3331,2897,2593,1670,1655,1581,1526,1381.MS m/z:350(M+1).
cm-1:3331,2897,2593,1670,1655,1581,1526,1381.MS m/z:350(M+1).
, http://www.100md.com
尽管最后两步收率较低,但前5步均高于文献,总收率〔相对于化合物(2)计算〕达45%,较文献〔6〕高11%,而且反应条件都比较温和,溶剂大部分可回收套用,具有实际应用价值,但因3-氨基喹宁环二盐酸盐价格较贵,且最后一步反应收率较文献低,有待继续研究提高.
参考文献
1,Azasetron Hydrochoride.Drugs Fut,1993,18(3):206~211
2,马卫东编译.5-HT3受体拮抗剂阿扎西隆(azasetron).国外医学合成药、生化药、制剂分册,1994,15(4):228~230
3,马培奇.肿瘤化、放疗所致恶心和呕吐防治药物的研究进展及其市场分析.中国制药信息,1998,14(7):9~13
, http://www.100md.com
4,Kawakita Takeshi,Haga keiichiro,Asano Kyoshi.Hyperemesis inhibitors containing benzoxazine compounds.Jpn Kokai Tokkyo Koho,JP08 27000〔96 27000〕.30 Jan 1996(CA 124:250944x)
5,Kawakita Takeshi,Hage keiichiro,Asano Kyoshi.Postoperative emesis inhibitors containing benzoxazine compounds.Jpn Kokai Tokkyo Koho,JP08 27001〔96 27001〕.30 Jan 1996(CA 124:250945y)
6,Kawakita T,Kuroita T,Yasumoto M,et al.Synthesis and pharmacology of 3,4-dihydro-3-oxo-1,4-benzoxazine-8-carboxamide derivatives,a new class of potent serotonin-3(5-HT3)receptor antagonists.Chem Pharm Bull,1992,40(3):624~630
7,Tahara T,Kawakita T,Yasumoto M,et al.Benzoxazine compounds and pharmaceutical use thereof.US 4892872.1990-01-09
8,Duda H,Ostaszynski A,Urbanski T.Halosalicylohydroxamic acids.I.Dihalosalicylohydroxamic acids.Bull Acad Polon Sci,Ser Sci Chim,13(5),341~347(CA63:16255b)
收稿日期:2000-02-25, 百拇医药
单位:张雅芳 赵冬梅(沈阳药科大学药物合成室,沈阳 110015);杨淑敏(河南华利制药厂,平顶山 467001);徐冰珠(广昌动物保健品公司,番禺 511442)
关键词:5-HT3受体拮抗剂;阿扎西隆;合成
中国药物化学杂志000218 摘要 以水杨酸甲酯为起始原料,经氯代、硝化等8步反应合成5-HT3受体拮抗剂阿扎西隆,以化合物(2)计总收率为45%(文献〔6〕收率为34%),其结构经IR,1H-NMR和MS确证.
Synthesis of the 5-HT3 Receptor Antagonist Azasetron
, http://www.100md.com
Zhang Yafang Zhao Dongmei Yang Shumin Xu Bingzhu
(The Lab.of Drug Synthesis,Shenyang Pharmaceutical University,Shenyang 110015)
Abstract The 5-HT3 receptor antagonist azasetron was synthesized from methyl salicylate through an eight-step synthetic route with chlorination,nitration,etc.The total yield was 45%(calculated on 2).The yield reported in literature〔6〕 was 34%.It was characterized by IR,1H-NMR and MS.
, 百拇医药
Key words 5-HT3 receptor antagonist;azasetron;synthesis
阿扎西隆(azasetron,Y-25130,1)〔1,2〕,商品名为Serotone,化学名:(±)-N-(1-氮杂双环〔2.2.2〕辛-3-基)-6-氯-4-甲基-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-甲酰胺盐酸盐.由吉富制药(Yoshitomi pharm.Ind.Ltd.)和日本烟草(Japan Tobacco)公司共同研究开发,于1994年在日本首次上市.阿扎西隆为强效、高选择性、使用安全、副作用低的5-HT3受体拮抗剂,用于预防和治疗肿瘤化疗、放疗和手术后引起的恶心和呕吐.该药的特点是不仅能有效抑制急性恶心和呕吐,而且对延迟性恶心和呕吐的疗效更佳〔3~5〕.
阿扎西隆的合成主要有两条路线〔6,7〕,文献〔6〕是以5-氯-2-羟基苯甲酸甲酯(2)为起始原料,经硝化、还原得中间体(4),(4)与氯乙酰氯发生缩合、环合反应得共同中间体(5),再经甲基化、水解、氯化、胺解和成盐制得产物.文献〔7〕是以5-氯-2-乙氧羰基甲氧基苯甲酸甲酯为起始原料,经硝化、还原,同时发生分子内的亲核取代(酯的胺解)反应,环合得中间体(5).两种起始原料均无商品供应,都需自行合成.本文作者主要参考文献〔6〕设计了如图1所示的合成路线.

, 百拇医药
Fig.1 The synthetic route
化合物(2)的合成文献多用氯气氯化,本文改用浓盐酸和过氧化氢为氯代试剂,操作方便,产物较纯.化合物(4)的合成文献使用铁粉和氯化胺水溶液,本文改用铁酸还原法.化合物(6)的合成文献使用碘甲烷,本文改用硫酸二甲酯,收率较高.化合物(1)的合成文献使用3-氨基喹宁环(游离碱),本文直接使用其二盐酸盐,产物经IR,1H-NMR,MS确证其结构.
1 实验部分
熔点用毛细管法测定,温度未经校正.IR用Bruker IFS-55型红外光谱仪测定.1H-NMR用ARX-300核磁共振波谱仪测定.MS用Finnigan公司LCQ型液相色-质联用仪测定.
1.1 5-氯-2-羟基苯甲酸甲酯(2)的制备
, 百拇医药
于500 mL三颈瓶中依次加入15.2 g(0.1 mol)水杨酸甲酯、160 mL冰乙酸、17 mL(约0.2 mol)浓盐酸,搅拌溶解,在室温下滴加12.5 mL(约0.12 mol)30%过氧化氢,反应2 h,倾入冰水中,析出白色固体,抽滤,水洗,真空干燥,得白色粉末15.4 g,收率:83%,mp 44~47℃(文献〔8〕mp 48℃).
1.2 5-氯-2-羟基-3-硝基苯甲酸甲酯(3)的制备
将化合物(2)37.4 g(0.2 mol)溶于100 mL浓硫酸中,搅拌,冰水浴冷却,于0~5℃缓慢滴加9.2 mL(约0.27 mol)硝酸和9.2 mL硫酸组成的混酸,加毕,继续反应1 h,倾入碎冰中,析出黄色固体,抽滤,水洗,醇洗,得浅黄色粉末43 g,收率:93%,mp 159~162℃(文献〔6〕mp 164℃,收率:86%).
, http://www.100md.com 1.3 3-氨基-5-氯-2-羟基苯甲酸甲酯(4)的制备
将500 mL四颈瓶分别安装机械搅拌器、回流冷凝器、温度计和恒压滴液漏斗,加入9.8 g(0.04 mol)化合物(3)、200 mL甲苯及9.5 g(0.17 mol)铁粉,快速搅拌,加热,约20 min滴加盐酸水溶液(V∶V=1∶10)40 mL,维持微回流状态至反应完全(1~2 h),通过温热硅藻土抽滤,分出甲苯层,无水硫酸钠干燥,过滤,旋转蒸发至干,得浅灰色粉末8 g,收率:94%,mp 86~89℃.乙醇重结晶得灰白色小片晶,mp 89~91℃(文献〔6〕mp 92~93℃,收率:79%).
1.4 6-氯-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-羧酸甲酯(5)的制备
将8.9 g(44 mmol)化合物(4)溶于200 mL氯仿中,加入100 mL饱和碳酸氢钠,搅拌,冷却至10℃以下缓慢滴加6.0 g(53 mmol)氯乙酰氯的10 mL氯仿的溶液,继续反应2 h,分出氯仿层,水洗,无水硫酸钠干燥,过滤,旋转蒸发至干得中间体5-氯-3-氯乙酰氨基-2-羟基苯甲酸甲酯,用70 mL DMF溶解,加入6.0 g无水碳酸钾,在70℃搅拌反应2 h,冷后倾入冰水中,抽滤,水洗,乙醇洗,得白色粉末(5)10 g,收率:93%,mp 237~240℃(文献〔6〕收率:90%,mp 239~241℃).
, http://www.100md.com
1.5 6-氯-4-甲基-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-羧酸甲酯(6)的制备
于250 mL三颈瓶中依次加入9.7 g(40 mmol)化合物(5)和50 mL DMF,搅拌使溶,再加入8.3 g(60 mmol)无水碳酸钾,滴加7.6 g(60 mmol)硫酸二甲酯,室温反应2 h,然后缓慢升温至50℃,再反应1 h,将反应混合物倾入冰水中,抽滤,水洗,醇洗.得白色粉末(6)9.6 g,收率:93%,mp 148~150℃(文献〔6〕 mp 150~152℃,收率:82%).
1.6 6-氯-4-甲基-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-羧酸(7)的制备
于250 mL三颈瓶中加10.2 g(40 mmol)化合物(6)、60 mL乙醇及100 mL 5%氢氧化钠,搅拌过夜,旋转蒸发回收大部分乙醇,剩余物冷却,用1∶1盐酸酸化,抽滤,水洗,干燥,得白色粉末(7)8.9 g,收率:92%,mp 237~238℃,乙醇重结晶得白色针状结晶,mp 237~239℃(文献〔6〕 mp 236~238℃,收率:81.5%).1H-NMR(DMSO-d6)δ:3.287(s,3H,—CH3),4.730(s,2H,—CH2CO),7.355,7.410(dd,2H,Ar-H),Ca.13.4(s,1H,—COOH).IR(KBr)
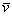 cm-1:3441,3100~3005,1733,1657,1582,1469,1439,1192,1088.
cm-1:3441,3100~3005,1733,1657,1582,1469,1439,1192,1088., 百拇医药
1.7 6-氯-4-甲基-3-氧代-3,4-二氢-2H-1,4-苯并嗪-8-甲酰氯(8)的制备
于500 mL三颈瓶中依次加入7.3 g(30 mmol)化合物(7)、100 mL 1,2-二氯乙烷、4.5 mL(约60 mmol)二氯亚砜和2滴DMF,搅拌,60℃反应2 h,降温,驱除系统中的氯化氢和二氧化硫等刺激性气体后,充分旋转蒸发至干,得微黄色疏松固体(8),直接用于下步反应.
1.8 阿扎西隆盐酸盐(1)的合成
将上步得到的化合物(8)加入250 mL氯仿中,振摇溶解,再加5.0 g(0.025 mol)3-氨基喹宁环二盐酸盐及13 g(0.125 mol)无水碳酸钠,室温搅拌2 d,加水100 mL,分出氯仿层,再用氯仿(100 mL×3)提取水层,合并有机相,水洗,无水硫酸镁干燥,回收氯仿,乙醇-异丙醚重结晶,无水乙醇溶解,加浓盐酸成盐,抽滤,醇洗,干燥,得白色粉末晶(1)6.3 g,收率:65%〔文献〔6〕mp 305℃(分解),收率:82%;文献〔7〕 mp 281℃(分解)〕.1H-NMR(D2O)δ:1.99(m),2.27(d),3.10~3.29(m),3.72(q),4.29(t)(共12H为喹宁环氢),3.18(s,3H,—CH3),4.65(s,2H,—O—CH2),7.22(s,2H,Ar-H).IR(KBr)
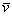 cm-1:3331,2897,2593,1670,1655,1581,1526,1381.MS m/z:350(M+1).
cm-1:3331,2897,2593,1670,1655,1581,1526,1381.MS m/z:350(M+1)., http://www.100md.com
尽管最后两步收率较低,但前5步均高于文献,总收率〔相对于化合物(2)计算〕达45%,较文献〔6〕高11%,而且反应条件都比较温和,溶剂大部分可回收套用,具有实际应用价值,但因3-氨基喹宁环二盐酸盐价格较贵,且最后一步反应收率较文献低,有待继续研究提高.
参考文献
1,Azasetron Hydrochoride.Drugs Fut,1993,18(3):206~211
2,马卫东编译.5-HT3受体拮抗剂阿扎西隆(azasetron).国外医学合成药、生化药、制剂分册,1994,15(4):228~230
3,马培奇.肿瘤化、放疗所致恶心和呕吐防治药物的研究进展及其市场分析.中国制药信息,1998,14(7):9~13
, http://www.100md.com
4,Kawakita Takeshi,Haga keiichiro,Asano Kyoshi.Hyperemesis inhibitors containing benzoxazine compounds.Jpn Kokai Tokkyo Koho,JP08 27000〔96 27000〕.30 Jan 1996(CA 124:250944x)
5,Kawakita Takeshi,Hage keiichiro,Asano Kyoshi.Postoperative emesis inhibitors containing benzoxazine compounds.Jpn Kokai Tokkyo Koho,JP08 27001〔96 27001〕.30 Jan 1996(CA 124:250945y)
6,Kawakita T,Kuroita T,Yasumoto M,et al.Synthesis and pharmacology of 3,4-dihydro-3-oxo-1,4-benzoxazine-8-carboxamide derivatives,a new class of potent serotonin-3(5-HT3)receptor antagonists.Chem Pharm Bull,1992,40(3):624~630
7,Tahara T,Kawakita T,Yasumoto M,et al.Benzoxazine compounds and pharmaceutical use thereof.US 4892872.1990-01-09
8,Duda H,Ostaszynski A,Urbanski T.Halosalicylohydroxamic acids.I.Dihalosalicylohydroxamic acids.Bull Acad Polon Sci,Ser Sci Chim,13(5),341~347(CA63:16255b)
收稿日期:2000-02-25, 百拇医药