胰岛素微粒剂的体外释药、小鼠体内分布与绝对生物利用度
作者:王思玲 苏德森 顾学裘 张景海
单位:王思玲 苏德森 顾学裘(沈阳药科大学药学系);张景海(制药系, 沈阳 110015)
关键词:胰岛素微粒剂;放射免疫分析;体外释药;放射性;生物利用度;组织分布
沈阳药科大学学报000201 摘 要:采用放射免疫分析方法测定了胰岛素微粒剂的体外释药性.用放射性标记技术制备了125Ⅰ-胰岛素微粒制剂,且以微粒剂中125Ⅰ-胰岛素的放射性计数为指标,研究了125Ⅰ-胰岛素在小鼠体内的生物利用度与组织分布. 研究表明:微粒剂在不同pH值的磷酸盐缓冲液中,释药规律接近一级动力学方程:ln(Q∞-Q)=bt+A,相关系数为rpH 2.5=-0.939 8、rpH 7.0=-0.993 3,但更好地符合自拟释药方程:Q=Q∞bt/(1+bt),相关系数为rpH 2.5=-0.995 2、rpH 7.0=-0.996 9.小鼠口服绝对生物利用度为11.51%±4.41%.125Ⅰ-胰岛素在小鼠脏器的同位素强度分布依次为肝、肾、心、肺、脾.
, http://www.100md.com
分类号:R94
Release Characteristics, Absolute Bioavailability and Distribution of the Insulin Microparticles(INS-MP)in Mice
Wang Siling Su Desen Gu Xueqiu Zhang Jinghai
(Department of Pharmacy; Shenyang Pharmaceutical University, Shenyang 110015)
Abstract:The release characteristics of INS-MP were measured by the use of RIA. Using 125Ⅰ labelled insulin,the preparation,absolute bioavailability and distribution of the 125Ⅰinsulin microparticles in mice were studied according to the remaining activities of 125Ⅰinsulin radioactivities.The studies indicated that the insulin-releasing profiles in vitro approached to the first order equation ln(Q∞-Q)=bt+A,rpH 2.5=-0.939 8、rpH 7.0=-0.993 3,and more fitted to the self-draft equation Q=Q∞bt/(1+bt),rpH 2.5=-0.995 2、rpH 7.0=-0.996 9.The absolute bioavailability was 11.51%±4.41%,the distribution sequence of isotope intensity of 125Ⅰ labelled insulin in mice′tissues was as follows:liver,kidney,heart,lungs and spleen.
, 百拇医药
Key words:insulin microparticles; radioimmunoassay; releasing in vitro; radioactivity; bioavailability; tissue distribution▲
胰岛素(insulin)作为降血糖生化药,自1923年开始应用于治疗糖尿病(diabetes)已有75年的历史,迄今为止仍是胰岛素依赖性糖尿病(IDDM)患者的首选药. 就胰岛素口服给药制剂而言,普遍存在的问题是吸收差、生物利用度低.作者制得的胰岛素微粒剂,小鼠口服后,可使外源性胰岛素进入血液循环,小鼠口服绝对生物利用度较高.对其制剂的释药性研究目前较普遍采用的方法为高效液相色谱法及紫外分析法,采用放射免疫分析法国内外未见报道.
1 实验材料
昆明种小鼠(18~22 g,雌雄兼用,由本校动物中心提供);胰岛素原料(27.6 u/mg,徐州万帮生化制药厂);胰岛素标准品(27 u/mg,中国生物制品检定所);125Ⅰ-胰岛素放射免疫分析药盒(中国原子能科学研究院);Na125Ⅰ(中国原子能科学院标记生产,使用时比活性为135.25 mci/mL);氯胺T。3H2O(佘山化工厂);Sephadex G-25(瑞典进口);明胶(A型,沈阳试剂二厂);胰岛素微粒剂(自制);TCL-16B高速台式离心机(上海安亭科学仪器厂);Kontron-IIr计数器(瑞士);HR全自动释放仪(美国).
, http://www.100md.com
2 方法与结果
2.1 微粒剂中胰岛素放射免疫测定方法与方法验证
2.1.1 胰岛素放射免疫分析工作曲线的建立〔1,2〕
精密配制胰岛素标准溶液5.00、10.0、20.0、40.0、80.0及160 mIU/L共6份,按表1分别进行胰岛素放射免疫测定,在半对数纸上绘制标准浓度点5.00 mIU/L~160 mIU/L与相应的B/B0%的标准曲线,见图1.血样中胰岛素的含量可由其B/B0%的值从标准曲线上查得.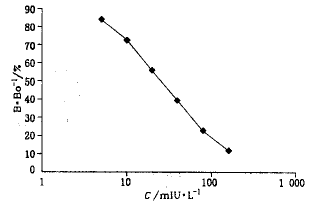
Fig.1 RIA standard curve for insulin
, 百拇医药 Tab.1 Insulin radioimmunoassay(RIA)
T tube /mL
Standard curve groups /mL
Assay /mL
Unspecific tube
Original tube
Standard tube
Incubation reagent
0.2
0.1
Insulin standard solution
, http://www.100md.com
0.1
Assay samples
0.1
Insulin antibodies
0.1
0.1
0.1
125Ⅰ-insulin
0.1
0.1
0.1
0.1
, http://www.100md.com
0.1
Stir evenly 37℃ 2 h
Separation reagent
0.5
0.5
0.5
0.5
Stir evenly,at room temperature for 15 min
充分摇匀3.5×103 r/min离心15 min,弃去上清液后测定沉淀放射性强度.
非特异NSB=706/23 097×100%=3.1%;
, http://www.100md.com
最大结合率B0=11 561/23 097×100%=50.0%.
2.1.2 微粒剂中胰岛素放射免疫分析回收率实验
精密配制胰岛素标准溶液0.5 mg/mL(13.5 IU/mL),以胰岛素与空白辅料质量之比1∶50按表2用量混合6份样品,分别回收各份样品中胰岛素,作放射免疫测定,结果见表2.
Tab.2 Recoveries of the measurement method Preparation/n
Insulin/IU
Insulin(Adjuvant)/mg
Measure/IU
, http://www.100md.com
Recovery/%
1
135.0
5.0(250)
132.3
98.0
2
135.0
5.0(250)
133.0
98.5
3
67.51
, 百拇医药
2.5(125)
66.91
99.1
4
67.50
2.5(125)
67.81
100.4
5
27.01
1.0(50)
26.70
98.9
, http://www.100md.com
6
27.00
1.0(50)
26.81
99.3
平均回收率99.0%±0.74%,变异系数为0.75%2.2 胰岛素微粒剂的体外释药2.2.1 体外释药试验〔3,4〕
精密称取制剂10.0 g置于1 000 mL(37±1)℃恒温介质(pH=7.0或pH=2.5 PBS)中,定时取样5 mL,同时补充等量的释放介质,样品以0.8 μm微孔滤膜过滤,取滤液定容作放射免疫活性测定,按右式计算累积释药百分率,释药数据见表3.
累积释药百分率(Q)=(CnVT+Cn-1Vs)/(S L)×100%.
, http://www.100md.com
Tab.3 Release profiles of INS-MP at various media(n=3) Time /min×10-2
0.50
1.00
2.00
3.00
4.50
6.00
9.00
pH 7.0 BB-10/%
24.5±2.1
, 百拇医药
22.0±1.4
21.1±1.7
20.4±2.3
19.2±1.5
18.6±0.9
18.1±3.3
Q/%
65.9±3.7
78.3±2.2
84.7±4.4
88.5±4.4
91.2±2.0
, 百拇医药
93.4±1.7
95.6±1.1
pH 2.5 BB-10/%
23.9±1.4
21.7±1.9
20.8±2.1
19.5±0.9
18.3±0.5
17.7±1.1
17.4±0.7
Q′/%
, 百拇医药
66.2±2.4
81.7±3.1
86.6±3.0
91.7±2.7
93.6±2.5
94.5±0.8
96.1±0.3
式中Cn:n次取样时药物浓度(IU/mL);VT:释药介质总体积(mL);Vs:取样体积(mL);S:称取的制剂总量(mg);L:制剂标示含量(IU/mg);n:取样次数(n=1、2、3……7;当n=1时,Cn-1=C0=0);Q:累积释药百分率(%).
, 百拇医药
2.2.2释药动力学方程模拟
将表3释药数据处理后,得表4.
Tab.4 Release profiles and fitted equations of INS-MP at different media 1/t×102
2.00
1.00
0.50
0.33
0.22
0.17
0.11
, 百拇医药
1/Q×102
1.518
1.277
1.181
1.130
1.096
1.071
1.048
1/Q′×102
1.510
1.224
1.155
, http://www.100md.com
1.090
1.068
1.058
1.040
1/Q-t-1
1/Q=0.241 0 t-1+1.040×10-2
r=0.996 9
1/Q′-t-1
1/Q′=0.241 7 t-1+1.013×10-2
r=0.995 2
, http://www.100md.com
结果可见1/Q(1/Q′)与1/t线性关系较好. 将释药数据分别按照零级、一级、Higuchi、Baker-Lonsdale(Spherical Matrix)模型拟合,结果见表5.Tab.5 Fitted equations and correlation coefficients of release profiles of INS-MP Model
employed
Fitted equation
pH 7.0
pH 2.5
Zero order
Q=2.852×10-2t+74.75 r=0.836 4
, 百拇医药
Q=2.713×10-2t+77.12 r=0.779 4
First order
ln(Q∞-Q )=-4.110×10-3t+3.437
r=-0.993 3
ln(Q∞-Q)=-2.719×10-3t+3.120
r=-0.939 8
Higuchi
Q=1.168t1/2+64.62 r=0.918 2
, 百拇医药 Q=1.133t1/2+67.08 r=0.873 2
Baker-Lonsdale
3/2[1-(1-Q)2/3]-Q=1.037×10-3t+0.165 6
r=-0.917 9
3/2[1-(1-Q)2/3]-Q=1.099×10-3t+0.182 5 r=-0.900 4
*1/Q=At-1+B
or
1/Q=0.241 0 t-1+1.040×10-2
, 百拇医药
r=0.996 9
1/Q′=0.242 7t-1+1.013×10-2
r=0.995 2
Q=Q∞bt/(1+bt)or
Q=Q∞4.314×10-2t/(1+4.314×10-2t) or
Q=Q∞4.176×10-2t/(1+4.176×10-2t)
*Self-draft
2.3 125Ⅰ-胰岛素标记
, http://www.100md.com
125Ⅰ-胰岛素标记参照氯胺T法〔5,6〕,在1.5 mL离心管中加入10 mg/mL胰岛素溶液(0.05 mol/L,pH7.4 PBS)200 μL与10 mciNa125Ⅰ混匀后,再加20 mg/mL氯胺T溶液(0.05 mol/L,pH7.4 PBS)80 μL,振荡,反应3 min后,加80 mg/mL焦亚硫酸钠溶液(0.05 mol/L,pH7.4 PBS)320 μL,振荡5 min,以终止反应,滴加1%KI溶液至无碘色出现为止.
上述标记液经Sephadex G-25层析柱(洗脱液0.1 mol/L,pH5.8 PBS),除去游离的125Ⅰ及标记液小分子化合物,层析图谱见图2,合并第一个洗脱峰溶液,冷冻真空干燥后,-20℃保存备用.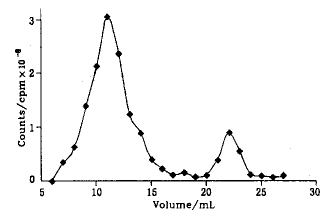
Fig.2 Separation of 125Ⅰ-labelled insulin from 〔125〕iodide on sephadex G-25
, 百拇医药
2.4 125Ⅰ-胰岛素微粒剂制备
取40 mg胰岛素及10 mg 125I-胰岛素以混合0.2 mol/L pH5.8 PBS配成0.1%胰岛素溶液,搅拌下缓慢滴加等体积的明胶溶液(0.2mol/L,pH5.8 PBS)得絮状混悬液,离心、弃去上清液得胰岛素明胶复合物,加入0.2 mol/L的pH5.8 PBS使复合物浓度为32 mg/L,按复合物与空白脂质体质量体积比8∶1加入空白脂质体,高速匀浆、分散,冷冻干燥,过筛得胰岛素微粒制剂.
2.5 微粒剂绝对生物利用度〔7,8〕
取体重20~21 g小鼠120只,雌雄各半,随机均分20组,每组6只. 其中10组小鼠按17 IU/kg剂量给小鼠灌服125Ⅰ-胰岛素的微粒剂,于给药后0.5、1.0、2.0、4.0、6.0、8.0、12.0、16.0、20.0、24.0 h各时间点取1组小鼠的全血约1.0 mL,于1.5 mL离心管中,以1.5×104 r/min离心5 min,取血清后于-20℃冷冻备用. 另外10组小鼠,按0.43 IU/kg剂量给小鼠尾静脉注射制备125Ⅰ-胰岛素微粒剂时的原料(125Ⅰ-胰岛素+胰岛素),在给药0.08、0.17、0.34、0.50、1.00、2.00、4.00、6.00、8.00、12.00 h各时间点取1组小鼠的全血约1.0 mL,于1.5 mL离心管,以1.5×104 r/min离心5 min,取血清后于-20℃冷冻备用.
, 百拇医药
按文献〔9,10〕方法,分别取上述所采集的各实验点血清样400 μL,加200 μL胰岛素抗体,摇匀后置37℃保温2 h,加500 μL分离试剂,摇匀后以3.5×103 r/min离心15 min,弃去上清液后,测定沉淀物的放射性计数,结果见图3. 另取一定量前述给小鼠注射及口服的125Ⅰ-胰岛素样品,测定该样放射性计数,并求出每单位胰岛素的放射性计数.
Fig.3 Pharmacokinetic profiles of 125Ⅰ-insulin radioactivities of INS-MP in mice
1—INS-MP(17.00 u/kg iv); 2—INS(0.43 u/kg po)
, 百拇医药 按下述公式计算口服胰岛素微粒剂的绝对生物利用度(F),计算结果见表6.
F=(AUCp.o/Dosep.o)/(AUCi.v/Dosei.v)×100%.
AUCp.o为实验动物灌服微粒剂后血清125Ⅰ-胰岛素计数曲线下面积;Dosep.o为实验动物微粒剂给药剂量125Ⅰ-胰岛素计数;AUCi.v为实验动物尾静脉注射后血清125Ⅰ-胰岛素计数曲线下面积;Dosei.v为实验动物尾静脉注射给药剂量的125Ⅰ-胰岛素计数.
Tab.6 The results of absolute bioavailability calculated Dose/u。kg-1
, 百拇医药
Via
Tmax/h
Cmax/cpm
AUC/cpm×h
F/%
17
p.o
1.00
2 916±210
16 180±
1 040
11.51±4.41
, 百拇医药
0.43
i.v
0.08
2 898±200
3 526±
236
2.6 微粒剂125Ⅰ-胰岛素在体内分布〔10〕 在本实验“2.5”中,给小鼠灌服125Ⅰ-胰岛素微粒剂后1.0、2.0、4.0、8.0、12.0、24.0 h各时间点取样后,立即处死小鼠并剖取肝、心、脾、肺和肾,用生理盐水漂洗3次,以除去残留血液,精密称取50 mg,测定各样本放射性计数.以实验小鼠口服剂量的总放射性计数为基数,计算各时间点各脏器中放射性残留率,结果见图4.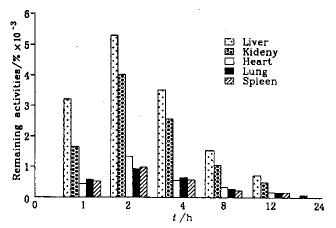
, 百拇医药
Fig.4 Distribution of 125Ⅰ-insulin radioactivities in mice′tissues
3 讨论
由体外释药结果可见:微粒剂的释药规律符合1/Q=bt-1+A(或Q=Q∞bt/(1+bt))动力学方程,释药15 h累积释放胰岛素量达到最大值96.8%~99.0%,体外释药时间较体内释药时间更长(动物服药后,药效持续8~10 h). 因为体内释药过程比体外释药过程更复杂,除体外的因素外,主要是体内的各种因素,诸如各种蛋白水解酶、胃肠道分泌液、肠道中的胆汁和胰液等.另外由于制剂中明胶等辅料在胃肠道中被逐步降解等而使它们所形成的相应结构被破坏,如脂质体膜结构、明胶的三维网状结构等,从而使其中的胰岛素更快被释放并被降解,体内药物的释放不是一个累积的过程(而体外释药是释放与吸附的动态平衡过程).上述综合因素,均可促使体内释药速度加快.
, 百拇医药
有关释药方程Q=Q∞bt/(1+bt):Q∞为最大累积释放量,b为一常数. 当温度、介质、制剂材料一定时,Q∞、b不变. 为便于从实验数据计算Q∞与b值,将上式改写为1/Q=1/Q∞+1/Q∞bt(or 1/Q=bt-1+A).以1/Q对1/t作图,得一直线,斜率为1/Q∞b,截距为1/Q∞,可求Q∞,则b=截距/斜率. Q=Q∞bt/(1+bt)很好地描述微粒剂释放胰岛素的全过程:当bt1,即释放初期:Q=Q∞bt表示在一定温度下,释放量与时间成正比,释放曲线几乎是直线;当bt1,即释放后期:Q=Q∞表示释放达到饱和后,就不再随时间的变化而变化,释放曲线几乎成水平线. 微粒剂释放胰岛素的过程极其复杂,涉及到微粒组成材料的性质、微粒密度、表面电荷、胰岛素在微粒中的部位和药物与微粒间的物理化学作用,还有释药环境等诸因素. 要详尽推导出该公式,还需要解决许多理论问题,如微粒表面是否均匀,微粒表面胰岛素相互之间有无作用力等,作者意在通过实验数据找到微粒剂释药的规律. 该方程能否用于描述其它固体制剂的体外释药规律,还需要作大量试验加以验证.
, 百拇医药
在一般药物的生物利用度测定中,较普遍采用的检测方法是HPLC法,就胰岛素而言,采用通用的检测方法不能解决其特异性问题,又因剂量小,用生物法也会产生较大的实验误差,为此,综合各种因素,作者采用125Ⅰ-胰岛素作为口服微粒剂的外源性有效成分,以提高实验检测的灵敏度,同时利用胰岛素免疫沉淀反应提高实验检测的灵敏度. 实验结果表明:微粒剂中125Ⅰ-胰岛素经胃肠道被实验动物吸收进入血液,并在给药后1 h左右达到最高,且400 μL血样中的125Ⅰ-胰岛素占口服剂量的0.146%. 实验结果可见,口服微粒剂的125Ⅰ-胰岛素在实验动物血液滞留时间较注射给予的125Ⅰ-胰岛素的明显延长,分析微粒剂中的胰岛素以一种或几种复合物形式被机体吸收,这种被吸收的复合物不仅减缓了血液中的各种蛋白酶对胰岛素的降解,同时也表现出缓释的作用. 微粒剂中125Ⅰ-胰岛素在实验动物的肝、心、脾、肺和肾分布情况同注射给药的分布情况类同,但微粒剂中的125Ⅰ-胰岛素在这些脏器的残留时间较注射给药的明显延长,这同上述血清125Ⅰ-胰岛素残留情况相吻合.
, http://www.100md.com
参考文献:
[1]中国原子能科学研究院.125Ⅰ-胰岛素放射免疫分析药盒说明书.北京:中国原子能科学研究院,1997.
[2]王浩丹,周申. 生物医学标记示踪技术.北京:人民卫生出版社,1995.69
[3]Leucuta SE. The kinetics of in vitro release and the pharmacokinetics of miotic response in rabbits of gelatin and album in microspheres with pilocarpine. Int J Pharm,1989,54(1):71~78
[4]张强,丁继军,叶国庆,等.口服胰岛素毫微球的体外释药及对糖尿病大鼠的降血糖作用.药学学报,1998,33(2):152~156
, http://www.100md.com
[5]Greenwood FC,Hunter WM. The preparation of 131Ⅰ-Laelled human growth hormone of high specific radioactivity. Biochem J,1963,89(1):114~123
[6]Benjamin W,Dong GL. Assay of plasma insulin in human subjects by immunological methods. Nature,1959,184(21):1648~1649
[7]Schipper GM,Stefan GR,Verhoef JC,et al. Nasal insulin delivery with dimetyl-β-cyclodextrin as absorption enhancer in rabbits:power more effective than liqui formulations. Pharm Res,1993,10(5):682~686
, 百拇医药
[8]Willan A,Blair A,Thomas W,et al. Intranasal bioav-ailability of insulin powder formulations:effect of permeation enhancer-to-protein ratio. J Pharm Sci,1991,80(8):725~729
[9]王树歧,赵秋宇,王波,等. PEG2修饰125I-L-天冬酰胺酶在小鼠体内的分布与代谢. 药物生物技术,1996,3(1):18~21
[10]尤育初,钱林法,赵永彦,等.125Ⅰ-人胸腺素的标记及其在小鼠体内的分布与代谢研究. 中国生化药物杂志,1996,17(2):70~72
收稿日期:1999-05-17, http://www.100md.com
单位:王思玲 苏德森 顾学裘(沈阳药科大学药学系);张景海(制药系, 沈阳 110015)
关键词:胰岛素微粒剂;放射免疫分析;体外释药;放射性;生物利用度;组织分布
沈阳药科大学学报000201 摘 要:采用放射免疫分析方法测定了胰岛素微粒剂的体外释药性.用放射性标记技术制备了125Ⅰ-胰岛素微粒制剂,且以微粒剂中125Ⅰ-胰岛素的放射性计数为指标,研究了125Ⅰ-胰岛素在小鼠体内的生物利用度与组织分布. 研究表明:微粒剂在不同pH值的磷酸盐缓冲液中,释药规律接近一级动力学方程:ln(Q∞-Q)=bt+A,相关系数为rpH 2.5=-0.939 8、rpH 7.0=-0.993 3,但更好地符合自拟释药方程:Q=Q∞bt/(1+bt),相关系数为rpH 2.5=-0.995 2、rpH 7.0=-0.996 9.小鼠口服绝对生物利用度为11.51%±4.41%.125Ⅰ-胰岛素在小鼠脏器的同位素强度分布依次为肝、肾、心、肺、脾.
, http://www.100md.com
分类号:R94
Release Characteristics, Absolute Bioavailability and Distribution of the Insulin Microparticles(INS-MP)in Mice
Wang Siling Su Desen Gu Xueqiu Zhang Jinghai
(Department of Pharmacy; Shenyang Pharmaceutical University, Shenyang 110015)
Abstract:The release characteristics of INS-MP were measured by the use of RIA. Using 125Ⅰ labelled insulin,the preparation,absolute bioavailability and distribution of the 125Ⅰinsulin microparticles in mice were studied according to the remaining activities of 125Ⅰinsulin radioactivities.The studies indicated that the insulin-releasing profiles in vitro approached to the first order equation ln(Q∞-Q)=bt+A,rpH 2.5=-0.939 8、rpH 7.0=-0.993 3,and more fitted to the self-draft equation Q=Q∞bt/(1+bt),rpH 2.5=-0.995 2、rpH 7.0=-0.996 9.The absolute bioavailability was 11.51%±4.41%,the distribution sequence of isotope intensity of 125Ⅰ labelled insulin in mice′tissues was as follows:liver,kidney,heart,lungs and spleen.
, 百拇医药
Key words:insulin microparticles; radioimmunoassay; releasing in vitro; radioactivity; bioavailability; tissue distribution▲
胰岛素(insulin)作为降血糖生化药,自1923年开始应用于治疗糖尿病(diabetes)已有75年的历史,迄今为止仍是胰岛素依赖性糖尿病(IDDM)患者的首选药. 就胰岛素口服给药制剂而言,普遍存在的问题是吸收差、生物利用度低.作者制得的胰岛素微粒剂,小鼠口服后,可使外源性胰岛素进入血液循环,小鼠口服绝对生物利用度较高.对其制剂的释药性研究目前较普遍采用的方法为高效液相色谱法及紫外分析法,采用放射免疫分析法国内外未见报道.
1 实验材料
昆明种小鼠(18~22 g,雌雄兼用,由本校动物中心提供);胰岛素原料(27.6 u/mg,徐州万帮生化制药厂);胰岛素标准品(27 u/mg,中国生物制品检定所);125Ⅰ-胰岛素放射免疫分析药盒(中国原子能科学研究院);Na125Ⅰ(中国原子能科学院标记生产,使用时比活性为135.25 mci/mL);氯胺T。3H2O(佘山化工厂);Sephadex G-25(瑞典进口);明胶(A型,沈阳试剂二厂);胰岛素微粒剂(自制);TCL-16B高速台式离心机(上海安亭科学仪器厂);Kontron-IIr计数器(瑞士);HR全自动释放仪(美国).
, http://www.100md.com
2 方法与结果
2.1 微粒剂中胰岛素放射免疫测定方法与方法验证
2.1.1 胰岛素放射免疫分析工作曲线的建立〔1,2〕
精密配制胰岛素标准溶液5.00、10.0、20.0、40.0、80.0及160 mIU/L共6份,按表1分别进行胰岛素放射免疫测定,在半对数纸上绘制标准浓度点5.00 mIU/L~160 mIU/L与相应的B/B0%的标准曲线,见图1.血样中胰岛素的含量可由其B/B0%的值从标准曲线上查得.

Fig.1 RIA standard curve for insulin
, 百拇医药 Tab.1 Insulin radioimmunoassay(RIA)
T tube /mL
Standard curve groups /mL
Assay /mL
Unspecific tube
Original tube
Standard tube
Incubation reagent
0.2
0.1
Insulin standard solution
, http://www.100md.com
0.1
Assay samples
0.1
Insulin antibodies
0.1
0.1
0.1
125Ⅰ-insulin
0.1
0.1
0.1
0.1
, http://www.100md.com
0.1
Stir evenly 37℃ 2 h
Separation reagent
0.5
0.5
0.5
0.5
Stir evenly,at room temperature for 15 min
充分摇匀3.5×103 r/min离心15 min,弃去上清液后测定沉淀放射性强度.
非特异NSB=706/23 097×100%=3.1%;
, http://www.100md.com
最大结合率B0=11 561/23 097×100%=50.0%.
2.1.2 微粒剂中胰岛素放射免疫分析回收率实验
精密配制胰岛素标准溶液0.5 mg/mL(13.5 IU/mL),以胰岛素与空白辅料质量之比1∶50按表2用量混合6份样品,分别回收各份样品中胰岛素,作放射免疫测定,结果见表2.
Tab.2 Recoveries of the measurement method Preparation/n
Insulin/IU
Insulin(Adjuvant)/mg
Measure/IU
, http://www.100md.com
Recovery/%
1
135.0
5.0(250)
132.3
98.0
2
135.0
5.0(250)
133.0
98.5
3
67.51
, 百拇医药
2.5(125)
66.91
99.1
4
67.50
2.5(125)
67.81
100.4
5
27.01
1.0(50)
26.70
98.9
, http://www.100md.com
6
27.00
1.0(50)
26.81
99.3
平均回收率99.0%±0.74%,变异系数为0.75%2.2 胰岛素微粒剂的体外释药2.2.1 体外释药试验〔3,4〕
精密称取制剂10.0 g置于1 000 mL(37±1)℃恒温介质(pH=7.0或pH=2.5 PBS)中,定时取样5 mL,同时补充等量的释放介质,样品以0.8 μm微孔滤膜过滤,取滤液定容作放射免疫活性测定,按右式计算累积释药百分率,释药数据见表3.
累积释药百分率(Q)=(CnVT+Cn-1Vs)/(S L)×100%.
, http://www.100md.com
Tab.3 Release profiles of INS-MP at various media(n=3) Time /min×10-2
0.50
1.00
2.00
3.00
4.50
6.00
9.00
pH 7.0 BB-10/%
24.5±2.1
, 百拇医药
22.0±1.4
21.1±1.7
20.4±2.3
19.2±1.5
18.6±0.9
18.1±3.3
Q/%
65.9±3.7
78.3±2.2
84.7±4.4
88.5±4.4
91.2±2.0
, 百拇医药
93.4±1.7
95.6±1.1
pH 2.5 BB-10/%
23.9±1.4
21.7±1.9
20.8±2.1
19.5±0.9
18.3±0.5
17.7±1.1
17.4±0.7
Q′/%
, 百拇医药
66.2±2.4
81.7±3.1
86.6±3.0
91.7±2.7
93.6±2.5
94.5±0.8
96.1±0.3
式中Cn:n次取样时药物浓度(IU/mL);VT:释药介质总体积(mL);Vs:取样体积(mL);S:称取的制剂总量(mg);L:制剂标示含量(IU/mg);n:取样次数(n=1、2、3……7;当n=1时,Cn-1=C0=0);Q:累积释药百分率(%).
, 百拇医药
2.2.2释药动力学方程模拟
将表3释药数据处理后,得表4.
Tab.4 Release profiles and fitted equations of INS-MP at different media 1/t×102
2.00
1.00
0.50
0.33
0.22
0.17
0.11
, 百拇医药
1/Q×102
1.518
1.277
1.181
1.130
1.096
1.071
1.048
1/Q′×102
1.510
1.224
1.155
, http://www.100md.com
1.090
1.068
1.058
1.040
1/Q-t-1
1/Q=0.241 0 t-1+1.040×10-2
r=0.996 9
1/Q′-t-1
1/Q′=0.241 7 t-1+1.013×10-2
r=0.995 2
, http://www.100md.com
结果可见1/Q(1/Q′)与1/t线性关系较好. 将释药数据分别按照零级、一级、Higuchi、Baker-Lonsdale(Spherical Matrix)模型拟合,结果见表5.Tab.5 Fitted equations and correlation coefficients of release profiles of INS-MP Model
employed
Fitted equation
pH 7.0
pH 2.5
Zero order
Q=2.852×10-2t+74.75 r=0.836 4
, 百拇医药
Q=2.713×10-2t+77.12 r=0.779 4
First order
ln(Q∞-Q )=-4.110×10-3t+3.437
r=-0.993 3
ln(Q∞-Q)=-2.719×10-3t+3.120
r=-0.939 8
Higuchi
Q=1.168t1/2+64.62 r=0.918 2
, 百拇医药 Q=1.133t1/2+67.08 r=0.873 2
Baker-Lonsdale
3/2[1-(1-Q)2/3]-Q=1.037×10-3t+0.165 6
r=-0.917 9
3/2[1-(1-Q)2/3]-Q=1.099×10-3t+0.182 5 r=-0.900 4
*1/Q=At-1+B
or
1/Q=0.241 0 t-1+1.040×10-2
, 百拇医药
r=0.996 9
1/Q′=0.242 7t-1+1.013×10-2
r=0.995 2
Q=Q∞bt/(1+bt)or
Q=Q∞4.314×10-2t/(1+4.314×10-2t) or
Q=Q∞4.176×10-2t/(1+4.176×10-2t)
*Self-draft
2.3 125Ⅰ-胰岛素标记
, http://www.100md.com
125Ⅰ-胰岛素标记参照氯胺T法〔5,6〕,在1.5 mL离心管中加入10 mg/mL胰岛素溶液(0.05 mol/L,pH7.4 PBS)200 μL与10 mciNa125Ⅰ混匀后,再加20 mg/mL氯胺T溶液(0.05 mol/L,pH7.4 PBS)80 μL,振荡,反应3 min后,加80 mg/mL焦亚硫酸钠溶液(0.05 mol/L,pH7.4 PBS)320 μL,振荡5 min,以终止反应,滴加1%KI溶液至无碘色出现为止.
上述标记液经Sephadex G-25层析柱(洗脱液0.1 mol/L,pH5.8 PBS),除去游离的125Ⅰ及标记液小分子化合物,层析图谱见图2,合并第一个洗脱峰溶液,冷冻真空干燥后,-20℃保存备用.

Fig.2 Separation of 125Ⅰ-labelled insulin from 〔125〕iodide on sephadex G-25
, 百拇医药
2.4 125Ⅰ-胰岛素微粒剂制备
取40 mg胰岛素及10 mg 125I-胰岛素以混合0.2 mol/L pH5.8 PBS配成0.1%胰岛素溶液,搅拌下缓慢滴加等体积的明胶溶液(0.2mol/L,pH5.8 PBS)得絮状混悬液,离心、弃去上清液得胰岛素明胶复合物,加入0.2 mol/L的pH5.8 PBS使复合物浓度为32 mg/L,按复合物与空白脂质体质量体积比8∶1加入空白脂质体,高速匀浆、分散,冷冻干燥,过筛得胰岛素微粒制剂.
2.5 微粒剂绝对生物利用度〔7,8〕
取体重20~21 g小鼠120只,雌雄各半,随机均分20组,每组6只. 其中10组小鼠按17 IU/kg剂量给小鼠灌服125Ⅰ-胰岛素的微粒剂,于给药后0.5、1.0、2.0、4.0、6.0、8.0、12.0、16.0、20.0、24.0 h各时间点取1组小鼠的全血约1.0 mL,于1.5 mL离心管中,以1.5×104 r/min离心5 min,取血清后于-20℃冷冻备用. 另外10组小鼠,按0.43 IU/kg剂量给小鼠尾静脉注射制备125Ⅰ-胰岛素微粒剂时的原料(125Ⅰ-胰岛素+胰岛素),在给药0.08、0.17、0.34、0.50、1.00、2.00、4.00、6.00、8.00、12.00 h各时间点取1组小鼠的全血约1.0 mL,于1.5 mL离心管,以1.5×104 r/min离心5 min,取血清后于-20℃冷冻备用.
, 百拇医药
按文献〔9,10〕方法,分别取上述所采集的各实验点血清样400 μL,加200 μL胰岛素抗体,摇匀后置37℃保温2 h,加500 μL分离试剂,摇匀后以3.5×103 r/min离心15 min,弃去上清液后,测定沉淀物的放射性计数,结果见图3. 另取一定量前述给小鼠注射及口服的125Ⅰ-胰岛素样品,测定该样放射性计数,并求出每单位胰岛素的放射性计数.

Fig.3 Pharmacokinetic profiles of 125Ⅰ-insulin radioactivities of INS-MP in mice
1—INS-MP(17.00 u/kg iv); 2—INS(0.43 u/kg po)
, 百拇医药 按下述公式计算口服胰岛素微粒剂的绝对生物利用度(F),计算结果见表6.
F=(AUCp.o/Dosep.o)/(AUCi.v/Dosei.v)×100%.
AUCp.o为实验动物灌服微粒剂后血清125Ⅰ-胰岛素计数曲线下面积;Dosep.o为实验动物微粒剂给药剂量125Ⅰ-胰岛素计数;AUCi.v为实验动物尾静脉注射后血清125Ⅰ-胰岛素计数曲线下面积;Dosei.v为实验动物尾静脉注射给药剂量的125Ⅰ-胰岛素计数.
Tab.6 The results of absolute bioavailability calculated Dose/u。kg-1
, 百拇医药
Via
Tmax/h
Cmax/cpm
AUC/cpm×h
F/%
17
p.o
1.00
2 916±210
16 180±
1 040
11.51±4.41
, 百拇医药
0.43
i.v
0.08
2 898±200
3 526±
236
2.6 微粒剂125Ⅰ-胰岛素在体内分布〔10〕 在本实验“2.5”中,给小鼠灌服125Ⅰ-胰岛素微粒剂后1.0、2.0、4.0、8.0、12.0、24.0 h各时间点取样后,立即处死小鼠并剖取肝、心、脾、肺和肾,用生理盐水漂洗3次,以除去残留血液,精密称取50 mg,测定各样本放射性计数.以实验小鼠口服剂量的总放射性计数为基数,计算各时间点各脏器中放射性残留率,结果见图4.

, 百拇医药
Fig.4 Distribution of 125Ⅰ-insulin radioactivities in mice′tissues
3 讨论
由体外释药结果可见:微粒剂的释药规律符合1/Q=bt-1+A(或Q=Q∞bt/(1+bt))动力学方程,释药15 h累积释放胰岛素量达到最大值96.8%~99.0%,体外释药时间较体内释药时间更长(动物服药后,药效持续8~10 h). 因为体内释药过程比体外释药过程更复杂,除体外的因素外,主要是体内的各种因素,诸如各种蛋白水解酶、胃肠道分泌液、肠道中的胆汁和胰液等.另外由于制剂中明胶等辅料在胃肠道中被逐步降解等而使它们所形成的相应结构被破坏,如脂质体膜结构、明胶的三维网状结构等,从而使其中的胰岛素更快被释放并被降解,体内药物的释放不是一个累积的过程(而体外释药是释放与吸附的动态平衡过程).上述综合因素,均可促使体内释药速度加快.
, 百拇医药
有关释药方程Q=Q∞bt/(1+bt):Q∞为最大累积释放量,b为一常数. 当温度、介质、制剂材料一定时,Q∞、b不变. 为便于从实验数据计算Q∞与b值,将上式改写为1/Q=1/Q∞+1/Q∞bt(or 1/Q=bt-1+A).以1/Q对1/t作图,得一直线,斜率为1/Q∞b,截距为1/Q∞,可求Q∞,则b=截距/斜率. Q=Q∞bt/(1+bt)很好地描述微粒剂释放胰岛素的全过程:当bt1,即释放初期:Q=Q∞bt表示在一定温度下,释放量与时间成正比,释放曲线几乎是直线;当bt1,即释放后期:Q=Q∞表示释放达到饱和后,就不再随时间的变化而变化,释放曲线几乎成水平线. 微粒剂释放胰岛素的过程极其复杂,涉及到微粒组成材料的性质、微粒密度、表面电荷、胰岛素在微粒中的部位和药物与微粒间的物理化学作用,还有释药环境等诸因素. 要详尽推导出该公式,还需要解决许多理论问题,如微粒表面是否均匀,微粒表面胰岛素相互之间有无作用力等,作者意在通过实验数据找到微粒剂释药的规律. 该方程能否用于描述其它固体制剂的体外释药规律,还需要作大量试验加以验证.
, 百拇医药
在一般药物的生物利用度测定中,较普遍采用的检测方法是HPLC法,就胰岛素而言,采用通用的检测方法不能解决其特异性问题,又因剂量小,用生物法也会产生较大的实验误差,为此,综合各种因素,作者采用125Ⅰ-胰岛素作为口服微粒剂的外源性有效成分,以提高实验检测的灵敏度,同时利用胰岛素免疫沉淀反应提高实验检测的灵敏度. 实验结果表明:微粒剂中125Ⅰ-胰岛素经胃肠道被实验动物吸收进入血液,并在给药后1 h左右达到最高,且400 μL血样中的125Ⅰ-胰岛素占口服剂量的0.146%. 实验结果可见,口服微粒剂的125Ⅰ-胰岛素在实验动物血液滞留时间较注射给予的125Ⅰ-胰岛素的明显延长,分析微粒剂中的胰岛素以一种或几种复合物形式被机体吸收,这种被吸收的复合物不仅减缓了血液中的各种蛋白酶对胰岛素的降解,同时也表现出缓释的作用. 微粒剂中125Ⅰ-胰岛素在实验动物的肝、心、脾、肺和肾分布情况同注射给药的分布情况类同,但微粒剂中的125Ⅰ-胰岛素在这些脏器的残留时间较注射给药的明显延长,这同上述血清125Ⅰ-胰岛素残留情况相吻合.
, http://www.100md.com
参考文献:
[1]中国原子能科学研究院.125Ⅰ-胰岛素放射免疫分析药盒说明书.北京:中国原子能科学研究院,1997.
[2]王浩丹,周申. 生物医学标记示踪技术.北京:人民卫生出版社,1995.69
[3]Leucuta SE. The kinetics of in vitro release and the pharmacokinetics of miotic response in rabbits of gelatin and album in microspheres with pilocarpine. Int J Pharm,1989,54(1):71~78
[4]张强,丁继军,叶国庆,等.口服胰岛素毫微球的体外释药及对糖尿病大鼠的降血糖作用.药学学报,1998,33(2):152~156
, http://www.100md.com
[5]Greenwood FC,Hunter WM. The preparation of 131Ⅰ-Laelled human growth hormone of high specific radioactivity. Biochem J,1963,89(1):114~123
[6]Benjamin W,Dong GL. Assay of plasma insulin in human subjects by immunological methods. Nature,1959,184(21):1648~1649
[7]Schipper GM,Stefan GR,Verhoef JC,et al. Nasal insulin delivery with dimetyl-β-cyclodextrin as absorption enhancer in rabbits:power more effective than liqui formulations. Pharm Res,1993,10(5):682~686
, 百拇医药
[8]Willan A,Blair A,Thomas W,et al. Intranasal bioav-ailability of insulin powder formulations:effect of permeation enhancer-to-protein ratio. J Pharm Sci,1991,80(8):725~729
[9]王树歧,赵秋宇,王波,等. PEG2修饰125I-L-天冬酰胺酶在小鼠体内的分布与代谢. 药物生物技术,1996,3(1):18~21
[10]尤育初,钱林法,赵永彦,等.125Ⅰ-人胸腺素的标记及其在小鼠体内的分布与代谢研究. 中国生化药物杂志,1996,17(2):70~72
收稿日期:1999-05-17, http://www.100md.com