4NQO诱发两种品系大鼠舌癌过程中p53蛋白的表达特点
作者:李铁军
单位:北京医科大学口腔医学院病理科,100081
关键词:基因;p53;致癌性试验;大鼠
中华口腔医学杂志000215 【摘要】 目的 了解Dark-Agouti (DA)和Wistar/Furth (WF)两种品系的大鼠舌粘膜上皮在4-硝基喹啉-1-氧化物(4-nitroquinoline 1-oxide,4NQO)诱导舌癌过程中p53蛋白表达的动态变化。方法 实验动物的饮水中加入4NQO(0.001%),观察第2、4、8、12、16和26周时实验大鼠舌粘膜对p53的免疫组化表达。结果 p53的阳性反应在DA大鼠舌粘膜中出现早,且随着实验的推移,舌粘膜内的p53阳性细胞簇数目趋于增加,特别在实验后期尤为显著;WF大鼠各实验组间p53表达的水平较低,且变化不大。 结论 p53蛋白的表达水平反应了DA和WF大鼠对4NQO诱发舌癌易感性的差异。
, 百拇医药
Expression of p53 protein during 4NQO-induced lingual carcinogenesis in two strains of rats
LI Tiejun.
( Department of Oral Pathology, School of Stomatology, Beijing Medical University, Beijing 100081,China)
【Abstract】 Objective To investigate p53 protein expression during lingual carcinogenesis in two strains of rats. Methods Dark-Agouti (DA) and Wistar/Furth (WF) rats were administrated with 4-nitroquinoline 1-oxide (4NQO) in drinking water and expression of p53 was studied using experimental materials obtained at 2, 4, 8, 12, 16, and 26 weeks of 4NQO treatment. Results Epithelial clusters of p53 positive cells appeared earlier and more in numbers in DA rats than in WF. A marked increase of p53+ clusters in DA rats was noted at later stages of the experiment, whereas those in WF rats appeared to be unchanged. Conclusions These results suggest that there may be genetically determined variations in the p53 response to 4NQO between DA and WF rats, and these differences may contribute to their contrasting susceptibility during lingual carcinogenesis.
, 百拇医药
【Key words】 Genes,p53; Carcinogenicity tests; Rats
水溶性致癌剂4-硝基喹啉-1-氧化物(4-nitro-quinoline 1-oxide,4NQO)可诱发大鼠口腔粘膜的鳞状细胞癌[1],通过饮水给药,这种模型的癌发生率高,稳定性和重复性好,可模拟上皮过度增生、异常增生、原位癌以及浸润癌等一系列鳞癌发生过程中的典型病理过程。Kitano等[2]发现不同品系的大鼠对4NQO诱发舌癌的敏感性有所不同。在相同的实验条件下,Dark-Agouti (DA)和Wistar/Furth (WF)大鼠的舌癌发生率之间差异有显著性,其中DA大鼠的舌癌发生率高,常为多发性、巨大型 (直径>7 mm)肿瘤,而WF大鼠则表现出较低的易感性[2,3]。不同大鼠品系间实验性舌癌发生的差异提示某些遗传性易患因素在癌发生过程中可能起重要作用。p53基因编码的核蛋白对 DNA的转录和复制均有重要调控作用,野生型p53蛋白可阻止DNA受损细胞从G1期进入S期,抑制异常细胞的过度增殖;但其突变型则失去对细胞生长的调节作用,可促进细胞的恶性转化[4]。p53抑癌基因结构和功能的异常与大多数人类恶性肿瘤的发生密切相关[4]。在人类口腔癌的发生过程中,p53基因突变常出现在早期,且可呈多发性分布,为癌前和癌细胞克隆的扩增提供选择优势[5,6]。然而,在大鼠的化学致癌模型中有关p53基因异常的报道不多[7],仅个别报道涉及大鼠的口腔癌模型[8]。本研究旨在观察DA和WF品系大鼠的舌粘膜上皮在4NQO诱发舌癌的过程中p53蛋白表达的动态变化,比较其在两种品系大鼠间的差异,探讨其与大鼠实验性舌癌遗传性易患因素之间的相关关系。
, http://www.100md.com
材料和方法
一、动物实验和组织处理
近交系DA和WF大鼠分别购于日本静冈实验动物中心和日本广岛大学实验动物系。收集6周龄雄性DA和WF大鼠各42只,其中实验组各30只,对照组各12只。所有大鼠均饲养于铁丝笼具内(5~6只/笼),给予充足的基础食物和饮水。实验组动物的饮水中加入水溶性4NQO (终浓度为0.001%; 约7 mg/kg体重每天),而对照组则仅给予饮用水。在实验进行至第2、4、8、12、16和26周末时,采用过量乙醚、氯仿吸入法处死大鼠,其中实验组各5只,对照组各2只。从会厌部至口底前缘整体分离舌体,观察其大体形态,并沿舌体纵轴方向正中剖开,固定于10% 中性甲醛液中24~48 h,常规组织处理,石蜡包埋、切片,HE染色,组织学观察。
二、免疫组化染色及其评价
5 μm厚切片脱蜡,经等级酒精水化后,放入0.01 mol枸橼酸缓冲液 (pH 6.0),微波炉(800 W) 加热20 min,经3%过氧化氢阻断内源性氧化酶后,滴加 p53抗体 (CM5, 英国Novocastra公司;1:400,室温 1 h;该抗体是针对重组小鼠p53蛋白的兔抗血清,可与大鼠野生型及突变型 p53蛋白反应)。检测系统采用链亲和素/过氧化物酶技术 (LSAB试剂盒,美国DAKO公司),经DAB底物染色和适度苏木素复染后,脱水、透明、封片。所有试剂的稀释及切片冲洗均采用Tris缓冲液 (0.05 mol, pH 7.6)。光镜下细胞核呈明确棕褐色染色者视为阳性细胞。对所诱发的大鼠舌癌病变中的染色仅作定性评价,即记录p53阳性或阴性肿瘤;在非癌肿区舌粘膜内(包括邻近和远离舌癌的粘膜区域),p53阳性细胞常聚集成簇并散在分布于上皮的基底和(或)副基底层,因此对非癌肿区上皮内的 p53阳性细胞簇作了计数,即在镜下沿舌粘膜的全长(舌背及舌腹)连续记录 p53阳性细胞簇的数目。DA和 WF大鼠各组间计数资料的统计学处理采用Mann-Whitney U检验 (StatView-4.02 软件)。
, http://www.100md.com
结果
一、动物实验观察
所有对照组大鼠均无舌粘膜病变,实验组大鼠则随实验的进行而出现不同程度的舌粘膜病损,直至发生鳞状细胞癌。然而,DA和WF系大鼠对4NQO诱发舌癌的易感性存在明显差异(表1)。实验第8周末时,DA大鼠的舌粘膜即开始出现上皮异常增生,WF大鼠则到第12周末时才发生类似表现。随后,上皮异常增生病变的数目逐渐增加,这在DA大鼠实验组间更为明显。DA大鼠舌癌的发生也较WF大鼠出现的早而频繁,实验第16周末即有1只DA大鼠发生舌癌 (图1)。26周时实验组的5只DA大鼠均有舌癌形成,其中1只大鼠舌部同时发生3个肿瘤,而WF大鼠仅有1只发生了舌癌。

图1 DA大鼠于实验第16周发生了第1例舌癌(×) 图2 第16周DA大鼠舌粘膜内的p53阳性细胞簇(×150)
, 百拇医药
表1 4NQO诱发DA和WF大鼠舌癌实验的观察 组别
(周)
DA大鼠
WF大鼠
对照组
实验组
对照组
实验组
2
○○
○○○○○
○○
○○○○○
, http://www.100md.com
4
○○
○○○○○
○○
○○○○○
8
○○
◎◎◎◎○
○○
○○○○○
12
○○
◎◎◎◎◎
, http://www.100md.com
○○
◎◎◎◎○
16
○○
●◎◎◎◎
○○
◎◎◎◎◎
26
○○
●●●●●
○○
●◎◎◎◎
注:表内每个符号代表1只大鼠,其中○表示舌粘膜无病变;◎表示舌粘膜出现异常增生;●表示发生舌癌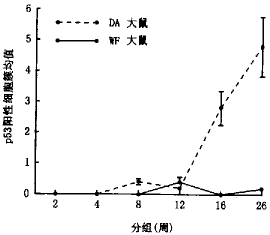
, http://www.100md.com
图3 各实验组p53阳性细胞簇计数均数
二、p53免疫组化染色
对照组大鼠的所有舌体标本均呈p53阴性。实验早期,2周和4周组大鼠的舌体标本中未见p53阳性染色。DA大鼠的舌粘膜内的p53阳性细胞于第8周末时出现,而WF大鼠舌粘膜内的p53阳性细胞则出现于第12周末。这些阳性细胞聚集成簇,散在分布于舌粘膜上皮的基底层和(或)副基底层(图2);大多数p53阳性 细胞簇发生于上皮呈异常增生的区域,约25%的阳性灶位于正常区域;随着实验时间的推移,DA大鼠的非癌肿区舌粘膜内p53阳性细胞簇数目趋于增加,特别是在实验后期 (16周和26周组) ;而WF大鼠各组间的计数值变化不明显。统计学处理表明: 16周和26周组DA与WF大鼠的p53阳性细胞簇计数值之间差异有显著性 (P<0.05,图3)。实验组DA大鼠所发生的8个舌癌中5个可见p53阳性染色(图4),其中发生于同一动物的3个舌癌中有2个呈p53阳性染色,1个呈阴性染色;实验组WF大鼠所发生的唯一1例舌癌不表达p53。在2只26周组DA大鼠中,虽然所诱发的舌癌不表达p53,但其非癌肿区舌粘膜中可见p53阳性细胞的存在。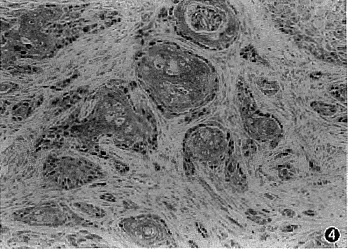
, 百拇医药
图4 呈p53阳性的舌癌癌巢,阳性细胞多为癌巢周边的基底细胞(×150)
讨论
与人类自然发生的肿瘤相比,化学致癌剂所诱发的啮齿类动物原发性肿瘤发生p53异常的频率较低[7]。Suzui等[8] 未能在4NQO诱发的F344大鼠舌癌中检测到p53基因突变,但该研究未作p53的免疫组化观察。本研究发现:对致癌剂较敏感的DA系大鼠的舌粘膜表达p53蛋白的水平显著高于易感性较差的WF系大鼠,DA大鼠舌粘膜内的p53阳性细胞簇计数在实验后期显著增加,而WF 大鼠各实验组间计数值的变化不大,提示两种品系的大鼠p53抑癌基因对4NQO的反应可能存在某些遗传性差异,这可能是导致两种大鼠对致癌剂敏感性各异的重要原因。p53基因突变可导致其蛋白产物构型的改变、稳定性增加,从而在细胞内聚积并可用免疫组化方法检测。但本实验所采用的免疫抗血清可检测野生型和突变型p53蛋白,而且其他非基因突变性机制,如:mdm2基因蛋白或病毒蛋白与细胞间的相互作用,也可引起p53蛋白的稳定和聚积[9,10],因此p53免疫组化的过度表达并不能直接反应p53基因的突变与否。显然,对本研究检测出的特定细胞群 (如表达或不表达p53蛋白的癌或癌前病变细胞)作进一步的分子生物学分析,将有助于明确p53抑癌基因在大鼠化学致癌机制中的作用。
, http://www.100md.com
本研究还发现,在4NQO处理后的大鼠舌粘膜中p53阳性细胞常聚集成簇,虽然大多数阳性细胞簇位于上皮异常增生处,但也有部分细胞簇出现在远离癌肿、呈正常组织学图象的粘膜区域,而且在某些邻近或远隔呈p53阴性舌癌的粘膜区域也有散在分布。这些结果一方面提示抗体CM5可能作为一种较敏感的癌前或癌病变的标记,应用于大鼠化学致癌模型,这些不表现异常增生的p53阳性上皮灶可能代表尚无明确组织学改变的早期恶变细胞。另一方面,舌粘膜这种多灶性p53阳性细胞簇以及同一大鼠舌粘膜的癌前或癌病变对p53表达的不一致性似乎支持所谓“肿瘤发生野 (field origin of tumor)”的概念,该观点认为上皮性肿瘤可“跳跃式”地发生于多个区域,这些多发性转化灶细胞可能具有不同的原始表型[6]。
志谢 本研究为《日本文部省96年度奖励研究(A)》资助项目的部分内容,感谢日本鹿儿岛大学齿学部的北野元生教授在动物实验方面所给予的指导和帮助
参考文献:
, http://www.100md.com
[1] Wallenius K, Lekholm U. Oral cancer in rats induced by the water-soluble carcinogen 4-nitrochinoline N-oxide. Odontol Revy, 1973, 24: 39-48.
[2] Kitano M, Hatano H, Shisa H. Strain difference of susceptibility to 4-nitroquinoline 1-oxide-induced tongue carcinoma in rats. Jpn J Cancer Res,1992, 83: 843-850.
[3] Li TJ, Hirayama Y, Kitano M. Glutathione S-transferase Pi-class as a tumor marker in lingual preneoplastic and neoplastic lesions of rats and humans. Virchows Arch,1997, 431: 37-43.
, http://www.100md.com
[4] Levine AJ, Momand J, Finlay CA. The p53 tumor suppressor gene. Nature,1991, 351: 453-456.
[5] Boyle PO, Hakim J, Kock W, et al. The incidence of p53 mutations increases with progression of head and neck cancer. Cancer Res,1993, 53: 4477-4480.
[6] Ogden GR, Hall PA. Field change, clonality, and early epithelial cancer: possible lessons from p53. J Pathol,1997, 181: 127-129.
[7] Greenblatt MS, Bennett WP, Hollstein M, et al. Mutations in the p53 tumor suppressor gene: clues to cancer etiology and molecular pathogenesis. Cancer Res,1994, 54: 4855-4878.
, 百拇医药
[8] Suzui M, Yoshimi N, Tanaka T, et al. Infrequent Ha-ras mutations and absence of Ki-ras, N-ras and p53 mutations in 4-nitroquinoline 1-oxide-induced rat oral lesions. Mol Carcinog,1995, 14: 294-298.
[9] Wu X, Boyle JH, Olson DC, et al. The p53-mdm-2 autoregulatory feedback loop. Genes Dev,1993, 7: 1126-1132.
[10] Scheffner M, Werness BA, Huibregtse JM, et al. The E6 oncoprotein encoded by human papillomavirus type 16 and 18 promotes degradation of p53. Cell,1990, 63: 1129-1136.
收稿日期:1999-01-18, http://www.100md.com
单位:北京医科大学口腔医学院病理科,100081
关键词:基因;p53;致癌性试验;大鼠
中华口腔医学杂志000215 【摘要】 目的 了解Dark-Agouti (DA)和Wistar/Furth (WF)两种品系的大鼠舌粘膜上皮在4-硝基喹啉-1-氧化物(4-nitroquinoline 1-oxide,4NQO)诱导舌癌过程中p53蛋白表达的动态变化。方法 实验动物的饮水中加入4NQO(0.001%),观察第2、4、8、12、16和26周时实验大鼠舌粘膜对p53的免疫组化表达。结果 p53的阳性反应在DA大鼠舌粘膜中出现早,且随着实验的推移,舌粘膜内的p53阳性细胞簇数目趋于增加,特别在实验后期尤为显著;WF大鼠各实验组间p53表达的水平较低,且变化不大。 结论 p53蛋白的表达水平反应了DA和WF大鼠对4NQO诱发舌癌易感性的差异。
, 百拇医药
Expression of p53 protein during 4NQO-induced lingual carcinogenesis in two strains of rats
LI Tiejun.
( Department of Oral Pathology, School of Stomatology, Beijing Medical University, Beijing 100081,China)
【Abstract】 Objective To investigate p53 protein expression during lingual carcinogenesis in two strains of rats. Methods Dark-Agouti (DA) and Wistar/Furth (WF) rats were administrated with 4-nitroquinoline 1-oxide (4NQO) in drinking water and expression of p53 was studied using experimental materials obtained at 2, 4, 8, 12, 16, and 26 weeks of 4NQO treatment. Results Epithelial clusters of p53 positive cells appeared earlier and more in numbers in DA rats than in WF. A marked increase of p53+ clusters in DA rats was noted at later stages of the experiment, whereas those in WF rats appeared to be unchanged. Conclusions These results suggest that there may be genetically determined variations in the p53 response to 4NQO between DA and WF rats, and these differences may contribute to their contrasting susceptibility during lingual carcinogenesis.
, 百拇医药
【Key words】 Genes,p53; Carcinogenicity tests; Rats
水溶性致癌剂4-硝基喹啉-1-氧化物(4-nitro-quinoline 1-oxide,4NQO)可诱发大鼠口腔粘膜的鳞状细胞癌[1],通过饮水给药,这种模型的癌发生率高,稳定性和重复性好,可模拟上皮过度增生、异常增生、原位癌以及浸润癌等一系列鳞癌发生过程中的典型病理过程。Kitano等[2]发现不同品系的大鼠对4NQO诱发舌癌的敏感性有所不同。在相同的实验条件下,Dark-Agouti (DA)和Wistar/Furth (WF)大鼠的舌癌发生率之间差异有显著性,其中DA大鼠的舌癌发生率高,常为多发性、巨大型 (直径>7 mm)肿瘤,而WF大鼠则表现出较低的易感性[2,3]。不同大鼠品系间实验性舌癌发生的差异提示某些遗传性易患因素在癌发生过程中可能起重要作用。p53基因编码的核蛋白对 DNA的转录和复制均有重要调控作用,野生型p53蛋白可阻止DNA受损细胞从G1期进入S期,抑制异常细胞的过度增殖;但其突变型则失去对细胞生长的调节作用,可促进细胞的恶性转化[4]。p53抑癌基因结构和功能的异常与大多数人类恶性肿瘤的发生密切相关[4]。在人类口腔癌的发生过程中,p53基因突变常出现在早期,且可呈多发性分布,为癌前和癌细胞克隆的扩增提供选择优势[5,6]。然而,在大鼠的化学致癌模型中有关p53基因异常的报道不多[7],仅个别报道涉及大鼠的口腔癌模型[8]。本研究旨在观察DA和WF品系大鼠的舌粘膜上皮在4NQO诱发舌癌的过程中p53蛋白表达的动态变化,比较其在两种品系大鼠间的差异,探讨其与大鼠实验性舌癌遗传性易患因素之间的相关关系。
, http://www.100md.com
材料和方法
一、动物实验和组织处理
近交系DA和WF大鼠分别购于日本静冈实验动物中心和日本广岛大学实验动物系。收集6周龄雄性DA和WF大鼠各42只,其中实验组各30只,对照组各12只。所有大鼠均饲养于铁丝笼具内(5~6只/笼),给予充足的基础食物和饮水。实验组动物的饮水中加入水溶性4NQO (终浓度为0.001%; 约7 mg/kg体重每天),而对照组则仅给予饮用水。在实验进行至第2、4、8、12、16和26周末时,采用过量乙醚、氯仿吸入法处死大鼠,其中实验组各5只,对照组各2只。从会厌部至口底前缘整体分离舌体,观察其大体形态,并沿舌体纵轴方向正中剖开,固定于10% 中性甲醛液中24~48 h,常规组织处理,石蜡包埋、切片,HE染色,组织学观察。
二、免疫组化染色及其评价
5 μm厚切片脱蜡,经等级酒精水化后,放入0.01 mol枸橼酸缓冲液 (pH 6.0),微波炉(800 W) 加热20 min,经3%过氧化氢阻断内源性氧化酶后,滴加 p53抗体 (CM5, 英国Novocastra公司;1:400,室温 1 h;该抗体是针对重组小鼠p53蛋白的兔抗血清,可与大鼠野生型及突变型 p53蛋白反应)。检测系统采用链亲和素/过氧化物酶技术 (LSAB试剂盒,美国DAKO公司),经DAB底物染色和适度苏木素复染后,脱水、透明、封片。所有试剂的稀释及切片冲洗均采用Tris缓冲液 (0.05 mol, pH 7.6)。光镜下细胞核呈明确棕褐色染色者视为阳性细胞。对所诱发的大鼠舌癌病变中的染色仅作定性评价,即记录p53阳性或阴性肿瘤;在非癌肿区舌粘膜内(包括邻近和远离舌癌的粘膜区域),p53阳性细胞常聚集成簇并散在分布于上皮的基底和(或)副基底层,因此对非癌肿区上皮内的 p53阳性细胞簇作了计数,即在镜下沿舌粘膜的全长(舌背及舌腹)连续记录 p53阳性细胞簇的数目。DA和 WF大鼠各组间计数资料的统计学处理采用Mann-Whitney U检验 (StatView-4.02 软件)。
, http://www.100md.com
结果
一、动物实验观察
所有对照组大鼠均无舌粘膜病变,实验组大鼠则随实验的进行而出现不同程度的舌粘膜病损,直至发生鳞状细胞癌。然而,DA和WF系大鼠对4NQO诱发舌癌的易感性存在明显差异(表1)。实验第8周末时,DA大鼠的舌粘膜即开始出现上皮异常增生,WF大鼠则到第12周末时才发生类似表现。随后,上皮异常增生病变的数目逐渐增加,这在DA大鼠实验组间更为明显。DA大鼠舌癌的发生也较WF大鼠出现的早而频繁,实验第16周末即有1只DA大鼠发生舌癌 (图1)。26周时实验组的5只DA大鼠均有舌癌形成,其中1只大鼠舌部同时发生3个肿瘤,而WF大鼠仅有1只发生了舌癌。


图1 DA大鼠于实验第16周发生了第1例舌癌(×) 图2 第16周DA大鼠舌粘膜内的p53阳性细胞簇(×150)
, 百拇医药
表1 4NQO诱发DA和WF大鼠舌癌实验的观察 组别
(周)
DA大鼠
WF大鼠
对照组
实验组
对照组
实验组
2
○○
○○○○○
○○
○○○○○
, http://www.100md.com
4
○○
○○○○○
○○
○○○○○
8
○○
◎◎◎◎○
○○
○○○○○
12
○○
◎◎◎◎◎
, http://www.100md.com
○○
◎◎◎◎○
16
○○
●◎◎◎◎
○○
◎◎◎◎◎
26
○○
●●●●●
○○
●◎◎◎◎
注:表内每个符号代表1只大鼠,其中○表示舌粘膜无病变;◎表示舌粘膜出现异常增生;●表示发生舌癌

, http://www.100md.com
图3 各实验组p53阳性细胞簇计数均数
二、p53免疫组化染色
对照组大鼠的所有舌体标本均呈p53阴性。实验早期,2周和4周组大鼠的舌体标本中未见p53阳性染色。DA大鼠的舌粘膜内的p53阳性细胞于第8周末时出现,而WF大鼠舌粘膜内的p53阳性细胞则出现于第12周末。这些阳性细胞聚集成簇,散在分布于舌粘膜上皮的基底层和(或)副基底层(图2);大多数p53阳性 细胞簇发生于上皮呈异常增生的区域,约25%的阳性灶位于正常区域;随着实验时间的推移,DA大鼠的非癌肿区舌粘膜内p53阳性细胞簇数目趋于增加,特别是在实验后期 (16周和26周组) ;而WF大鼠各组间的计数值变化不明显。统计学处理表明: 16周和26周组DA与WF大鼠的p53阳性细胞簇计数值之间差异有显著性 (P<0.05,图3)。实验组DA大鼠所发生的8个舌癌中5个可见p53阳性染色(图4),其中发生于同一动物的3个舌癌中有2个呈p53阳性染色,1个呈阴性染色;实验组WF大鼠所发生的唯一1例舌癌不表达p53。在2只26周组DA大鼠中,虽然所诱发的舌癌不表达p53,但其非癌肿区舌粘膜中可见p53阳性细胞的存在。

, 百拇医药
图4 呈p53阳性的舌癌癌巢,阳性细胞多为癌巢周边的基底细胞(×150)
讨论
与人类自然发生的肿瘤相比,化学致癌剂所诱发的啮齿类动物原发性肿瘤发生p53异常的频率较低[7]。Suzui等[8] 未能在4NQO诱发的F344大鼠舌癌中检测到p53基因突变,但该研究未作p53的免疫组化观察。本研究发现:对致癌剂较敏感的DA系大鼠的舌粘膜表达p53蛋白的水平显著高于易感性较差的WF系大鼠,DA大鼠舌粘膜内的p53阳性细胞簇计数在实验后期显著增加,而WF 大鼠各实验组间计数值的变化不大,提示两种品系的大鼠p53抑癌基因对4NQO的反应可能存在某些遗传性差异,这可能是导致两种大鼠对致癌剂敏感性各异的重要原因。p53基因突变可导致其蛋白产物构型的改变、稳定性增加,从而在细胞内聚积并可用免疫组化方法检测。但本实验所采用的免疫抗血清可检测野生型和突变型p53蛋白,而且其他非基因突变性机制,如:mdm2基因蛋白或病毒蛋白与细胞间的相互作用,也可引起p53蛋白的稳定和聚积[9,10],因此p53免疫组化的过度表达并不能直接反应p53基因的突变与否。显然,对本研究检测出的特定细胞群 (如表达或不表达p53蛋白的癌或癌前病变细胞)作进一步的分子生物学分析,将有助于明确p53抑癌基因在大鼠化学致癌机制中的作用。
, http://www.100md.com
本研究还发现,在4NQO处理后的大鼠舌粘膜中p53阳性细胞常聚集成簇,虽然大多数阳性细胞簇位于上皮异常增生处,但也有部分细胞簇出现在远离癌肿、呈正常组织学图象的粘膜区域,而且在某些邻近或远隔呈p53阴性舌癌的粘膜区域也有散在分布。这些结果一方面提示抗体CM5可能作为一种较敏感的癌前或癌病变的标记,应用于大鼠化学致癌模型,这些不表现异常增生的p53阳性上皮灶可能代表尚无明确组织学改变的早期恶变细胞。另一方面,舌粘膜这种多灶性p53阳性细胞簇以及同一大鼠舌粘膜的癌前或癌病变对p53表达的不一致性似乎支持所谓“肿瘤发生野 (field origin of tumor)”的概念,该观点认为上皮性肿瘤可“跳跃式”地发生于多个区域,这些多发性转化灶细胞可能具有不同的原始表型[6]。
志谢 本研究为《日本文部省96年度奖励研究(A)》资助项目的部分内容,感谢日本鹿儿岛大学齿学部的北野元生教授在动物实验方面所给予的指导和帮助
参考文献:
, http://www.100md.com
[1] Wallenius K, Lekholm U. Oral cancer in rats induced by the water-soluble carcinogen 4-nitrochinoline N-oxide. Odontol Revy, 1973, 24: 39-48.
[2] Kitano M, Hatano H, Shisa H. Strain difference of susceptibility to 4-nitroquinoline 1-oxide-induced tongue carcinoma in rats. Jpn J Cancer Res,1992, 83: 843-850.
[3] Li TJ, Hirayama Y, Kitano M. Glutathione S-transferase Pi-class as a tumor marker in lingual preneoplastic and neoplastic lesions of rats and humans. Virchows Arch,1997, 431: 37-43.
, http://www.100md.com
[4] Levine AJ, Momand J, Finlay CA. The p53 tumor suppressor gene. Nature,1991, 351: 453-456.
[5] Boyle PO, Hakim J, Kock W, et al. The incidence of p53 mutations increases with progression of head and neck cancer. Cancer Res,1993, 53: 4477-4480.
[6] Ogden GR, Hall PA. Field change, clonality, and early epithelial cancer: possible lessons from p53. J Pathol,1997, 181: 127-129.
[7] Greenblatt MS, Bennett WP, Hollstein M, et al. Mutations in the p53 tumor suppressor gene: clues to cancer etiology and molecular pathogenesis. Cancer Res,1994, 54: 4855-4878.
, 百拇医药
[8] Suzui M, Yoshimi N, Tanaka T, et al. Infrequent Ha-ras mutations and absence of Ki-ras, N-ras and p53 mutations in 4-nitroquinoline 1-oxide-induced rat oral lesions. Mol Carcinog,1995, 14: 294-298.
[9] Wu X, Boyle JH, Olson DC, et al. The p53-mdm-2 autoregulatory feedback loop. Genes Dev,1993, 7: 1126-1132.
[10] Scheffner M, Werness BA, Huibregtse JM, et al. The E6 oncoprotein encoded by human papillomavirus type 16 and 18 promotes degradation of p53. Cell,1990, 63: 1129-1136.
收稿日期:1999-01-18, http://www.100md.com