重组HIV-1腺病毒伴随病毒的构建及表达
作者:管永军 刘海鹰 朱跃科 周玲 杜宾 曾毅
单位:管永军 刘海鹰 朱跃科 周玲 曾毅(中国预防医学科学院病毒学研究所肿瘤爱滋病室 北京 100052);杜宾(美国哈佛大学医学院微生物学研究所)
关键词:HIV-1;T淋巴细胞;细胞毒性;依赖病毒属
中华实验和临床病毒学杂志000405 【摘要】 目的 构建带有HIV-1 gag或gp120基因的重组腺病毒伴随病毒AAV-HIV gag或AAV-HIV gp120。方法 共转染法获取重组AAV-HIV;免疫酶法检测病毒滴度。结果 测定制备的重组腺病毒伴随病毒AAVgag42,AAVgp42,AAVgpRj6,病毒滴度在104~105范围。结论 构建了带有gag和gp120基因的重组AAV-HIV,可以感染真核细胞并有较高的表达,可以用于做靶细胞,为发展新型的HIV-1重组AAV病毒载体活疫苗打下基础。
, 百拇医药
Construction and expression of recombinant adeno-associated HIV-1 virus
GUAN Yongjun,LIU Haiying,ZHU Yueke
(Institute of Virology, Chinese Academy of Preventive Medicine,Beijing 100052,China)
【Abstract】 Objective Plasmid of AAV vector with HIV-1 gag and gp 120 were constructed respectively. Methods The recombinant AAV-HIV gag and gp120 viruses were obtained by co-transfection of AAV-HIV plasmid and Adenovirus 5 in 293 cells. Results The recombinant AAV-HIV virus expressed well and the titer of the recombinant viruses were between 104-105. Conclusion The recombinant AAV-HIV virus can be used to infect the target cells for detection of cellular immunity and for vaccine studies.
, 百拇医药
【Key words】 HIV-1; T lymphocytes,cytotoxic; Adeno-associated viruses
艾滋病毒在全球的迅速传播已严重威胁人类的生命安全,预防和控制艾滚病的传播必须研制出安全有效的艾滋病毒疫苗已成为共识。我们用克隆的中国HIV-1代表性流行毒株的基因,构建了HIV-1 gag及gp12基因的重组腺病毒伴随病毒(AAV)表达质粒和重组AAV-HIV病毒;感染真核细胞并表达,用免疫酶法检测病毒滴度,为发展新型的HIV-1重组AAV病毒载体活疫苗打下了基础。
1 材料和方法
1.1 菌株及质粒 大肠埃希菌DH5α为本室保存。中国HIV-1毒株的gag及gp120基因克隆系列质粒均为本室构建。本文所用HIV-1毒株是1995年初从云南瑞丽地区17名HIV-1抗体阳性的静脉吸毒者(IDU)的静脉血中分离出来,经分析,12株为B亚型,5株为C亚型〔1〕。真核细胞表达质粒pCMV-GFP含CMV的IE启动子和SV40 PloyA及多克隆位点。重组质粒pSSV9含AAV-2的全基因组,在
, http://www.100md.com
近基因组两端处各有一个人工插入的Xba Ⅰ位点,它将编码区和ITR分开,质粒骨架为pEMBL8;辅助质粒pAd8是pSSV9的衍生质粒,其中AAV-2的两端ITR都由5型人腺病毒(Ad5)的109 bp末端重复序列所取代,含野生型AAV-2的所有编码序列。AAV表达载体ACPUF5含有AAV的两端ITR及CMV IE启动子、SV40 PolyA及多克隆位点。质粒pSSV9、ACPUF5和pAd8由美国哈佛大学医学院的杜宾先生馈赠。
1.2 细胞和毒株 293细胞为人胚肾上皮细胞系,培养于含10%小牛血清的Eagle培养基中(另含1%谷氨酰胺,1%青、链霉素)。小牛血清购自哈尔滨市兽医研究所。P815细胞为Balb/C小鼠的淋巴细胞系,培养于含10%小牛血清的1640培养基中。5型人腺病毒株(Ad5)为本室保存。
1.3 工具酶和试剂 各种限制性内切酶购自Promega公司;放射性同位素51Cr购自杜邦公司。
, http://www.100md.com
1.4 HIV-1 gag及gp120基因的重组AAV载体的构建 用Xba Ⅰ/Sal Ⅰ从gag或gag-V3基因克隆质粒上切下gag基因片段,组入AAV载体pACPUF5的CMV启动子下游Xba Ⅰ/Sal Ⅰ位点中,得到中间AAV载体AAV gag42-Ⅰ及AAV gag268V3Rj6-Ⅰ;再将pACPUF5的Xho Ⅰ/Sal Ⅰ小片段插入AAV gag42-Ⅰ的Sal Ⅰ位点,最终得到gag基因的AAV载体pAAV gag42。用EcoR Ⅰ/Xho Ⅰ将C亚型的gp120基因(gp120-Rj6)组入AAV gag268V3Rj6-Ⅰ的EcoR Ⅰ/Xho Ⅰ位点中,得到中间载体AAV gpRj6-Ⅰ,再将pACPUF5的Xho Ⅰ/Sal Ⅰ小片段插入中间载体AAVgpRj6-Ⅰ的Xho Ⅰ/Sal Ⅰ位点,最终得到C亚型gp120基因的AAV载体pAAVgp120-Rj6。
1.5 重组AAV病毒的获得及病毒滴度的测定 取生长16~24 h 293细胞,用无血清培养液洗涤细胞3次,Ad5感染2 h,去掉感染液,用载体质粒和包装质粒Ad8(1∶5)共转染细胞,72 h收获细胞,反复冻融3次,5 000 r/min离心5 min去细胞碎片,所得病毒悬液经56℃ 30 min灭活腺病毒。制备1∶10、1∶102、1∶103倍稀释的病毒悬液,感染105/ml传代24 h的P815细胞,培养48 h后,细胞涂片,冷丙酮固定,用免疫酶法检测阳性细胞的百分比,病毒滴度为阳性细胞的百分比×病毒稀释倍数×105。
, 百拇医药
1.6 免疫酶检测(EIA) 将细胞用PBS溶液(150 mmol/L NaCl,15 mmol/L Na3PO4,pH7.3)洗涤3次;贴壁细胞用4℃固定液(2%甲醛和0.2%戊二醛的PBS)固定15 min,悬浮细胞涂片后用4℃丙酮固定15 min,PBS洗3遍。覆盖抗原特异性的第一抗体或待检血清,37℃孵育30 min,PBS洗3遍;覆盖HRP标记的抗第一抗体的第二抗体,37℃孵育30 min,PBS洗3遍;于辣根过氧化物酶底物中显色5~10 min;显微镜下观察,阳性细胞染成棕色。
2 结果
2.1 含HIV-1 gag或gp120基因的AAV载体的构建 AAV表达载体质粒的构建流程见图1,图2。如方法所述构建了B亚型gag基因的AAV载体pAAVgag42,C亚型gp120基因的AAV载体pAAVgp120-Rj6。
2.2 重组质粒的鉴定 pAAVgag42用Xba Ⅰ/Sal Ⅰ双酶切应得到5.3 kb及3.0 kb大小的两条带,用Pvu Ⅱ酶切应得到4.0 kb,2.1 kb,1.2 kb及1.0 kb大小的四条带;pAAVgp120-Rj6用Pvu Ⅱ酶切应得到4.0 kb,1.6 kb,1.5 kb及1.0 kb大小的四条带,Pst Ⅰ酶切应得到7.0 kb及1.2 kb大小的两条带,EcoR Ⅰ/Pst Ⅰ双酶切应得到5.5 kb,1.5 kb及1.2 kb大小的3条带,限制性内切酶分析鉴定,均与预计大小一致。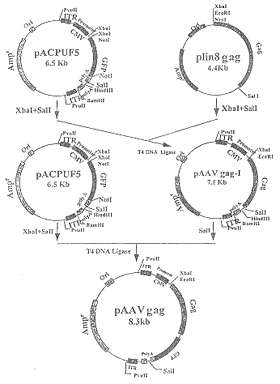
, http://www.100md.com
图1 重组AAV-gag(B亚型)表达载体质粒的构建
Fig.1 Construction of recombinant AAV-gag plasmid(B subtype)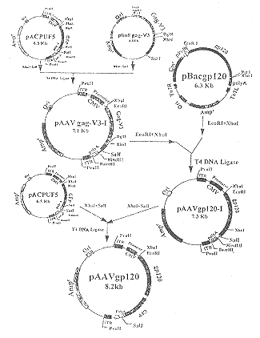
图2 AAV-gp120(C亚型)表达载体质粒的构建
Fig.2 Construction of recombinant AAV-gp120 plasmid(C subtype)
2.3 AAV-HIV-1的表达 通过共转染分别制备了gag基因和gp120基因的重组腺病毒伴随病毒AAVgag42、AAVgpRj6,测定它们的滴度在104~105范围。图版ⅠA为重组AAV感染P815细胞用HIV-1阳性血清进行免疫酶法检测的结果,表明重组AAV可以转导HIV-1基因入宿主细胞表达。
, http://www.100md.com
3 讨论
重组AAV可作为一种转导性载体,通过病毒感染的方式将外源基因导入到细胞中,并可整合于宿主染色体得到稳定的表达。与逆转录病毒载体相比,重组AAV载体能转导有丝分裂后细胞和分化终端细胞。AAV具有超感染的特性,可进行重复感染,同时人类至今还未发现同AAV直接相关的疾病,这些特点使它具有进行人类疾病基因治疗的应用前景〔2〕。由于在我国流行的HIV-1多为B、C亚型,gag基因序列在各亚型间较为保守,我们选择HIV-1B亚型gag基因;我们曾于1995年从云南静脉吸毒者HIV-1阳性血中分离出5株HIV-1C亚型毒株,对gp120中最重要的中和抗体决定簇V3环序列进行了对比分析,发现V3环序列变化极小〔1〕,所以选择HIV-1C亚型gp120基因。我们构建了可转导HIV-1 gag或gp120基因进入真核细胞并表达的重组AAV-HIV gag或AAV-HIV gp120。其中我们构建HIV重组AAV的另一主要目的是用作一类新型的HIV-1重组病毒载体活疫苗,为发展适合中国流行株的重组病毒疫苗奠定基础。
, http://www.100md.com
我们首次用中国流行毒株做DNA免疫,观察其免疫反应,特别是细胞免疫反应。进一步要做主要亚型B、C的gp120,目前国际上还没有人用AAV作载体研究HIV疫苗。用重组AAV作疫苗的唯一报道是表达HSV外膜糖蛋白的重组AAV,其动物免疫反应比DNA疫苗及蛋白疫苗的均要好〔3〕。目前需要解决的是如何提高重组AAV的滴度和避免野毒及辅助病毒的污染问题,最近Xiao X〔4,5〕等用基因工程技术解决了这两个技术问题。因此重组AAV HIV-1疫苗具有良好的前景。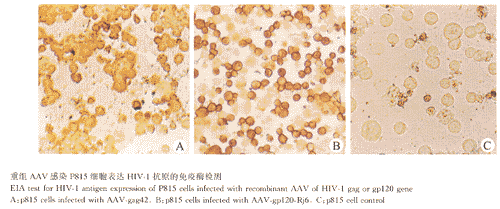
图版 ⅠA 管永军等.重组HIV-1腺病毒伴随病毒的构建及表达
Plate ⅠA GUAN Yongjun,et al.Construction and expression of recombinant adeno-associated HIV-1 virus
, 百拇医药
(Original article p.322)
参 考 文 献
1,管永军,陈钧,邵一鸣,等.云南瑞丽人免疫缺陷病毒感染者gp120基因C2-V3区的序列测定和亚型分析.中华实验和临床病毒学杂志,1997,11:8-12.
2,侯云德.动物病毒载体与基因治疗的现状和前景.现代分子病毒学选论.北京:科学出版社,1994,9-17.
3,Manning WC,Paliard X,Zhou SZ,et al.Genetic immunization with adeno-associated virus vectors expressing herpes simplex virus type 2 glycoproteins B and D.J Virol,1997,71:7960-7962.
, http://www.100md.com
4,Xiao X,Li J,Richard JS,et al.Production of high-titer recombinant adeno-associated virus vectors in the absence of helper adenovirus. J Virol,1998,72:2224-2232.
5,Xiao X,Li J, Richard JS,et al.Efficient long-term gene transfer into muscle tissue of immunocompetent mice by adeno-associated virus vector.J Virol,1996,70:8098-8108.
(收稿日期:2000-02-14), http://www.100md.com
单位:管永军 刘海鹰 朱跃科 周玲 曾毅(中国预防医学科学院病毒学研究所肿瘤爱滋病室 北京 100052);杜宾(美国哈佛大学医学院微生物学研究所)
关键词:HIV-1;T淋巴细胞;细胞毒性;依赖病毒属
中华实验和临床病毒学杂志000405 【摘要】 目的 构建带有HIV-1 gag或gp120基因的重组腺病毒伴随病毒AAV-HIV gag或AAV-HIV gp120。方法 共转染法获取重组AAV-HIV;免疫酶法检测病毒滴度。结果 测定制备的重组腺病毒伴随病毒AAVgag42,AAVgp42,AAVgpRj6,病毒滴度在104~105范围。结论 构建了带有gag和gp120基因的重组AAV-HIV,可以感染真核细胞并有较高的表达,可以用于做靶细胞,为发展新型的HIV-1重组AAV病毒载体活疫苗打下基础。
, 百拇医药
Construction and expression of recombinant adeno-associated HIV-1 virus
GUAN Yongjun,LIU Haiying,ZHU Yueke
(Institute of Virology, Chinese Academy of Preventive Medicine,Beijing 100052,China)
【Abstract】 Objective Plasmid of AAV vector with HIV-1 gag and gp 120 were constructed respectively. Methods The recombinant AAV-HIV gag and gp120 viruses were obtained by co-transfection of AAV-HIV plasmid and Adenovirus 5 in 293 cells. Results The recombinant AAV-HIV virus expressed well and the titer of the recombinant viruses were between 104-105. Conclusion The recombinant AAV-HIV virus can be used to infect the target cells for detection of cellular immunity and for vaccine studies.
, 百拇医药
【Key words】 HIV-1; T lymphocytes,cytotoxic; Adeno-associated viruses
艾滋病毒在全球的迅速传播已严重威胁人类的生命安全,预防和控制艾滚病的传播必须研制出安全有效的艾滋病毒疫苗已成为共识。我们用克隆的中国HIV-1代表性流行毒株的基因,构建了HIV-1 gag及gp12基因的重组腺病毒伴随病毒(AAV)表达质粒和重组AAV-HIV病毒;感染真核细胞并表达,用免疫酶法检测病毒滴度,为发展新型的HIV-1重组AAV病毒载体活疫苗打下了基础。
1 材料和方法
1.1 菌株及质粒 大肠埃希菌DH5α为本室保存。中国HIV-1毒株的gag及gp120基因克隆系列质粒均为本室构建。本文所用HIV-1毒株是1995年初从云南瑞丽地区17名HIV-1抗体阳性的静脉吸毒者(IDU)的静脉血中分离出来,经分析,12株为B亚型,5株为C亚型〔1〕。真核细胞表达质粒pCMV-GFP含CMV的IE启动子和SV40 PloyA及多克隆位点。重组质粒pSSV9含AAV-2的全基因组,在
, http://www.100md.com
近基因组两端处各有一个人工插入的Xba Ⅰ位点,它将编码区和ITR分开,质粒骨架为pEMBL8;辅助质粒pAd8是pSSV9的衍生质粒,其中AAV-2的两端ITR都由5型人腺病毒(Ad5)的109 bp末端重复序列所取代,含野生型AAV-2的所有编码序列。AAV表达载体ACPUF5含有AAV的两端ITR及CMV IE启动子、SV40 PolyA及多克隆位点。质粒pSSV9、ACPUF5和pAd8由美国哈佛大学医学院的杜宾先生馈赠。
1.2 细胞和毒株 293细胞为人胚肾上皮细胞系,培养于含10%小牛血清的Eagle培养基中(另含1%谷氨酰胺,1%青、链霉素)。小牛血清购自哈尔滨市兽医研究所。P815细胞为Balb/C小鼠的淋巴细胞系,培养于含10%小牛血清的1640培养基中。5型人腺病毒株(Ad5)为本室保存。
1.3 工具酶和试剂 各种限制性内切酶购自Promega公司;放射性同位素51Cr购自杜邦公司。
, http://www.100md.com
1.4 HIV-1 gag及gp120基因的重组AAV载体的构建 用Xba Ⅰ/Sal Ⅰ从gag或gag-V3基因克隆质粒上切下gag基因片段,组入AAV载体pACPUF5的CMV启动子下游Xba Ⅰ/Sal Ⅰ位点中,得到中间AAV载体AAV gag42-Ⅰ及AAV gag268V3Rj6-Ⅰ;再将pACPUF5的Xho Ⅰ/Sal Ⅰ小片段插入AAV gag42-Ⅰ的Sal Ⅰ位点,最终得到gag基因的AAV载体pAAV gag42。用EcoR Ⅰ/Xho Ⅰ将C亚型的gp120基因(gp120-Rj6)组入AAV gag268V3Rj6-Ⅰ的EcoR Ⅰ/Xho Ⅰ位点中,得到中间载体AAV gpRj6-Ⅰ,再将pACPUF5的Xho Ⅰ/Sal Ⅰ小片段插入中间载体AAVgpRj6-Ⅰ的Xho Ⅰ/Sal Ⅰ位点,最终得到C亚型gp120基因的AAV载体pAAVgp120-Rj6。
1.5 重组AAV病毒的获得及病毒滴度的测定 取生长16~24 h 293细胞,用无血清培养液洗涤细胞3次,Ad5感染2 h,去掉感染液,用载体质粒和包装质粒Ad8(1∶5)共转染细胞,72 h收获细胞,反复冻融3次,5 000 r/min离心5 min去细胞碎片,所得病毒悬液经56℃ 30 min灭活腺病毒。制备1∶10、1∶102、1∶103倍稀释的病毒悬液,感染105/ml传代24 h的P815细胞,培养48 h后,细胞涂片,冷丙酮固定,用免疫酶法检测阳性细胞的百分比,病毒滴度为阳性细胞的百分比×病毒稀释倍数×105。
, 百拇医药
1.6 免疫酶检测(EIA) 将细胞用PBS溶液(150 mmol/L NaCl,15 mmol/L Na3PO4,pH7.3)洗涤3次;贴壁细胞用4℃固定液(2%甲醛和0.2%戊二醛的PBS)固定15 min,悬浮细胞涂片后用4℃丙酮固定15 min,PBS洗3遍。覆盖抗原特异性的第一抗体或待检血清,37℃孵育30 min,PBS洗3遍;覆盖HRP标记的抗第一抗体的第二抗体,37℃孵育30 min,PBS洗3遍;于辣根过氧化物酶底物中显色5~10 min;显微镜下观察,阳性细胞染成棕色。
2 结果
2.1 含HIV-1 gag或gp120基因的AAV载体的构建 AAV表达载体质粒的构建流程见图1,图2。如方法所述构建了B亚型gag基因的AAV载体pAAVgag42,C亚型gp120基因的AAV载体pAAVgp120-Rj6。
2.2 重组质粒的鉴定 pAAVgag42用Xba Ⅰ/Sal Ⅰ双酶切应得到5.3 kb及3.0 kb大小的两条带,用Pvu Ⅱ酶切应得到4.0 kb,2.1 kb,1.2 kb及1.0 kb大小的四条带;pAAVgp120-Rj6用Pvu Ⅱ酶切应得到4.0 kb,1.6 kb,1.5 kb及1.0 kb大小的四条带,Pst Ⅰ酶切应得到7.0 kb及1.2 kb大小的两条带,EcoR Ⅰ/Pst Ⅰ双酶切应得到5.5 kb,1.5 kb及1.2 kb大小的3条带,限制性内切酶分析鉴定,均与预计大小一致。

, http://www.100md.com
图1 重组AAV-gag(B亚型)表达载体质粒的构建
Fig.1 Construction of recombinant AAV-gag plasmid(B subtype)

图2 AAV-gp120(C亚型)表达载体质粒的构建
Fig.2 Construction of recombinant AAV-gp120 plasmid(C subtype)
2.3 AAV-HIV-1的表达 通过共转染分别制备了gag基因和gp120基因的重组腺病毒伴随病毒AAVgag42、AAVgpRj6,测定它们的滴度在104~105范围。图版ⅠA为重组AAV感染P815细胞用HIV-1阳性血清进行免疫酶法检测的结果,表明重组AAV可以转导HIV-1基因入宿主细胞表达。
, http://www.100md.com
3 讨论
重组AAV可作为一种转导性载体,通过病毒感染的方式将外源基因导入到细胞中,并可整合于宿主染色体得到稳定的表达。与逆转录病毒载体相比,重组AAV载体能转导有丝分裂后细胞和分化终端细胞。AAV具有超感染的特性,可进行重复感染,同时人类至今还未发现同AAV直接相关的疾病,这些特点使它具有进行人类疾病基因治疗的应用前景〔2〕。由于在我国流行的HIV-1多为B、C亚型,gag基因序列在各亚型间较为保守,我们选择HIV-1B亚型gag基因;我们曾于1995年从云南静脉吸毒者HIV-1阳性血中分离出5株HIV-1C亚型毒株,对gp120中最重要的中和抗体决定簇V3环序列进行了对比分析,发现V3环序列变化极小〔1〕,所以选择HIV-1C亚型gp120基因。我们构建了可转导HIV-1 gag或gp120基因进入真核细胞并表达的重组AAV-HIV gag或AAV-HIV gp120。其中我们构建HIV重组AAV的另一主要目的是用作一类新型的HIV-1重组病毒载体活疫苗,为发展适合中国流行株的重组病毒疫苗奠定基础。
, http://www.100md.com
我们首次用中国流行毒株做DNA免疫,观察其免疫反应,特别是细胞免疫反应。进一步要做主要亚型B、C的gp120,目前国际上还没有人用AAV作载体研究HIV疫苗。用重组AAV作疫苗的唯一报道是表达HSV外膜糖蛋白的重组AAV,其动物免疫反应比DNA疫苗及蛋白疫苗的均要好〔3〕。目前需要解决的是如何提高重组AAV的滴度和避免野毒及辅助病毒的污染问题,最近Xiao X〔4,5〕等用基因工程技术解决了这两个技术问题。因此重组AAV HIV-1疫苗具有良好的前景。

图版 ⅠA 管永军等.重组HIV-1腺病毒伴随病毒的构建及表达
Plate ⅠA GUAN Yongjun,et al.Construction and expression of recombinant adeno-associated HIV-1 virus
, 百拇医药
(Original article p.322)
参 考 文 献
1,管永军,陈钧,邵一鸣,等.云南瑞丽人免疫缺陷病毒感染者gp120基因C2-V3区的序列测定和亚型分析.中华实验和临床病毒学杂志,1997,11:8-12.
2,侯云德.动物病毒载体与基因治疗的现状和前景.现代分子病毒学选论.北京:科学出版社,1994,9-17.
3,Manning WC,Paliard X,Zhou SZ,et al.Genetic immunization with adeno-associated virus vectors expressing herpes simplex virus type 2 glycoproteins B and D.J Virol,1997,71:7960-7962.
, http://www.100md.com
4,Xiao X,Li J,Richard JS,et al.Production of high-titer recombinant adeno-associated virus vectors in the absence of helper adenovirus. J Virol,1998,72:2224-2232.
5,Xiao X,Li J, Richard JS,et al.Efficient long-term gene transfer into muscle tissue of immunocompetent mice by adeno-associated virus vector.J Virol,1996,70:8098-8108.
(收稿日期:2000-02-14), http://www.100md.com