苦瓜的化学成分研究
作者:肖志艳 陈迪华 斯建勇
单位:中国医学科学院 中国协和医科大学药用植物研究所 北京 100094
关键词:苦瓜;降糖成分;苦瓜脑苷
中草药000805摘 要 为寻找降糖活性成分,利用多种层析技术,从苦瓜Momordica charantia果实的醇提物中分得5 个化合物。根据包括2D-NMR在内的各种光谱数据,分别鉴定为:苦瓜脑苷(momor-cerebroside, Ⅰ)、大豆脑苷Ⅰ(soya-cerebroside Ⅰ,Ⅱ)、苦瓜亭(charantin, Ⅲ)、尿嘧啶(uracil, Ⅳ)及β-谷甾醇。其中化合物Ⅰ、Ⅱ为本属中首次分得;化合物Ⅲ为文献报道的降糖有效成分。
苦瓜Momordica charantia L. 为葫芦科Cucurbitaceae苦瓜属植物,未熟的苦瓜鲜品或干燥切片均可入药,具有清热解毒和明目之功效。我们在初步的药理试验中发现,鲜苦瓜果汁可明显增强链脲霉素型糖尿病小鼠的糖耐量并降低其血糖高峰值,其效果优于阳性对照药降糖灵。这一发现促使我们对苦瓜的化学成分作进一步的研究。
, 百拇医药
有报道[1]苦瓜果实的氯仿部分存在具有显著降糖作用的活性成分。我们从苦瓜果实醇提物氯仿部分得到了5 个化合物,分别确定为:苦瓜脑苷(momor-cerebroside, Ⅰ)、大豆脑苷Ⅰ(soya-cerebroside Ⅰ,Ⅱ)、苦瓜亭(charantin, Ⅲ)、尿嘧啶(uracil, Ⅳ)及β-谷甾醇(β-sitosterol, Ⅴ)。其中,苦瓜脑苷Ⅰ及大豆脑苷Ⅰ(Ⅱ)系本属首次分出;苦瓜亭(Ⅲ)为文献报道的降糖有效成分[2]。
1 仪器和材料
熔点采用Fisher-Johns型熔点测定仪测定(温度未校正);红外光谱采用KBr压片,以Perkin-Elmer 983 G型红外光谱仪测定;核磁共振谱以Bruker AM-500型核磁共振仪测定,TMS为内标;质谱以Zabspec型质谱仪测定。层析用硅胶由青岛海洋化工厂生产(柱层析:粗孔硅胶100~200 目;薄层层析:硅胶G高效预制板)。层析用溶剂均为分析纯。苦瓜果实于1997年8月采自江西省赣州市。
, 百拇医药
2 提取和分离
取鲜苦瓜20 kg切片,95%工业乙醇热浸提取4 次,浓缩提取液至3 L,以氯仿-水分配,将氯仿层蒸干,得干膏70 g。该部分经反复硅胶柱层析后,分离得到化合物Ⅰ~Ⅴ。
3 鉴定
化合物Ⅰ:白色结晶性粉末(90%乙醇),17 mg, mp 143 ℃~145 ℃,FAB-MS (m/z):866〔(M+Na)+,16〕,682,384,280;SIMS (m/z):842.666 6〔(M-H)+,计算值:842.672 6〕,确定分子量为843,分子式为C48H93O10N。IR光谱显示存在羟基、酰胺键及脂肪长链。13CNMR中δ 175.6,51.8处的信号及δ 29.9处强的(CH2)n信号;1HNMR中δ 1.30处的强(CH2)n信号及δ 0.85处的2 个末端甲基信号表明该化合物为神经酰胺类成分。13CNMR中δ 105.6,78.5,75.2,71.6,62.7及1HNMR中δ4.95(d,7.7 Hz)表明Ⅰ为-β葡萄糖苷,即脑苷类化合物(cerebrosides)。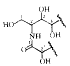
, http://www.100md.com
图1 化合物Ⅰ的结构片断
由13C-1H COSY谱,可归属A链 C-2上的氢信号δ 5.28。它与δ 4.71,4.52(H-1α,H-1β)及δ 4.28(H-3)处的信号的有偶合。结合13C-1H COSY谱,归属C-1信号δ70.5,C-3信号δ 76.0。而在HMBC谱中,C-3信号δ 76.0与δ 4.18(H-4)的质子信号相关;羰基信号δ 175.6与δ 4.57(H-2′),处的信号相关。因此,可判断A链的C-3、C-4位,B链的C-2′位均为羟基,即化合物Ⅰ的结构中存在如图1的结构片断。
神经酰胺部分A、B链的组成由质谱碎片m/z 280(A链-H2O)及384(羰基麦氏重排碎片+H)确定。13CNMR谱中的δ130.9,130.7表明结构中有一双键,通过烯丙位碳的化学位移值(δ33.3,33.0)判断为反式双键[3];由1H-1HCOSY、13C-1HCOSY及HMBC谱, 可依次归属13CNMR及1HNMR信号(表1),并可确定△8,9双键。
, 百拇医药
表1 化合物Ⅰ的13CNMR(125 MHz)和1HNMR(500 MHz)的光谱数据(C5D5N) No
δc
δH(J/Hz)
No
δc
δH(J/Hz)
sphingosine moiety
fatty acid moiety
1
70.5
, http://www.100md.com
4.71(dd,10.6,6.7)
1′
175.6
4.52(dd,10.6,4.5)
2′
72.6
4.57
2
51.8
5.28
3′
35.7
1.99,2.19
, http://www.100md.com
3
76.0
4.28(t-like)
4′
25.9
1.76
4
72.6
4.18
5′~21′
30.0~29.5
1.30~1.24
5
, 百拇医药
33.9
1.89,2.25
22′
32.1
1.30~1.24
6
26.6
1.76,1.98
23′
22.9
1.30~1.24
7
33.3
, 百拇医药
2.19
24′
14.2
0.85
8
130.9
5.50(m)
hexose moiety
9
130.7
5.50(m)
1″
105.6
, http://www.100md.com
4.95(d,7.7)
10
33.0
1.98
2″
75.2
4.00
11~15
30.0~29.5
1.30~1.24
3″
78.5
4.18
, 百拇医药
16
32.1
1.30~1.24
4″
71.6
4.18
17
22.9
1.30~1.24
5″
78.5
3.86
18
, http://www.100md.com
14.2
0.85
6″
62.7
4.33(dd,9.1,5.3)
4.48(dd,6.2)
综上所述,确定化合物Ⅰ的结构为:8(E)-N-(2′-D-羟基-二十四烷酰基)-1-O-β-D-吡喃葡萄糖基-8-烯-十八鞘氨醇(8[E]-N-[2′-hydroxy-tetracosoyl]-1-O-β-D-glucopyranosy1-8-en-octadecasphingenine,如图 2)。该结构由Edgar 等[4]在对黑麦Secale cerale L. cv. Puma. 的总脑苷作气质分析时首次提出,本文系首次以单体形式从自然界分得该化合物,并首次报道其光谱数据。因此,命名为苦瓜脑苷(momor-cerebroside)。
, 百拇医药
图2 化合物Ⅰ的化学结构式
化合物Ⅱ : 白色结晶性粉末( 90%乙醇),30 mg,mp 180 ℃~182 ℃,IR、1H,13CNMR数据与文献[5]中,大豆脑苷Ⅰ(soya-cerebroside Ⅰ,即4[E],8[E]-N-[2′-D-羟基-十六烷酰基]-1-O-β-D-吡喃葡萄糖苷-4,8-二烯-十八鞘氨醇)的数据一致。
化合物Ⅲ:白色粉末,680 mg,mp 247 ℃~250 ℃。将其13CNMR(C5D5N)数据与文献[6]中报道的胡萝卜苷、文献[7]中报道的5,25-豆甾二烯棕榈酸酯葡萄糖苷的数据比较,结合其它光谱学数据可知,该化合物为文献[8]中报道的苦瓜亭(charantin),即胡萝卜苷与5,25-豆甾二烯醇葡萄糖苷的混合物。
, http://www.100md.com
化合物Ⅳ:黄色粉末112 mg,mp 236 ℃~238 ℃(分解),IR、FAB-MS及13CNMR数据与文献[9]报道的尿嘧啶的数据一致。
化合物Ⅴ:白色针晶(丙酮)20 mg,mp 137 ℃~138 ℃,与β-谷甾醇标准品混合,熔点不下降,与标准品Co-TLC及Co-IR的比较,均表明与β-谷甾醇一致。
致谢:本所标本馆潘瑞乐同志鉴定生药;北京微量化学研究所分析中心代测NMR谱;军事医学科学院质谱室及中国科学院质谱室代测MS谱;本所分析室代测IR谱。
肖志艳 女,中国医学科学院中国协和医科大学1999届硕士研究生
参考文献
1,Day C, Crutwright T, Pvovest J, et al. Planta Med,1990,56:426
, 百拇医药
2,Lotlikar M M. Indian J Pharm, 1966,28(5):129
3,方乍浦,曾宪仪,熊淑玲.天然产物研究与开发,1996,8(3):20
4,Cahoon E B and Lynch D V. Plant Physiol, 1991,95:58
5,Shibuya H, Kawashima K, Sakagami M, et al. Chem Pharm Bull,1990,38(11):2933
6,陈英杰,徐缓绪,马启风,等.药学学报,1987,22(9):685
7,Guevara A P, Lin-Sylianco C Y, Dayrit F M. Phytochemistry, 1989,28(6):1721
8,Sucrow W. Tetrahedron Lett,1965,26:2217
9,陈靖宇,陈建民,肖培根.中国协和医科大学中国医学科学院博士学位论文.1997:31
(1999-06-10收稿), http://www.100md.com
单位:中国医学科学院 中国协和医科大学药用植物研究所 北京 100094
关键词:苦瓜;降糖成分;苦瓜脑苷
中草药000805摘 要 为寻找降糖活性成分,利用多种层析技术,从苦瓜Momordica charantia果实的醇提物中分得5 个化合物。根据包括2D-NMR在内的各种光谱数据,分别鉴定为:苦瓜脑苷(momor-cerebroside, Ⅰ)、大豆脑苷Ⅰ(soya-cerebroside Ⅰ,Ⅱ)、苦瓜亭(charantin, Ⅲ)、尿嘧啶(uracil, Ⅳ)及β-谷甾醇。其中化合物Ⅰ、Ⅱ为本属中首次分得;化合物Ⅲ为文献报道的降糖有效成分。
苦瓜Momordica charantia L. 为葫芦科Cucurbitaceae苦瓜属植物,未熟的苦瓜鲜品或干燥切片均可入药,具有清热解毒和明目之功效。我们在初步的药理试验中发现,鲜苦瓜果汁可明显增强链脲霉素型糖尿病小鼠的糖耐量并降低其血糖高峰值,其效果优于阳性对照药降糖灵。这一发现促使我们对苦瓜的化学成分作进一步的研究。
, 百拇医药
有报道[1]苦瓜果实的氯仿部分存在具有显著降糖作用的活性成分。我们从苦瓜果实醇提物氯仿部分得到了5 个化合物,分别确定为:苦瓜脑苷(momor-cerebroside, Ⅰ)、大豆脑苷Ⅰ(soya-cerebroside Ⅰ,Ⅱ)、苦瓜亭(charantin, Ⅲ)、尿嘧啶(uracil, Ⅳ)及β-谷甾醇(β-sitosterol, Ⅴ)。其中,苦瓜脑苷Ⅰ及大豆脑苷Ⅰ(Ⅱ)系本属首次分出;苦瓜亭(Ⅲ)为文献报道的降糖有效成分[2]。
1 仪器和材料
熔点采用Fisher-Johns型熔点测定仪测定(温度未校正);红外光谱采用KBr压片,以Perkin-Elmer 983 G型红外光谱仪测定;核磁共振谱以Bruker AM-500型核磁共振仪测定,TMS为内标;质谱以Zabspec型质谱仪测定。层析用硅胶由青岛海洋化工厂生产(柱层析:粗孔硅胶100~200 目;薄层层析:硅胶G高效预制板)。层析用溶剂均为分析纯。苦瓜果实于1997年8月采自江西省赣州市。
, 百拇医药
2 提取和分离
取鲜苦瓜20 kg切片,95%工业乙醇热浸提取4 次,浓缩提取液至3 L,以氯仿-水分配,将氯仿层蒸干,得干膏70 g。该部分经反复硅胶柱层析后,分离得到化合物Ⅰ~Ⅴ。
3 鉴定
化合物Ⅰ:白色结晶性粉末(90%乙醇),17 mg, mp 143 ℃~145 ℃,FAB-MS (m/z):866〔(M+Na)+,16〕,682,384,280;SIMS (m/z):842.666 6〔(M-H)+,计算值:842.672 6〕,确定分子量为843,分子式为C48H93O10N。IR光谱显示存在羟基、酰胺键及脂肪长链。13CNMR中δ 175.6,51.8处的信号及δ 29.9处强的(CH2)n信号;1HNMR中δ 1.30处的强(CH2)n信号及δ 0.85处的2 个末端甲基信号表明该化合物为神经酰胺类成分。13CNMR中δ 105.6,78.5,75.2,71.6,62.7及1HNMR中δ4.95(d,7.7 Hz)表明Ⅰ为-β葡萄糖苷,即脑苷类化合物(cerebrosides)。

, http://www.100md.com
图1 化合物Ⅰ的结构片断
由13C-1H COSY谱,可归属A链 C-2上的氢信号δ 5.28。它与δ 4.71,4.52(H-1α,H-1β)及δ 4.28(H-3)处的信号的有偶合。结合13C-1H COSY谱,归属C-1信号δ70.5,C-3信号δ 76.0。而在HMBC谱中,C-3信号δ 76.0与δ 4.18(H-4)的质子信号相关;羰基信号δ 175.6与δ 4.57(H-2′),处的信号相关。因此,可判断A链的C-3、C-4位,B链的C-2′位均为羟基,即化合物Ⅰ的结构中存在如图1的结构片断。
神经酰胺部分A、B链的组成由质谱碎片m/z 280(A链-H2O)及384(羰基麦氏重排碎片+H)确定。13CNMR谱中的δ130.9,130.7表明结构中有一双键,通过烯丙位碳的化学位移值(δ33.3,33.0)判断为反式双键[3];由1H-1HCOSY、13C-1HCOSY及HMBC谱, 可依次归属13CNMR及1HNMR信号(表1),并可确定△8,9双键。
, 百拇医药
表1 化合物Ⅰ的13CNMR(125 MHz)和1HNMR(500 MHz)的光谱数据(C5D5N) No
δc
δH(J/Hz)
No
δc
δH(J/Hz)
sphingosine moiety
fatty acid moiety
1
70.5
, http://www.100md.com
4.71(dd,10.6,6.7)
1′
175.6
4.52(dd,10.6,4.5)
2′
72.6
4.57
2
51.8
5.28
3′
35.7
1.99,2.19
, http://www.100md.com
3
76.0
4.28(t-like)
4′
25.9
1.76
4
72.6
4.18
5′~21′
30.0~29.5
1.30~1.24
5
, 百拇医药
33.9
1.89,2.25
22′
32.1
1.30~1.24
6
26.6
1.76,1.98
23′
22.9
1.30~1.24
7
33.3
, 百拇医药
2.19
24′
14.2
0.85
8
130.9
5.50(m)
hexose moiety
9
130.7
5.50(m)
1″
105.6
, http://www.100md.com
4.95(d,7.7)
10
33.0
1.98
2″
75.2
4.00
11~15
30.0~29.5
1.30~1.24
3″
78.5
4.18
, 百拇医药
16
32.1
1.30~1.24
4″
71.6
4.18
17
22.9
1.30~1.24
5″
78.5
3.86
18
, http://www.100md.com
14.2
0.85
6″
62.7
4.33(dd,9.1,5.3)
4.48(dd,6.2)
综上所述,确定化合物Ⅰ的结构为:8(E)-N-(2′-D-羟基-二十四烷酰基)-1-O-β-D-吡喃葡萄糖基-8-烯-十八鞘氨醇(8[E]-N-[2′-hydroxy-tetracosoyl]-1-O-β-D-glucopyranosy1-8-en-octadecasphingenine,如图 2)。该结构由Edgar 等[4]在对黑麦Secale cerale L. cv. Puma. 的总脑苷作气质分析时首次提出,本文系首次以单体形式从自然界分得该化合物,并首次报道其光谱数据。因此,命名为苦瓜脑苷(momor-cerebroside)。

, 百拇医药
图2 化合物Ⅰ的化学结构式
化合物Ⅱ : 白色结晶性粉末( 90%乙醇),30 mg,mp 180 ℃~182 ℃,IR、1H,13CNMR数据与文献[5]中,大豆脑苷Ⅰ(soya-cerebroside Ⅰ,即4[E],8[E]-N-[2′-D-羟基-十六烷酰基]-1-O-β-D-吡喃葡萄糖苷-4,8-二烯-十八鞘氨醇)的数据一致。
化合物Ⅲ:白色粉末,680 mg,mp 247 ℃~250 ℃。将其13CNMR(C5D5N)数据与文献[6]中报道的胡萝卜苷、文献[7]中报道的5,25-豆甾二烯棕榈酸酯葡萄糖苷的数据比较,结合其它光谱学数据可知,该化合物为文献[8]中报道的苦瓜亭(charantin),即胡萝卜苷与5,25-豆甾二烯醇葡萄糖苷的混合物。
, http://www.100md.com
化合物Ⅳ:黄色粉末112 mg,mp 236 ℃~238 ℃(分解),IR、FAB-MS及13CNMR数据与文献[9]报道的尿嘧啶的数据一致。
化合物Ⅴ:白色针晶(丙酮)20 mg,mp 137 ℃~138 ℃,与β-谷甾醇标准品混合,熔点不下降,与标准品Co-TLC及Co-IR的比较,均表明与β-谷甾醇一致。
致谢:本所标本馆潘瑞乐同志鉴定生药;北京微量化学研究所分析中心代测NMR谱;军事医学科学院质谱室及中国科学院质谱室代测MS谱;本所分析室代测IR谱。
肖志艳 女,中国医学科学院中国协和医科大学1999届硕士研究生
参考文献
1,Day C, Crutwright T, Pvovest J, et al. Planta Med,1990,56:426
, 百拇医药
2,Lotlikar M M. Indian J Pharm, 1966,28(5):129
3,方乍浦,曾宪仪,熊淑玲.天然产物研究与开发,1996,8(3):20
4,Cahoon E B and Lynch D V. Plant Physiol, 1991,95:58
5,Shibuya H, Kawashima K, Sakagami M, et al. Chem Pharm Bull,1990,38(11):2933
6,陈英杰,徐缓绪,马启风,等.药学学报,1987,22(9):685
7,Guevara A P, Lin-Sylianco C Y, Dayrit F M. Phytochemistry, 1989,28(6):1721
8,Sucrow W. Tetrahedron Lett,1965,26:2217
9,陈靖宇,陈建民,肖培根.中国协和医科大学中国医学科学院博士学位论文.1997:31
(1999-06-10收稿), http://www.100md.com