细胞凋亡和Fas/FasL基因在小鼠病毒性心肌炎发病中的作用
韩波 马沛然 刘芳 王延军 劳平 蒋莎义 孙杰
摘 要 目的 探讨细胞毒T淋巴细胞(CTL)经Fas/FasL介导的细胞凋亡在柯萨奇病毒B3 (CVB3) 病毒性心肌炎(VM)小鼠发病中的作用。方法 采用电镜技术及原位末端标记法(TUNEL)检测小鼠心肌组织的细胞凋亡,同时采用免疫组化、逆转录-聚合酶链反应(RT-PCR)及原位杂交3种方法检测心肌炎小鼠不同时期心肌组织中Fas与FasL基因转录与蛋白的表达。结果 (1)各期病鼠心肌组织中的TUNEL阳性的心肌细胞凋亡检出率为79%,中、重度VM小鼠的检出率明显高于轻度VM小鼠(P<0.05)。平均心肌细胞凋亡百分率为(8±6)%。感染后第7~14天心肌细胞凋亡百分率明显高于第21~28天(P<0.05)。 (2)感染后第7~14天,病鼠心肌组织中,主要表达于心肌细胞的Fas mRNA及蛋白和主要表达于浸润淋巴细胞的FasL mRNA 及蛋白均明显增强(P<0.01)。FasL蛋白表达水平与心肌病变积分呈正相关(r=0.89, P<0.01)。结论 细胞毒T淋巴细胞通过Fas/FasL基因径路介导的心肌细胞凋亡与病毒性心肌炎的发病过程有关。
, http://www.100md.com
关键词:小鼠;柯萨奇病毒B组;心肌炎;T淋巴细胞;脱噬作用;抗原,CD95
目前的研究表明,细胞毒T淋巴细胞(cytotoxic T lymphocyte ,CTL)介导的细胞毒作用是致病毒性心肌炎(viral myocarditis,VM)心肌细胞损伤的主要原因。Fas/FasL径路是CTL致靶细胞损伤的主要途径之一[1]。VM存在心肌细胞凋亡,然而其分子调控机制尚未阐明。为此,本研究检测柯萨奇病毒B3 (coxsackie virus B3, CVB3)所致 VM小鼠不同时期心肌组织中心肌细胞凋亡和Fas/FasL基因转录与蛋白表达水平,探讨CTL 经Fas/FasL介导的细胞凋亡在VM发病中的作用。
材料和方法
一、 CVB3心肌炎动物模型的制备
, 百拇医药
由山东省医学科学院提供CVB3病毒(Nancy株)。 125只4~6周龄雄性Balb/c小鼠由山东医科大学动物实验中心提供。随机将小鼠分成2组:实验组100只,每只腹腔接种0.12 ml含109 TCID50CVB3的病毒液。对照组25只,腹腔接种等量生理盐水。分别于接种后第7、10、14、21、28天,随机取实验组小鼠20只、对照组小鼠5只,将其处死。取其心脏,半数冻存于-80℃冰箱,待做逆转录-聚合酶链反应(RT-PCR)及冰冻切片;半数用4%多聚甲醛固定,待做HE染色、免疫组化、TUNEL法检测,每批取2只病鼠的心肌用2.5%戊二醛固定,待做电镜检测。
二、病理学检查
常规HE染色,光镜下观察心肌病理变化,并计算心肌病变积分。即每张切片取5个视野,计算每个视野中炎性细胞浸润及坏死区域面积与整个视野的面积之比。无病变计0分,<25%计1分,25%~50%计2分,50%~75%计3分,>75%计4分。
, 百拇医药
三、TUNEL法原位检测心肌细胞凋亡
利用寡核苷酸末端脱氧核糖核酸转移酶(TdT)介导的dUTP缺口末端标记法检测。结果判定:随机计数5个高倍镜(×400)视野的心肌细胞总数及阳性心肌细胞数,按公式:阳性细胞/细胞总数×100%,计算心肌凋亡细胞百分率。
四、免疫组化检测Fas、FasL抗原
兔抗大鼠多克隆抗体Fas、FasL及SABC复合物均购自武汉博士德生物工程有限公司。按常规SABC法进行免疫组化检测,DAB染色,以PBS取代一抗和二抗作空白对照,光镜下观察结果。在MPIAS-500图像分析仪上,每个切片取5个高倍镜视野,测量心肌组织中阳性染色细胞的吸光度。
五、RT-PCR
采用Trizol(购自美国GBICO公司)提取总RNA,按AMV逆转录及PCR说明进行RT-PCR。引物序列:Fas: 5′-GACCCAGAATACCAAGTGCA-3′,5′-TCT-GTTCTGCTGTGTCTTGG-3′; FasL:5′-ATGGTTCTGG-TGGCTCTGGT-3′, 5′-GTTTAGGGGCTGGTTGTTGC-3′; 内参照基因β-actin: 5′-TGGAATCCTGTGGCATCC-ATGAAC-3′, 5′-TAAACGCAGCTCAGTAACAGTCCG-3′。可分别扩增436 bp的Fas cDNA、360 bp的FasL cDNA及349 bp的β-actin cDNA序列[1,2]。扩增条件为94℃ 4 min, 94℃ 30 s,57℃ 30 s,72℃ 60 s,循环30次。在0.5 TBE电泳缓冲液中电压为 80 V电泳1 h,紫外灯下观察结果。并以PCR Marker作为标准分子量参照进行产物鉴定。用岛津-CS薄层扫描仪,测定PCR产物电泳条带的密度积分,计算Fas产物的相对量。计算公式:Fas相对量= Fas产物电泳条带密度/β-actin电泳条带密度×100%。
, 百拇医药
六、原位杂交
质粒来源(均由第二军医大学钱其军博士惠赠):小鼠Fas cDNA载体质粒为pBluescript KS(+),酶切位点为EcoR I。人FasL cDNA载体质粒为pBluescript-Ⅱ,酶切位点为Xbal-Ⅰ。按地高辛随机引物标记试剂盒(购自德国BM公司)说明书制备Fas cDNA、FasL cDNA探针,并按核酸检测试剂盒(购自德国BM公司)说明的步骤检测探针浓度。采用原位杂交检测心肌组织(冰冻切片)中Fas、FasL mRNA,以PBR322探针作为空白对照。图像分析同免疫组化。
七、统计学分析
计量资料用X±s,采用PEMS统计软件包进行F-q′检验,计数资料应用精确卡方检验和秩和检验,部分指标间作直线相关分析,P<0.05,差异具有显著性。
结果
, http://www.100md.com
一、CVB3心肌炎小鼠心肌的病理变化
实验组小鼠于接种后第7天即见有明显的心肌细胞坏死和淋巴细胞浸润,第10~14天病变达高峰,第21天部分炎性病灶开始吸收,代之以纤维化,第28天多数病灶吸收。总感染率为86%,平均病变积分为(2.4±1.1)分。
二、CVB3心肌炎小鼠心肌细胞凋亡的检测
经电镜检查可见到小鼠凋亡的心肌细胞(图1),其检出率为50%(5/10)(还可见血管内皮细胞及间质细胞)。而正常对照组中2只小鼠均未见到凋亡细胞(图2)。经TUNEL法检测细胞凋亡,含有DNA片段的凋亡细胞核呈紫兰色,正常细胞核为淡红色。凋亡的心肌细胞,多分布在心内膜、心外膜下及炎症灶周围,还可见呈阳性染色的血管内皮细胞及浸润淋巴细胞。实验组中小鼠心肌细胞凋亡的检出率为79%(15/19),中、重度病鼠心肌细胞凋亡的检出率(14/14)较轻度病鼠(1/5)明显升高(P<0.05)。平均心肌细胞凋亡百分率为(8±6)%,感染后7~14 d小鼠心肌细胞凋亡百分率(中位数为8%)较21~28 d小鼠心肌细胞凋亡百分率(中位数为5%)明显升高(T=42,P<0.05)。检测正常对照组中小鼠5只,均未见到凋亡细胞。
, 百拇医药
图1 CVB3 VM小鼠心肌细胞凋亡图像 (电镜 ×10 000)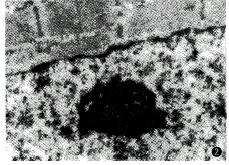
图2 正常小鼠心肌细胞图像 (电镜 ×10 000)
三、免疫组化检测Fas、FasL蛋白在CVB3心肌炎小鼠不同时期心肌组织中的表达
实验组中,Fas蛋白阳性染色细胞多为分布于炎症灶周围的心肌细胞、少量浸润细胞及血管内皮细胞,FasL阳性染色细胞主要为炎症灶内的浸润细胞及周围的心肌细胞。由表1可见,Fas和FasL 蛋白表达均于第7天明显增加,第10~14天达高峰,第21~28天下降。而且FasL蛋白表达水平与病变积分呈显著正相关(r=0.89,P<0.01)。
, http://www.100md.com
表1 Fas、FasL蛋白在CVB3心肌炎小鼠不同时期
心肌组织中的表达(X±s,吸光度A值)
组别
Fas
FasL
病变积分
对照组
0.081±0.032
0.033±0.020
0
实验组
第 7天
, 百拇医药
0.127±0.026*
0.114±0.006*
2.18±1.07
第10天
0.130±0.032*
0.120±0.011*
2.78±1.11
第14天
0.113±0.019*
0.107±0.009*
, http://www.100md.com
2.61±1.04
第21天
0.096±0.032*
0.085±0.006*
2.19±1.05
第28天
0.087±0.021
0.071±0.020*
2.01±0.97
F值
117.22
, 百拇医药
1 224.49
P值
<0.001
<0.001
注:与对照组相比,*P<0.01;对照组及实验组每批鼠数均为10只 四、RT-PCR检测Fas mRNA、FasL mRNA在CVB3心肌炎小鼠心肌中的表达
由表2可见,CVB3心肌炎小鼠Fas mRNA第7天即明显升高,第10~14天达高峰,第21天开始逐渐下降。定性RT-PCR显示,实验组小鼠心肌组织中FasL mRNA检出率为92%(23/25),较正常对照组的30%(3/10)明显增加(P=0.000 5)。
表2 Fas mRNA在CVB3心肌炎小鼠心肌组织
, http://www.100md.com
各期的改变(X±s, %)
组别
鼠数
Fas/β-action
对照组
5
21±5
实验组
第 7天
5
39±8*
第10天
5
, 百拇医药
46±12*
第14天
5
36±9*
第21天
5
27±9**
第28天
5
23±6
F值
12.87
, 百拇医药
P值
<0.001
注:与对照组相比,*P<0.01,**P<0.05 五、原位杂交检测Fas mRNA、FasL mRNA的表达情况
Fas mRNA阳性染色颗粒主要分布在炎症周围的心肌细胞及少量浸润细胞胞浆内;FasL mRNA阳性染色颗粒主要分布在浸润的淋巴细胞及部分炎症周围的心肌细胞胞浆内。由表3可见,在感染第7~14天Fas、FasL mRNA 均显著升高,第21~28天下降。
表3 Fas、FasL mRNA在CVB3心肌炎小鼠心肌
组织中的表达(X±s,吸光度A值)
组别
, 百拇医药
鼠数
Fas mRNA
FasL mRNA
对照组
10
0.32±0.03
0.20±0.04
实验组
第 7~14天
10
0.44±0.06*
0.48±0.03*
, 百拇医药
第21~28天
10
0.34±0.06*
0.38±0.15*
F值
1 586.31
1 384.40
P值
<0.001
<0.001
注:与对照组相比,*P<0.01
, 百拇医药
讨论
1994年Kawano等[3]首次报道心肌炎患者存在心肌细胞凋亡现象,此后陆续有学者通过对心肌炎患者的心肌活检和动物实验证实[4,5]。然而,心肌细胞凋亡与VM的病变程度及病程的关系如何,尚未见报道。我们利用电镜观察发现,每批病鼠心肌中均存在心肌细胞凋亡。应用TUNEL法检测发现,病鼠中心肌细胞凋亡阳性检出率为79%,而正常对照组中未见到凋亡细胞,可能是因数目极少的缘故。中、重度 VM病鼠细胞凋亡检出率显著高于轻度病鼠。感染第7天开始心肌细胞凋亡百分率明显升高,第10~14天达高峰,第21天后明显降低,表明细胞凋亡参与了心肌炎疾病的发展过程。
CTL介导的细胞毒作用是VM的主要发病机制,然而其分子机制尚未阐明。目前的研究表明,VM中心肌细胞浸润的CTL包括CD+4和CD+8。而CD+4细胞,往往通过Fas/FasL显示其CTL的杀伤活性。CD+8 T细胞则通过Fas/FasL和穿孔素-粒酶两种方式显示其CTL活性[6]。Fas是细胞膜表面受体蛋白,属于肿瘤坏死因子(TNF)及神经生长因子受体(NGFR)超家族成员。Fas 主要表达于成熟的淋巴细胞、心脏等; FasL 是Fas的配体,为TNF 同源的Ⅱ型穿膜蛋白,主要表达于活化的T淋巴细胞。细胞膜表面的FasL ,可与靶细胞表面的Fas 受体结合,向细胞内传导死亡信号,使靶细胞在数小时内发生凋亡。体外实验已证实,CTL可以通过Fas/FasL 路径导致心室肌细胞凋亡[7],而且Fas/FasL系统参与了心脏中CTL介导的疾病如心脏移植排异反应[8]。Toyozaki等[5]的研究表明,外周血血清可溶性FasL升高的VM患者TUNEL阳性心肌细胞显著增加,提示Fas/FasL诱导 的细胞凋亡参与了VM 的发病机制。本研究结果显示,感染第7天的心肌细胞Fas mRNA及Fas蛋白和心肌浸润细胞FasL mRNA及FasL蛋白表达明显增强,细胞凋亡增加,第10~14天心肌Fas mRNA及Fas蛋白及浸润细胞FasL mRNA及蛋白表达均达高峰,细胞凋亡亦达高峰,且凋亡的心肌细胞多分布于炎症细胞周围。第21天开始三者均渐下降。推测心肌细胞凋亡可能是由于浸润细胞表面的FasL与心肌细胞表面的Fas相结合所致。而且FasL蛋白的表达与心肌病变密切相关,表明Fas/ FasL系统参与了VM的发病机制。
, 百拇医药
本研究的结果显示,感染第7~14天的小鼠心肌组织可见少量浸润细胞发生凋亡,连续切片显示,多数浸润细胞表达FasL蛋白,少数还表达 Fas蛋白,因此心肌浸润细胞存在Fas/ FasL介导的细胞凋亡。此外,CVB3感染后的病鼠心肌细胞可表达FasL蛋白,同时发现凋亡的心肌细胞并非均在浸润细胞周围,也可呈散在分布,故推测表达FasL的心肌细胞可能通过旁分泌或自分泌的形式导致相邻表达Fas的心肌细胞自身死亡。
总之,细胞凋亡是VM造成心肌损伤的原因之一,Fas/ FasL系统参与其分子调控,经Fas/FasL介导的细胞凋亡可能是CTL导致VM心肌损伤的作用机制之一。
作者单位:韩波(250021 济南,山东省立医院儿科)
马沛然(250021 济南,山东省立医院儿科)
刘芳(250021 济南,山东省立医院儿科)
, 百拇医药
蒋莎义(250021 济南,山东省立医院儿科)
孙杰(250021 济南,山东省立医院儿科)
王延军(中心实验室)
劳平(中心实验室)
参考文献
1,anabuchi S, Koyanagi M, Kawasaki A, et al. Fas and its ligand in a general mechanism of T-cell-mediated cytotoxicity. Proc Natl Acad Sci USA,1994,91:4930-4934.
2,Tanaka M, Ito H, Adachi S, et al. Hypoxia induces apoptosis with enhanced expression of Fas antigen messenger RNA in cultured neonatal rat cardiomyocytes. Circ Res, 1994, 75:426-433.
, 百拇医药
3,Kawano H, Okada R, Kauano Y, et al.Apoptosis in acute and chronic myocarditis. Jpn Heart J,1994,35:745-750.
4,Huber SA.Coxsackievirus-induced myocarditis is dependent on distinct immunopathogenic responses in different strains of mice.Lab Invest, 1997,76:691-701.
5,Toyozaki T, Hiroe M, Tanaka M. Levels of soluble Fas ligand in myocarditis.Am J Cardio, 1998,82:246-248.
6,宋建勋. CTL细胞毒作用机制的研究进展. 国外医学免疫学分册,1997,20:203-206.
, 百拇医药
7,Fella B,Shilkrut M,Less H,et al.Fas(CD95/APO-1)-medited damage to ventricular myocytes induced by cytotoxic T lymphocytes from perforin-deficient mice :a major role for inositol 1,4,5-Trisphophate.Circ Rec,1998,82:438-450.
8,Kageyama Y,Li X,Suzuki S,et al.Apoptosis is involved in acute cardiac allograft rejection in rats.Ann Thorac Surg, 1998,65:1604-1609., http://www.100md.com
摘 要 目的 探讨细胞毒T淋巴细胞(CTL)经Fas/FasL介导的细胞凋亡在柯萨奇病毒B3 (CVB3) 病毒性心肌炎(VM)小鼠发病中的作用。方法 采用电镜技术及原位末端标记法(TUNEL)检测小鼠心肌组织的细胞凋亡,同时采用免疫组化、逆转录-聚合酶链反应(RT-PCR)及原位杂交3种方法检测心肌炎小鼠不同时期心肌组织中Fas与FasL基因转录与蛋白的表达。结果 (1)各期病鼠心肌组织中的TUNEL阳性的心肌细胞凋亡检出率为79%,中、重度VM小鼠的检出率明显高于轻度VM小鼠(P<0.05)。平均心肌细胞凋亡百分率为(8±6)%。感染后第7~14天心肌细胞凋亡百分率明显高于第21~28天(P<0.05)。 (2)感染后第7~14天,病鼠心肌组织中,主要表达于心肌细胞的Fas mRNA及蛋白和主要表达于浸润淋巴细胞的FasL mRNA 及蛋白均明显增强(P<0.01)。FasL蛋白表达水平与心肌病变积分呈正相关(r=0.89, P<0.01)。结论 细胞毒T淋巴细胞通过Fas/FasL基因径路介导的心肌细胞凋亡与病毒性心肌炎的发病过程有关。
, http://www.100md.com
关键词:小鼠;柯萨奇病毒B组;心肌炎;T淋巴细胞;脱噬作用;抗原,CD95
目前的研究表明,细胞毒T淋巴细胞(cytotoxic T lymphocyte ,CTL)介导的细胞毒作用是致病毒性心肌炎(viral myocarditis,VM)心肌细胞损伤的主要原因。Fas/FasL径路是CTL致靶细胞损伤的主要途径之一[1]。VM存在心肌细胞凋亡,然而其分子调控机制尚未阐明。为此,本研究检测柯萨奇病毒B3 (coxsackie virus B3, CVB3)所致 VM小鼠不同时期心肌组织中心肌细胞凋亡和Fas/FasL基因转录与蛋白表达水平,探讨CTL 经Fas/FasL介导的细胞凋亡在VM发病中的作用。
材料和方法
一、 CVB3心肌炎动物模型的制备
, 百拇医药
由山东省医学科学院提供CVB3病毒(Nancy株)。 125只4~6周龄雄性Balb/c小鼠由山东医科大学动物实验中心提供。随机将小鼠分成2组:实验组100只,每只腹腔接种0.12 ml含109 TCID50CVB3的病毒液。对照组25只,腹腔接种等量生理盐水。分别于接种后第7、10、14、21、28天,随机取实验组小鼠20只、对照组小鼠5只,将其处死。取其心脏,半数冻存于-80℃冰箱,待做逆转录-聚合酶链反应(RT-PCR)及冰冻切片;半数用4%多聚甲醛固定,待做HE染色、免疫组化、TUNEL法检测,每批取2只病鼠的心肌用2.5%戊二醛固定,待做电镜检测。
二、病理学检查
常规HE染色,光镜下观察心肌病理变化,并计算心肌病变积分。即每张切片取5个视野,计算每个视野中炎性细胞浸润及坏死区域面积与整个视野的面积之比。无病变计0分,<25%计1分,25%~50%计2分,50%~75%计3分,>75%计4分。
, 百拇医药
三、TUNEL法原位检测心肌细胞凋亡
利用寡核苷酸末端脱氧核糖核酸转移酶(TdT)介导的dUTP缺口末端标记法检测。结果判定:随机计数5个高倍镜(×400)视野的心肌细胞总数及阳性心肌细胞数,按公式:阳性细胞/细胞总数×100%,计算心肌凋亡细胞百分率。
四、免疫组化检测Fas、FasL抗原
兔抗大鼠多克隆抗体Fas、FasL及SABC复合物均购自武汉博士德生物工程有限公司。按常规SABC法进行免疫组化检测,DAB染色,以PBS取代一抗和二抗作空白对照,光镜下观察结果。在MPIAS-500图像分析仪上,每个切片取5个高倍镜视野,测量心肌组织中阳性染色细胞的吸光度。
五、RT-PCR
采用Trizol(购自美国GBICO公司)提取总RNA,按AMV逆转录及PCR说明进行RT-PCR。引物序列:Fas: 5′-GACCCAGAATACCAAGTGCA-3′,5′-TCT-GTTCTGCTGTGTCTTGG-3′; FasL:5′-ATGGTTCTGG-TGGCTCTGGT-3′, 5′-GTTTAGGGGCTGGTTGTTGC-3′; 内参照基因β-actin: 5′-TGGAATCCTGTGGCATCC-ATGAAC-3′, 5′-TAAACGCAGCTCAGTAACAGTCCG-3′。可分别扩增436 bp的Fas cDNA、360 bp的FasL cDNA及349 bp的β-actin cDNA序列[1,2]。扩增条件为94℃ 4 min, 94℃ 30 s,57℃ 30 s,72℃ 60 s,循环30次。在0.5 TBE电泳缓冲液中电压为 80 V电泳1 h,紫外灯下观察结果。并以PCR Marker作为标准分子量参照进行产物鉴定。用岛津-CS薄层扫描仪,测定PCR产物电泳条带的密度积分,计算Fas产物的相对量。计算公式:Fas相对量= Fas产物电泳条带密度/β-actin电泳条带密度×100%。
, 百拇医药
六、原位杂交
质粒来源(均由第二军医大学钱其军博士惠赠):小鼠Fas cDNA载体质粒为pBluescript KS(+),酶切位点为EcoR I。人FasL cDNA载体质粒为pBluescript-Ⅱ,酶切位点为Xbal-Ⅰ。按地高辛随机引物标记试剂盒(购自德国BM公司)说明书制备Fas cDNA、FasL cDNA探针,并按核酸检测试剂盒(购自德国BM公司)说明的步骤检测探针浓度。采用原位杂交检测心肌组织(冰冻切片)中Fas、FasL mRNA,以PBR322探针作为空白对照。图像分析同免疫组化。
七、统计学分析
计量资料用X±s,采用PEMS统计软件包进行F-q′检验,计数资料应用精确卡方检验和秩和检验,部分指标间作直线相关分析,P<0.05,差异具有显著性。
结果
, http://www.100md.com
一、CVB3心肌炎小鼠心肌的病理变化
实验组小鼠于接种后第7天即见有明显的心肌细胞坏死和淋巴细胞浸润,第10~14天病变达高峰,第21天部分炎性病灶开始吸收,代之以纤维化,第28天多数病灶吸收。总感染率为86%,平均病变积分为(2.4±1.1)分。
二、CVB3心肌炎小鼠心肌细胞凋亡的检测
经电镜检查可见到小鼠凋亡的心肌细胞(图1),其检出率为50%(5/10)(还可见血管内皮细胞及间质细胞)。而正常对照组中2只小鼠均未见到凋亡细胞(图2)。经TUNEL法检测细胞凋亡,含有DNA片段的凋亡细胞核呈紫兰色,正常细胞核为淡红色。凋亡的心肌细胞,多分布在心内膜、心外膜下及炎症灶周围,还可见呈阳性染色的血管内皮细胞及浸润淋巴细胞。实验组中小鼠心肌细胞凋亡的检出率为79%(15/19),中、重度病鼠心肌细胞凋亡的检出率(14/14)较轻度病鼠(1/5)明显升高(P<0.05)。平均心肌细胞凋亡百分率为(8±6)%,感染后7~14 d小鼠心肌细胞凋亡百分率(中位数为8%)较21~28 d小鼠心肌细胞凋亡百分率(中位数为5%)明显升高(T=42,P<0.05)。检测正常对照组中小鼠5只,均未见到凋亡细胞。

, 百拇医药
图1 CVB3 VM小鼠心肌细胞凋亡图像 (电镜 ×10 000)

图2 正常小鼠心肌细胞图像 (电镜 ×10 000)
三、免疫组化检测Fas、FasL蛋白在CVB3心肌炎小鼠不同时期心肌组织中的表达
实验组中,Fas蛋白阳性染色细胞多为分布于炎症灶周围的心肌细胞、少量浸润细胞及血管内皮细胞,FasL阳性染色细胞主要为炎症灶内的浸润细胞及周围的心肌细胞。由表1可见,Fas和FasL 蛋白表达均于第7天明显增加,第10~14天达高峰,第21~28天下降。而且FasL蛋白表达水平与病变积分呈显著正相关(r=0.89,P<0.01)。
, http://www.100md.com
表1 Fas、FasL蛋白在CVB3心肌炎小鼠不同时期
心肌组织中的表达(X±s,吸光度A值)
组别
Fas
FasL
病变积分
对照组
0.081±0.032
0.033±0.020
0
实验组
第 7天
, 百拇医药
0.127±0.026*
0.114±0.006*
2.18±1.07
第10天
0.130±0.032*
0.120±0.011*
2.78±1.11
第14天
0.113±0.019*
0.107±0.009*
, http://www.100md.com
2.61±1.04
第21天
0.096±0.032*
0.085±0.006*
2.19±1.05
第28天
0.087±0.021
0.071±0.020*
2.01±0.97
F值
117.22
, 百拇医药
1 224.49
P值
<0.001
<0.001
注:与对照组相比,*P<0.01;对照组及实验组每批鼠数均为10只 四、RT-PCR检测Fas mRNA、FasL mRNA在CVB3心肌炎小鼠心肌中的表达
由表2可见,CVB3心肌炎小鼠Fas mRNA第7天即明显升高,第10~14天达高峰,第21天开始逐渐下降。定性RT-PCR显示,实验组小鼠心肌组织中FasL mRNA检出率为92%(23/25),较正常对照组的30%(3/10)明显增加(P=0.000 5)。
表2 Fas mRNA在CVB3心肌炎小鼠心肌组织
, http://www.100md.com
各期的改变(X±s, %)
组别
鼠数
Fas/β-action
对照组
5
21±5
实验组
第 7天
5
39±8*
第10天
5
, 百拇医药
46±12*
第14天
5
36±9*
第21天
5
27±9**
第28天
5
23±6
F值
12.87
, 百拇医药
P值
<0.001
注:与对照组相比,*P<0.01,**P<0.05 五、原位杂交检测Fas mRNA、FasL mRNA的表达情况
Fas mRNA阳性染色颗粒主要分布在炎症周围的心肌细胞及少量浸润细胞胞浆内;FasL mRNA阳性染色颗粒主要分布在浸润的淋巴细胞及部分炎症周围的心肌细胞胞浆内。由表3可见,在感染第7~14天Fas、FasL mRNA 均显著升高,第21~28天下降。
表3 Fas、FasL mRNA在CVB3心肌炎小鼠心肌
组织中的表达(X±s,吸光度A值)
组别
, 百拇医药
鼠数
Fas mRNA
FasL mRNA
对照组
10
0.32±0.03
0.20±0.04
实验组
第 7~14天
10
0.44±0.06*
0.48±0.03*
, 百拇医药
第21~28天
10
0.34±0.06*
0.38±0.15*
F值
1 586.31
1 384.40
P值
<0.001
<0.001
注:与对照组相比,*P<0.01
, 百拇医药
讨论
1994年Kawano等[3]首次报道心肌炎患者存在心肌细胞凋亡现象,此后陆续有学者通过对心肌炎患者的心肌活检和动物实验证实[4,5]。然而,心肌细胞凋亡与VM的病变程度及病程的关系如何,尚未见报道。我们利用电镜观察发现,每批病鼠心肌中均存在心肌细胞凋亡。应用TUNEL法检测发现,病鼠中心肌细胞凋亡阳性检出率为79%,而正常对照组中未见到凋亡细胞,可能是因数目极少的缘故。中、重度 VM病鼠细胞凋亡检出率显著高于轻度病鼠。感染第7天开始心肌细胞凋亡百分率明显升高,第10~14天达高峰,第21天后明显降低,表明细胞凋亡参与了心肌炎疾病的发展过程。
CTL介导的细胞毒作用是VM的主要发病机制,然而其分子机制尚未阐明。目前的研究表明,VM中心肌细胞浸润的CTL包括CD+4和CD+8。而CD+4细胞,往往通过Fas/FasL显示其CTL的杀伤活性。CD+8 T细胞则通过Fas/FasL和穿孔素-粒酶两种方式显示其CTL活性[6]。Fas是细胞膜表面受体蛋白,属于肿瘤坏死因子(TNF)及神经生长因子受体(NGFR)超家族成员。Fas 主要表达于成熟的淋巴细胞、心脏等; FasL 是Fas的配体,为TNF 同源的Ⅱ型穿膜蛋白,主要表达于活化的T淋巴细胞。细胞膜表面的FasL ,可与靶细胞表面的Fas 受体结合,向细胞内传导死亡信号,使靶细胞在数小时内发生凋亡。体外实验已证实,CTL可以通过Fas/FasL 路径导致心室肌细胞凋亡[7],而且Fas/FasL系统参与了心脏中CTL介导的疾病如心脏移植排异反应[8]。Toyozaki等[5]的研究表明,外周血血清可溶性FasL升高的VM患者TUNEL阳性心肌细胞显著增加,提示Fas/FasL诱导 的细胞凋亡参与了VM 的发病机制。本研究结果显示,感染第7天的心肌细胞Fas mRNA及Fas蛋白和心肌浸润细胞FasL mRNA及FasL蛋白表达明显增强,细胞凋亡增加,第10~14天心肌Fas mRNA及Fas蛋白及浸润细胞FasL mRNA及蛋白表达均达高峰,细胞凋亡亦达高峰,且凋亡的心肌细胞多分布于炎症细胞周围。第21天开始三者均渐下降。推测心肌细胞凋亡可能是由于浸润细胞表面的FasL与心肌细胞表面的Fas相结合所致。而且FasL蛋白的表达与心肌病变密切相关,表明Fas/ FasL系统参与了VM的发病机制。
, 百拇医药
本研究的结果显示,感染第7~14天的小鼠心肌组织可见少量浸润细胞发生凋亡,连续切片显示,多数浸润细胞表达FasL蛋白,少数还表达 Fas蛋白,因此心肌浸润细胞存在Fas/ FasL介导的细胞凋亡。此外,CVB3感染后的病鼠心肌细胞可表达FasL蛋白,同时发现凋亡的心肌细胞并非均在浸润细胞周围,也可呈散在分布,故推测表达FasL的心肌细胞可能通过旁分泌或自分泌的形式导致相邻表达Fas的心肌细胞自身死亡。
总之,细胞凋亡是VM造成心肌损伤的原因之一,Fas/ FasL系统参与其分子调控,经Fas/FasL介导的细胞凋亡可能是CTL导致VM心肌损伤的作用机制之一。
作者单位:韩波(250021 济南,山东省立医院儿科)
马沛然(250021 济南,山东省立医院儿科)
刘芳(250021 济南,山东省立医院儿科)
, 百拇医药
蒋莎义(250021 济南,山东省立医院儿科)
孙杰(250021 济南,山东省立医院儿科)
王延军(中心实验室)
劳平(中心实验室)
参考文献
1,anabuchi S, Koyanagi M, Kawasaki A, et al. Fas and its ligand in a general mechanism of T-cell-mediated cytotoxicity. Proc Natl Acad Sci USA,1994,91:4930-4934.
2,Tanaka M, Ito H, Adachi S, et al. Hypoxia induces apoptosis with enhanced expression of Fas antigen messenger RNA in cultured neonatal rat cardiomyocytes. Circ Res, 1994, 75:426-433.
, 百拇医药
3,Kawano H, Okada R, Kauano Y, et al.Apoptosis in acute and chronic myocarditis. Jpn Heart J,1994,35:745-750.
4,Huber SA.Coxsackievirus-induced myocarditis is dependent on distinct immunopathogenic responses in different strains of mice.Lab Invest, 1997,76:691-701.
5,Toyozaki T, Hiroe M, Tanaka M. Levels of soluble Fas ligand in myocarditis.Am J Cardio, 1998,82:246-248.
6,宋建勋. CTL细胞毒作用机制的研究进展. 国外医学免疫学分册,1997,20:203-206.
, 百拇医药
7,Fella B,Shilkrut M,Less H,et al.Fas(CD95/APO-1)-medited damage to ventricular myocytes induced by cytotoxic T lymphocytes from perforin-deficient mice :a major role for inositol 1,4,5-Trisphophate.Circ Rec,1998,82:438-450.
8,Kageyama Y,Li X,Suzuki S,et al.Apoptosis is involved in acute cardiac allograft rejection in rats.Ann Thorac Surg, 1998,65:1604-1609., http://www.100md.com