�������Թ��������յ�ƽ����ϸ����ֳ��Ӱ��
�������Թ��������յ�ƽ����ϸ����ֳ��Ӱ��
�˽��� ���ڹ� ���� ������
ժ Ҫ Ŀ��:̽��������(Probucol) ��H2O2�յ���ƽ����ϸ��(SMCs) ��ֳ���������á�����:����ϸ����������3H-TdR���뷨�۲�0.1��100 ��mol/L Probucol������ţѪ��(NCS)��������(H2O2)��SMCs��ֳ���������á����:10 ��mol/L��100 ��mol/L Probucol����96 h��������10%NCS�̼���SMCs��ֳ����1,10 ��100 ��mol/L Probucol����72 h��96 h������������10 ��mol/L H2O2�̼���SMCs��ֳ���ҳ�Ũ��������(P<0.05,P<0.01)������:Probucol����NCS��H2O2�̼�������������SMCs��ֳ����ʾ����ڶ�������Ӳ���;�Ƥǻ�ڹ�״����������������խ�ķ��ο��ܾ���Ӧ��ǰ����
, ��Ĵҽҩ
�ؼ��ʣ���������ƽ����ϸ������ֳ
����Ѫ��ƽ����ϸ��(SMCs)��ֳ������������Ӳ��(AS)�;�Ƥǻ�ڹ�״����������(PTCA)������խ(RS)�������Ҫ����֮һ[1]��Ѱ����Ч����SMCs��ֳ��ҩ����AS��RS�����о��е�һ����Ҫ���⡣�����������ʴ̼���AS��RS�γɵ���Ҫ����֮һ��Ѫ����Ƥϸ����л�Լ�һϵ����ƤԴ�������ͷŵ��������̽�������Ũ�ȵ������������ʡ����ֲ�Ѫ�����˺�������������Ũ��Ҳ��������[2]����������(H2O2)����Ϊ�����������ʴ�����ʵ�鷢��H2O2�յ��˺���Ѫ��ƽ����ϸ��(VSMCs)��Ѫ����Ƥ��������(VEGF)mRNA�ʼ��������Ա������ߡ�����AS��������������ģ���У��ɼ�����ֲ���������Ĥ��VEGF�ȶ������������4������[3]����������������(Probucol)��һ����Ч�����͵ĵ���Ѫ֬�Ϳ�ASҩ������������о����ִ�ҩ���ܿ�������PTCA����RS���˽��ۻ����һ��ʵ��֤ʵ���䷢������Ҳ�д���һ���о�[4]�����о�ּ��̽��Probucol��SMCs��ֳ��Ӱ�죬���ڽ�ʾProbucol��AS��RS�����е�ijЩ���û��ƣ���֧�����ٴ�Ӧ�á�
, ��Ĵҽҩ
1 ���Ϻͷ���
1.1 ��Ҫʵ����Ʒ RPMI 1640����Һ������ţѪ��(NCS)��Gibco��˾��Ʒ�� Probucol��Ʒ����Է�������:516.16,�е�������ҩ������ʱ���ڶ�������(DMSO���¹�Merck��˾��Ʒ)��DMSO��Ũ�ȵ���0.1%[5]��H2O2�����������Ϻ����ֻ�������Ʒ������������30%���ȵ���ø��Difco���ڷ�װ��3H-���������������(3H-TdR)���Ϻ�ԭ�����о���������Ȼ�ȣ�1.11��1 014 Bq/mmol���ܻ�ȣ�3.7��109 Bq��SMC���壺�ÿ���ƽ������������(SMA)������Dako��˾��Ʒ��
1.2 ����SMCs����[6]��������200��250 g SD����(�ڶ���ҽ��ѧʵ�鶯�������ṩ)������������������ȡ�������ضΣ���Hirata��֯���鷨���в�ƽ������֯����ֲ������ƿ�ڣ�����RPMI 1640����Һ(��15% NCS��1%����ù��)����37�棬5% CO2������������Լ2��5 h�����ᷭת����ƿ��ʹ��֯���������Һ�У�����������ϸ������֯���Ե������3 d����������Һһ�Σ����������ܵ�ϸ���㣬��0.25%�ȵ���ø����ϸ��������������SMCs�ļ�����������������۲�ɼ�SMCs�����Σ�ƽ����������״���У��ܼ���ϡ�账������ʡ���ȡ�״������SMA���������黯Ⱦɫ���ɼ�Ⱦ���ػ�ɫ������ϸ����֤ʵΪSMCs������Ϊ95%���ϡ�ʵ�����3��8��ϸ����ϸ��ͬ��������������3��8������״̬���õ�SMCs��������뺬10% NCS��RPMI 1640����Һ�Ƴɵ�ϸ����Һ����5��104 ��/ml��100 ��l/������96 �װ��У�����24 h�ɺ�0.5% NCS�� RPMI 1640�������壬����56 h��ʹ90%ϸ����ֹ��G0/G1�ڣ����á�
, ��Ĵҽҩ
1.3 3H-TdR���뷨[7]�ⶨSMCs��ֳ ����ϸ������ֹ����ǰ18��24 h����3H-TdR 3.7��106 Bq/�ף�������Ӧ�Ĺ۲�ʱ������ֹ�����������壬0.25%��ø����������ö�ͷϸ���ռ����ռ���Ʒ�ڲ�����ά��ֽ�ϣ���ɡ����ռ��˲�ͬ��Ʒ����ֽ�ֱ����Һ��ƿ��������˸Һ���ڦ�Һ�����в�ÿ�����������ֵ(cpm)���������Bqֵ��
1.4 ϸ���������۲�SMCs����ֳ��� ����ϸ��������Ӧ�Ĺ۲�ʱ������ֹ��������0.25%��ø�����������200 ��l/�����������У���0.01 mol/L PBS����ɾ��ȵ�ϸ����Һ������ϸ�������������
1.5 Probucol��NCS��SMCs��ֳ���õ�Ӱ��۲� ʵ���Ϊ(1) �����飺10%NCS��(2)��ҩ�飺10%NCS+ Probucol��Probucol��Ũ�ȷֱ�Ϊ0.1��1��10��100 ��mol/L��(3)��ý�飺0.1% DMSO+10% NCS������ϸ����������3H-TdR���뷨�ⶨϸ����ֳ�����
, ��Ĵҽҩ
1.6 Probucol��H2O2��SMCs��ֳ���õ�Ӱ��۲� �������ױ������ʵ�Ũ�ȵ�H2O2�����Դٽ�SMCs��ֳ[8]��������Ԥʵ���з���10 ��mol/L H2O2��SMCs����ֳ�������������ʱ�ʵ��ѡ��10 ��mol/L H2O2��Ϊ�̼�SMCs��Ч��ֳ��Ũ�ȡ�ʵ���Ϊ(1)�����飺 10 ��mol/L H2O2��(2)��ҩ�飺10 ��mol/L H2O2 + Probucol��Probucol��Ũ�ȷֱ�Ϊ0.1��1��10��100 ��mol/L��(3)��ý�飺 0.1% DMSO+2% NCS������ϸ����������3H-TdR���뷨�ⶨϸ����ֳ�����
1.7 ͳ��ѧ���� ������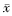 ��s��ʾ���������Ƚϲ���SAS�������з��������
��s��ʾ���������Ƚϲ���SAS�������з��������
, http://www.100md.com
2 �� ��
2.1 Probucol��NCS�ٴ���������SMCs��ֳ���õ�Ӱ�� ��ͬŨ��(0.1��1��10��100 ��mol/L)Probucol�����������Ĵ���������SMCs 48��72 h��ϸ��������3H-TdR����ֵ�������ȽϾ��������Բ���(P>0.05)��˵����ʱProbucol��10% NCS�����SMCs��ֳ�������������á�����ͬŨ��Probucol����96 h�� 10��100 ��mol/L Probucol��ϸ����ֳ���ܵ��������ƣ��ҳ�Ũ��������ϵ(P<0.05��P<0.01)����ϸ������ֵ����ó���ϸ�����������ʷֱ�Ϊ(17.8��2.5)%��(22.2��1.9)%�� ��3H-TdR����ֵ����ó��������ʷֱ�Ϊ(20.6��3.2)%�� (36.0��2.4)%����1��ʾ�˲��ֽ����
2.2 Probucol��10 ��mol/L H2O2�ٴ���������SMCs��ֳ���õ�Ӱ�� ��ͬŨ��(0.1��1��10��100 ��mol/L)Probucol������SMCs 48 h��ϸ��������3H-TdR����ֵ�������ȽϾ��������Բ���(P>0.05)��˵����ʱProbucol��10 ��mol/L H2O2�����SMCs��ֳ�������������á���������ʱ���ӳ���72 ��96 hʱ��1��10��100 ��mol/L Probucol���������Ƚ�ϸ��������3H-TdR����ֵ�����Խ���(P<0.05,P<0.01)����Ũ��������(��2)����������72 h������3��Ũ������ϸ������ֵ����ó��������ʷֱ�Ϊ (16.3��0.8)%,(31.5��1.4)%,(48.0��3.3)%������3H-TdR �������ó��������ʷֱ�Ϊ(21.4��2.6)%,(39.2��3.2)%,(67.4��4.6)%;����96 h����ϸ�������ó��������ʷֱ�Ϊ(16.5��1.8)%,(29.8��2.7)%,(47.9��3.0)%������3H-TdR�������ó��������ʷֱ�Ϊ(24.6��2.1)%,(32.8��2.9)%,(50.6��3.7)% ��
, ��Ĵҽҩ
�� 1 ��ͬʱ�䡢Ũ��Probucol��10%NCS��SMCs��ֳ���õ�Ӱ��
Tab 1 Effects of Probucol on SMCs proliferfation stimulated by NCS
(n=6��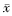 ��s)
��s)
Group
Cell number (��104 )
Incorporation of3H-TdR (A/Bq)
, ��Ĵҽҩ
72 h
96 h
72h
96 h
Control(10%NCS)
8.25��1.34
11.25��2.14
48.87��12.67
64.70��14.38
Probucol (cB/��mol.L-1)
0.1
, ��Ĵҽҩ
8.00��0.96
10.25��1.77
50.17��16.50
66.33��13.50
1
8.18��0.46
10.95��1.15
50.07��11.45
58.75��10.83
10
7.88��1.58
9.05��1.86*��
, http://www.100md.com
47.50��9.77
51.40��13.08*��
100
8.16��1.51
7.35��1.39**��������
46.50��17.18
41.43��11.40**��������
0.1%DMSO
9.05��1.48
11.75��0.98
49.25��14.17
, http://www.100md.com
61.48��16.50
*P<0.05,**P <0.01 vs control group; ��P<0.05�� ����P <0.01 vs 1 ��mol/L Probucol group; ����P<0.01 vs 10 ��mol/L Probucol group�� 2 ��ͬʱ�䡢Ũ��Probucol��10 ��mol/L H2O2��SMCs��ֳ���õ�Ӱ��
Tab 2 Effects of Probucol on SMCs proliferfation evoked by H2O2
(n=6��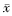 ��s)
��s)
, ��Ĵҽҩ
Group
Cell number(��104 )
Incorporation of 3 H-TdR (A/Bq)
48 h
72 h
96 h
48 h
72 h
96 h
A
6.15��1.30
, ��Ĵҽҩ
8.18��1.15
6.05��0.45
25.43��6.67
52.13��8.45
24.27��7.08
B
6.35��0.80
7.95��0.65
5.85��1.01
27.00��9.18
49.83��11.45
22.97��9.67
, ��Ĵҽҩ
C
6.85��1.20
6.85��1.35*��
5.05��1.00*��
28.27��10.40
48.32��5.83*��
21.43��6.06*��
D
5.96��0.65
5.60��1.70**����
, ��Ĵҽҩ
4.25��1.55**����
26.33��4.38
30.75��10.50 **����
16.67��4.40**����
E
6.05��1.15
4.25��0.75**��������
3.15��0.45**��������
25.68��6.50
18.67��4.85**��������
, http://www.100md.com
12.33��3.26**��������
F
5.75��0.68
5.86��0.56
4.25��0.62
16.33��4.80
9.67��3.77
8.67��4.18
A��10 ��mol/L H2O2��B��10 ��mol/L H2O2 +0.1 ��mol/L Probucol��C��10 ��mol/L H2O2 +1 ��mol/L Probucol��D��10 ��mol/L H2O2 +10 ��mol/L Probucol�� E��10 ��mol/L H2O2 +100 ��mol/L Probucol �� F��0.1%DMSO +2% NCS�� *P<0.05,** P <0.01 vs group A; ��P<0.05,����P <0.01 vs group B; ����P <0.01 vs group D
, http://www.100md.com
3 �� ��
PTCA����RS��AS���䷢�����ƿ����Ƕ������ء�����;����ͬ���õĽ�����ֲ�Ѫ������������֢��Ӧ��Ѫ˨�γɣ������������ʴ̼�����AS��RS�γɵIJ�����������������������ʴ̼�����ֲ�Ѫ�������ѱ���Ϊ��һ���dz���Ҫ�����أ����ƻ�����Χ�����ķ��ӣ�ʹ֬�����������ԣ��γ���ĭϸ�������ɼ����ת¼���ӣ��������ϸ�����ӡ�ø��ճ�����ӷ��ڣ��̼����������ź��絰��øC(PKC)����ٽ�ԭ������c-fos��c-myc����Ӷ��ٽ���SMCs��ֳ��Ǩ�ƺ�ϸ�����������[9]��PTCA������ϸ����Ѫ����Ĥ�ֲ��ۼ��ͷŴ������������Ӻ����������������⣬��ϸ��Ҳ��Ѫ����Χ��Ĥ��ۼ��������Ժ�Ѫ�ֲܾ����γɡ�Ѫ����������Ѫ���ع��������[2]��
Probucol��һ����֬�Կ������������е���Ѫ֬����AS���ã����P�ٴ�ʵ����ʾ����PTCA����RS��������������[3]�����о�֤ʵProbucol��NCS��H2O2��SMCs��ֳ�����������ã��ҳ�Ũ�������ԡ�����NCS�������������Ӻ�ϸ����ֳ���ʣ�������ͨ·�����ƽϸ��ӡ�����ʵ��֤ʵProbucol����ֹѪС��Դ��������(PDGF)������1(IL-1)���ڣ�����Ѫ��ϸ��ճ������1(VCAM-1)������ϸ������̼�����(M-CSF)��������µ�[10]��Probucol��Ϊ�������������ڿ�����������Դ�������������ʶ�ϸ���Ķ������ã���������ijЩϸ�����ӵķ��ڣ�������VSMCs������ֳ����Щ�����Ǵ�ҩ�������ڿ�����Ч����AS��RS�Ļ����㡣�������Ƕ����������������������õ�������ʶ�����о������ʾ��Probucol������Ѫ�����˺���Ĥ����������Ӳ���γɾ��л������ã��临�ӵ����û��������һ���о���
, ��Ĵҽҩ
�����
[1]������.Ѫ�ܳ�������ƽ����ϸ����ֳ�Ļ���[J].����ҽѧ.��Ѫ�ܼ����ֲ�,1997,24(6):10-12.
[2]Cane A,Breton M,Koumanov K,et al.Oxidant-induced arachidonic acid release and impairment of fatty acid acylation in vascular smooth muscle cells[J].Am J Physiol,1998,274(4 Pt 1):C1040-1046.
[3]Ruef JR,Hu ZY,Yin LY,et al.Induction of vascular endothelial growth factor in ballon-injured baboon arteries.A novel role for reactive oxygen species in atherosclerosis[J].Circ Res,1997,81(1):24-33.
, ��Ĵҽҩ
[4]Yokoi H,Daida H,Kuwabara Y,et al.Effectiveness of an antioxidant in preventing restenosis after percutaneous transluminal coronary angioplasty[J].J Am Coll Cardiol,1997,30(4):855-862.
[5]Akeson AL,Woods CW,Mosher LB,et al.Inhibition of IL-1�� expression in THP-1 cells by Probucol and tocopherol[J].Atherosclerosis,1991,86(2-3):261-270.
[6]Hirata Y,Tarugi Y,Takata S.CGRP receptor in cultured vascular smooth muscle and endothelial cells[J].Biochem Biophys Res Commun,1988,151(3):1113-1121.
, http://www.100md.com
[7]Sun Q.Growth stimulation of 3T3 fibroblasts by cystatin[J].Exp Cell Res,1989,180(1):150-160.
[8]Herbert JM,Bono F,Savi P.The mitogenic effect of H2O2 for vascular smooth muscle cells is mediated by an increase of the affinity of basic fibroblast growth factor for its receptor[J].FEBS Letters,1996,395(1):43-47.
[9]Rao GN,Berk BC.Active oxygen species stimulate vascular smooth muscle cell growth and proto-oncogene expression[J].Circ Res,1992,70(3):593-599.
[10]Fruebis J,Gonzalez V,Silvestre M,et al.Effect of Probucol treatment on gene expression of VCAM-1,MCP-1 and M-CSF in the aotic wall of LDLreceptor-deficient rabbits during early atherogenesis[J].Arterioscler Thromb Vasc Biol,1997,17(7):1281-1302., ��Ĵҽҩ
�˽��� ���ڹ� ���� ������
ժ Ҫ Ŀ��:̽��������(Probucol) ��H2O2�յ���ƽ����ϸ��(SMCs) ��ֳ���������á�����:����ϸ����������3H-TdR���뷨�۲�0.1��100 ��mol/L Probucol������ţѪ��(NCS)��������(H2O2)��SMCs��ֳ���������á����:10 ��mol/L��100 ��mol/L Probucol����96 h��������10%NCS�̼���SMCs��ֳ����1,10 ��100 ��mol/L Probucol����72 h��96 h������������10 ��mol/L H2O2�̼���SMCs��ֳ���ҳ�Ũ��������(P<0.05,P<0.01)������:Probucol����NCS��H2O2�̼�������������SMCs��ֳ����ʾ����ڶ�������Ӳ���;�Ƥǻ�ڹ�״����������������խ�ķ��ο��ܾ���Ӧ��ǰ����
, ��Ĵҽҩ
�ؼ��ʣ���������ƽ����ϸ������ֳ
����Ѫ��ƽ����ϸ��(SMCs)��ֳ������������Ӳ��(AS)�;�Ƥǻ�ڹ�״����������(PTCA)������խ(RS)�������Ҫ����֮һ[1]��Ѱ����Ч����SMCs��ֳ��ҩ����AS��RS�����о��е�һ����Ҫ���⡣�����������ʴ̼���AS��RS�γɵ���Ҫ����֮һ��Ѫ����Ƥϸ����л�Լ�һϵ����ƤԴ�������ͷŵ��������̽�������Ũ�ȵ������������ʡ����ֲ�Ѫ�����˺�������������Ũ��Ҳ��������[2]����������(H2O2)����Ϊ�����������ʴ�����ʵ�鷢��H2O2�յ��˺���Ѫ��ƽ����ϸ��(VSMCs)��Ѫ����Ƥ��������(VEGF)mRNA�ʼ��������Ա������ߡ�����AS��������������ģ���У��ɼ�����ֲ���������Ĥ��VEGF�ȶ������������4������[3]����������������(Probucol)��һ����Ч�����͵ĵ���Ѫ֬�Ϳ�ASҩ������������о����ִ�ҩ���ܿ�������PTCA����RS���˽��ۻ����һ��ʵ��֤ʵ���䷢������Ҳ�д���һ���о�[4]�����о�ּ��̽��Probucol��SMCs��ֳ��Ӱ�죬���ڽ�ʾProbucol��AS��RS�����е�ijЩ���û��ƣ���֧�����ٴ�Ӧ�á�
, ��Ĵҽҩ
1 ���Ϻͷ���
1.1 ��Ҫʵ����Ʒ RPMI 1640����Һ������ţѪ��(NCS)��Gibco��˾��Ʒ�� Probucol��Ʒ����Է�������:516.16,�е�������ҩ������ʱ���ڶ�������(DMSO���¹�Merck��˾��Ʒ)��DMSO��Ũ�ȵ���0.1%[5]��H2O2�����������Ϻ����ֻ�������Ʒ������������30%���ȵ���ø��Difco���ڷ�װ��3H-���������������(3H-TdR)���Ϻ�ԭ�����о���������Ȼ�ȣ�1.11��1 014 Bq/mmol���ܻ�ȣ�3.7��109 Bq��SMC���壺�ÿ���ƽ������������(SMA)������Dako��˾��Ʒ��
1.2 ����SMCs����[6]��������200��250 g SD����(�ڶ���ҽ��ѧʵ�鶯�������ṩ)������������������ȡ�������ضΣ���Hirata��֯���鷨���в�ƽ������֯����ֲ������ƿ�ڣ�����RPMI 1640����Һ(��15% NCS��1%����ù��)����37�棬5% CO2������������Լ2��5 h�����ᷭת����ƿ��ʹ��֯���������Һ�У�����������ϸ������֯���Ե������3 d����������Һһ�Σ����������ܵ�ϸ���㣬��0.25%�ȵ���ø����ϸ��������������SMCs�ļ�����������������۲�ɼ�SMCs�����Σ�ƽ����������״���У��ܼ���ϡ�账������ʡ���ȡ�״������SMA���������黯Ⱦɫ���ɼ�Ⱦ���ػ�ɫ������ϸ����֤ʵΪSMCs������Ϊ95%���ϡ�ʵ�����3��8��ϸ����ϸ��ͬ��������������3��8������״̬���õ�SMCs��������뺬10% NCS��RPMI 1640����Һ�Ƴɵ�ϸ����Һ����5��104 ��/ml��100 ��l/������96 �װ��У�����24 h�ɺ�0.5% NCS�� RPMI 1640�������壬����56 h��ʹ90%ϸ����ֹ��G0/G1�ڣ����á�
, ��Ĵҽҩ
1.3 3H-TdR���뷨[7]�ⶨSMCs��ֳ ����ϸ������ֹ����ǰ18��24 h����3H-TdR 3.7��106 Bq/�ף�������Ӧ�Ĺ۲�ʱ������ֹ�����������壬0.25%��ø����������ö�ͷϸ���ռ����ռ���Ʒ�ڲ�����ά��ֽ�ϣ���ɡ����ռ��˲�ͬ��Ʒ����ֽ�ֱ����Һ��ƿ��������˸Һ���ڦ�Һ�����в�ÿ�����������ֵ(cpm)���������Bqֵ��
1.4 ϸ���������۲�SMCs����ֳ��� ����ϸ��������Ӧ�Ĺ۲�ʱ������ֹ��������0.25%��ø�����������200 ��l/�����������У���0.01 mol/L PBS����ɾ��ȵ�ϸ����Һ������ϸ�������������
1.5 Probucol��NCS��SMCs��ֳ���õ�Ӱ��۲� ʵ���Ϊ(1) �����飺10%NCS��(2)��ҩ�飺10%NCS+ Probucol��Probucol��Ũ�ȷֱ�Ϊ0.1��1��10��100 ��mol/L��(3)��ý�飺0.1% DMSO+10% NCS������ϸ����������3H-TdR���뷨�ⶨϸ����ֳ�����
, ��Ĵҽҩ
1.6 Probucol��H2O2��SMCs��ֳ���õ�Ӱ��۲� �������ױ������ʵ�Ũ�ȵ�H2O2�����Դٽ�SMCs��ֳ[8]��������Ԥʵ���з���10 ��mol/L H2O2��SMCs����ֳ�������������ʱ�ʵ��ѡ��10 ��mol/L H2O2��Ϊ�̼�SMCs��Ч��ֳ��Ũ�ȡ�ʵ���Ϊ(1)�����飺 10 ��mol/L H2O2��(2)��ҩ�飺10 ��mol/L H2O2 + Probucol��Probucol��Ũ�ȷֱ�Ϊ0.1��1��10��100 ��mol/L��(3)��ý�飺 0.1% DMSO+2% NCS������ϸ����������3H-TdR���뷨�ⶨϸ����ֳ�����
1.7 ͳ��ѧ���� ������
, http://www.100md.com
2 �� ��
2.1 Probucol��NCS�ٴ���������SMCs��ֳ���õ�Ӱ�� ��ͬŨ��(0.1��1��10��100 ��mol/L)Probucol�����������Ĵ���������SMCs 48��72 h��ϸ��������3H-TdR����ֵ�������ȽϾ��������Բ���(P>0.05)��˵����ʱProbucol��10% NCS�����SMCs��ֳ�������������á�����ͬŨ��Probucol����96 h�� 10��100 ��mol/L Probucol��ϸ����ֳ���ܵ��������ƣ��ҳ�Ũ��������ϵ(P<0.05��P<0.01)����ϸ������ֵ����ó���ϸ�����������ʷֱ�Ϊ(17.8��2.5)%��(22.2��1.9)%�� ��3H-TdR����ֵ����ó��������ʷֱ�Ϊ(20.6��3.2)%�� (36.0��2.4)%����1��ʾ�˲��ֽ����
2.2 Probucol��10 ��mol/L H2O2�ٴ���������SMCs��ֳ���õ�Ӱ�� ��ͬŨ��(0.1��1��10��100 ��mol/L)Probucol������SMCs 48 h��ϸ��������3H-TdR����ֵ�������ȽϾ��������Բ���(P>0.05)��˵����ʱProbucol��10 ��mol/L H2O2�����SMCs��ֳ�������������á���������ʱ���ӳ���72 ��96 hʱ��1��10��100 ��mol/L Probucol���������Ƚ�ϸ��������3H-TdR����ֵ�����Խ���(P<0.05,P<0.01)����Ũ��������(��2)����������72 h������3��Ũ������ϸ������ֵ����ó��������ʷֱ�Ϊ (16.3��0.8)%,(31.5��1.4)%,(48.0��3.3)%������3H-TdR �������ó��������ʷֱ�Ϊ(21.4��2.6)%,(39.2��3.2)%,(67.4��4.6)%;����96 h����ϸ�������ó��������ʷֱ�Ϊ(16.5��1.8)%,(29.8��2.7)%,(47.9��3.0)%������3H-TdR�������ó��������ʷֱ�Ϊ(24.6��2.1)%,(32.8��2.9)%,(50.6��3.7)% ��
, ��Ĵҽҩ
�� 1 ��ͬʱ�䡢Ũ��Probucol��10%NCS��SMCs��ֳ���õ�Ӱ��
Tab 1 Effects of Probucol on SMCs proliferfation stimulated by NCS
(n=6��
Group
Cell number (��104 )
Incorporation of3H-TdR (A/Bq)
, ��Ĵҽҩ
72 h
96 h
72h
96 h
Control(10%NCS)
8.25��1.34
11.25��2.14
48.87��12.67
64.70��14.38
Probucol (cB/��mol.L-1)
0.1
, ��Ĵҽҩ
8.00��0.96
10.25��1.77
50.17��16.50
66.33��13.50
1
8.18��0.46
10.95��1.15
50.07��11.45
58.75��10.83
10
7.88��1.58
9.05��1.86*��
, http://www.100md.com
47.50��9.77
51.40��13.08*��
100
8.16��1.51
7.35��1.39**��������
46.50��17.18
41.43��11.40**��������
0.1%DMSO
9.05��1.48
11.75��0.98
49.25��14.17
, http://www.100md.com
61.48��16.50
*P<0.05,**P <0.01 vs control group; ��P<0.05�� ����P <0.01 vs 1 ��mol/L Probucol group; ����P<0.01 vs 10 ��mol/L Probucol group�� 2 ��ͬʱ�䡢Ũ��Probucol��10 ��mol/L H2O2��SMCs��ֳ���õ�Ӱ��
Tab 2 Effects of Probucol on SMCs proliferfation evoked by H2O2
(n=6��
, ��Ĵҽҩ
Group
Cell number(��104 )
Incorporation of 3 H-TdR (A/Bq)
48 h
72 h
96 h
48 h
72 h
96 h
A
6.15��1.30
, ��Ĵҽҩ
8.18��1.15
6.05��0.45
25.43��6.67
52.13��8.45
24.27��7.08
B
6.35��0.80
7.95��0.65
5.85��1.01
27.00��9.18
49.83��11.45
22.97��9.67
, ��Ĵҽҩ
C
6.85��1.20
6.85��1.35*��
5.05��1.00*��
28.27��10.40
48.32��5.83*��
21.43��6.06*��
D
5.96��0.65
5.60��1.70**����
, ��Ĵҽҩ
4.25��1.55**����
26.33��4.38
30.75��10.50 **����
16.67��4.40**����
E
6.05��1.15
4.25��0.75**��������
3.15��0.45**��������
25.68��6.50
18.67��4.85**��������
, http://www.100md.com
12.33��3.26**��������
F
5.75��0.68
5.86��0.56
4.25��0.62
16.33��4.80
9.67��3.77
8.67��4.18
A��10 ��mol/L H2O2��B��10 ��mol/L H2O2 +0.1 ��mol/L Probucol��C��10 ��mol/L H2O2 +1 ��mol/L Probucol��D��10 ��mol/L H2O2 +10 ��mol/L Probucol�� E��10 ��mol/L H2O2 +100 ��mol/L Probucol �� F��0.1%DMSO +2% NCS�� *P<0.05,** P <0.01 vs group A; ��P<0.05,����P <0.01 vs group B; ����P <0.01 vs group D
, http://www.100md.com
3 �� ��
PTCA����RS��AS���䷢�����ƿ����Ƕ������ء�����;����ͬ���õĽ�����ֲ�Ѫ������������֢��Ӧ��Ѫ˨�γɣ������������ʴ̼�����AS��RS�γɵIJ�����������������������ʴ̼�����ֲ�Ѫ�������ѱ���Ϊ��һ���dz���Ҫ�����أ����ƻ�����Χ�����ķ��ӣ�ʹ֬�����������ԣ��γ���ĭϸ�������ɼ����ת¼���ӣ��������ϸ�����ӡ�ø��ճ�����ӷ��ڣ��̼����������ź��絰��øC(PKC)����ٽ�ԭ������c-fos��c-myc����Ӷ��ٽ���SMCs��ֳ��Ǩ�ƺ�ϸ�����������[9]��PTCA������ϸ����Ѫ����Ĥ�ֲ��ۼ��ͷŴ������������Ӻ����������������⣬��ϸ��Ҳ��Ѫ����Χ��Ĥ��ۼ��������Ժ�Ѫ�ֲܾ����γɡ�Ѫ����������Ѫ���ع��������[2]��
Probucol��һ����֬�Կ������������е���Ѫ֬����AS���ã����P�ٴ�ʵ����ʾ����PTCA����RS��������������[3]�����о�֤ʵProbucol��NCS��H2O2��SMCs��ֳ�����������ã��ҳ�Ũ�������ԡ�����NCS�������������Ӻ�ϸ����ֳ���ʣ�������ͨ·�����ƽϸ��ӡ�����ʵ��֤ʵProbucol����ֹѪС��Դ��������(PDGF)������1(IL-1)���ڣ�����Ѫ��ϸ��ճ������1(VCAM-1)������ϸ������̼�����(M-CSF)��������µ�[10]��Probucol��Ϊ�������������ڿ�����������Դ�������������ʶ�ϸ���Ķ������ã���������ijЩϸ�����ӵķ��ڣ�������VSMCs������ֳ����Щ�����Ǵ�ҩ�������ڿ�����Ч����AS��RS�Ļ����㡣�������Ƕ����������������������õ�������ʶ�����о������ʾ��Probucol������Ѫ�����˺���Ĥ����������Ӳ���γɾ��л������ã��临�ӵ����û��������һ���о���
, ��Ĵҽҩ
�����
[1]������.Ѫ�ܳ�������ƽ����ϸ����ֳ�Ļ���[J].����ҽѧ.��Ѫ�ܼ����ֲ�,1997,24(6):10-12.
[2]Cane A,Breton M,Koumanov K,et al.Oxidant-induced arachidonic acid release and impairment of fatty acid acylation in vascular smooth muscle cells[J].Am J Physiol,1998,274(4 Pt 1):C1040-1046.
[3]Ruef JR,Hu ZY,Yin LY,et al.Induction of vascular endothelial growth factor in ballon-injured baboon arteries.A novel role for reactive oxygen species in atherosclerosis[J].Circ Res,1997,81(1):24-33.
, ��Ĵҽҩ
[4]Yokoi H,Daida H,Kuwabara Y,et al.Effectiveness of an antioxidant in preventing restenosis after percutaneous transluminal coronary angioplasty[J].J Am Coll Cardiol,1997,30(4):855-862.
[5]Akeson AL,Woods CW,Mosher LB,et al.Inhibition of IL-1�� expression in THP-1 cells by Probucol and tocopherol[J].Atherosclerosis,1991,86(2-3):261-270.
[6]Hirata Y,Tarugi Y,Takata S.CGRP receptor in cultured vascular smooth muscle and endothelial cells[J].Biochem Biophys Res Commun,1988,151(3):1113-1121.
, http://www.100md.com
[7]Sun Q.Growth stimulation of 3T3 fibroblasts by cystatin[J].Exp Cell Res,1989,180(1):150-160.
[8]Herbert JM,Bono F,Savi P.The mitogenic effect of H2O2 for vascular smooth muscle cells is mediated by an increase of the affinity of basic fibroblast growth factor for its receptor[J].FEBS Letters,1996,395(1):43-47.
[9]Rao GN,Berk BC.Active oxygen species stimulate vascular smooth muscle cell growth and proto-oncogene expression[J].Circ Res,1992,70(3):593-599.
[10]Fruebis J,Gonzalez V,Silvestre M,et al.Effect of Probucol treatment on gene expression of VCAM-1,MCP-1 and M-CSF in the aotic wall of LDLreceptor-deficient rabbits during early atherogenesis[J].Arterioscler Thromb Vasc Biol,1997,17(7):1281-1302., ��Ĵҽҩ