ICAM-1蛋白和mRNA在慢性乙型肝炎肝组织中的表达
ICAM-1蛋白和mRNA在慢性乙型肝炎肝组织中的表达
张绪清 顾长海
摘 要 目的:探讨肝组织细胞间粘附分子-1(ICAM-1)表达在慢性乙型肝炎(CHB)发病机制中的作用。方法:用原位杂交和免疫组织化学技术检测11例正常人和50例慢性HBV感染者肝内ICAM-1 mRNA和蛋白表达情况。结果:正常人和慢性无症状HBsAg携带者肝细胞无ICAM-1 mRNA和ICAM-1表达,CHB患者肝细胞ICAM-1 mRNA和ICAM-1表达增强,阳性肝细胞多分布在汇管区周围和腺泡内炎症坏死区域;重度CHB患者肝细胞ICAM-1 mRNA和ICAM-1表达显著强于中、轻度CHB患者(P< 0.05);肝细胞ICAM-1表达强度与肝组织炎症活动度呈显著正相关(P< 0.01);肝细胞ICAM-1表达强的患者肝功能显著差于ICAM-1表达弱者(P< 0.05)。结论:肝细胞ICAM-1表达在慢性乙型肝炎肝细胞坏死中起重要作用,肝细胞ICAM-1表达水平能较好反映其肝损害程度和肝功能状况。
, http://www.100md.com
关键词:乙型病毒性肝炎;细胞间粘附分子-1
细胞粘附分子-1(Intercellular adhesion molecule-1,ICAM-1)属免疫球蛋白超家族成员, 其配体是淋巴细胞功能相关抗原-1(Lymphocyte function associated antigen-1, LFA-1)[1]。ICAM-1/LFA-1相互作用能介导淋巴细胞与血管内皮细胞粘附,促进淋巴细胞向组织中浸润[1,2]。本研究拟在探讨肝组织ICAM-1表达在慢性乙型肝炎免疫发病机制中的作用。
1 材料与方法
1.1 对象
50例慢性HBV感染者,男42例,女8例,平均年龄33.4岁,其中慢性无症状HBsAg携带者(AsC)5例,慢性肝炎45例。正常人11例均为意外事故死亡者,HBsAg、抗HCV、HBVDNA、HCVRNA均阴性。
, http://www.100md.com
1.2 试剂
鼠抗人ICAM-1单克隆抗体为丹麦Dako公司产品,SP法试剂盒和DAB显色试剂盒均为福州迈新公司产品;反义寡核苷酸(AS)由上海生化所合成,其序列为5′GGGACCCATAGCGAGGCTGAGGTTGCAA3′,与ICAM-1 mRNA 5′末端翻译起始位点序列(nt63-81)互补;寡核苷酸3′末端地高辛(DIG)标记试剂盒和碱性磷酸酶标记的抗地高辛抗体(抗-DIG-AP)由德国宝灵曼公司提供。
1.3 方法
1.3.1 肝组织标本保存及切片制备 每例肝组织分成两部分,一部分用10%甲醛溶液固定送病理制成石蜡切片作常规病理检查;另一部分用PLP溶液固定、8.5%蔗糖/PBS溶液漂洗后置液氮中保存,并制成5 μm厚的冰冻切片。
1.3.2 制备DIG标记的寡核苷酸探针 按试剂盒提供的方法对AS进行3′末端标记。
, http://www.100md.com
1.3.3 肝内抗原表达 用免疫组化SP法对肝组织冰冻切片进行染色,DAB显色,苏木素复染、封片。对照设置:1实验阳性片为阳性对照;2不加抗体为阴性对照。在排除非特异性着色的情况下,光镜见棕黄色颗粒为阳性。染色强度分级参照Chu等提出的标准。无肝细胞着色为-,<10%的肝细胞着色为+,10%~50%为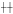 ,>50%为
,>50%为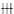 。
。
1.3.4 原位杂交检测肝组织ICAM-1 mRNA 用DIG标记的寡核苷酸探针按照《非放射性杂交技术》介绍的方法[3]对肝组织冰冻切片进行原位杂交,并用抗DIG-AP和NBT/BCIP进行染色和显色。光镜下见紫色颗粒为阳性,肝细胞ICAM-1 mRNA表达强度分级与ICAM-1表达强度分级相同,对照设置:不加探针为阴性对照。
, http://www.100md.com
1.3.5 血清总胆红素(TB)、丙氨酸转氨酶(ALT)、门冬氨酸转氨酶(AST)和凝血酶原时间由检验科检测,根据凝血酶原时间推算凝血酶原活动度(PTa)。血清HBVDNA用PCR法检测,血清HBsAg、抗HBs、HBeAg、抗HBe、抗HBc用ELISA法检测。
1.3.6 统计学处理 用秩和检验,等级相关分析和t检验。
2 结果
2.1 肝组织ICAM-1 mRNA和ICAM-1表达
正常人和慢性无症状HBsAg携带者肝组织内,肝窦内皮、Kupffer细胞和血管内皮细胞有少量ICAM-1 mRNA和ICAM-1表达,肝细胞无ICAM-1 mRNA和ICAM-1表达。慢性乙型肝炎患者肝细胞出现不同程度ICAM-1 mRNA和ICAM-1表达,且肝窦内皮、血管内皮细胞ICAM-1 mRNA和ICAM-1表达增强。肝细胞ICAM-1 mRNA表达多呈胞浆型,少数伴有核着色,见图1。在中、重度慢性肝炎,阳性肝细胞多呈局灶性分布; 在轻度慢性肝炎,阳性肝细胞多呈散在分布。肝细胞ICAM-1表达多呈膜型,有的伴有胞浆着色,未见核型,见图2。在中、重度慢性乙型肝炎,ICAM-1阳性肝细胞多呈局灶性分布、呈蜂窝状,阳性肝细胞多分布在汇管区周围和腺泡炎症坏死区域。在轻微炎细胞浸润部位,ICAM-1表达局限在肝窦内皮和肝细胞肝窦侧,但在有严重炎细胞浸润的碎片状坏死和灶性死区域,ICAM-1表达分布在整个肝细胞表面。重度慢性肝炎患者肝组织ICAM-1 mRNA和ICAM-1表达明显强于中度慢性肝炎(P< 0.05),中度慢性肝炎患者肝组织ICAM-1 mRNA和ICAM-1表达也明显强于轻度慢性肝炎(P< 0.05),见表1。肝细胞ICAM-1 mRNA表达水平与ICAM-1表达水平的一致性较好,两者间相关非常显著(P< 0.01)。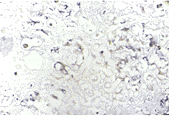
, 百拇医药
图1 重度慢性乙型肝炎肝细胞ICAM-1 mRNA表达
原位杂交, 肝细胞、肝窦内皮和血管内皮细胞大
量表达ICAM-1 mRNA (NBT/BCIP×100)
Fig 1 ICAM-1 mRNA expression in liver tissue with
severe chronic hepatitis B with in situ hybridiza
tion. Stronger expression of ICAM-1 mRNA in
hepatocytes, hepatic sinusoidal lining cells and
, 百拇医药
vessel endothelial cells (NBT/BCIP×100)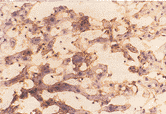
图2 中度慢性乙型肝炎肝组织ICAM-1表达,碎片状
坏死区,许多肝细胞增强表达ICAM-1,部分呈蜂
窝状, 阳性表达分布在整个肝细胞表面,伴许多
炎细胞浸润 (S-P×200)
Fig 2 ICAM-1 expression in liver tissue with moderate
chronic hepatitis B. In the area of piecemeal
, 百拇医药
necrosis, enhanced ICAM-1 expression in many
hepatocytes, partly with a local honey comb pat
tern, infiltrated by numerous inflammatory cells(S-P×200)
表1 乙型肝炎患者肝细胞ICAM-1和ICAM-1 mRNA表达
Tab1 ICAM-1 and ICAM-1 mRNA expression on hepatocytes of patients with viral hepatitis B
n
ICAM-1
, 百拇医药
ICAM-1 mRNA
HBeAg(+)
HBVDNA(+)
-
+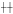
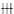
-
+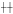
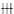
, 百拇医药
Healthy
11
11
0
0
0
11
0
0
0
0
0
AsC
5
, 百拇医药
5
0
0
0
5
0
0
0
4(80%)
5(100%)
CHB(Mi)
15
0
9
, http://www.100md.com
6
0
0
9
6
0
9(60%)
10(67%)
CHB(Mo)
15
0
1
9
5
, 百拇医药
0
0
9
6
4(27%)
5(33%)
CHB(S)
15
0
2
2
11
0
0
, http://www.100md.com
2
13
3(20%)
4(27%)
2.2 肝细胞ICAM-1表达与肝组织炎症,见表2表2 肝细胞ICAM-1 表达与炎症活动度
Tab2 The levels of ICAM-1 expression in hepatocytes
and inflammatory activities in liver
Grade of liver
inflammation(G)
, http://www.100md.com n
ICAM-1
-
+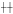
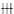
0
16
16
0
0
, http://www.100md.com
0
1
10
0
8
2
0
2
5
0
1
4
0
3
, http://www.100md.com
15
0
0
11
4
4
15
0
0
0
15
慢性乙型肝炎患者肝组织炎症越明显,其肝细胞膜ICAM-1表达则越强,两者之间呈显著正相关,P<0.01。
2.3 肝细胞ICAM-1表达与肝功能,见表3表3 肚细胞ICAM-1表达与肝功能
, 百拇医药
Tab3 The levels of ICAM-1 expression in hepatocytes
and the liver functions
ICAM-1
n
ALT(IU/L)
AST(IU/L)
TB(μmol/L)
(%)
PTa
+
9
, 百拇医药
43±17
54±29
14.9±4.0
90.6±9.5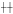
17
139±105*
137±123*
29.8±10.6#
85.2±11.1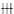
, http://www.100md.com
19
194±82*
226±76*
114.0±35.5*
56.4±10.2
*:P<0.01 vs ICAM-1(+) group;
#:P<0.05 vs ICAM-1(+) and (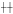 ) groups
) groups
肝细胞ICAM-1表达强的患者血清ALT、AST、TB水平显著高于ICAM-1表达弱者;ICAM-1表达强的患者凝血酶原活动度显著低于ICAM-1表达弱者。
, 百拇医药
2.4 肝细胞ICAM-1表达与HBV复制标志
HBV感染者肝细胞ICAM-1表达水平越高,其血清HBeAg、HBVDNA阳性率则越低,两者间呈显著负相关,见表4。
表4 HBV感染者肝细胞ICAM-1表达与HBV复制标志
Tab4 The levels of ICAM-1 expression in hepatocytes
and HBV replication markers
ICAM-1
n
HBeAg(+)
HBVDNA(+)
, http://www.100md.com
-
5
4(80%)
5(100%)
+
9
8(89%)
8(89%)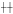
17
5(29%)
7(41%)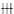
, 百拇医药
19
3(16%)
44(21%)
Total
50
20(40%)
24(48%)
3 讨论
正常人肝细胞不表达ICAM-1,但存在ICAM-1基因。本结果显示HBV感染者肝内ICAM-1表达水平与ICAM-1 mRNA表达水平的一致性较好,提示HBV感染是通过促进肝细胞ICAM-1基因转录而诱导ICAM-1的表达增强。HBV能直接或通过IL-1、IFNγ、TNF-α等细胞因子间接诱导肝细胞增强表达ICAM-1[3,4]。
, 百拇医药
Del Pozo等[5]报告在淋巴细胞-内皮细胞相互作用中趋化因子诱导T细胞极化、形成胞浆突起;ICAM-1/LFA-1在胞浆突起介导的淋巴细胞募集过程中起重要作用,并促进T细胞的跨内皮迁移运动。慢性乙型肝炎肝血管内皮和肝窦内皮ICAM-1 mRNA和ICAM-1增强表达有利于淋巴细胞通过上述类似机制向肝组织中浸润,为CTL攻击靶细胞创造必要的条件。本研究发现,肝组织无炎症损伤者肝细胞缺乏ICAM-1 mRNA和ICAM-1表达,而慢性乙型肝炎患者肝细胞出现不同程度ICAM-1 mRNA和ICAM-1表达,而且其表达程度随着组织炎症损害的加重而增强,提示肝组织炎症存在和严重程度与肝细胞表达ICAM-1及水平有关。
在轻微炎细胞浸润部位,ICAM-1表达局限在肝窦内皮和肝细胞肝窦侧,但在有严重炎细胞浸润的碎片状坏死和灶性坏死区域,ICAM-1表达分布在整个肝细胞表面。说明肝细胞坏死与肝细胞膜ICAM-1表达有关,ICAM-1在慢性乙型肝炎肝细胞坏死中起重要作用,CTL细胞借助ICAM-1/LFA-1与肝细胞粘附、发挥细胞毒作用,导致肝细胞坏死[6]。血清HBeAg、HBVDNA是反映HBV感染者体内病毒复制活跃的重要指标。HBV感染者肝细胞ICAM-1表达越强,其血清HBeAg、HBVDNA阳性率则越低,提示肝细胞ICAM-1增强表达有利于机体清除病毒,说明肝细胞缺乏或低水平表达ICAM-1可能是慢性HBV感染持续存在的重要原因。
, http://www.100md.com
CHB患者肝损害越重,其肝细胞ICAM-1表达越强;肝细胞ICAM-1表达越强的患者肝功能也越差。说明肝细胞ICAM-1表达水平能较好反映CHB患者肝损害程度和肝功能状况。
Essani等[7]报道抗ICAM-1和抗LFA-1的单克隆抗体能阻断内毒素血症所致鼠急性炎症性肝损伤。Stepkowski等[8]报道针对鼠ICAM-1 mRNA的反义核酸阻断心脏移植排斥反应的发生。我们推测用针对人ICAM-1 mRNA的反义核酸抑制肝细胞ICAM-1表达,或者用抗ICAM-1和抗LFA-1的单克隆抗体对预防乙型肝炎肝组织炎症坏死应有一定的帮助。
作者简介:张绪清(1965.10), 男, 湖北省鄂州市人, 博士,主治医师, 讲师,主要从事乙型肝炎发病机制方面的研究,发表论文20余篇。
张绪清(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
, http://www.100md.com
顾长海(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
参考文献
[1] Wawryk S O, Novotny J R, Wick I P, et al. The role of the FA1/interaction in human leukocyte homing and adhesion[J]. Immunol Rev,1989,108(1):135-161.
[2] 张绪清,顾长海.细胞间粘附分子1与肝病[J].中华肝脏 病杂志,1997,5(2):110-112.
[3] Sano K, Nagaki M, Sugiyama A, et al. Effects of cytokines on the binding of leukocytes to cultured rat hepatocytes and on the expression of ICAM-1 by hepatocytes[J]. Dig Dis Sci,1999,44 (4):796-805.
, 百拇医药
[4] Hu K Q, Yu C H, Vierling J M. Upregulation of intercellular adhesion molecule 1 transcription by hepatitis B virus X protein [J]. Proc Natl Acad Sci, USA, 1992, 89(23): 11 441- 11 445.
[5] Del Pozo M A, Cabanas C, Montoya M C, et al. ICAMs redistributed by chemokines to cellular uropods as a mechanism for recruitment of T lymphocytes[J]. J Cell Bio, 1997, 137(2):493-508.
[6] Stewart M P, Cabanas C, Hogg N, et al. T cell adhesion to intercellular adhesion molecule1 is controlled by cell spreading and the activation of integrin LFA1[J]. J Immunology,1996,156(13):1 810-1 817.
, 百拇医药
[7] Essani N A, Fisher M A, Farhood A, et al. Cytokineinduced upregulation of hepatic intercellular adhesion molecule1 messenger RNA expression and its role in the pathophysiology of murine endotoxin shock and acute liver failure[J]. Hepatology,1995,21(5):1 632-1 639.
[8] Stepkowski S M, Tu Y, Condon T P, et al. Induction of transplantation tolerance by treatement with oligonucleodtides and antiLFA-1 monoclonal antibodies[J]. Transplantation Proceedings,1995,27(1):113., http://www.100md.com
张绪清 顾长海
摘 要 目的:探讨肝组织细胞间粘附分子-1(ICAM-1)表达在慢性乙型肝炎(CHB)发病机制中的作用。方法:用原位杂交和免疫组织化学技术检测11例正常人和50例慢性HBV感染者肝内ICAM-1 mRNA和蛋白表达情况。结果:正常人和慢性无症状HBsAg携带者肝细胞无ICAM-1 mRNA和ICAM-1表达,CHB患者肝细胞ICAM-1 mRNA和ICAM-1表达增强,阳性肝细胞多分布在汇管区周围和腺泡内炎症坏死区域;重度CHB患者肝细胞ICAM-1 mRNA和ICAM-1表达显著强于中、轻度CHB患者(P< 0.05);肝细胞ICAM-1表达强度与肝组织炎症活动度呈显著正相关(P< 0.01);肝细胞ICAM-1表达强的患者肝功能显著差于ICAM-1表达弱者(P< 0.05)。结论:肝细胞ICAM-1表达在慢性乙型肝炎肝细胞坏死中起重要作用,肝细胞ICAM-1表达水平能较好反映其肝损害程度和肝功能状况。
, http://www.100md.com
关键词:乙型病毒性肝炎;细胞间粘附分子-1
细胞粘附分子-1(Intercellular adhesion molecule-1,ICAM-1)属免疫球蛋白超家族成员, 其配体是淋巴细胞功能相关抗原-1(Lymphocyte function associated antigen-1, LFA-1)[1]。ICAM-1/LFA-1相互作用能介导淋巴细胞与血管内皮细胞粘附,促进淋巴细胞向组织中浸润[1,2]。本研究拟在探讨肝组织ICAM-1表达在慢性乙型肝炎免疫发病机制中的作用。
1 材料与方法
1.1 对象
50例慢性HBV感染者,男42例,女8例,平均年龄33.4岁,其中慢性无症状HBsAg携带者(AsC)5例,慢性肝炎45例。正常人11例均为意外事故死亡者,HBsAg、抗HCV、HBVDNA、HCVRNA均阴性。
, http://www.100md.com
1.2 试剂
鼠抗人ICAM-1单克隆抗体为丹麦Dako公司产品,SP法试剂盒和DAB显色试剂盒均为福州迈新公司产品;反义寡核苷酸(AS)由上海生化所合成,其序列为5′GGGACCCATAGCGAGGCTGAGGTTGCAA3′,与ICAM-1 mRNA 5′末端翻译起始位点序列(nt63-81)互补;寡核苷酸3′末端地高辛(DIG)标记试剂盒和碱性磷酸酶标记的抗地高辛抗体(抗-DIG-AP)由德国宝灵曼公司提供。
1.3 方法
1.3.1 肝组织标本保存及切片制备 每例肝组织分成两部分,一部分用10%甲醛溶液固定送病理制成石蜡切片作常规病理检查;另一部分用PLP溶液固定、8.5%蔗糖/PBS溶液漂洗后置液氮中保存,并制成5 μm厚的冰冻切片。
1.3.2 制备DIG标记的寡核苷酸探针 按试剂盒提供的方法对AS进行3′末端标记。
, http://www.100md.com
1.3.3 肝内抗原表达 用免疫组化SP法对肝组织冰冻切片进行染色,DAB显色,苏木素复染、封片。对照设置:1实验阳性片为阳性对照;2不加抗体为阴性对照。在排除非特异性着色的情况下,光镜见棕黄色颗粒为阳性。染色强度分级参照Chu等提出的标准。无肝细胞着色为-,<10%的肝细胞着色为+,10%~50%为
1.3.4 原位杂交检测肝组织ICAM-1 mRNA 用DIG标记的寡核苷酸探针按照《非放射性杂交技术》介绍的方法[3]对肝组织冰冻切片进行原位杂交,并用抗DIG-AP和NBT/BCIP进行染色和显色。光镜下见紫色颗粒为阳性,肝细胞ICAM-1 mRNA表达强度分级与ICAM-1表达强度分级相同,对照设置:不加探针为阴性对照。
, http://www.100md.com
1.3.5 血清总胆红素(TB)、丙氨酸转氨酶(ALT)、门冬氨酸转氨酶(AST)和凝血酶原时间由检验科检测,根据凝血酶原时间推算凝血酶原活动度(PTa)。血清HBVDNA用PCR法检测,血清HBsAg、抗HBs、HBeAg、抗HBe、抗HBc用ELISA法检测。
1.3.6 统计学处理 用秩和检验,等级相关分析和t检验。
2 结果
2.1 肝组织ICAM-1 mRNA和ICAM-1表达
正常人和慢性无症状HBsAg携带者肝组织内,肝窦内皮、Kupffer细胞和血管内皮细胞有少量ICAM-1 mRNA和ICAM-1表达,肝细胞无ICAM-1 mRNA和ICAM-1表达。慢性乙型肝炎患者肝细胞出现不同程度ICAM-1 mRNA和ICAM-1表达,且肝窦内皮、血管内皮细胞ICAM-1 mRNA和ICAM-1表达增强。肝细胞ICAM-1 mRNA表达多呈胞浆型,少数伴有核着色,见图1。在中、重度慢性肝炎,阳性肝细胞多呈局灶性分布; 在轻度慢性肝炎,阳性肝细胞多呈散在分布。肝细胞ICAM-1表达多呈膜型,有的伴有胞浆着色,未见核型,见图2。在中、重度慢性乙型肝炎,ICAM-1阳性肝细胞多呈局灶性分布、呈蜂窝状,阳性肝细胞多分布在汇管区周围和腺泡炎症坏死区域。在轻微炎细胞浸润部位,ICAM-1表达局限在肝窦内皮和肝细胞肝窦侧,但在有严重炎细胞浸润的碎片状坏死和灶性死区域,ICAM-1表达分布在整个肝细胞表面。重度慢性肝炎患者肝组织ICAM-1 mRNA和ICAM-1表达明显强于中度慢性肝炎(P< 0.05),中度慢性肝炎患者肝组织ICAM-1 mRNA和ICAM-1表达也明显强于轻度慢性肝炎(P< 0.05),见表1。肝细胞ICAM-1 mRNA表达水平与ICAM-1表达水平的一致性较好,两者间相关非常显著(P< 0.01)。

, 百拇医药
图1 重度慢性乙型肝炎肝细胞ICAM-1 mRNA表达
原位杂交, 肝细胞、肝窦内皮和血管内皮细胞大
量表达ICAM-1 mRNA (NBT/BCIP×100)
Fig 1 ICAM-1 mRNA expression in liver tissue with
severe chronic hepatitis B with in situ hybridiza
tion. Stronger expression of ICAM-1 mRNA in
hepatocytes, hepatic sinusoidal lining cells and
, 百拇医药
vessel endothelial cells (NBT/BCIP×100)

图2 中度慢性乙型肝炎肝组织ICAM-1表达,碎片状
坏死区,许多肝细胞增强表达ICAM-1,部分呈蜂
窝状, 阳性表达分布在整个肝细胞表面,伴许多
炎细胞浸润 (S-P×200)
Fig 2 ICAM-1 expression in liver tissue with moderate
chronic hepatitis B. In the area of piecemeal
, 百拇医药
necrosis, enhanced ICAM-1 expression in many
hepatocytes, partly with a local honey comb pat
tern, infiltrated by numerous inflammatory cells(S-P×200)
表1 乙型肝炎患者肝细胞ICAM-1和ICAM-1 mRNA表达
Tab1 ICAM-1 and ICAM-1 mRNA expression on hepatocytes of patients with viral hepatitis B
n
ICAM-1
, 百拇医药
ICAM-1 mRNA
HBeAg(+)
HBVDNA(+)
-
+
-
+
, 百拇医药
Healthy
11
11
0
0
0
11
0
0
0
0
0
AsC
5
, 百拇医药
5
0
0
0
5
0
0
0
4(80%)
5(100%)
CHB(Mi)
15
0
9
, http://www.100md.com
6
0
0
9
6
0
9(60%)
10(67%)
CHB(Mo)
15
0
1
9
5
, 百拇医药
0
0
9
6
4(27%)
5(33%)
CHB(S)
15
0
2
2
11
0
0
, http://www.100md.com
2
13
3(20%)
4(27%)
2.2 肝细胞ICAM-1表达与肝组织炎症,见表2表2 肝细胞ICAM-1 表达与炎症活动度
Tab2 The levels of ICAM-1 expression in hepatocytes
and inflammatory activities in liver
Grade of liver
inflammation(G)
, http://www.100md.com n
ICAM-1
-
+
0
16
16
0
0
, http://www.100md.com
0
1
10
0
8
2
0
2
5
0
1
4
0
3
, http://www.100md.com
15
0
0
11
4
4
15
0
0
0
15
慢性乙型肝炎患者肝组织炎症越明显,其肝细胞膜ICAM-1表达则越强,两者之间呈显著正相关,P<0.01。
2.3 肝细胞ICAM-1表达与肝功能,见表3表3 肚细胞ICAM-1表达与肝功能
, 百拇医药
Tab3 The levels of ICAM-1 expression in hepatocytes
and the liver functions
ICAM-1
n
ALT(IU/L)
AST(IU/L)
TB(μmol/L)
(%)
PTa
+
9
, 百拇医药
43±17
54±29
14.9±4.0
90.6±9.5
17
139±105*
137±123*
29.8±10.6#
85.2±11.1
, http://www.100md.com
19
194±82*
226±76*
114.0±35.5*
56.4±10.2
*:P<0.01 vs ICAM-1(+) group;
#:P<0.05 vs ICAM-1(+) and (
肝细胞ICAM-1表达强的患者血清ALT、AST、TB水平显著高于ICAM-1表达弱者;ICAM-1表达强的患者凝血酶原活动度显著低于ICAM-1表达弱者。
, 百拇医药
2.4 肝细胞ICAM-1表达与HBV复制标志
HBV感染者肝细胞ICAM-1表达水平越高,其血清HBeAg、HBVDNA阳性率则越低,两者间呈显著负相关,见表4。
表4 HBV感染者肝细胞ICAM-1表达与HBV复制标志
Tab4 The levels of ICAM-1 expression in hepatocytes
and HBV replication markers
ICAM-1
n
HBeAg(+)
HBVDNA(+)
, http://www.100md.com
-
5
4(80%)
5(100%)
+
9
8(89%)
8(89%)
17
5(29%)
7(41%)
, 百拇医药
19
3(16%)
44(21%)
Total
50
20(40%)
24(48%)
3 讨论
正常人肝细胞不表达ICAM-1,但存在ICAM-1基因。本结果显示HBV感染者肝内ICAM-1表达水平与ICAM-1 mRNA表达水平的一致性较好,提示HBV感染是通过促进肝细胞ICAM-1基因转录而诱导ICAM-1的表达增强。HBV能直接或通过IL-1、IFNγ、TNF-α等细胞因子间接诱导肝细胞增强表达ICAM-1[3,4]。
, 百拇医药
Del Pozo等[5]报告在淋巴细胞-内皮细胞相互作用中趋化因子诱导T细胞极化、形成胞浆突起;ICAM-1/LFA-1在胞浆突起介导的淋巴细胞募集过程中起重要作用,并促进T细胞的跨内皮迁移运动。慢性乙型肝炎肝血管内皮和肝窦内皮ICAM-1 mRNA和ICAM-1增强表达有利于淋巴细胞通过上述类似机制向肝组织中浸润,为CTL攻击靶细胞创造必要的条件。本研究发现,肝组织无炎症损伤者肝细胞缺乏ICAM-1 mRNA和ICAM-1表达,而慢性乙型肝炎患者肝细胞出现不同程度ICAM-1 mRNA和ICAM-1表达,而且其表达程度随着组织炎症损害的加重而增强,提示肝组织炎症存在和严重程度与肝细胞表达ICAM-1及水平有关。
在轻微炎细胞浸润部位,ICAM-1表达局限在肝窦内皮和肝细胞肝窦侧,但在有严重炎细胞浸润的碎片状坏死和灶性坏死区域,ICAM-1表达分布在整个肝细胞表面。说明肝细胞坏死与肝细胞膜ICAM-1表达有关,ICAM-1在慢性乙型肝炎肝细胞坏死中起重要作用,CTL细胞借助ICAM-1/LFA-1与肝细胞粘附、发挥细胞毒作用,导致肝细胞坏死[6]。血清HBeAg、HBVDNA是反映HBV感染者体内病毒复制活跃的重要指标。HBV感染者肝细胞ICAM-1表达越强,其血清HBeAg、HBVDNA阳性率则越低,提示肝细胞ICAM-1增强表达有利于机体清除病毒,说明肝细胞缺乏或低水平表达ICAM-1可能是慢性HBV感染持续存在的重要原因。
, http://www.100md.com
CHB患者肝损害越重,其肝细胞ICAM-1表达越强;肝细胞ICAM-1表达越强的患者肝功能也越差。说明肝细胞ICAM-1表达水平能较好反映CHB患者肝损害程度和肝功能状况。
Essani等[7]报道抗ICAM-1和抗LFA-1的单克隆抗体能阻断内毒素血症所致鼠急性炎症性肝损伤。Stepkowski等[8]报道针对鼠ICAM-1 mRNA的反义核酸阻断心脏移植排斥反应的发生。我们推测用针对人ICAM-1 mRNA的反义核酸抑制肝细胞ICAM-1表达,或者用抗ICAM-1和抗LFA-1的单克隆抗体对预防乙型肝炎肝组织炎症坏死应有一定的帮助。
作者简介:张绪清(1965.10), 男, 湖北省鄂州市人, 博士,主治医师, 讲师,主要从事乙型肝炎发病机制方面的研究,发表论文20余篇。
张绪清(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
, http://www.100md.com
顾长海(第三军医大学附属西南医院感染病科、全军传染病专科中心,重庆 400038)
参考文献
[1] Wawryk S O, Novotny J R, Wick I P, et al. The role of the FA1/interaction in human leukocyte homing and adhesion[J]. Immunol Rev,1989,108(1):135-161.
[2] 张绪清,顾长海.细胞间粘附分子1与肝病[J].中华肝脏 病杂志,1997,5(2):110-112.
[3] Sano K, Nagaki M, Sugiyama A, et al. Effects of cytokines on the binding of leukocytes to cultured rat hepatocytes and on the expression of ICAM-1 by hepatocytes[J]. Dig Dis Sci,1999,44 (4):796-805.
, 百拇医药
[4] Hu K Q, Yu C H, Vierling J M. Upregulation of intercellular adhesion molecule 1 transcription by hepatitis B virus X protein [J]. Proc Natl Acad Sci, USA, 1992, 89(23): 11 441- 11 445.
[5] Del Pozo M A, Cabanas C, Montoya M C, et al. ICAMs redistributed by chemokines to cellular uropods as a mechanism for recruitment of T lymphocytes[J]. J Cell Bio, 1997, 137(2):493-508.
[6] Stewart M P, Cabanas C, Hogg N, et al. T cell adhesion to intercellular adhesion molecule1 is controlled by cell spreading and the activation of integrin LFA1[J]. J Immunology,1996,156(13):1 810-1 817.
, 百拇医药
[7] Essani N A, Fisher M A, Farhood A, et al. Cytokineinduced upregulation of hepatic intercellular adhesion molecule1 messenger RNA expression and its role in the pathophysiology of murine endotoxin shock and acute liver failure[J]. Hepatology,1995,21(5):1 632-1 639.
[8] Stepkowski S M, Tu Y, Condon T P, et al. Induction of transplantation tolerance by treatement with oligonucleodtides and antiLFA-1 monoclonal antibodies[J]. Transplantation Proceedings,1995,27(1):113., http://www.100md.com