盐酸左旋氧氟沙星胶囊人体生物利用度
作者:马越鸣 曾照宏 陈波 冒国光 钟秋 严文魁 查晓娟 孙瑞元
单位:马越鸣(皖南医学院药理学教研室);曾照宏 陈波 冒国光 钟秋 严文魁 查晓娟 孙瑞元(弋矶山医院临床医学研究所,芜湖241001)
关键词:盐酸左旋氧氟沙星药代动力学生物利用度高效液相色谱法
中国临床药理学与治疗学000413
目的研究左旋氧氟沙星胶囊的人体药代动力学及相对生物利用度。方法12名健康志愿者随机交叉口服单剂量200mg盐酸左旋氧氟沙星胶囊和左旋氧氟沙星片剂,采用高效液相色谱法测定左旋氧氟沙星血药浓度,用一级吸收的二室模型拟合血浓_时间数据,用方差分析和双单侧t检验进行制剂的等效性分析。结果胶囊的药代动力学参数为Cmax=(3.18±0.57)mg·L-1,tmax=(0.83±0.33)h,AUC0~24=(20.0±2.9)mg·h·L-1,t1/2(β)=(7.8±2.0)h;片剂的药代动力学参数为Cmax=(2.96±0.43)mg·L-1,tmax=(0.96±0.33)h,AUC0~24=(21.5±1.9)mg·h·L-1,t1/2(β)=(6.82±0.84)h,胶囊的相对生物利用度为(93.0±11.8)%。结论盐酸左旋氧氟沙星胶囊和左旋氧氟沙星片剂具有生物等效性。
, 百拇医药
中图分类号R978
Relative bioavailability of levofloxacin hydrohloride capsule in healthy volunteers
MA Yue_Ming
(Department of Pharmacology,Wannan Medical College,Wuhu,241001)
ZHENG Zao_Hong CHEN Bo MAO Guo_Guang ZHONG Qiu YAN Wen_Kui ZHA Xiao_Juan SUN Rui_Yuan
(Institute of Clinical Medicine,Yijishan Hospital, Wannan Medical College,Wuhu 241001)
, http://www.100md.com
Aim To investigate the pharmacokinetics and relative bioavailability of levofloxacin hydrochloride capsule.Methods A single 200 mg oral dose of either capsule or tablet was given to 12 healthy male volunteers in randomized self_crossover way.Plasma levofloxacin concentration was determined by high performance liquid chromatography. The concentration_time data of levofloxacin was fitted to two_compartment model with first_order absorption and the bioequivalence of the two formulations were evaluated by the analysis of variance and the two one_sided t_test. Results The pharmacokinetic parameters were as follows:capsule:Cmax=(3.18± 0.57) mg· L-1, tmax=(0.83± 0.33) h, AUC0~ 24=(19.95± 2.86) mg· h· L-1,t1/2(β )=(7.75± 2.04) h; tablet : Cmax=(2.96± 0.43) mg· L-1,tmax=(0.96± 0.33) h, AUC0~ 24=(21.49± 1.88) mg· h· L-1,t1/2(β )=(6.82± 0.84) h. Relative bioavailability of capsule was (93.0± 11.8)% compared with tablet. Conclusion The two formulations are of bioequivalence.
, http://www.100md.com
Key words levofloxacin hydrochloride; pharmacokinetics; bioavailability; HPLC
左旋氧氟沙星(levofloxacin)是氧氟沙星的S(-)对映体,具有广谱高效的抗菌作用,抗菌活性是氧氟沙星的2倍,而毒副作用比氧氟沙星更小,且口服吸收完全,血药浓度较高[1]。该药首先由日本研制开发,在国外已广泛用于临床。本文报道盐酸左旋氧氟沙星胶囊在人体的药代动力学参数及相对生物利用度试验结果,为胶囊临床评价提供依据。
1 材料与方法
1.1药品及试剂试验制剂:盐酸左旋氧氟沙星胶囊,每粒110mg(含左旋氧氟沙星100mg),合肥海通药物研究所研制,批号980213。参比制剂:左旋氧氟沙星片,商品名为可乐必妥,每片含左旋氧氟沙星100mg,日本第一制药株式会社产品,批号LT407。标准品:盐酸左旋氧氟沙星对照品,合肥海通药物研究所提供,批号:970316。内标:诺氟沙星,昆山制药厂产品,批号:900092。乙腈为光谱纯,甲醇、二氯甲烷、溴化四丁铵、磷酸和磷酸盐均为分析纯。
, http://www.100md.com
1.2仪器Waters高效液相色谱系统,717plus自动进样器,996二极管阵列检测器,Millennium
1.3血药浓度测定方法[2]色谱条件:色谱柱为HypersilODS150mm×4.6mm,5μm,大连化物所,柱温30℃;流动相为0.01mol.L-1KH2PO4∶0.01mol.L-1溴化四丁铵∶乙腈∶三乙胺(45∶44∶10∶1),磷酸调至pH2.8,0.45μm微孔滤膜过滤,流速1.0ml.min-1;检测波长295nm。
1.4提取方法取血浆0.5ml,加入内标液(100mg.L-1)20μl,混匀,加0.1mol.L-1磷酸二氢钠缓冲液(pH7.0)1.0ml,混匀,加入二氯甲烷5.0ml,涡旋10mim,3000r.min-1离心10mim,取有机相约4ml,N2下吹干,残渣用流动相100μl溶解,取20μl进样。
, http://www.100md.com
1.5方法学考察标准曲线:以血浆左旋氧氟沙星浓度为0.091、0.454、0.908、1.816、3.632和5.448mg.L-1测定峰面积,以样品峰面积与内标峰面积比值(f)对浓度(C)进行回归,考察线性范围。采用血浆左旋氧氟沙星浓度为0.091,0.908,5.448mg.L-1,测定回收率、日内及日间变异。以信噪比=3计算分析方法的最低检出限。
1.6受试者与试验方法
1.6.1受试者12名健康男性志愿者,均为本院在校学生。体重(60.9±4.4)kg,年龄(21.2±0.9)岁,身高(169.2±5.4)cm。受试者无肝、肾疾病史,全面体格检查及实验室检查(其中包括心肺、血压、肾、肝功能、血、尿常规)均健康。受试者了解受试须知后,签署知情同意书,受试前2wk内未服过任何药物,受试前禁食12h,试验期间禁烟、酒、茶,并由医护人员进行健康监护。
, http://www.100md.com
1.6.2试验方案采用双交叉试验设计,受试者根据体重,随机分成2组,每组6人。一组先口服试验制剂(T),后口服参比制剂(R),即TOR;另一组先口服参比制剂,后口服试验制剂,即ROT。两种制剂间隔1wk。晨7:00两组分别口服试验制剂和参比制剂各200mg(100mg×2),温开水200ml送服。服药后1h后自由进水,服药后4,10h统一进食。受试者在给药前及给药后0.25、0.5、1、1.5、2、3、4、6、8、12、24h取静脉血3ml。血样经肝素抗凝,离心制备血浆,置-20℃冰箱保存待测。
1.7数据分析实验数据用药代动力学3p87程序选择房室模型,计算药代参数。两种制剂的药代参数用配对t值法进行显著性检验,以判断药代动力学参数的差异是否有显著意义。以梯形法计算曲线下面积(AUC0~24),用AUC估算生物利用度,公式:
F=AUC(T)/AUC(R)×100%
AUC和Cmax用方差分析和双向单侧t检验(以80%~125%为等效标准)[3],进行生物等效性检验,tmax用Wilcoxon法进行显著性检验。
, 百拇医药
2 结果
2.1血药浓度测定方法评价空白血浆、血浆加左旋氧氟沙星标准品及内标和志愿者服药后血浆的色谱图表明,血浆中杂质及代谢物不干扰样品及内标的测定。
线性范围:左旋氧氟沙星浓度(C)在0.091~5.448mg.L-1中与峰面积比(f)呈良好的线性关系,回归方程:f=1.2285C+0.0399;r=0.9998,最低检出限:0.05mg.L-1。在0.091~5.448mg.L-1标准浓度下平均回收率为99.7%~83.4%,日内变异系数为6.7%~9.0%和日间变异系数为9.6%~9.3%。
2.1血药浓度健康受试者口服盐酸左旋氧氟沙星胶囊和左旋氧氟沙星片剂后,血药浓度_时间数据见图1。可见胶囊和片剂血浓经时过程变化趋势一致,在口服后0.25h即可检测到血药浓度,在1h左右达峰浓度,至24h分别降至(0.19±0.09)和(0.18±0.03)mg.L-1,为峰浓度的十分之一以下。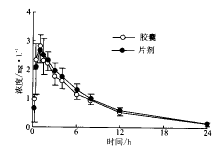
, 百拇医药
图1 12名志愿者口服单剂量左旋氧氟沙星200mg的血浆浓度_时间曲线
2.3药代动力学参数经3p87程序计算,显示左旋氧氟沙星符合带一级吸收的二房室模型,单剂量口服左旋氧氟沙星的药代动力学参数结果见表1。其中Cmax、tmax为血药浓度的达峰时间和峰浓度,均为实测值。两种制剂的药代动力学参数经配对t检验,tmax经Wilcoxon检验,差异无显著意义。
2.4生物利用度以左旋氧氟沙星片为参比制剂,用AUC0~24估算左旋氧氟沙星胶囊的相对生物利用度(F),结果见表2,F的90%可信限为86.9%~99.1%。
2.5生物等效性检验AUC0~24和Cmax在经对数转换后,进行方差分析和双向单侧t检验,结果表明两种制剂的药代动力学参数ln(AUC0~24)、ln(Cmax)的方差分析结果表明制剂间、周期间和个体间的差异均无显著意义。双单侧t检验表明高侧t值及低侧t值均大于t0.05,说明两制剂在生物利用度方面具有生物等效性。试验过程中受试者未出现任何不良反应。
, 百拇医药
表1 志愿者口服单剂量左旋氧氟沙星200mg的药代动力学参数(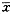 ±s,n=12) 参数
±s,n=12) 参数
胶囊
t1/2(a)h
0.76±0.51
0.83±0.63
t1/2(b)h
7.8±2.0
6.82±0.84
t1/2(ka)h
0.23±0.27
, 百拇医药
0.29±0.23
tmax/h
0.83±0.33
0.96±0.33
Cmax/mg.L-1
3.18±0.57
2.96±0.43
CL/L.h-1
9.3±1.4
8.64±0.67
Vd/L
, 百拇医药
50±12
54±16
AUC0~24/mg.h.L-1
20.0±2.9
21.5±1.9
表2左旋氧氟沙星胶囊的生物利用度 专愿者
周期
AUC0~24(胶囊)
周期
AUC0-24(片)
F/%
1
, 百拇医药
2
20.56
1
26.13
78.7
2
1
16.23
2
20.56
82.9
3
1
, http://www.100md.com 21.07
2
21.44
98.3
4
2
19.72
1
20.51
96.2
5
1
27.67
, http://www.100md.com 2
23.17
119.4
6
1
18.37
2
19.79
92.8
7
2
19.28
1
23.17
, http://www.100md.com
83.2
8
1
20.84
2
20.93
99.6
9
2
19.52
1
21.99
88.8
, 百拇医药
10
2
20.56
1
19.58
105.0
11
1
17.04
2
20.55
82.9
12
, 百拇医药
2
48.58
1
20.08
92.5
均数
-
19.95
-
21.49
93.0
标准差
-
, 百拇医药
4.83
-
1.88
11.8
3 讨论
本研究采用高效液相色谱法测定左旋氧氟沙星浓度,方法的专属性高,线性范围包括了所有体内血药浓度实测数据点,高、中、低三个浓度水平的回收率均>80%,日内及日间变异均<10%,达到了生物样品测定及生物利用度试验的要求。
结果表明左旋氧氟沙星胶囊与片剂的药代动力学参数相近,生物利用度符合要求,胶囊与片剂相比达到生物等效。两种制剂的Cmax、tmax、AUC0~24、Vd、t1/2与文献报道[4,5]基本一致。在计算生物利用度时,AUC0~∞在估算0~∞剩余面积时往往有较大误差,故本文中采用AUC0-24来计算生物利用度(F)。个别点的F超出了80%~125%范围之外,但这并不影响生物等效性判断,因为生物等效的结论是根据双单侧检验的结果来决定的。
, http://www.100md.com
马越鸣,女,教授,主要研究定量药理学。
孙瑞元,男,教授,国家药品审评委员,国家药典委员会委员。
参 考 文 献
1,Davis R,Bryson HM. Levofloxacin:a review of its antibacterial activity, pharmacokinetics and thera_ peutic efficacy.Drugs,1994;47:678
2,孙春华.反相高效液相色谱法测定血浆中左旋氧氟沙星浓度.药物分析杂志 ,1995;15(Suppl):572
3,黄圣凯,韩可勤.生物等效性评价的几种统计方法.中国临床药理学杂志,1993;9:43
4,Nakashima M,Uematsu T,Kanamani M,et al.Phase I study of levofloxacin.(S)_(_)_ofloxacin.Jpn J Clin Pharm Ther, 1992;23:515
5,曹国颖,孙春华,李可欣,等.可乐必妥在健康志愿者及下呼吸道感染病人中的药代动力学及咯痰浓度的研究.中国临床药理学杂志,1995;11:219
2000-05-18收稿,2000-07-05修回, http://www.100md.com
单位:马越鸣(皖南医学院药理学教研室);曾照宏 陈波 冒国光 钟秋 严文魁 查晓娟 孙瑞元(弋矶山医院临床医学研究所,芜湖241001)
关键词:盐酸左旋氧氟沙星药代动力学生物利用度高效液相色谱法
中国临床药理学与治疗学000413
目的研究左旋氧氟沙星胶囊的人体药代动力学及相对生物利用度。方法12名健康志愿者随机交叉口服单剂量200mg盐酸左旋氧氟沙星胶囊和左旋氧氟沙星片剂,采用高效液相色谱法测定左旋氧氟沙星血药浓度,用一级吸收的二室模型拟合血浓_时间数据,用方差分析和双单侧t检验进行制剂的等效性分析。结果胶囊的药代动力学参数为Cmax=(3.18±0.57)mg·L-1,tmax=(0.83±0.33)h,AUC0~24=(20.0±2.9)mg·h·L-1,t1/2(β)=(7.8±2.0)h;片剂的药代动力学参数为Cmax=(2.96±0.43)mg·L-1,tmax=(0.96±0.33)h,AUC0~24=(21.5±1.9)mg·h·L-1,t1/2(β)=(6.82±0.84)h,胶囊的相对生物利用度为(93.0±11.8)%。结论盐酸左旋氧氟沙星胶囊和左旋氧氟沙星片剂具有生物等效性。
, 百拇医药
中图分类号R978
Relative bioavailability of levofloxacin hydrohloride capsule in healthy volunteers
MA Yue_Ming
(Department of Pharmacology,Wannan Medical College,Wuhu,241001)
ZHENG Zao_Hong CHEN Bo MAO Guo_Guang ZHONG Qiu YAN Wen_Kui ZHA Xiao_Juan SUN Rui_Yuan
(Institute of Clinical Medicine,Yijishan Hospital, Wannan Medical College,Wuhu 241001)
, http://www.100md.com
Aim To investigate the pharmacokinetics and relative bioavailability of levofloxacin hydrochloride capsule.Methods A single 200 mg oral dose of either capsule or tablet was given to 12 healthy male volunteers in randomized self_crossover way.Plasma levofloxacin concentration was determined by high performance liquid chromatography. The concentration_time data of levofloxacin was fitted to two_compartment model with first_order absorption and the bioequivalence of the two formulations were evaluated by the analysis of variance and the two one_sided t_test. Results The pharmacokinetic parameters were as follows:capsule:Cmax=(3.18± 0.57) mg· L-1, tmax=(0.83± 0.33) h, AUC0~ 24=(19.95± 2.86) mg· h· L-1,t1/2(β )=(7.75± 2.04) h; tablet : Cmax=(2.96± 0.43) mg· L-1,tmax=(0.96± 0.33) h, AUC0~ 24=(21.49± 1.88) mg· h· L-1,t1/2(β )=(6.82± 0.84) h. Relative bioavailability of capsule was (93.0± 11.8)% compared with tablet. Conclusion The two formulations are of bioequivalence.
, http://www.100md.com
Key words levofloxacin hydrochloride; pharmacokinetics; bioavailability; HPLC
左旋氧氟沙星(levofloxacin)是氧氟沙星的S(-)对映体,具有广谱高效的抗菌作用,抗菌活性是氧氟沙星的2倍,而毒副作用比氧氟沙星更小,且口服吸收完全,血药浓度较高[1]。该药首先由日本研制开发,在国外已广泛用于临床。本文报道盐酸左旋氧氟沙星胶囊在人体的药代动力学参数及相对生物利用度试验结果,为胶囊临床评价提供依据。
1 材料与方法
1.1药品及试剂试验制剂:盐酸左旋氧氟沙星胶囊,每粒110mg(含左旋氧氟沙星100mg),合肥海通药物研究所研制,批号980213。参比制剂:左旋氧氟沙星片,商品名为可乐必妥,每片含左旋氧氟沙星100mg,日本第一制药株式会社产品,批号LT407。标准品:盐酸左旋氧氟沙星对照品,合肥海通药物研究所提供,批号:970316。内标:诺氟沙星,昆山制药厂产品,批号:900092。乙腈为光谱纯,甲醇、二氯甲烷、溴化四丁铵、磷酸和磷酸盐均为分析纯。
, http://www.100md.com
1.2仪器Waters高效液相色谱系统,717plus自动进样器,996二极管阵列检测器,Millennium
1.3血药浓度测定方法[2]色谱条件:色谱柱为HypersilODS150mm×4.6mm,5μm,大连化物所,柱温30℃;流动相为0.01mol.L-1KH2PO4∶0.01mol.L-1溴化四丁铵∶乙腈∶三乙胺(45∶44∶10∶1),磷酸调至pH2.8,0.45μm微孔滤膜过滤,流速1.0ml.min-1;检测波长295nm。
1.4提取方法取血浆0.5ml,加入内标液(100mg.L-1)20μl,混匀,加0.1mol.L-1磷酸二氢钠缓冲液(pH7.0)1.0ml,混匀,加入二氯甲烷5.0ml,涡旋10mim,3000r.min-1离心10mim,取有机相约4ml,N2下吹干,残渣用流动相100μl溶解,取20μl进样。
, http://www.100md.com
1.5方法学考察标准曲线:以血浆左旋氧氟沙星浓度为0.091、0.454、0.908、1.816、3.632和5.448mg.L-1测定峰面积,以样品峰面积与内标峰面积比值(f)对浓度(C)进行回归,考察线性范围。采用血浆左旋氧氟沙星浓度为0.091,0.908,5.448mg.L-1,测定回收率、日内及日间变异。以信噪比=3计算分析方法的最低检出限。
1.6受试者与试验方法
1.6.1受试者12名健康男性志愿者,均为本院在校学生。体重(60.9±4.4)kg,年龄(21.2±0.9)岁,身高(169.2±5.4)cm。受试者无肝、肾疾病史,全面体格检查及实验室检查(其中包括心肺、血压、肾、肝功能、血、尿常规)均健康。受试者了解受试须知后,签署知情同意书,受试前2wk内未服过任何药物,受试前禁食12h,试验期间禁烟、酒、茶,并由医护人员进行健康监护。
, http://www.100md.com
1.6.2试验方案采用双交叉试验设计,受试者根据体重,随机分成2组,每组6人。一组先口服试验制剂(T),后口服参比制剂(R),即TOR;另一组先口服参比制剂,后口服试验制剂,即ROT。两种制剂间隔1wk。晨7:00两组分别口服试验制剂和参比制剂各200mg(100mg×2),温开水200ml送服。服药后1h后自由进水,服药后4,10h统一进食。受试者在给药前及给药后0.25、0.5、1、1.5、2、3、4、6、8、12、24h取静脉血3ml。血样经肝素抗凝,离心制备血浆,置-20℃冰箱保存待测。
1.7数据分析实验数据用药代动力学3p87程序选择房室模型,计算药代参数。两种制剂的药代参数用配对t值法进行显著性检验,以判断药代动力学参数的差异是否有显著意义。以梯形法计算曲线下面积(AUC0~24),用AUC估算生物利用度,公式:
F=AUC(T)/AUC(R)×100%
AUC和Cmax用方差分析和双向单侧t检验(以80%~125%为等效标准)[3],进行生物等效性检验,tmax用Wilcoxon法进行显著性检验。
, 百拇医药
2 结果
2.1血药浓度测定方法评价空白血浆、血浆加左旋氧氟沙星标准品及内标和志愿者服药后血浆的色谱图表明,血浆中杂质及代谢物不干扰样品及内标的测定。
线性范围:左旋氧氟沙星浓度(C)在0.091~5.448mg.L-1中与峰面积比(f)呈良好的线性关系,回归方程:f=1.2285C+0.0399;r=0.9998,最低检出限:0.05mg.L-1。在0.091~5.448mg.L-1标准浓度下平均回收率为99.7%~83.4%,日内变异系数为6.7%~9.0%和日间变异系数为9.6%~9.3%。
2.1血药浓度健康受试者口服盐酸左旋氧氟沙星胶囊和左旋氧氟沙星片剂后,血药浓度_时间数据见图1。可见胶囊和片剂血浓经时过程变化趋势一致,在口服后0.25h即可检测到血药浓度,在1h左右达峰浓度,至24h分别降至(0.19±0.09)和(0.18±0.03)mg.L-1,为峰浓度的十分之一以下。

, 百拇医药
图1 12名志愿者口服单剂量左旋氧氟沙星200mg的血浆浓度_时间曲线
2.3药代动力学参数经3p87程序计算,显示左旋氧氟沙星符合带一级吸收的二房室模型,单剂量口服左旋氧氟沙星的药代动力学参数结果见表1。其中Cmax、tmax为血药浓度的达峰时间和峰浓度,均为实测值。两种制剂的药代动力学参数经配对t检验,tmax经Wilcoxon检验,差异无显著意义。
2.4生物利用度以左旋氧氟沙星片为参比制剂,用AUC0~24估算左旋氧氟沙星胶囊的相对生物利用度(F),结果见表2,F的90%可信限为86.9%~99.1%。
2.5生物等效性检验AUC0~24和Cmax在经对数转换后,进行方差分析和双向单侧t检验,结果表明两种制剂的药代动力学参数ln(AUC0~24)、ln(Cmax)的方差分析结果表明制剂间、周期间和个体间的差异均无显著意义。双单侧t检验表明高侧t值及低侧t值均大于t0.05,说明两制剂在生物利用度方面具有生物等效性。试验过程中受试者未出现任何不良反应。
, 百拇医药
表1 志愿者口服单剂量左旋氧氟沙星200mg的药代动力学参数(
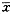 ±s,n=12) 参数
±s,n=12) 参数胶囊
t1/2(a)h
0.76±0.51
0.83±0.63
t1/2(b)h
7.8±2.0
6.82±0.84
t1/2(ka)h
0.23±0.27
, 百拇医药
0.29±0.23
tmax/h
0.83±0.33
0.96±0.33
Cmax/mg.L-1
3.18±0.57
2.96±0.43
CL/L.h-1
9.3±1.4
8.64±0.67
Vd/L
, 百拇医药
50±12
54±16
AUC0~24/mg.h.L-1
20.0±2.9
21.5±1.9
表2左旋氧氟沙星胶囊的生物利用度 专愿者
周期
AUC0~24(胶囊)
周期
AUC0-24(片)
F/%
1
, 百拇医药
2
20.56
1
26.13
78.7
2
1
16.23
2
20.56
82.9
3
1
, http://www.100md.com 21.07
2
21.44
98.3
4
2
19.72
1
20.51
96.2
5
1
27.67
, http://www.100md.com 2
23.17
119.4
6
1
18.37
2
19.79
92.8
7
2
19.28
1
23.17
, http://www.100md.com
83.2
8
1
20.84
2
20.93
99.6
9
2
19.52
1
21.99
88.8
, 百拇医药
10
2
20.56
1
19.58
105.0
11
1
17.04
2
20.55
82.9
12
, 百拇医药
2
48.58
1
20.08
92.5
均数
-
19.95
-
21.49
93.0
标准差
-
, 百拇医药
4.83
-
1.88
11.8
3 讨论
本研究采用高效液相色谱法测定左旋氧氟沙星浓度,方法的专属性高,线性范围包括了所有体内血药浓度实测数据点,高、中、低三个浓度水平的回收率均>80%,日内及日间变异均<10%,达到了生物样品测定及生物利用度试验的要求。
结果表明左旋氧氟沙星胶囊与片剂的药代动力学参数相近,生物利用度符合要求,胶囊与片剂相比达到生物等效。两种制剂的Cmax、tmax、AUC0~24、Vd、t1/2与文献报道[4,5]基本一致。在计算生物利用度时,AUC0~∞在估算0~∞剩余面积时往往有较大误差,故本文中采用AUC0-24来计算生物利用度(F)。个别点的F超出了80%~125%范围之外,但这并不影响生物等效性判断,因为生物等效的结论是根据双单侧检验的结果来决定的。
, http://www.100md.com
马越鸣,女,教授,主要研究定量药理学。
孙瑞元,男,教授,国家药品审评委员,国家药典委员会委员。
参 考 文 献
1,Davis R,Bryson HM. Levofloxacin:a review of its antibacterial activity, pharmacokinetics and thera_ peutic efficacy.Drugs,1994;47:678
2,孙春华.反相高效液相色谱法测定血浆中左旋氧氟沙星浓度.药物分析杂志 ,1995;15(Suppl):572
3,黄圣凯,韩可勤.生物等效性评价的几种统计方法.中国临床药理学杂志,1993;9:43
4,Nakashima M,Uematsu T,Kanamani M,et al.Phase I study of levofloxacin.(S)_(_)_ofloxacin.Jpn J Clin Pharm Ther, 1992;23:515
5,曹国颖,孙春华,李可欣,等.可乐必妥在健康志愿者及下呼吸道感染病人中的药代动力学及咯痰浓度的研究.中国临床药理学杂志,1995;11:219
2000-05-18收稿,2000-07-05修回, http://www.100md.com