人胆汁中罗红霉素代谢产物的研究
作者:李雪庆 钟大放* 吴硕东1 王爱民 田蕾 于宏1
单位:(沈阳药科大学药物代谢与药物动力学实验室,沈阳 110015; 1中国医科大学第二附属医院,沈阳 110001)
关键词:罗红霉素;代谢物;人胆汁;高效液相色谱-离子阱质谱法
药学学报990112.htm 摘要 目的:研究人胆汁中罗红霉素的代谢转化产物。方法:采用高效液相色谱-离子阱质谱法,对患者po罗红霉素后的胆汁样品进行了分析。结果:发现了13个代谢产物,分别为罗红霉素的(9Z)-异构体及其(9E)-,(9Z)-N-去甲基和N-双去甲基衍生物和(9E)-及(9Z)-脱克拉定糖衍生物,(9E)-和(9Z)-红霉素肟及其(9E)-和(9Z)-N-去甲基及N-双去甲基衍生物,其中9种为新发现的代谢物。结论:罗红霉素及其代谢物均可在体内发生几何异构化。
, 百拇医药
STUDIES ON METABOLITES OF ROXITHROMYCIN IN HUMAN BILE
Li Xueqing (Li XQ), Zhong Dafang (Zhong DF)*, Wu Shuodong (Wu SD)1,Wang Aimin (Wang AM), Tian Lei (Tian L) and Yu Hong (Yu H)1
(Laboratory of Drug Metabolism and Pharmacokinetics, Shenyang Pharmaceutical University,Shenyang 110015; 1The Second Affiliated Hospital, China Medical University, Shenyang 110001)
, 百拇医药
ABSTRACT AIM: To study the metabolites of roxithromycin (RXM) in the bile of a patient, who had received an oral dose of 150 mg RXM after gallbladder operation. METHODS: High-performance liquid chromatography/ion trap mass spectrometry was used to determinate RXM and its metabolites in human bile. The bile sample was collected, extracted with diethyl ether and separated on a C18 reversed-phase column with (+)ESI-MSn detection. RESULTS: RXM and its thirteen metabolites were identified in the sample based on reference substances and mass spectra. These include descladinose-RXM (M1), erythromycin-oxime (M2) and its N-mono- and N-didemethylated derivatives (M4 and M6), N-mono- and didemethylated derivatives of RXM (M3 and M5), as well as the (9Z)-epimeric isomers of RXM and all its above metabolites (M7~M13). The ratios of (9Z)- to (9E)-isomers were found to be between 0.11~0.79. The parent drug remained was about 20% of the total bile metabolites. CONCLUSION: The metabolic pathways of RXM observed in the human bile are therefore quite different to those in human plasma and urine. The identification of the isomerization of the oximes of RXM derivatives represents a novel biotransformation pathway.
, http://www.100md.com
KEY WORDS roxithromycin; metabolites; human bile; HPLC/MS
*Corresponding author
罗红霉素(RXM)化学名为(9E)-[O-[(2-甲氧基乙氧基)甲基]肟基]红霉素,属半合成大环内酯类抗生素。临床主要用于治疗呼吸道及泌尿道感染、皮肤和软组织感染等[1]。对罗红霉素代谢产物的分析和检测已有报道[2~6],在尿中检出4种代谢产物,分别为罗红霉素的N-去甲基和N-双去甲基衍生物、罗红霉素脱克拉定糖衍生物以及红霉素肟。尽管证明罗红霉素主要经胆汁排泄,但未见对胆汁中代谢产物的报道。近年来发展起来的LC/MS联用技术能直接分析溶液样品,特别适合分析复杂介质中极性强、难挥发或热不稳定的化合物,在药物代谢研究中得到了越来越广泛的应用。本文采用(+)ESI-MSn离子阱技术,对一名患者po罗红霉素后胆汁中罗红霉素的代谢物进行了定性分析,并用HPLC/MSn联用法对代谢物及其相对含量进行了初步研究。在实验中共检出13种代谢物,其中9种未见报道。
, 百拇医药
材料与方法
试剂与仪器 罗红霉素片(沈阳埃默药业有限公司);罗红霉素对照品(粗品,含量95.4%)及红霉素肟对照品(粗品,含量96.0%)由沈阳华泰药物研究所提供;其余化学品均为市售分析纯;流动相所用有机溶剂为色谱纯。
美国Finnigan公司LCQ型液相色谱-质谱联用仪,包括APCI(大气压化学电离)、ESI(电喷雾电离)源以及LCQ数据处理系统,并配有直接进样用注射泵和250 μl进样器;日本岛津公司LC-10AD泵,包括7125 Rheodyne进样阀。
胆汁样品收集 胆管结石患者(女性,60岁,肾功能正常,肝功能恢复正常)胆囊切除、胆管切开取石、T形管引流术后,于恢复稳定期po罗红霉素片150 mg(bid)。由T形引流管收集服药后1.5~5 h流出的胆汁,于冰箱-30℃冷冻保存,待测。
胆汁样品的前处理 方法1:取Sep-Pak C8固相萃取柱,用水3 ml、甲醇3 ml、水3 ml依次进行洗涤,待用。取胆汁样品0.5 ml,以蒸馏水0.5 ml稀释后,用微孔滤膜(0.45 μm)过滤。滤液以30 滴.min-1的速度通过上述已活化的Sep-Pak C8固相萃取柱。用水3 ml洗涤后,再用甲醇2 ml洗脱。洗脱液用于(+)ESI-MSn分析。方法2:另取胆汁样品0.5 ml,加入Na2CO3溶液(0.1 mol.L-1)100 μl及重蒸乙醚3 ml,涡流混合3 min,离心10 min。分取有机层,于40℃下氮气流吹干。残留物以流动相100 μl溶解,用于HPLC/MSn分析。
, 百拇医药
(+)ESI-MSn分析条件 离子源喷射电压:4.0 kV;毛细管温度:150℃;毛细管电压:27 V;鞘气(N2);流速:0.3 L.min-1;注射泵进样速度:10 μl.min-1;采集范围:m/z 150~1000。
样品的(+)ESI-MSn分析方法 取胆汁固相萃取洗脱液,用注射泵将其直接导入ESI离子源,选择正离子方式检测。先用全扫描一级质谱方式获得待测物的准分子离子峰[M+H]+,然后利用(+)ESI-MSn离子阱技术对准分子离子峰及其碎片离子峰进行多级质谱分析,获得相应的子离子质谱图。
HPLC-MSn分析条件 色谱柱:Kromasil C18不锈钢柱(5 μm粒径,200 mm×4.6 mm ID,天津凯德公司);流动相:甲醇―乙腈―水(含10 mmol.L-1醋酸铵)(10∶43∶47);流速:0.3 ml.min-1;柱温:20℃;进样量:20 μl。质谱参数设置:离子源喷射电压4.25 kV;毛细管温度180℃;毛细管电压30 V;鞘气流速0.75 L.min-1;辅助气流速0.15 L.min-1。采用全扫描一级质谱、选择离子检测(SIM)及选择离子二级全扫描质谱(full scan MS2) 3种方式同时测定。
, http://www.100md.com
结果
1 胆汁中代谢产物的(+)ESI-MSn分析
在(+)ESI-MS全扫描一级质谱条件下,测得胆汁中有一组罗红霉素相关物质的准分子离子峰,分别为m/z 837,823,749,735和679,其中m/z 837,823,679和749分别与罗红霉素及文献报道[2]的3个代谢产物(罗红霉素的N-去甲基衍生物、脱克拉定糖衍生物及红霉素肟)的质荷比相符,均为[M+H]+峰。根据报道的另一个代谢产物(罗红霉素的N-双去甲基衍生物,其分子量为808)及上述观察结果推测还可能存在红霉素肟的N-双去甲基衍生物(分子量为720)。本文采用全扫描检测时局部放大及选择离子检测的方法,观察到m/z 809,721质荷比处均有较弱的准分子离子峰[M+H]+存在。为进一步了解这些物质的质谱断裂规律,本文采用ESI-MSn离子阱技术分别对这7个准分子离子进行MS2级质谱分析。发现除m/z 679离子外,均有丢失中性碎片158 u的子离子产生,它们可能是由母离子脱去克拉定糖生成。对m/z 837,749进一步进行MS3级质谱分析,并与罗红霉素及红霉素肟同样条件下所得的各级质谱对照,质谱断裂规律完全一致,证明胆汁样品中存在罗红霉素及代谢物红霉素肟。根据文献报道及质谱断裂规律,判断m/z 823和809两准分子离子是罗红霉素N-去甲基和N-双去甲基代谢物,m/z 679为罗红霉素脱克拉定糖代谢物。新发现的m/z 735和721两准分子离子分别比红霉素肟少14和28个质量数,即分子中分别脱去1个及2个甲基,根据其质谱断裂情况及上述代谢物的质谱特征,可判断二者为红霉素肟N-去甲基和N-双去甲基代谢物。胆汁中各化合物相应的(+)ESI-MS2全扫描质谱图见图1。

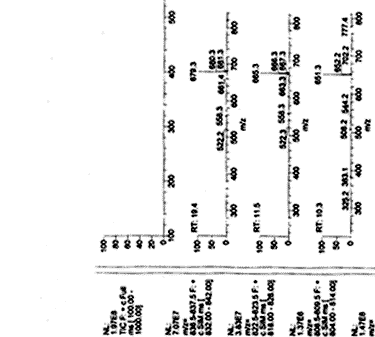



, http://www.100md.com
2 胆汁中代谢物的HPLC/MSn色谱-质谱行为
在(+)ESI-MSn的研究基础上,本文选择m/z 837,823,809,749,735,721和679 7个离子进行HPLC/MSn分析。图1包括了胆汁样品经色谱分离后得到的总离子流色谱图和选择离子检测(SIM)色谱图。从各SIM色谱图观察,并经总离子流质谱和MS2级质谱确认,发现每个SIM色谱图中均出现一对MS1级和MS2级质谱完全相同的色谱峰。因为罗红霉素结构中具有一个(9E)-构型的肟醚结构,推测它很可能在代谢过程中发生异构化,生成(9Z)-异构体,因而出现两个色谱峰。本文考察了罗红霉素对照品,发现除在30.3 min保留时间的主峰外,在19.4 min处还有一个含量小于1%的小峰,其MS1级和MS2级质谱与罗红霉素完全相同,判断即为合成过程中引入的(9Z)-异构体(罗红霉素片剂中未检出该异构体);而胆汁中SIM方式检测m/z 837离子观察到的两色谱峰的保留时间与对照品中观察到的色谱峰一致,因而可认为19.4 min色谱峰对应的物质是罗红霉素的(9Z)-异构体代谢物。同理,通过红霉素肟对照品的研究,证明保留时间12.2及15.7 min分别为(9Z)-和(9E)-红霉素肟代谢物。推测其余各对代谢物也均为(9Z)-和(9E)-异构体代谢物,(9Z)-较(9E)-异构体先出峰。罗红霉素及其代谢产物的HPLC/MSn数据见表1。本文采用HPLC-ECD法对胆汁样品的色谱行为进行考察,发现质谱检测中m/z 679和749所对应的色谱峰在电化学检测器上都有响应,说明它们结构中的氨基糖没有发生变化,进一步证明m/z 679峰为罗红霉素脱克拉定糖代谢物。
, http://www.100md.com
Tab 1 HPLC/MS data of roxithromycin (RXM) and its metabolites (M1~M13) Compound
tR
/min
MS1
MS2
m/z(M+H)+
m/z (%)
m/z
m/z (%)
m/z
, http://www.100md.com
RXM
(9E)
30.3
837
679(100)
661
558
522
M7
(9Z)
19.4
837
679(100)
, 百拇医药
661
558
522
M3
(9E)
15.1
823
665(100)
647
558
522
M10
(9Z)
, http://www.100md.com
11.5
823
665(100)
647
558
522
M5
(9E)
11.8
809
651(100)
544
508
, 百拇医药
M12
(9Z)
10.3
809
651(100)
544
508
M2
(9E)
15.7
749
591(100)
558
, 百拇医药
540
434
M9
(9Z)
12.2
749
591(100)
558
540
434
M4
(9E)
12.3
, 百拇医药
735
577(100)
544
508
434
M11
(9Z)
10.7
735
577(100)
544
508
434
, http://www.100md.com
M6
(9E)
11.6
721
563(100)
494
434
M13
(9Z)
10.3
721
563(100)
494
, 百拇医药
434
M1
(9E)
15.1
679
558
540
522(100)
504
M8
(9Z)
11.7
679
, 百拇医药
558
540
522(100)
504
MS1: Full scan MS; MS2: Full scan MS/MS.3 代谢途径
综合以上的研究结果,推测罗红霉素在人体内的代谢途径见图2。
将同一加样胆汁样品(罗红霉素4 μg.ml-1)经方法2提取后所得溶液重复进样6次,计算仪器响应的重现性,罗红霉素峰面积的相对标准偏差(RSD)为3.1%,说明仪器定量的重现性良好。根据胆汁中各代谢物以SIM方式检测的色谱峰面积,
, 百拇医药
Fig 2 Proposed metabolic pathways of roxithromycin (RXM) in human.
估算各组分相对含量,结果见图3。通过与加样胆汁样品比较,求出胆汁样品中罗红霉素浓度为4.26 μg.ml-1。
讨论
ESI是一种软电离方式,利用ESI-MSn离子阱技术可在温和条件下获得待测物的准分子离子峰。MSn多级质谱可给出丰富的化合物分子的结构信息,特别由于其选择性强,碎片离子质谱图重现性好,使这项技术在未知化合物的推测中具有非常重要的意义。本文采用HPLC/MSn联用技术,进一步从色谱行为上确证了代谢产物, 并发现了发生构型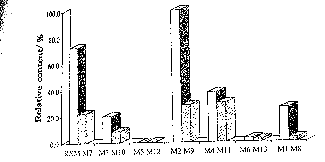
, 百拇医药
Fig 3 Relative contents of roxithromycin (RXM) and its metabolites (M1~M13) in human bile. Compounds with 9E configuration;
Compounds with 9E configuration; Compounds with 9Z configuration.
Compounds with 9Z configuration.
转化的代谢产物,丰富了对药物代谢产物立体选择性规律的认识。
本项研究结果初步表明在人胆汁中罗红霉素代谢产物的量远大于原形药,这与文献[2,3]报道的血浆及尿中的代谢情况有所不同。胆汁中罗红霉素原形药浓度占总代谢物的20%左右,罗红霉素及代谢物含量由多到少依次排列为:M2,RXM,M4,M11,M9,M1,M7,M3,M10,M6,M8,M13,M12,M5。值得注意的是,罗红霉素及其代谢物均可在体内发生几何异构化,(9Z)-与(9E)-异构体的浓度比值介于0.11~0.79之间,进一步的研究正在进行中。
, 百拇医药
基金项目:国家自然科学基金资助项目(39625025)
*联系人 Tel:(024)23843711-3445,Fax:(024)23891576,E-mail:zhongdf@inw.com.cn
参考文献
1 任淑萍,孟雅君.罗红霉素国内临床应用研究进展.中国临床药理学杂志,1997,13∶124
2 Koyama M, Tateno M, Shirotsuka M, et al. Absorption, metabolism and excretion of RU28965 in humans. Chemotherapy, 1988,36(Suppl 4)∶164
3 Shirotsuka M, Yamamoto T, Hirayama M, et al. High performance liquid chromatography of RU28965 and its metabolites in body fluid. Chemotherapy, 1988,36(Suppl 4)∶138
, 百拇医药
4 Esumi Y, Zin Y, Ban S, et al. Absorption, distribution, metabolism and excretion of RU 28965 in animals. Chemotherapy, 1988,36(Suppl 4)∶148
5 Young RA, Gonzalez JP, Sorkin EM. Roxithromycin. A review of its antibacterial activity, pharmacokinetic properties and clinical efficacy. Drugs, 1989,37∶8
6 Markham A, Faulds D. Roxithromycin. An update of its antimicrobial activity, pharmacokinetic properties and therapeutic use. Drugs, 1994,48∶297
收稿日期: 1998-04-10, 百拇医药(李雪庆 钟大放* 吴硕东1 王爱民 田蕾 于宏1)
单位:(沈阳药科大学药物代谢与药物动力学实验室,沈阳 110015; 1中国医科大学第二附属医院,沈阳 110001)
关键词:罗红霉素;代谢物;人胆汁;高效液相色谱-离子阱质谱法
药学学报990112.htm 摘要 目的:研究人胆汁中罗红霉素的代谢转化产物。方法:采用高效液相色谱-离子阱质谱法,对患者po罗红霉素后的胆汁样品进行了分析。结果:发现了13个代谢产物,分别为罗红霉素的(9Z)-异构体及其(9E)-,(9Z)-N-去甲基和N-双去甲基衍生物和(9E)-及(9Z)-脱克拉定糖衍生物,(9E)-和(9Z)-红霉素肟及其(9E)-和(9Z)-N-去甲基及N-双去甲基衍生物,其中9种为新发现的代谢物。结论:罗红霉素及其代谢物均可在体内发生几何异构化。
, 百拇医药
STUDIES ON METABOLITES OF ROXITHROMYCIN IN HUMAN BILE
Li Xueqing (Li XQ), Zhong Dafang (Zhong DF)*, Wu Shuodong (Wu SD)1,Wang Aimin (Wang AM), Tian Lei (Tian L) and Yu Hong (Yu H)1
(Laboratory of Drug Metabolism and Pharmacokinetics, Shenyang Pharmaceutical University,Shenyang 110015; 1The Second Affiliated Hospital, China Medical University, Shenyang 110001)
, 百拇医药
ABSTRACT AIM: To study the metabolites of roxithromycin (RXM) in the bile of a patient, who had received an oral dose of 150 mg RXM after gallbladder operation. METHODS: High-performance liquid chromatography/ion trap mass spectrometry was used to determinate RXM and its metabolites in human bile. The bile sample was collected, extracted with diethyl ether and separated on a C18 reversed-phase column with (+)ESI-MSn detection. RESULTS: RXM and its thirteen metabolites were identified in the sample based on reference substances and mass spectra. These include descladinose-RXM (M1), erythromycin-oxime (M2) and its N-mono- and N-didemethylated derivatives (M4 and M6), N-mono- and didemethylated derivatives of RXM (M3 and M5), as well as the (9Z)-epimeric isomers of RXM and all its above metabolites (M7~M13). The ratios of (9Z)- to (9E)-isomers were found to be between 0.11~0.79. The parent drug remained was about 20% of the total bile metabolites. CONCLUSION: The metabolic pathways of RXM observed in the human bile are therefore quite different to those in human plasma and urine. The identification of the isomerization of the oximes of RXM derivatives represents a novel biotransformation pathway.
, http://www.100md.com
KEY WORDS roxithromycin; metabolites; human bile; HPLC/MS
*Corresponding author
罗红霉素(RXM)化学名为(9E)-[O-[(2-甲氧基乙氧基)甲基]肟基]红霉素,属半合成大环内酯类抗生素。临床主要用于治疗呼吸道及泌尿道感染、皮肤和软组织感染等[1]。对罗红霉素代谢产物的分析和检测已有报道[2~6],在尿中检出4种代谢产物,分别为罗红霉素的N-去甲基和N-双去甲基衍生物、罗红霉素脱克拉定糖衍生物以及红霉素肟。尽管证明罗红霉素主要经胆汁排泄,但未见对胆汁中代谢产物的报道。近年来发展起来的LC/MS联用技术能直接分析溶液样品,特别适合分析复杂介质中极性强、难挥发或热不稳定的化合物,在药物代谢研究中得到了越来越广泛的应用。本文采用(+)ESI-MSn离子阱技术,对一名患者po罗红霉素后胆汁中罗红霉素的代谢物进行了定性分析,并用HPLC/MSn联用法对代谢物及其相对含量进行了初步研究。在实验中共检出13种代谢物,其中9种未见报道。
, 百拇医药
材料与方法
试剂与仪器 罗红霉素片(沈阳埃默药业有限公司);罗红霉素对照品(粗品,含量95.4%)及红霉素肟对照品(粗品,含量96.0%)由沈阳华泰药物研究所提供;其余化学品均为市售分析纯;流动相所用有机溶剂为色谱纯。
美国Finnigan公司LCQ型液相色谱-质谱联用仪,包括APCI(大气压化学电离)、ESI(电喷雾电离)源以及LCQ数据处理系统,并配有直接进样用注射泵和250 μl进样器;日本岛津公司LC-10AD泵,包括7125 Rheodyne进样阀。
胆汁样品收集 胆管结石患者(女性,60岁,肾功能正常,肝功能恢复正常)胆囊切除、胆管切开取石、T形管引流术后,于恢复稳定期po罗红霉素片150 mg(bid)。由T形引流管收集服药后1.5~5 h流出的胆汁,于冰箱-30℃冷冻保存,待测。
胆汁样品的前处理 方法1:取Sep-Pak C8固相萃取柱,用水3 ml、甲醇3 ml、水3 ml依次进行洗涤,待用。取胆汁样品0.5 ml,以蒸馏水0.5 ml稀释后,用微孔滤膜(0.45 μm)过滤。滤液以30 滴.min-1的速度通过上述已活化的Sep-Pak C8固相萃取柱。用水3 ml洗涤后,再用甲醇2 ml洗脱。洗脱液用于(+)ESI-MSn分析。方法2:另取胆汁样品0.5 ml,加入Na2CO3溶液(0.1 mol.L-1)100 μl及重蒸乙醚3 ml,涡流混合3 min,离心10 min。分取有机层,于40℃下氮气流吹干。残留物以流动相100 μl溶解,用于HPLC/MSn分析。
, 百拇医药
(+)ESI-MSn分析条件 离子源喷射电压:4.0 kV;毛细管温度:150℃;毛细管电压:27 V;鞘气(N2);流速:0.3 L.min-1;注射泵进样速度:10 μl.min-1;采集范围:m/z 150~1000。
样品的(+)ESI-MSn分析方法 取胆汁固相萃取洗脱液,用注射泵将其直接导入ESI离子源,选择正离子方式检测。先用全扫描一级质谱方式获得待测物的准分子离子峰[M+H]+,然后利用(+)ESI-MSn离子阱技术对准分子离子峰及其碎片离子峰进行多级质谱分析,获得相应的子离子质谱图。
HPLC-MSn分析条件 色谱柱:Kromasil C18不锈钢柱(5 μm粒径,200 mm×4.6 mm ID,天津凯德公司);流动相:甲醇―乙腈―水(含10 mmol.L-1醋酸铵)(10∶43∶47);流速:0.3 ml.min-1;柱温:20℃;进样量:20 μl。质谱参数设置:离子源喷射电压4.25 kV;毛细管温度180℃;毛细管电压30 V;鞘气流速0.75 L.min-1;辅助气流速0.15 L.min-1。采用全扫描一级质谱、选择离子检测(SIM)及选择离子二级全扫描质谱(full scan MS2) 3种方式同时测定。
, http://www.100md.com
结果
1 胆汁中代谢产物的(+)ESI-MSn分析
在(+)ESI-MS全扫描一级质谱条件下,测得胆汁中有一组罗红霉素相关物质的准分子离子峰,分别为m/z 837,823,749,735和679,其中m/z 837,823,679和749分别与罗红霉素及文献报道[2]的3个代谢产物(罗红霉素的N-去甲基衍生物、脱克拉定糖衍生物及红霉素肟)的质荷比相符,均为[M+H]+峰。根据报道的另一个代谢产物(罗红霉素的N-双去甲基衍生物,其分子量为808)及上述观察结果推测还可能存在红霉素肟的N-双去甲基衍生物(分子量为720)。本文采用全扫描检测时局部放大及选择离子检测的方法,观察到m/z 809,721质荷比处均有较弱的准分子离子峰[M+H]+存在。为进一步了解这些物质的质谱断裂规律,本文采用ESI-MSn离子阱技术分别对这7个准分子离子进行MS2级质谱分析。发现除m/z 679离子外,均有丢失中性碎片158 u的子离子产生,它们可能是由母离子脱去克拉定糖生成。对m/z 837,749进一步进行MS3级质谱分析,并与罗红霉素及红霉素肟同样条件下所得的各级质谱对照,质谱断裂规律完全一致,证明胆汁样品中存在罗红霉素及代谢物红霉素肟。根据文献报道及质谱断裂规律,判断m/z 823和809两准分子离子是罗红霉素N-去甲基和N-双去甲基代谢物,m/z 679为罗红霉素脱克拉定糖代谢物。新发现的m/z 735和721两准分子离子分别比红霉素肟少14和28个质量数,即分子中分别脱去1个及2个甲基,根据其质谱断裂情况及上述代谢物的质谱特征,可判断二者为红霉素肟N-去甲基和N-双去甲基代谢物。胆汁中各化合物相应的(+)ESI-MS2全扫描质谱图见图1。






, http://www.100md.com
2 胆汁中代谢物的HPLC/MSn色谱-质谱行为
在(+)ESI-MSn的研究基础上,本文选择m/z 837,823,809,749,735,721和679 7个离子进行HPLC/MSn分析。图1包括了胆汁样品经色谱分离后得到的总离子流色谱图和选择离子检测(SIM)色谱图。从各SIM色谱图观察,并经总离子流质谱和MS2级质谱确认,发现每个SIM色谱图中均出现一对MS1级和MS2级质谱完全相同的色谱峰。因为罗红霉素结构中具有一个(9E)-构型的肟醚结构,推测它很可能在代谢过程中发生异构化,生成(9Z)-异构体,因而出现两个色谱峰。本文考察了罗红霉素对照品,发现除在30.3 min保留时间的主峰外,在19.4 min处还有一个含量小于1%的小峰,其MS1级和MS2级质谱与罗红霉素完全相同,判断即为合成过程中引入的(9Z)-异构体(罗红霉素片剂中未检出该异构体);而胆汁中SIM方式检测m/z 837离子观察到的两色谱峰的保留时间与对照品中观察到的色谱峰一致,因而可认为19.4 min色谱峰对应的物质是罗红霉素的(9Z)-异构体代谢物。同理,通过红霉素肟对照品的研究,证明保留时间12.2及15.7 min分别为(9Z)-和(9E)-红霉素肟代谢物。推测其余各对代谢物也均为(9Z)-和(9E)-异构体代谢物,(9Z)-较(9E)-异构体先出峰。罗红霉素及其代谢产物的HPLC/MSn数据见表1。本文采用HPLC-ECD法对胆汁样品的色谱行为进行考察,发现质谱检测中m/z 679和749所对应的色谱峰在电化学检测器上都有响应,说明它们结构中的氨基糖没有发生变化,进一步证明m/z 679峰为罗红霉素脱克拉定糖代谢物。
, http://www.100md.com
Tab 1 HPLC/MS data of roxithromycin (RXM) and its metabolites (M1~M13) Compound
tR
/min
MS1
MS2
m/z(M+H)+
m/z (%)
m/z
m/z (%)
m/z
, http://www.100md.com
RXM
(9E)
30.3
837
679(100)
661
558
522
M7
(9Z)
19.4
837
679(100)
, 百拇医药
661
558
522
M3
(9E)
15.1
823
665(100)
647
558
522
M10
(9Z)
, http://www.100md.com
11.5
823
665(100)
647
558
522
M5
(9E)
11.8
809
651(100)
544
508
, 百拇医药
M12
(9Z)
10.3
809
651(100)
544
508
M2
(9E)
15.7
749
591(100)
558
, 百拇医药
540
434
M9
(9Z)
12.2
749
591(100)
558
540
434
M4
(9E)
12.3
, 百拇医药
735
577(100)
544
508
434
M11
(9Z)
10.7
735
577(100)
544
508
434
, http://www.100md.com
M6
(9E)
11.6
721
563(100)
494
434
M13
(9Z)
10.3
721
563(100)
494
, 百拇医药
434
M1
(9E)
15.1
679
558
540
522(100)
504
M8
(9Z)
11.7
679
, 百拇医药
558
540
522(100)
504
MS1: Full scan MS; MS2: Full scan MS/MS.3 代谢途径
综合以上的研究结果,推测罗红霉素在人体内的代谢途径见图2。
将同一加样胆汁样品(罗红霉素4 μg.ml-1)经方法2提取后所得溶液重复进样6次,计算仪器响应的重现性,罗红霉素峰面积的相对标准偏差(RSD)为3.1%,说明仪器定量的重现性良好。根据胆汁中各代谢物以SIM方式检测的色谱峰面积,

, 百拇医药
Fig 2 Proposed metabolic pathways of roxithromycin (RXM) in human.
估算各组分相对含量,结果见图3。通过与加样胆汁样品比较,求出胆汁样品中罗红霉素浓度为4.26 μg.ml-1。
讨论
ESI是一种软电离方式,利用ESI-MSn离子阱技术可在温和条件下获得待测物的准分子离子峰。MSn多级质谱可给出丰富的化合物分子的结构信息,特别由于其选择性强,碎片离子质谱图重现性好,使这项技术在未知化合物的推测中具有非常重要的意义。本文采用HPLC/MSn联用技术,进一步从色谱行为上确证了代谢产物, 并发现了发生构型

, 百拇医药
Fig 3 Relative contents of roxithromycin (RXM) and its metabolites (M1~M13) in human bile.
 Compounds with 9E configuration;
Compounds with 9E configuration; Compounds with 9Z configuration.
Compounds with 9Z configuration.转化的代谢产物,丰富了对药物代谢产物立体选择性规律的认识。
本项研究结果初步表明在人胆汁中罗红霉素代谢产物的量远大于原形药,这与文献[2,3]报道的血浆及尿中的代谢情况有所不同。胆汁中罗红霉素原形药浓度占总代谢物的20%左右,罗红霉素及代谢物含量由多到少依次排列为:M2,RXM,M4,M11,M9,M1,M7,M3,M10,M6,M8,M13,M12,M5。值得注意的是,罗红霉素及其代谢物均可在体内发生几何异构化,(9Z)-与(9E)-异构体的浓度比值介于0.11~0.79之间,进一步的研究正在进行中。
, 百拇医药
基金项目:国家自然科学基金资助项目(39625025)
*联系人 Tel:(024)23843711-3445,Fax:(024)23891576,E-mail:zhongdf@inw.com.cn
参考文献
1 任淑萍,孟雅君.罗红霉素国内临床应用研究进展.中国临床药理学杂志,1997,13∶124
2 Koyama M, Tateno M, Shirotsuka M, et al. Absorption, metabolism and excretion of RU28965 in humans. Chemotherapy, 1988,36(Suppl 4)∶164
3 Shirotsuka M, Yamamoto T, Hirayama M, et al. High performance liquid chromatography of RU28965 and its metabolites in body fluid. Chemotherapy, 1988,36(Suppl 4)∶138
, 百拇医药
4 Esumi Y, Zin Y, Ban S, et al. Absorption, distribution, metabolism and excretion of RU 28965 in animals. Chemotherapy, 1988,36(Suppl 4)∶148
5 Young RA, Gonzalez JP, Sorkin EM. Roxithromycin. A review of its antibacterial activity, pharmacokinetic properties and clinical efficacy. Drugs, 1989,37∶8
6 Markham A, Faulds D. Roxithromycin. An update of its antimicrobial activity, pharmacokinetic properties and therapeutic use. Drugs, 1994,48∶297
收稿日期: 1998-04-10, 百拇医药(李雪庆 钟大放* 吴硕东1 王爱民 田蕾 于宏1)