泰国产攀援鱼藤的异黄酮苷成分
作者:李典鹏 欧阳明安 Chaweewan Jansakwl1 杨崇仁2
单位:(中国科学院广西植物研究所,桂林 541006; 1泰国宋卡王子大学生理系,泰国宋卡 90112;2中国科学院昆明植物研究所, 昆明 650204)
关键词:攀援鱼藤;异黄酮苷;攀援鱼藤苷甲;攀援鱼藤苷乙
药学学报990110.htm摘要 目的: 对泰国产攀援鱼藤[Derris scandens (Roxb.) Benth]地上部分的化学成分进行分离、鉴定。方法: 采用各种层析色谱技术进行分离。从攀援鱼藤中分离得到2个化合物,用IR,UV,MS,1HNMR,13CNMR,2DNMR光谱鉴定化合物。结果: 经光谱鉴定化合物结构为: 4′-甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖基(1→6)]-β-D-葡萄吡喃糖苷(I)和4′,8-二甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖基(1→6)]-β-D-葡萄吡喃糖苷(II), 分别命名为攀援鱼藤苷甲(derriscanoside A)和攀援鱼藤苷乙(derriscanoside B)。结论: 化合物(I), (II)为新的异黄酮苷类化合物。
, http://www.100md.com
TWO ISOFLAVONOID GLYCOSIDES FROM DERRIS SCANDENS
Li Dianpeng(Li DP), Ouyang Mingan(Ouyang MA),Chaweewan Jansakwl1 and Yang Chongren(Yang CR)2
(Guangxi Institute of Botany, Chinese Academy of Sciences, Guilin 541006;
1Department of Physiology, Prince of Songkhla University, Hatyai, Songkhla 90112;
2Kunming Institute of Botany, Chinese Academy of Sciences, Kunming 650204)
, 百拇医药
ABSTRACT AIM: To investigate the chemical constituents of the aerial parts of Derris Scandens. METHODS: To isolate chemical constituent, solvent extraction together with column chromatography were used. IR, UV, MS, NMR and chemical methods were used to determine the structure of the isolated constituents. RESULTS: The structures of the two constituents obtained were elucidated as 4′-methoxy-isoflavone-7-O-[α-L-rhamnopyranosyl(1→6)]-β-D-glucopyranoside(I) and 4′,8-dimethoxy-isoflanvone-7-O-[α-L-rhamnopyranosyl(1→6)]-β-D-glucopyranoside(II) which were named derriscanoside A and derriscanoside B respectively. CONCLUSION: Compound (I) and compound (II) are two new isoflavonoid glycosides.
, http://www.100md.com
KEY WORDS Derris scandens; isoflavonoid glycoside; derriscanoside A; derriscanoside B
攀援鱼藤系豆科(Leguminosae)鱼藤属(Derris)植物,为攀援灌木,主要分布于热带、亚热带地区,如印度、斯里兰卡、泰国等。有杀虫和降血压的功效[1,2],印度植物化学家对印度不同地区产的攀援鱼藤进行了化学成分研究,从其脂溶性氯仿提取部位分离得到几种具结构特征的异黄酮[3,4],但其水溶性配糖体成分未见报道。泰国产攀援鱼藤水煮液的醋酸乙酯部位有很好的降血压功效,为追踪活性,对该部位的化学成分进行研究,通过硅胶柱色谱,反相硅胶(RP-8)柱色谱等,得到2个新的异黄酮苷类化合物,分别命名为攀援鱼藤苷甲(derriscanoside A)和攀援鱼藤苷乙(derriscanoside B)。
化合物I 淡黄色粉末,mp 115℃~117℃,Molish反应和Mg-HCl反应均呈阳性,紫外光下呈棕色荧光,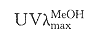 nm: 258,325(sh)呈典型的异黄酮紫外吸收;红外光谱数据显示有羟基(3410 cm-1,宽峰),羰基(1620 cm-1)及苷键(1055 cm-1,宽峰)。将I酸水解,TLC检查,与标准品对照表明有葡萄糖和鼠李糖存在,FAB-MS谱显示其分子量为576,根据元素分析及13CNMR, DEPT谱推定其分子式为C28H32O13,13CNMR给出了2个甲基、1个亚甲基、18个叔甲基及7个季碳信号;FAB-MS谱中给出分子离子峰m/z 576 M+,以及碎片离子峰267(M-162-147)-即失去1个葡萄糖和1个鼠李糖后的苷元碎片离子峰。13CNMR谱表明I为异黄酮
nm: 258,325(sh)呈典型的异黄酮紫外吸收;红外光谱数据显示有羟基(3410 cm-1,宽峰),羰基(1620 cm-1)及苷键(1055 cm-1,宽峰)。将I酸水解,TLC检查,与标准品对照表明有葡萄糖和鼠李糖存在,FAB-MS谱显示其分子量为576,根据元素分析及13CNMR, DEPT谱推定其分子式为C28H32O13,13CNMR给出了2个甲基、1个亚甲基、18个叔甲基及7个季碳信号;FAB-MS谱中给出分子离子峰m/z 576 M+,以及碎片离子峰267(M-162-147)-即失去1个葡萄糖和1个鼠李糖后的苷元碎片离子峰。13CNMR谱表明I为异黄酮
, 百拇医药
类化合物,δ 177.92为C-4羰基碳信号[5];1HNMR谱上有一组AA′BB′峰,δ 7.52(2H,d,J=8.5 Hz),6.99(2H,d,J=8.4 Hz)为C-4′有取代基的B环质子。I的苷元部分的13CNMR谱与文献报道的异黄酮苷元芒柄花素(Formononetin)基本相同[6]。13CNMR δ 55.80及1HNMR δ 3.76(3H,s)示有一甲氧基存在。13CNMR中δ 163.77(C-7),δ 159.05(C-4′)处于较低场,较一般的异黄酮其化学位移分别往低场移动约20 ppm,15 ppm,表明C-7,C-4′与氧相连,从NOESY谱中,我们观察到3′-H,5′-H与甲氧基的氢有空间相关点,证实甲氧基连在C-4′位,那么糖基一定取代在C-7位。1HNMR和13CNMR(表1)表明有一个β-D-葡萄吡喃糖信号,δ 5.05(1H,d,J=7.1 Hz葡萄糖1-H)和102.16,74.14,78.06,71.66,77.20,67.94;以及一α-L-鼠李吡喃糖信号δ 5.54(1H,brs,rha 1-Η),1.09(3H,d,J=6.0 Hz, rha 6-Η)和101.88,72.06,72.52,74.72,69.84,17.94。从13CNMR中我们看到葡萄糖的C-6信号δ 67.94向低场位移约5 ppm,表明末端鼠李糖与葡萄糖C-6相连,与已知物芦丁(Rudin)对照,二者糖部分信号基本相同[7]。1HNMR谱δ 7.13(dd,J=8.2,2.3,6-Η),这是因6-Η受邻位5-Η与间位8-Η偶合影响而形成的两个双重峰,1H-1H COSY谱中,5-H与6-H,5′-H与6′-H都有相关点,进一步证明我们结构推导的正确性,综上分析,推定化合物I的结构为4′-甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖基(1→6)]-β-D-葡萄吡喃糖苷(图1),命名为攀援鱼藤苷甲(derriscanoside A)。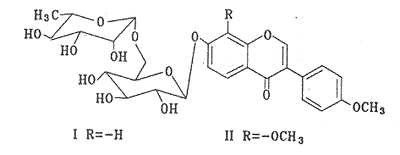
, 百拇医药
Fig 1 Structure of compounds I and II.
Tab 1 Chemical shifts of 13CNMR spectra of I and II C
I
II
C
I
II
2
155.41
153.41
Glu-1
, http://www.100md.com
102.16
100.68
3
125.64
123.05
2
74.14
71.69
4
177.92
174.70
3
78.06
, http://www.100md.com
76.55
5
128.20
120.17
4
71.66
69.76
6
117.20
114.06
5
77.20
75.66
, http://www.100md.com
7
163.23
153.63
6
67.94
66.35
8
105.13
137.04
rha-1
101.88
100.50
9
, http://www.100md.com
161.06
149.93
2
72.06
70.35
10
120.16
119.47
3
72.52
70.68
1′
125.32
, http://www.100md.com
123.66
4
74.72
73.24
2′
131.29
129.95
5
69.84
66.26
3′
114.67
113.58
, 百拇医药
6
17.94
17.65
4′
159.05
158.98
4′-OCH3
55.80
55.06
5′
114.67
113.58
8-OCH3
, 百拇医药
61.16
6′
131.29
129.95
化合物II 淡黄色晶体,mp 145℃~147℃,Molish和Mg-HCl反应均呈阳性,紫外光下呈棕色荧光,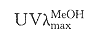 nm: 259,323(sh)呈典型异黄酮特征吸收,IR(KBr)cm-1显示有羟基(3400 cm-1,宽峰),羰基(1630 cm-1),苷键(1050 cm-1,宽峰),II酸水解TLC检出葡萄糖和鼠李糖,FAB-MS谱显示其分子量为606,根据元素分析及13CNMR, DEPT推定II的分子式为C29H34O14,其分子离子峰m/z 606。比较II和I的1HNMR和13CNMR谱,II较I多δ 61.61,3.92(3H,s)信号,即多1个甲氧基信号,这与II的分子量(606)比I分子量(576)大30(一个-OCH3)相吻合,II的C-8信号δ 137.04较I的C-8信号δ 105.13往低场位移约32 ppm,证明C-8位上氢被一甲氧基取代,从1HNMR中我们还注意到,6-H由I的2个双重峰δ 7.13(1H,dd,J=8.2,2.3 Hz)转为II的1个双重峰δ 7.32(1H,d,J=9.3 Hz)进一步证明C-8位上的H已被取代,因此推定II的结构为4′,8-二甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖(1→6)]-β-D-葡萄吡喃糖苷(图1),命名为攀援鱼藤苷乙(derriscanoside B)。实验部分
nm: 259,323(sh)呈典型异黄酮特征吸收,IR(KBr)cm-1显示有羟基(3400 cm-1,宽峰),羰基(1630 cm-1),苷键(1050 cm-1,宽峰),II酸水解TLC检出葡萄糖和鼠李糖,FAB-MS谱显示其分子量为606,根据元素分析及13CNMR, DEPT推定II的分子式为C29H34O14,其分子离子峰m/z 606。比较II和I的1HNMR和13CNMR谱,II较I多δ 61.61,3.92(3H,s)信号,即多1个甲氧基信号,这与II的分子量(606)比I分子量(576)大30(一个-OCH3)相吻合,II的C-8信号δ 137.04较I的C-8信号δ 105.13往低场位移约32 ppm,证明C-8位上氢被一甲氧基取代,从1HNMR中我们还注意到,6-H由I的2个双重峰δ 7.13(1H,dd,J=8.2,2.3 Hz)转为II的1个双重峰δ 7.32(1H,d,J=9.3 Hz)进一步证明C-8位上的H已被取代,因此推定II的结构为4′,8-二甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖(1→6)]-β-D-葡萄吡喃糖苷(图1),命名为攀援鱼藤苷乙(derriscanoside B)。实验部分
, http://www.100md.com
熔点用Koflar型显微溶点仪,温度未校正;IR用PE-577型光度计测定,KBr压片,UV用UV-210A光度计测定,MeOH为溶剂;MS用Finnigan-451质谱仪测定,FAB-,70 ev,1H,13CNMR在Bruker, AM-400超导核磁共振仪上测定,内标为TMS,溶剂分别为DMSO-d6,CD3OD;柱色谱用硅胶为青岛海洋化工厂产品。实验材料由泰国宋卡王子大学Chaweewan Jansakul博士提供并鉴定。
提取与分离
泰国产攀援鱼藤干燥地上部分的茎1 Kg用H2O煮3次,H2O煮液浓缩干燥得220 g,全部用H2O溶解后用EtOAc萃取5次,回收EtOAc,浓缩液得浸膏45 g,该部分经硅胶柱色谱,CHCl3―MeOH(20∶1~5∶1)梯度洗脱,洗脱物分成Fr 1~10个流份,Fr 3~4进行硅胶柱色谱,用CHCl3―MeOH(10∶1)洗脱,洗脱物再经RP-8柱色谱分离,洗脱溶剂为H2O―MeOH(1∶1),得化合物I(30 mg),化合物II(48 mg)。
, 百拇医药
鉴定
攀援鱼藤苷甲(I) 淡黄色粉末,mp 115℃~117℃,紫外光下有棕色荧光,分子式C28H32O13。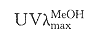 nm: 258,323(sh); IR(KBr) cm-1: 3410(-OH),2915,1630(=C=O),1370,1055(宽峰 苷键)。FAB MS m/z:576,276。 1HNMR(400 MHz,in DMSO-d6) δ: 8.39(s,2-H),8.5(d,J=9.0 Hz,5-H),7.52(d,J=8.5 Hz,2′,6′-H),7.22(d,J=2.3 Hz,8-H),7.13(dd,J=9.0,2.3 Hz,6-H),6.99(d,J=8.4 Hz,3′,5′-H),3.76(3H,s,OMe),1.09(3H,d,J=6.0 Hz,rha-6),5.05(1H,d,J=7.1 Hz,Glu-1),5.54(1H,brs,rha-1)。13CNMR谱数据见表1。
nm: 258,323(sh); IR(KBr) cm-1: 3410(-OH),2915,1630(=C=O),1370,1055(宽峰 苷键)。FAB MS m/z:576,276。 1HNMR(400 MHz,in DMSO-d6) δ: 8.39(s,2-H),8.5(d,J=9.0 Hz,5-H),7.52(d,J=8.5 Hz,2′,6′-H),7.22(d,J=2.3 Hz,8-H),7.13(dd,J=9.0,2.3 Hz,6-H),6.99(d,J=8.4 Hz,3′,5′-H),3.76(3H,s,OMe),1.09(3H,d,J=6.0 Hz,rha-6),5.05(1H,d,J=7.1 Hz,Glu-1),5.54(1H,brs,rha-1)。13CNMR谱数据见表1。
, 百拇医药
攀援鱼藤苷乙(II),淡黄色晶体,mp 145℃~147℃,紫外光下有棕色荧光。分子式C29H34O14,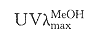 nm: 259,323(sh); IR(KBr) cm-1:3400(OH),2915,1630(=C=O),1370,1055(brs),810。FAB-MS m/z: 606,297。1HNMR(400 MHz,in CD3OD) δ: 8.46(1H,s,2-H),7.82(1H,d,J=9.0 Hz,5-H),7.52(2H,d,J=8.5 Hz,2′,6′-H),7.32(1H,d,J=9.0 Hz,6-H),6.99(2H,d,J=8.4 Hz,3′,5′-H),3.93(3H,s,8-OCH3),3.77(3H,s,4′-OCH3),1.07(3H,d,J=6.0 Hz,rhaH-6),5.07(1H,d,J=7.2 Hz,Glu-1),5.51(1H,brs,rha 1-H)。 13CNMR谱数据见表1。
nm: 259,323(sh); IR(KBr) cm-1:3400(OH),2915,1630(=C=O),1370,1055(brs),810。FAB-MS m/z: 606,297。1HNMR(400 MHz,in CD3OD) δ: 8.46(1H,s,2-H),7.82(1H,d,J=9.0 Hz,5-H),7.52(2H,d,J=8.5 Hz,2′,6′-H),7.32(1H,d,J=9.0 Hz,6-H),6.99(2H,d,J=8.4 Hz,3′,5′-H),3.93(3H,s,8-OCH3),3.77(3H,s,4′-OCH3),1.07(3H,d,J=6.0 Hz,rhaH-6),5.07(1H,d,J=7.2 Hz,Glu-1),5.51(1H,brs,rha 1-H)。 13CNMR谱数据见表1。
, 百拇医药
酸水解 分别取化合物I和II各约2 mg,加入MeOH 5 ml使溶解,再分别加入浓HCl 1 ml混合均匀,置于60℃水浴中3 h,水解完全,与葡萄糖和鼠李糖标准品共TLC,展开剂CHCl3―MeOH(5∶2.5),I和II均分别检出葡萄糖和鼠李糖。
致谢 中国科学院昆明植物研究所植物化学室仪器组测定所有光谱,刘玉清老师给予技术协助。
参考文献
1 吴征镒主编. 《西藏植物志》第二卷. 北京:科学出版社, 1985∶873
2 Srimannarana G, Subba Rao NV. New oxygen heterocylics from Derris Scandens and Mundulea suberosa. J Indian Chem Soc, 1974,11∶83
, http://www.100md.com
3 Falshaw CP, Harmer RA, Ollis WD, et al. Phytochmical examination of Derris Scandens. J Chem Soc(c), 1963,3∶374
4 Rao MN, Krupadanam GD, Srimannarayana G. Four isoflavones and two 3-aryl. coumarins from stens of Derris Scandens. Phytochemistry, 1994,37∶267
5 Park HH, Hakamatsuka T, Sankawa U, et al. Rapid metanolism of isoflavonoid in Elicitor-Treated cell suspension cultures of Pueraria lobata. Phytochemistry, 1995,38∶373
6 龚运淮. 天然有机化合物的13C核磁共振化学位移. 昆明: 云南科技出版社, 1986∶167
7 Rim MN, Le SBF, Paris N, et al. Flavonoids from Carthamus tinctorius flowers. Planta Med, 1992,58∶285
收稿日期: 1998-03-30, 百拇医药(李典鹏 欧阳明安 Chaweewan Jansakwl1 杨崇仁2)
单位:(中国科学院广西植物研究所,桂林 541006; 1泰国宋卡王子大学生理系,泰国宋卡 90112;2中国科学院昆明植物研究所, 昆明 650204)
关键词:攀援鱼藤;异黄酮苷;攀援鱼藤苷甲;攀援鱼藤苷乙
药学学报990110.htm摘要 目的: 对泰国产攀援鱼藤[Derris scandens (Roxb.) Benth]地上部分的化学成分进行分离、鉴定。方法: 采用各种层析色谱技术进行分离。从攀援鱼藤中分离得到2个化合物,用IR,UV,MS,1HNMR,13CNMR,2DNMR光谱鉴定化合物。结果: 经光谱鉴定化合物结构为: 4′-甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖基(1→6)]-β-D-葡萄吡喃糖苷(I)和4′,8-二甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖基(1→6)]-β-D-葡萄吡喃糖苷(II), 分别命名为攀援鱼藤苷甲(derriscanoside A)和攀援鱼藤苷乙(derriscanoside B)。结论: 化合物(I), (II)为新的异黄酮苷类化合物。
, http://www.100md.com
TWO ISOFLAVONOID GLYCOSIDES FROM DERRIS SCANDENS
Li Dianpeng(Li DP), Ouyang Mingan(Ouyang MA),Chaweewan Jansakwl1 and Yang Chongren(Yang CR)2
(Guangxi Institute of Botany, Chinese Academy of Sciences, Guilin 541006;
1Department of Physiology, Prince of Songkhla University, Hatyai, Songkhla 90112;
2Kunming Institute of Botany, Chinese Academy of Sciences, Kunming 650204)
, 百拇医药
ABSTRACT AIM: To investigate the chemical constituents of the aerial parts of Derris Scandens. METHODS: To isolate chemical constituent, solvent extraction together with column chromatography were used. IR, UV, MS, NMR and chemical methods were used to determine the structure of the isolated constituents. RESULTS: The structures of the two constituents obtained were elucidated as 4′-methoxy-isoflavone-7-O-[α-L-rhamnopyranosyl(1→6)]-β-D-glucopyranoside(I) and 4′,8-dimethoxy-isoflanvone-7-O-[α-L-rhamnopyranosyl(1→6)]-β-D-glucopyranoside(II) which were named derriscanoside A and derriscanoside B respectively. CONCLUSION: Compound (I) and compound (II) are two new isoflavonoid glycosides.
, http://www.100md.com
KEY WORDS Derris scandens; isoflavonoid glycoside; derriscanoside A; derriscanoside B
攀援鱼藤系豆科(Leguminosae)鱼藤属(Derris)植物,为攀援灌木,主要分布于热带、亚热带地区,如印度、斯里兰卡、泰国等。有杀虫和降血压的功效[1,2],印度植物化学家对印度不同地区产的攀援鱼藤进行了化学成分研究,从其脂溶性氯仿提取部位分离得到几种具结构特征的异黄酮[3,4],但其水溶性配糖体成分未见报道。泰国产攀援鱼藤水煮液的醋酸乙酯部位有很好的降血压功效,为追踪活性,对该部位的化学成分进行研究,通过硅胶柱色谱,反相硅胶(RP-8)柱色谱等,得到2个新的异黄酮苷类化合物,分别命名为攀援鱼藤苷甲(derriscanoside A)和攀援鱼藤苷乙(derriscanoside B)。
化合物I 淡黄色粉末,mp 115℃~117℃,Molish反应和Mg-HCl反应均呈阳性,紫外光下呈棕色荧光,
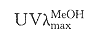 nm: 258,325(sh)呈典型的异黄酮紫外吸收;红外光谱数据显示有羟基(3410 cm-1,宽峰),羰基(1620 cm-1)及苷键(1055 cm-1,宽峰)。将I酸水解,TLC检查,与标准品对照表明有葡萄糖和鼠李糖存在,FAB-MS谱显示其分子量为576,根据元素分析及13CNMR, DEPT谱推定其分子式为C28H32O13,13CNMR给出了2个甲基、1个亚甲基、18个叔甲基及7个季碳信号;FAB-MS谱中给出分子离子峰m/z 576 M+,以及碎片离子峰267(M-162-147)-即失去1个葡萄糖和1个鼠李糖后的苷元碎片离子峰。13CNMR谱表明I为异黄酮
nm: 258,325(sh)呈典型的异黄酮紫外吸收;红外光谱数据显示有羟基(3410 cm-1,宽峰),羰基(1620 cm-1)及苷键(1055 cm-1,宽峰)。将I酸水解,TLC检查,与标准品对照表明有葡萄糖和鼠李糖存在,FAB-MS谱显示其分子量为576,根据元素分析及13CNMR, DEPT谱推定其分子式为C28H32O13,13CNMR给出了2个甲基、1个亚甲基、18个叔甲基及7个季碳信号;FAB-MS谱中给出分子离子峰m/z 576 M+,以及碎片离子峰267(M-162-147)-即失去1个葡萄糖和1个鼠李糖后的苷元碎片离子峰。13CNMR谱表明I为异黄酮, 百拇医药
类化合物,δ 177.92为C-4羰基碳信号[5];1HNMR谱上有一组AA′BB′峰,δ 7.52(2H,d,J=8.5 Hz),6.99(2H,d,J=8.4 Hz)为C-4′有取代基的B环质子。I的苷元部分的13CNMR谱与文献报道的异黄酮苷元芒柄花素(Formononetin)基本相同[6]。13CNMR δ 55.80及1HNMR δ 3.76(3H,s)示有一甲氧基存在。13CNMR中δ 163.77(C-7),δ 159.05(C-4′)处于较低场,较一般的异黄酮其化学位移分别往低场移动约20 ppm,15 ppm,表明C-7,C-4′与氧相连,从NOESY谱中,我们观察到3′-H,5′-H与甲氧基的氢有空间相关点,证实甲氧基连在C-4′位,那么糖基一定取代在C-7位。1HNMR和13CNMR(表1)表明有一个β-D-葡萄吡喃糖信号,δ 5.05(1H,d,J=7.1 Hz葡萄糖1-H)和102.16,74.14,78.06,71.66,77.20,67.94;以及一α-L-鼠李吡喃糖信号δ 5.54(1H,brs,rha 1-Η),1.09(3H,d,J=6.0 Hz, rha 6-Η)和101.88,72.06,72.52,74.72,69.84,17.94。从13CNMR中我们看到葡萄糖的C-6信号δ 67.94向低场位移约5 ppm,表明末端鼠李糖与葡萄糖C-6相连,与已知物芦丁(Rudin)对照,二者糖部分信号基本相同[7]。1HNMR谱δ 7.13(dd,J=8.2,2.3,6-Η),这是因6-Η受邻位5-Η与间位8-Η偶合影响而形成的两个双重峰,1H-1H COSY谱中,5-H与6-H,5′-H与6′-H都有相关点,进一步证明我们结构推导的正确性,综上分析,推定化合物I的结构为4′-甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖基(1→6)]-β-D-葡萄吡喃糖苷(图1),命名为攀援鱼藤苷甲(derriscanoside A)。

, 百拇医药
Fig 1 Structure of compounds I and II.
Tab 1 Chemical shifts of 13CNMR spectra of I and II C
I
II
C
I
II
2
155.41
153.41
Glu-1
, http://www.100md.com
102.16
100.68
3
125.64
123.05
2
74.14
71.69
4
177.92
174.70
3
78.06
, http://www.100md.com
76.55
5
128.20
120.17
4
71.66
69.76
6
117.20
114.06
5
77.20
75.66
, http://www.100md.com
7
163.23
153.63
6
67.94
66.35
8
105.13
137.04
rha-1
101.88
100.50
9
, http://www.100md.com
161.06
149.93
2
72.06
70.35
10
120.16
119.47
3
72.52
70.68
1′
125.32
, http://www.100md.com
123.66
4
74.72
73.24
2′
131.29
129.95
5
69.84
66.26
3′
114.67
113.58
, 百拇医药
6
17.94
17.65
4′
159.05
158.98
4′-OCH3
55.80
55.06
5′
114.67
113.58
8-OCH3
, 百拇医药
61.16
6′
131.29
129.95
化合物II 淡黄色晶体,mp 145℃~147℃,Molish和Mg-HCl反应均呈阳性,紫外光下呈棕色荧光,
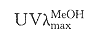 nm: 259,323(sh)呈典型异黄酮特征吸收,IR(KBr)cm-1显示有羟基(3400 cm-1,宽峰),羰基(1630 cm-1),苷键(1050 cm-1,宽峰),II酸水解TLC检出葡萄糖和鼠李糖,FAB-MS谱显示其分子量为606,根据元素分析及13CNMR, DEPT推定II的分子式为C29H34O14,其分子离子峰m/z 606。比较II和I的1HNMR和13CNMR谱,II较I多δ 61.61,3.92(3H,s)信号,即多1个甲氧基信号,这与II的分子量(606)比I分子量(576)大30(一个-OCH3)相吻合,II的C-8信号δ 137.04较I的C-8信号δ 105.13往低场位移约32 ppm,证明C-8位上氢被一甲氧基取代,从1HNMR中我们还注意到,6-H由I的2个双重峰δ 7.13(1H,dd,J=8.2,2.3 Hz)转为II的1个双重峰δ 7.32(1H,d,J=9.3 Hz)进一步证明C-8位上的H已被取代,因此推定II的结构为4′,8-二甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖(1→6)]-β-D-葡萄吡喃糖苷(图1),命名为攀援鱼藤苷乙(derriscanoside B)。实验部分
nm: 259,323(sh)呈典型异黄酮特征吸收,IR(KBr)cm-1显示有羟基(3400 cm-1,宽峰),羰基(1630 cm-1),苷键(1050 cm-1,宽峰),II酸水解TLC检出葡萄糖和鼠李糖,FAB-MS谱显示其分子量为606,根据元素分析及13CNMR, DEPT推定II的分子式为C29H34O14,其分子离子峰m/z 606。比较II和I的1HNMR和13CNMR谱,II较I多δ 61.61,3.92(3H,s)信号,即多1个甲氧基信号,这与II的分子量(606)比I分子量(576)大30(一个-OCH3)相吻合,II的C-8信号δ 137.04较I的C-8信号δ 105.13往低场位移约32 ppm,证明C-8位上氢被一甲氧基取代,从1HNMR中我们还注意到,6-H由I的2个双重峰δ 7.13(1H,dd,J=8.2,2.3 Hz)转为II的1个双重峰δ 7.32(1H,d,J=9.3 Hz)进一步证明C-8位上的H已被取代,因此推定II的结构为4′,8-二甲氧基-异黄酮-7-O-[α-L-鼠李吡喃糖(1→6)]-β-D-葡萄吡喃糖苷(图1),命名为攀援鱼藤苷乙(derriscanoside B)。实验部分, http://www.100md.com
熔点用Koflar型显微溶点仪,温度未校正;IR用PE-577型光度计测定,KBr压片,UV用UV-210A光度计测定,MeOH为溶剂;MS用Finnigan-451质谱仪测定,FAB-,70 ev,1H,13CNMR在Bruker, AM-400超导核磁共振仪上测定,内标为TMS,溶剂分别为DMSO-d6,CD3OD;柱色谱用硅胶为青岛海洋化工厂产品。实验材料由泰国宋卡王子大学Chaweewan Jansakul博士提供并鉴定。
提取与分离
泰国产攀援鱼藤干燥地上部分的茎1 Kg用H2O煮3次,H2O煮液浓缩干燥得220 g,全部用H2O溶解后用EtOAc萃取5次,回收EtOAc,浓缩液得浸膏45 g,该部分经硅胶柱色谱,CHCl3―MeOH(20∶1~5∶1)梯度洗脱,洗脱物分成Fr 1~10个流份,Fr 3~4进行硅胶柱色谱,用CHCl3―MeOH(10∶1)洗脱,洗脱物再经RP-8柱色谱分离,洗脱溶剂为H2O―MeOH(1∶1),得化合物I(30 mg),化合物II(48 mg)。
, 百拇医药
鉴定
攀援鱼藤苷甲(I) 淡黄色粉末,mp 115℃~117℃,紫外光下有棕色荧光,分子式C28H32O13。
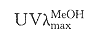 nm: 258,323(sh); IR(KBr) cm-1: 3410(-OH),2915,1630(=C=O),1370,1055(宽峰 苷键)。FAB MS m/z:576,276。 1HNMR(400 MHz,in DMSO-d6) δ: 8.39(s,2-H),8.5(d,J=9.0 Hz,5-H),7.52(d,J=8.5 Hz,2′,6′-H),7.22(d,J=2.3 Hz,8-H),7.13(dd,J=9.0,2.3 Hz,6-H),6.99(d,J=8.4 Hz,3′,5′-H),3.76(3H,s,OMe),1.09(3H,d,J=6.0 Hz,rha-6),5.05(1H,d,J=7.1 Hz,Glu-1),5.54(1H,brs,rha-1)。13CNMR谱数据见表1。
nm: 258,323(sh); IR(KBr) cm-1: 3410(-OH),2915,1630(=C=O),1370,1055(宽峰 苷键)。FAB MS m/z:576,276。 1HNMR(400 MHz,in DMSO-d6) δ: 8.39(s,2-H),8.5(d,J=9.0 Hz,5-H),7.52(d,J=8.5 Hz,2′,6′-H),7.22(d,J=2.3 Hz,8-H),7.13(dd,J=9.0,2.3 Hz,6-H),6.99(d,J=8.4 Hz,3′,5′-H),3.76(3H,s,OMe),1.09(3H,d,J=6.0 Hz,rha-6),5.05(1H,d,J=7.1 Hz,Glu-1),5.54(1H,brs,rha-1)。13CNMR谱数据见表1。, 百拇医药
攀援鱼藤苷乙(II),淡黄色晶体,mp 145℃~147℃,紫外光下有棕色荧光。分子式C29H34O14,
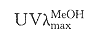 nm: 259,323(sh); IR(KBr) cm-1:3400(OH),2915,1630(=C=O),1370,1055(brs),810。FAB-MS m/z: 606,297。1HNMR(400 MHz,in CD3OD) δ: 8.46(1H,s,2-H),7.82(1H,d,J=9.0 Hz,5-H),7.52(2H,d,J=8.5 Hz,2′,6′-H),7.32(1H,d,J=9.0 Hz,6-H),6.99(2H,d,J=8.4 Hz,3′,5′-H),3.93(3H,s,8-OCH3),3.77(3H,s,4′-OCH3),1.07(3H,d,J=6.0 Hz,rhaH-6),5.07(1H,d,J=7.2 Hz,Glu-1),5.51(1H,brs,rha 1-H)。 13CNMR谱数据见表1。
nm: 259,323(sh); IR(KBr) cm-1:3400(OH),2915,1630(=C=O),1370,1055(brs),810。FAB-MS m/z: 606,297。1HNMR(400 MHz,in CD3OD) δ: 8.46(1H,s,2-H),7.82(1H,d,J=9.0 Hz,5-H),7.52(2H,d,J=8.5 Hz,2′,6′-H),7.32(1H,d,J=9.0 Hz,6-H),6.99(2H,d,J=8.4 Hz,3′,5′-H),3.93(3H,s,8-OCH3),3.77(3H,s,4′-OCH3),1.07(3H,d,J=6.0 Hz,rhaH-6),5.07(1H,d,J=7.2 Hz,Glu-1),5.51(1H,brs,rha 1-H)。 13CNMR谱数据见表1。, 百拇医药
酸水解 分别取化合物I和II各约2 mg,加入MeOH 5 ml使溶解,再分别加入浓HCl 1 ml混合均匀,置于60℃水浴中3 h,水解完全,与葡萄糖和鼠李糖标准品共TLC,展开剂CHCl3―MeOH(5∶2.5),I和II均分别检出葡萄糖和鼠李糖。
致谢 中国科学院昆明植物研究所植物化学室仪器组测定所有光谱,刘玉清老师给予技术协助。
参考文献
1 吴征镒主编. 《西藏植物志》第二卷. 北京:科学出版社, 1985∶873
2 Srimannarana G, Subba Rao NV. New oxygen heterocylics from Derris Scandens and Mundulea suberosa. J Indian Chem Soc, 1974,11∶83
, http://www.100md.com
3 Falshaw CP, Harmer RA, Ollis WD, et al. Phytochmical examination of Derris Scandens. J Chem Soc(c), 1963,3∶374
4 Rao MN, Krupadanam GD, Srimannarayana G. Four isoflavones and two 3-aryl. coumarins from stens of Derris Scandens. Phytochemistry, 1994,37∶267
5 Park HH, Hakamatsuka T, Sankawa U, et al. Rapid metanolism of isoflavonoid in Elicitor-Treated cell suspension cultures of Pueraria lobata. Phytochemistry, 1995,38∶373
6 龚运淮. 天然有机化合物的13C核磁共振化学位移. 昆明: 云南科技出版社, 1986∶167
7 Rim MN, Le SBF, Paris N, et al. Flavonoids from Carthamus tinctorius flowers. Planta Med, 1992,58∶285
收稿日期: 1998-03-30, 百拇医药(李典鹏 欧阳明安 Chaweewan Jansakwl1 杨崇仁2)