五味子的环二肽及其合成
作者:汪有初 周俊 谭宁华 丁中涛 江芯
单位:(中国科学院昆明植物研究所植物化学开放研究实验室,昆明 650204)
关键词:北五味子;五味子科;环二肽;合成
药学学报990105.htm 摘要 目的:研究五味子中的环肽成分。方法:用薄层色谱,硅胶及反向RP-18硅
胶柱层析色谱和谱学方法。结果:分离到3个天然的环二肽及由3个环二肽组成的一个混
合物并鉴定为环(亮-脯)(1),环(苯丙-脯)(2)和环(苯丙-亮)(3),环(苯丙-缬)(4),环(苯
丙-异亮)(5),环(苯丙-苯丙)(6),另外,合成了14个环二肽类似物。结论:首次从五味子
, 百拇医药
科植物北五味子中分离到环肽。环二肽2,6~8,14~20,经活性筛选表明,2,16及18有轻
微的钙拮抗效应,19及20显示出增强高钾所致收缩效应。其它环二肽及它们的活性筛选工
作正在进行中。
CYCLIC DIPEPTIDES FROM SCHIZANDRA
CHINENSIS AND THEIR SYNTHESES
Wang Youchu(Wang YC), Zhou Jun(Zhou J), Tan Ninghua(Tan NH),Ding Zhongtao(Ding ZT) and Jiang Xin(Jiang X)
(Laboratory of Phytochemistry, Kunming Institute of Botany,Chinese Academy of Sciences, Kunming 650204)
, 百拇医药
ABSTRACT AIM: To investigate cyclopeptides from the fruits of S.
chinensis. METHODS: Use thin layer chromatography, repeated silica gel
and RP-18 column chromatography together with spectra as well as synthetic
methods. RESULTS: Three naturally occurring cyclic dipeptides and a
mixture composed of three other new naturally occurring cyclic dipeptides
, 百拇医药
were obtained. Their structures were determined as cyclo-(leucyl-prolyl)
(1), cyclo-(phenyl-alanyl-prolyl) (2), cyclo-(phenylalanyl-leucyl) (3),cyclo-(phenylalanyl-valyl) (4), cyclo-(phenylalanyl-isoleucyl) (5) and
cyclo-(phenylalanyl-phenylalanyl) (6). In addition, fourteen analogous
cyclic peptides (7~20) were synthesized. CONCLUSION: Cyclopeptides were
isolated from S.chinensis (Schizandraceae) for the first time. The
, 百拇医药
bioactivity of some cyclic dipeptides on the contraction of rabbit aorta
strips with KCl (40 mmol.L-1) depolarization was tested. Cyclic
dipeptides 2, 6 and 18 showed slight calcium antagonism and 19, 20
can increase the contractile effect in high concentration of potassium.
Studies on the bioactivities of other cyclic dipeptides are in progress.
, 百拇医药
KEY WORDS schizandra chinensis; schizandraceae; cyclic peptides;
synthesis
北五味子(Schizandra chinensis Baill)的干燥果实为中药五味子的主要药材,功效甚广。用于肺喘虚咳,心悸失眠诸病[1]。化学成分研究比较深入。已报道的有
单萜、倍半萜、有机酸等。近年由于该药所含木脂素有很好的治疗肝炎功效,因而发
现近30个木脂素成分[2],如五味子素(schizandrin)、去氧五味子素
(deoxyschizandrin)和五味子醇(schizandrol)等。
, 百拇医药
从北五味子果实甲醇提取物的乙酸乙酯部位经正、反相色谱分离鉴定了3个环
二肽,即环(亮-脯)(1),环(苯丙-脯)(2)和环(苯丙-亮)(3)和一个由3个环二肽组成
的混合物,即环(苯丙-缬)(4),环(苯丙-异亮)(5)和环(苯丙-苯丙)(6)。这3个环二
肽组成的混合物由于量少,未能分离得到纯品。故在初步推定其结构后,合成了这3个
环二肽。用由这3个合成环二肽的混合物与分离的环二肽混合物进行MS及HPLC比较,二者是吻合的,故得以证明。在五味子科发现环肽尚属首次。
环二肽(cyclic dipeptides)有多种生物活性[3~5]。参照Ueda和Cook[6,7]
, 百拇医药
方法本文合成了北五味子中的6个环二肽和14个其它环二肽(共20个),它们是:环(甘
-脯)(7)[8],环(丙-脯)(8)[5],环(缬-脯)(9)[10],环(异亮-脯)(10)[11],环
(丝-脯)(11),环(苏-脯)(12),环(N-甲色-脯)(13),环(酪-酪)(14),环(亮-亮)
(15)[9],环(异亮-异亮)(16)[10],环(缬-缬)(17)[10],环(蛋-蛋)(18),环
(丙-丙)(19)[6],环(脯-脯)(20)[6],其中11~14,18是新化合物。其结构
, 百拇医药
(图1)经波谱鉴定。环二肽2,6~8,14~20经活性筛选表明,2,16及18随着浓
度的增加,具轻微的钙拮抗效应。19及20显示增强高钾所致收缩效应。其它环二
肽以及其它活性的筛选工作正在进行中。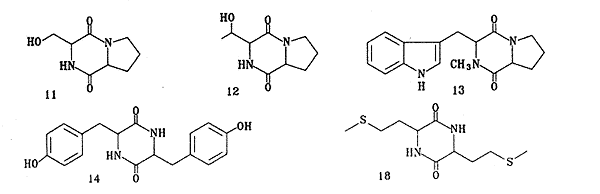
Fig 1 Structures of new compounds 11~14, 18.
实验部分
熔点为Koffler显微熔点仪测定,温度未校正。旋光用Horiba Sepa-300旋光测
定仪测定。紫外光谱用岛津UV-210A型紫外光谱仪。红外光谱用Perkin-Elmer 577
, 百拇医药
型红外光谱仪(KBr压片)。核磁共振谱用Bruker AM-400(400 MHz)和DRX-500(500
MHz)型核磁共振仪(氘代溶剂峰作为内标)。EI与FAB-MS用VG AutoSpec-3000型质
谱仪测定。高效液相色谱用岛津LC-4A型仪器(色谱柱:partisil ODS-2 alltech
4.6×250 mm;溶剂系统:CH3CN―H2O(3∶7),流速:0.4 ml.min-1;紫外检测,波长:
225 nm)。
五味子生药购自北京海淀区中心药店。
1 提取分离
, http://www.100md.com
五味子干果实9.8 kg经粉碎后,用工业甲醇回流提取4次,每次5 h。减压浓缩得
浸膏3150 g。该浸膏悬浮于水中,依次用石油醚、乙酸乙酯、正丁醇萃取。乙酸乙酯
部分浓缩得180 g,经硅胶柱(200~300目)色谱,用氯仿―甲醇(0~30%)依次洗脱,分
成4个部分,各部分经TLC检测,显环肽阳性反应部分进一步经硅胶H和RP-18反复色谱
分离,得到3个单体化合物1(38 mg),2(25 mg),3(22 mg)和1个由化合物4,5,6组成的
混合物(9 mg)。
2 鉴定
化合物1 针状结晶,mp 155~156℃,[α]11.7D -71.25°(CHCl3,0.4),茚三酮
, 百拇医药
显阴性,分子式为C11H18N2O2(m/z 210.1359, 1.0 mu)。IR(KBr) cm-1:3300,1650。1HNMR(CDCl3,δ):5.79(1H,br.s,NH),4.10(1H,t,J=8.0 Hz,α-Hpro),4.00(1H,dd,J=3.4,9.4 Hz,α-Hleu),3.63(2H,m,δ-Hpro),2.33(1H,m,β-Hpro),2.05(3H,m,β-Hpro,β-Hleu,γ-Hpro),1.89(1H,m,γ-Hpro),1.72(1H,m,γ-Hleu),1.50(1H,m,β-Hleu),0.98(3H,d,J=6.5 Hz,δ-Hleu),0.92(3H,d,J=3.7 Hz,δ-Hleu)。13CNMR(CDCl3,δ):170.0(CO),166.2(CO),59.0(CH,α-Cpro),53.5(CH,α-Cleu),45.5(CH2,δ-Cpro),38.8(CH2,β-Cleu),28.2(CH2,β-Cpro),24.8
1.0 mu)。IR(KBr) cm-1:3300,1650。1HNMR(CDCl3,δ):5.79(1H,br.s,NH),4.10(1H,t,J=8.0 Hz,α-Hpro),4.00(1H,dd,J=3.4,9.4 Hz,α-Hleu),3.63(2H,m,δ-Hpro),2.33(1H,m,β-Hpro),2.05(3H,m,β-Hpro,β-Hleu,γ-Hpro),1.89(1H,m,γ-Hpro),1.72(1H,m,γ-Hleu),1.50(1H,m,β-Hleu),0.98(3H,d,J=6.5 Hz,δ-Hleu),0.92(3H,d,J=3.7 Hz,δ-Hleu)。13CNMR(CDCl3,δ):170.0(CO),166.2(CO),59.0(CH,α-Cpro),53.5(CH,α-Cleu),45.5(CH2,δ-Cpro),38.8(CH2,β-Cleu),28.2(CH2,β-Cpro),24.8
, 百拇医药
(CH,γ-Cleu),23.2(CH3,δ-Cleu),22.8(CH2,γ-Cpro),21.3(CH3,δ-Cleu)。
化合物2 白色粉末,mp 138.5~139℃,[α]11.6D -192.59°(CHCl3,c
0.135)。茚三酮显阴性,分子式为C14H16N2O2(m/z 244.1200, 1.2 mu)。
1.2 mu)。
IR(KBr) cm-1:3300,1650。1HNMR(CDCl3,δ):7.27(5H,m),5.61(1H,br.s,NH),4.25(1H,dd,J=3.6,10.7 Hz,α-Hphe),4.06(1H,t,J=7.3 Hz,α-Hpro),3.59
, 百拇医药
(1H,m,β-Hphe),3.59(2H,m,δ-Hpro),2.75(1H,dd,J=10.7,14.4 Hz,β-Hphe),2.32(1H,m,β-Hpro),1.98(2H,m,γ-Hpro),1.89(1H,m,β-Hpro)。13CNMR
(CDCl3,δ):169.3(CO),165.1(CO),136.0(γ-Cphe),129.3(δ-Cphe),129.1
(ε-Cphe),127.6(ξ-Cphe),59.2(CH,α-Cpro),56.2(CH,α-Cphe),45.5
, 百拇医药
(CH2,δ-Cpro),36.9(CH2,β-Cphe),28.4(CH2,β-Cpro),22.5(CH2,γ-Cpro)。
化合物3 白色粉末,mp 261~263℃,[α]25D +21.0°(CH3OH,c 0.6),茚三酮显阴性,分子式为C15H20N2O2(m/z 260.1518, 1.7 mu)。IR(KBr)
1.7 mu)。IR(KBr)
cm-1:3300,1650。1HNMR(CD3OD,δ):7.25(5H,m),4.30(1H,t,J=4.6 Hz),3.65(1H,dd,J=4.2,10.8 Hz),3.26(1H,m),2.93(1H,dd,J=4.8,13.6 Hz),1.41(1H,m),0.84(2H,m),0.72(3H,d,J=6.6 Hz),0.67(3H,d,J=6.6 Hz)。
, http://www.100md.com
13CNMR(CD3OD,δ):170.6(CO),169.0(CO),136.8(C),131.8(CH),129.7
(CH),128.5(CH),57.5(CH),54.2(CH),45.3(CH2),40.3(CH2),24.7(CH),23.3(CH3),21.5(CH3)。
混合物 白色粉末,茚三酮显阴性,由于量少(9 mg),未分离。在HPLC
上有3个峰,保留时间分别为28.7,46.1及51.9 min。从EI质谱分析为分子量
246,260及294的3个环二肽组成的混合物,初步判定为环(苯丙-缬),环
, 百拇医药
(苯丙-异亮)和环(苯丙-苯丙)。我们合成了这3个化合物,将这3个化合物
及混和后分别做HPLC,EI质谱及高分辨EI质谱,发现保留时间、分子量和
分子式与天然混合物完全一致(表1)。
3 环二肽(1~20)的合成
参照Ueda[6]方法,环二肽1~5及7~13合成通法如下:
在L-氨基酸(20 mmol)的无水甲醇溶液中,于-10℃缓慢滴加亚硫酰氯
(27.8 mmol),在室温下搅拌2 d后,减压除去溶剂得无色或淡黄色油状物。
此油状物为L-氨基酸甲酯盐酸盐,无需纯化,直接用于反应。
, 百拇医药
Tab 1 HPLC retention time, EI-MS and HREI-MS of natural
and synthetic mixtures
Natural mixture
Synthetic mixture
4
5
6
4
5
6
Retention time
, http://www.100md.com
28.8
46.0
51.8
28.7
46.1
51.9
EI-MS m/z/%
294(22),260(32),246(54),204(30),175(26),155(20),141(32),127(47),120(31),113(44),99(26),91(100),77(22),72(28),65(31),57(40)
294(40),260(10),246(92),204(31),175(41),155(35),141(10),127(72),120(42),113(44),99(35),91(100),77(27),72(63),65(35),57(35)
, 百拇医药
HR-EI-MS
246.1372
( ,-0.3 mu)
,-0.3 mu)
260.1530
( ,-0.5 mu)
,-0.5 mu)
294.1371
( ,-0.3 mu)
,-0.3 mu)
246.1366
, 百拇医药 ( ,0.2 mu)
,0.2 mu)
260.1520
( ,0.4 mu)
,0.4 mu)
294.1369
( ,-0.1 mu)
,-0.1 mu)
将L-氨基酸(5 mmol),NaHCO3(10 mmol)溶于蒸馏水(10 ml),滴加苄氧酰
氯(6 mmol)的二氧六环溶液(10 ml)。反应混合物在室温搅拌2 d后,减压除去
, 百拇医药
溶剂,加蒸馏水(10 ml)稀释,用乙酸乙酯(10 ml)萃取。水层用0.5 mol.L-1的
柠檬酸酸化至pH 5左右,然后再用乙酸乙酯(30 ml)分别萃取3次,合并萃取物,无水硫酸钠干燥,减压蒸馏得油状物。将油状物经柱色谱分离得白色粉末。此
粉未经负离子FAB-MS证实为N-苄氧羰基-L-氨基酸。将上述的L-氨基酸甲酯
(2.7 mmol),N-苄氧羰基-L-氨基酸和三乙胺(2.7 mmol)混合于二氯甲烷
(10 ml)中,在0℃反应4 h,然后在室温反应过夜,过滤,减压除去溶剂,将残
余物溶于乙酸乙酯,依次用2%HCl,5%NaHCO3和水洗,无水硫酸钠干燥。减压
, http://www.100md.com
蒸馏后,在硅胶柱上纯化得白色粉末。将此粉末溶于甲醇(5 ml),加10%钯炭
催化下氢解,TLC监测反应,待反应毕,过滤除去催化剂,减压除去溶剂,残余物
经硅胶柱色谱纯化得环二肽。
参照Cook[7]方法,环二肽6,14~20合成通法如下:将L-氨基酸溶于无水
乙二醇中,加热回流24 h,冷却析出固体,将固体在乙醇中重结晶或硅胶柱色谱
得环二肽。结果见表2。
将L-氨基酸(5 mmol),NaHCO3(10 mmol)溶于蒸馏水(10 ml),滴加苄氧酰氯
(6 mmol)的二氧六环溶液(10 ml)。反应混合物在室温搅拌2 d后,减压除去溶
, http://www.100md.com
剂,加蒸馏水(10 ml)稀释,用乙酸乙酯(10 ml)萃取。水层用0.5 mol.L-1的柠檬
酸酸化至pH 5左右,然后再用乙酸乙酯(30 ml)分别萃取3次,合并萃取物,无水硫
酸钠干燥,减压蒸馏得油状物。将油状物经柱色谱分离得白色粉末。此粉未经负
离子FAB-MS证实为N-苄氧羰基-L-氨基酸。将上述的L-氨基酸甲酯(2.7 mmol),N-苄氧羰基-L-氨基酸和三乙胺(2.7 mmol)混合于二氯甲烷(10 ml)中,在0℃反
应4 h,然后在室温反应过夜,过滤,减压除去溶剂,将残余物溶于乙酸乙酯,依次
用2%HCl,5%NaHCO3和水洗,无水硫酸钠干燥。减压蒸馏后,在硅胶柱上纯化得白
, http://www.100md.com
色粉末。将此粉末溶于甲醇(5 ml),加10%钯炭催化下氢解,TLC监测反应,待反
应毕,过滤除去催化剂,减压除去溶剂,残余物经硅胶柱色谱纯化得环二肽。
参照Cook[7]方法,环二肽6,14~20合成通法如下:将L-氨基酸溶于无水
乙二醇中,加热回流24 h,冷却析出固体,将固体在乙醇中重结晶或硅胶柱色
谱得环二肽。结果见表2。Tab 2 Results of the synthesized cyclic dipeptides Compds
Form
Yield
/%
, 百拇医药
MP
/℃
[α]D°
EI-MS
/70 ev
m/z(%)
HR-EI-MS
/70 ev
calc.
1HNMR
13CNMR
11
, 百拇医药
Needle
crystal
89.1
-
-118.59
(CH3OH,c 0.39)
184[M]+
(6)
184.0833
(184.0848)
4.23(1H,m),4.16(1H,m),3.90(2H,m),3.58(1H,m),3.33(1H,m),2.31(1H,m),1.96(3H,m)
, 百拇医药
184.2(CO),178.8(CO),74.1(CH2),72.6(CH),70.6(CH),58.6(CH2),41.9(CH2),35.6(CH2)
12
Needle
crystal
85.2
-
-117.60
(CH3OH,c 0.304)
199
, http://www.100md.com [M+1]+
(21)
198.1011
(198.1004)
7.35(1H,NH,br.s),4.24
(1H,m),4.09(1H,m),4.00(1H,br.s),3.90(1H,m),3.55(1H,m),3.48(1H,m),2.30(1H,m),1.99(2H,m),1.87(1H,m),1.31(3H,d,J=6.5 Hz)
180.1(CO),175.3(CO),75.3(CH),69.5(CH),69.1(CH),55.0(CH2),38.2(CH2),32.2(CH2),29.7(CH3)
, http://www.100md.com
13
Needle
crystal
73.5
-
+77.26
(CH3OH,c 0.288)
297[M]+
(41)
297.1456
(297.1477)
9.82(1H,NH,br.s),8.40
, http://www.100md.com
(1H,d,J=8.0 Hz),8.06
(1H,m),7.91(1H,m),7.82
(1H,m),7.64(1H,m),5.02
(1H,br.s),4.48(2H,m),4.17(1H,m),4.02(1H,m),3.89(3H,s),3.69(1H,m),2.44(1H,m),2.05(1H,m),1.45(1H,m),0.54(1H,m)
166.4(CO),164.1(CO),135.8(C),127.2(C),123.8(CH),122.1(CH
×2),111.0(CH×2),107.8(C),63.1(CH),59.0(CH),44.4(CH2),32.2(CH3),28.2(CH2),27.2(CH2),20.4(CH2)
, 百拇医药
14
White
powder
58
280~282.5
-
326[M]+
(12)
326.1260
(326.1267)
11.39(br.s,OH),9.16(s,NH),7.24(4H×2,m),4.50(1H×2,m),3.29(1H×2,m),2.73(1H×2,m)
, http://www.100md.com
168.8(CO×2),159.2
(C×2),133.1(CH×2),128.8(CH×2),117.6
(C×2),58.9(CH×2),41.9(CH2×2)
18
White
powder
54.6
228~228.5
-
262[M]+
(49)
, 百拇医药
262.0805
(262.0810)
8.10(NH,s),4.32(1H×2,m),2.15(2H×2,m),2.20
(2H×2),1.90(3H×2,s)
169.9(CO×2),60.3
(C×2),31.0(CH2×2),30.1(CH2×2),16.9(CH3×2)
*联系人现址:国家医药管理局上海医药工业研究院新药研究室,上海 200437。Tel:(021)65442731-22, Fax:(021)62791715,E-mail:ychwang45@hotmail.com
, 百拇医药
参考文献
1 中华人民共和国卫生部药典.英文版.广州:广东科技出版社,1992∶82
2 Takeya T, Yamaki S, Itoh T, et al. A general synthesis of (±)-dibenzocyclooctadiene. Chem Pharm Bull, 1996,44∶909
3 秦文娟,孔庆芬,范志同,等.掌叶半夏化学成分的研究(III).
中草药,1984,15∶490
4 Kimura Y, Tani K, Kojima A, et al. Cyclo-(L-tryptophyl-
phenylalanyl), a new plant growth regulator from the fungus
, 百拇医药
Penicillium sp.. Phytochemistry, 1996,41∶665
5 Massharu K. Cyclic dipeptides for stress resistance in
plants. Jpn Kokai Tokkyo Koho JP 05 43, 408, 1993(CA 1993,119∶
295,133454y)
6 Ueda T, Saito M, Kato T, et al. Facile synthesis of cyclic
dipeptides and detection of racemization. Bull Chem Soc Jpn,1983,56∶568
, 百拇医药
7 Cook B, Hill RR, Jeffs GE. Efficient one-step synthesis of
diastereoisomeric cyclic dipeptides from amino acids: Three
diastereoisomers of cyclo-L-isoleucyl-L-isoleucine. J Chem Soc
Perkin Trans, 1992,10∶1199
8 Vicar J, Smolikova J, Blaha K. Amino acids and peptides.
CIX. Synthesis and infrared spectroscopy of 2,5-piperazinediones
, 百拇医药
derived from proline and pipecolic acid, Collect Czech Chem
Commun, 1972,37∶864
9 Nitecti DE, Halpern B, Westley JW. A simple route to
sterically pure diketopiperazines. J Org Chem, 1968,33∶864
10 Suzuki K, Sasaki Y, Endo N, et al. Acetic acid-catalyzed
diketopiperazine synthesis. Chem Pharm Bull, 1981,29∶233
11 Evzen K, Jiri K, Josef S, et al. 2,5-Dioxopiperazine
derivatives. Czech CS, 232,319,1986
收稿日期: 1997-10-13, 百拇医药
单位:(中国科学院昆明植物研究所植物化学开放研究实验室,昆明 650204)
关键词:北五味子;五味子科;环二肽;合成
药学学报990105.htm 摘要 目的:研究五味子中的环肽成分。方法:用薄层色谱,硅胶及反向RP-18硅
胶柱层析色谱和谱学方法。结果:分离到3个天然的环二肽及由3个环二肽组成的一个混
合物并鉴定为环(亮-脯)(1),环(苯丙-脯)(2)和环(苯丙-亮)(3),环(苯丙-缬)(4),环(苯
丙-异亮)(5),环(苯丙-苯丙)(6),另外,合成了14个环二肽类似物。结论:首次从五味子
, 百拇医药
科植物北五味子中分离到环肽。环二肽2,6~8,14~20,经活性筛选表明,2,16及18有轻
微的钙拮抗效应,19及20显示出增强高钾所致收缩效应。其它环二肽及它们的活性筛选工
作正在进行中。
CYCLIC DIPEPTIDES FROM SCHIZANDRA
CHINENSIS AND THEIR SYNTHESES
Wang Youchu(Wang YC), Zhou Jun(Zhou J), Tan Ninghua(Tan NH),Ding Zhongtao(Ding ZT) and Jiang Xin(Jiang X)
(Laboratory of Phytochemistry, Kunming Institute of Botany,Chinese Academy of Sciences, Kunming 650204)
, 百拇医药
ABSTRACT AIM: To investigate cyclopeptides from the fruits of S.
chinensis. METHODS: Use thin layer chromatography, repeated silica gel
and RP-18 column chromatography together with spectra as well as synthetic
methods. RESULTS: Three naturally occurring cyclic dipeptides and a
mixture composed of three other new naturally occurring cyclic dipeptides
, 百拇医药
were obtained. Their structures were determined as cyclo-(leucyl-prolyl)
(1), cyclo-(phenyl-alanyl-prolyl) (2), cyclo-(phenylalanyl-leucyl) (3),cyclo-(phenylalanyl-valyl) (4), cyclo-(phenylalanyl-isoleucyl) (5) and
cyclo-(phenylalanyl-phenylalanyl) (6). In addition, fourteen analogous
cyclic peptides (7~20) were synthesized. CONCLUSION: Cyclopeptides were
isolated from S.chinensis (Schizandraceae) for the first time. The
, 百拇医药
bioactivity of some cyclic dipeptides on the contraction of rabbit aorta
strips with KCl (40 mmol.L-1) depolarization was tested. Cyclic
dipeptides 2, 6 and 18 showed slight calcium antagonism and 19, 20
can increase the contractile effect in high concentration of potassium.
Studies on the bioactivities of other cyclic dipeptides are in progress.
, 百拇医药
KEY WORDS schizandra chinensis; schizandraceae; cyclic peptides;
synthesis
北五味子(Schizandra chinensis Baill)的干燥果实为中药五味子的主要药材,功效甚广。用于肺喘虚咳,心悸失眠诸病[1]。化学成分研究比较深入。已报道的有
单萜、倍半萜、有机酸等。近年由于该药所含木脂素有很好的治疗肝炎功效,因而发
现近30个木脂素成分[2],如五味子素(schizandrin)、去氧五味子素
(deoxyschizandrin)和五味子醇(schizandrol)等。
, 百拇医药
从北五味子果实甲醇提取物的乙酸乙酯部位经正、反相色谱分离鉴定了3个环
二肽,即环(亮-脯)(1),环(苯丙-脯)(2)和环(苯丙-亮)(3)和一个由3个环二肽组成
的混合物,即环(苯丙-缬)(4),环(苯丙-异亮)(5)和环(苯丙-苯丙)(6)。这3个环二
肽组成的混合物由于量少,未能分离得到纯品。故在初步推定其结构后,合成了这3个
环二肽。用由这3个合成环二肽的混合物与分离的环二肽混合物进行MS及HPLC比较,二者是吻合的,故得以证明。在五味子科发现环肽尚属首次。
环二肽(cyclic dipeptides)有多种生物活性[3~5]。参照Ueda和Cook[6,7]
, 百拇医药
方法本文合成了北五味子中的6个环二肽和14个其它环二肽(共20个),它们是:环(甘
-脯)(7)[8],环(丙-脯)(8)[5],环(缬-脯)(9)[10],环(异亮-脯)(10)[11],环
(丝-脯)(11),环(苏-脯)(12),环(N-甲色-脯)(13),环(酪-酪)(14),环(亮-亮)
(15)[9],环(异亮-异亮)(16)[10],环(缬-缬)(17)[10],环(蛋-蛋)(18),环
(丙-丙)(19)[6],环(脯-脯)(20)[6],其中11~14,18是新化合物。其结构
, 百拇医药
(图1)经波谱鉴定。环二肽2,6~8,14~20经活性筛选表明,2,16及18随着浓
度的增加,具轻微的钙拮抗效应。19及20显示增强高钾所致收缩效应。其它环二
肽以及其它活性的筛选工作正在进行中。

Fig 1 Structures of new compounds 11~14, 18.
实验部分
熔点为Koffler显微熔点仪测定,温度未校正。旋光用Horiba Sepa-300旋光测
定仪测定。紫外光谱用岛津UV-210A型紫外光谱仪。红外光谱用Perkin-Elmer 577
, 百拇医药
型红外光谱仪(KBr压片)。核磁共振谱用Bruker AM-400(400 MHz)和DRX-500(500
MHz)型核磁共振仪(氘代溶剂峰作为内标)。EI与FAB-MS用VG AutoSpec-3000型质
谱仪测定。高效液相色谱用岛津LC-4A型仪器(色谱柱:partisil ODS-2 alltech
4.6×250 mm;溶剂系统:CH3CN―H2O(3∶7),流速:0.4 ml.min-1;紫外检测,波长:
225 nm)。
五味子生药购自北京海淀区中心药店。
1 提取分离
, http://www.100md.com
五味子干果实9.8 kg经粉碎后,用工业甲醇回流提取4次,每次5 h。减压浓缩得
浸膏3150 g。该浸膏悬浮于水中,依次用石油醚、乙酸乙酯、正丁醇萃取。乙酸乙酯
部分浓缩得180 g,经硅胶柱(200~300目)色谱,用氯仿―甲醇(0~30%)依次洗脱,分
成4个部分,各部分经TLC检测,显环肽阳性反应部分进一步经硅胶H和RP-18反复色谱
分离,得到3个单体化合物1(38 mg),2(25 mg),3(22 mg)和1个由化合物4,5,6组成的
混合物(9 mg)。
2 鉴定
化合物1 针状结晶,mp 155~156℃,[α]11.7D -71.25°(CHCl3,0.4),茚三酮
, 百拇医药
显阴性,分子式为C11H18N2O2(m/z 210.1359,
 1.0 mu)。IR(KBr) cm-1:3300,1650。1HNMR(CDCl3,δ):5.79(1H,br.s,NH),4.10(1H,t,J=8.0 Hz,α-Hpro),4.00(1H,dd,J=3.4,9.4 Hz,α-Hleu),3.63(2H,m,δ-Hpro),2.33(1H,m,β-Hpro),2.05(3H,m,β-Hpro,β-Hleu,γ-Hpro),1.89(1H,m,γ-Hpro),1.72(1H,m,γ-Hleu),1.50(1H,m,β-Hleu),0.98(3H,d,J=6.5 Hz,δ-Hleu),0.92(3H,d,J=3.7 Hz,δ-Hleu)。13CNMR(CDCl3,δ):170.0(CO),166.2(CO),59.0(CH,α-Cpro),53.5(CH,α-Cleu),45.5(CH2,δ-Cpro),38.8(CH2,β-Cleu),28.2(CH2,β-Cpro),24.8
1.0 mu)。IR(KBr) cm-1:3300,1650。1HNMR(CDCl3,δ):5.79(1H,br.s,NH),4.10(1H,t,J=8.0 Hz,α-Hpro),4.00(1H,dd,J=3.4,9.4 Hz,α-Hleu),3.63(2H,m,δ-Hpro),2.33(1H,m,β-Hpro),2.05(3H,m,β-Hpro,β-Hleu,γ-Hpro),1.89(1H,m,γ-Hpro),1.72(1H,m,γ-Hleu),1.50(1H,m,β-Hleu),0.98(3H,d,J=6.5 Hz,δ-Hleu),0.92(3H,d,J=3.7 Hz,δ-Hleu)。13CNMR(CDCl3,δ):170.0(CO),166.2(CO),59.0(CH,α-Cpro),53.5(CH,α-Cleu),45.5(CH2,δ-Cpro),38.8(CH2,β-Cleu),28.2(CH2,β-Cpro),24.8, 百拇医药
(CH,γ-Cleu),23.2(CH3,δ-Cleu),22.8(CH2,γ-Cpro),21.3(CH3,δ-Cleu)。
化合物2 白色粉末,mp 138.5~139℃,[α]11.6D -192.59°(CHCl3,c
0.135)。茚三酮显阴性,分子式为C14H16N2O2(m/z 244.1200,
 1.2 mu)。
1.2 mu)。IR(KBr) cm-1:3300,1650。1HNMR(CDCl3,δ):7.27(5H,m),5.61(1H,br.s,NH),4.25(1H,dd,J=3.6,10.7 Hz,α-Hphe),4.06(1H,t,J=7.3 Hz,α-Hpro),3.59
, 百拇医药
(1H,m,β-Hphe),3.59(2H,m,δ-Hpro),2.75(1H,dd,J=10.7,14.4 Hz,β-Hphe),2.32(1H,m,β-Hpro),1.98(2H,m,γ-Hpro),1.89(1H,m,β-Hpro)。13CNMR
(CDCl3,δ):169.3(CO),165.1(CO),136.0(γ-Cphe),129.3(δ-Cphe),129.1
(ε-Cphe),127.6(ξ-Cphe),59.2(CH,α-Cpro),56.2(CH,α-Cphe),45.5
, 百拇医药
(CH2,δ-Cpro),36.9(CH2,β-Cphe),28.4(CH2,β-Cpro),22.5(CH2,γ-Cpro)。
化合物3 白色粉末,mp 261~263℃,[α]25D +21.0°(CH3OH,c 0.6),茚三酮显阴性,分子式为C15H20N2O2(m/z 260.1518,
 1.7 mu)。IR(KBr)
1.7 mu)。IR(KBr)cm-1:3300,1650。1HNMR(CD3OD,δ):7.25(5H,m),4.30(1H,t,J=4.6 Hz),3.65(1H,dd,J=4.2,10.8 Hz),3.26(1H,m),2.93(1H,dd,J=4.8,13.6 Hz),1.41(1H,m),0.84(2H,m),0.72(3H,d,J=6.6 Hz),0.67(3H,d,J=6.6 Hz)。
, http://www.100md.com
13CNMR(CD3OD,δ):170.6(CO),169.0(CO),136.8(C),131.8(CH),129.7
(CH),128.5(CH),57.5(CH),54.2(CH),45.3(CH2),40.3(CH2),24.7(CH),23.3(CH3),21.5(CH3)。
混合物 白色粉末,茚三酮显阴性,由于量少(9 mg),未分离。在HPLC
上有3个峰,保留时间分别为28.7,46.1及51.9 min。从EI质谱分析为分子量
246,260及294的3个环二肽组成的混合物,初步判定为环(苯丙-缬),环
, 百拇医药
(苯丙-异亮)和环(苯丙-苯丙)。我们合成了这3个化合物,将这3个化合物
及混和后分别做HPLC,EI质谱及高分辨EI质谱,发现保留时间、分子量和
分子式与天然混合物完全一致(表1)。
3 环二肽(1~20)的合成
参照Ueda[6]方法,环二肽1~5及7~13合成通法如下:
在L-氨基酸(20 mmol)的无水甲醇溶液中,于-10℃缓慢滴加亚硫酰氯
(27.8 mmol),在室温下搅拌2 d后,减压除去溶剂得无色或淡黄色油状物。
此油状物为L-氨基酸甲酯盐酸盐,无需纯化,直接用于反应。
, 百拇医药
Tab 1 HPLC retention time, EI-MS and HREI-MS of natural
and synthetic mixtures
Natural mixture
Synthetic mixture
4
5
6
4
5
6
Retention time
, http://www.100md.com
28.8
46.0
51.8
28.7
46.1
51.9
EI-MS m/z/%
294(22),260(32),246(54),204(30),175(26),155(20),141(32),127(47),120(31),113(44),99(26),91(100),77(22),72(28),65(31),57(40)
294(40),260(10),246(92),204(31),175(41),155(35),141(10),127(72),120(42),113(44),99(35),91(100),77(27),72(63),65(35),57(35)
, 百拇医药
HR-EI-MS
246.1372
(
 ,-0.3 mu)
,-0.3 mu)260.1530
(
 ,-0.5 mu)
,-0.5 mu)294.1371
(
 ,-0.3 mu)
,-0.3 mu)246.1366
, 百拇医药 (
 ,0.2 mu)
,0.2 mu)260.1520
(
 ,0.4 mu)
,0.4 mu)294.1369
(
 ,-0.1 mu)
,-0.1 mu)将L-氨基酸(5 mmol),NaHCO3(10 mmol)溶于蒸馏水(10 ml),滴加苄氧酰
氯(6 mmol)的二氧六环溶液(10 ml)。反应混合物在室温搅拌2 d后,减压除去
, 百拇医药
溶剂,加蒸馏水(10 ml)稀释,用乙酸乙酯(10 ml)萃取。水层用0.5 mol.L-1的
柠檬酸酸化至pH 5左右,然后再用乙酸乙酯(30 ml)分别萃取3次,合并萃取物,无水硫酸钠干燥,减压蒸馏得油状物。将油状物经柱色谱分离得白色粉末。此
粉未经负离子FAB-MS证实为N-苄氧羰基-L-氨基酸。将上述的L-氨基酸甲酯
(2.7 mmol),N-苄氧羰基-L-氨基酸和三乙胺(2.7 mmol)混合于二氯甲烷
(10 ml)中,在0℃反应4 h,然后在室温反应过夜,过滤,减压除去溶剂,将残
余物溶于乙酸乙酯,依次用2%HCl,5%NaHCO3和水洗,无水硫酸钠干燥。减压
, http://www.100md.com
蒸馏后,在硅胶柱上纯化得白色粉末。将此粉末溶于甲醇(5 ml),加10%钯炭
催化下氢解,TLC监测反应,待反应毕,过滤除去催化剂,减压除去溶剂,残余物
经硅胶柱色谱纯化得环二肽。
参照Cook[7]方法,环二肽6,14~20合成通法如下:将L-氨基酸溶于无水
乙二醇中,加热回流24 h,冷却析出固体,将固体在乙醇中重结晶或硅胶柱色谱
得环二肽。结果见表2。
将L-氨基酸(5 mmol),NaHCO3(10 mmol)溶于蒸馏水(10 ml),滴加苄氧酰氯
(6 mmol)的二氧六环溶液(10 ml)。反应混合物在室温搅拌2 d后,减压除去溶
, http://www.100md.com
剂,加蒸馏水(10 ml)稀释,用乙酸乙酯(10 ml)萃取。水层用0.5 mol.L-1的柠檬
酸酸化至pH 5左右,然后再用乙酸乙酯(30 ml)分别萃取3次,合并萃取物,无水硫
酸钠干燥,减压蒸馏得油状物。将油状物经柱色谱分离得白色粉末。此粉未经负
离子FAB-MS证实为N-苄氧羰基-L-氨基酸。将上述的L-氨基酸甲酯(2.7 mmol),N-苄氧羰基-L-氨基酸和三乙胺(2.7 mmol)混合于二氯甲烷(10 ml)中,在0℃反
应4 h,然后在室温反应过夜,过滤,减压除去溶剂,将残余物溶于乙酸乙酯,依次
用2%HCl,5%NaHCO3和水洗,无水硫酸钠干燥。减压蒸馏后,在硅胶柱上纯化得白
, http://www.100md.com
色粉末。将此粉末溶于甲醇(5 ml),加10%钯炭催化下氢解,TLC监测反应,待反
应毕,过滤除去催化剂,减压除去溶剂,残余物经硅胶柱色谱纯化得环二肽。
参照Cook[7]方法,环二肽6,14~20合成通法如下:将L-氨基酸溶于无水
乙二醇中,加热回流24 h,冷却析出固体,将固体在乙醇中重结晶或硅胶柱色
谱得环二肽。结果见表2。Tab 2 Results of the synthesized cyclic dipeptides Compds
Form
Yield
/%
, 百拇医药
MP
/℃
[α]D°
EI-MS
/70 ev
m/z(%)
HR-EI-MS
/70 ev
calc.
1HNMR
13CNMR
11
, 百拇医药
Needle
crystal
89.1
-
-118.59
(CH3OH,c 0.39)
184[M]+
(6)
184.0833
(184.0848)
4.23(1H,m),4.16(1H,m),3.90(2H,m),3.58(1H,m),3.33(1H,m),2.31(1H,m),1.96(3H,m)
, 百拇医药
184.2(CO),178.8(CO),74.1(CH2),72.6(CH),70.6(CH),58.6(CH2),41.9(CH2),35.6(CH2)
12
Needle
crystal
85.2
-
-117.60
(CH3OH,c 0.304)
199
, http://www.100md.com [M+1]+
(21)
198.1011
(198.1004)
7.35(1H,NH,br.s),4.24
(1H,m),4.09(1H,m),4.00(1H,br.s),3.90(1H,m),3.55(1H,m),3.48(1H,m),2.30(1H,m),1.99(2H,m),1.87(1H,m),1.31(3H,d,J=6.5 Hz)
180.1(CO),175.3(CO),75.3(CH),69.5(CH),69.1(CH),55.0(CH2),38.2(CH2),32.2(CH2),29.7(CH3)
, http://www.100md.com
13
Needle
crystal
73.5
-
+77.26
(CH3OH,c 0.288)
297[M]+
(41)
297.1456
(297.1477)
9.82(1H,NH,br.s),8.40
, http://www.100md.com
(1H,d,J=8.0 Hz),8.06
(1H,m),7.91(1H,m),7.82
(1H,m),7.64(1H,m),5.02
(1H,br.s),4.48(2H,m),4.17(1H,m),4.02(1H,m),3.89(3H,s),3.69(1H,m),2.44(1H,m),2.05(1H,m),1.45(1H,m),0.54(1H,m)
166.4(CO),164.1(CO),135.8(C),127.2(C),123.8(CH),122.1(CH
×2),111.0(CH×2),107.8(C),63.1(CH),59.0(CH),44.4(CH2),32.2(CH3),28.2(CH2),27.2(CH2),20.4(CH2)
, 百拇医药
14
White
powder
58
280~282.5
-
326[M]+
(12)
326.1260
(326.1267)
11.39(br.s,OH),9.16(s,NH),7.24(4H×2,m),4.50(1H×2,m),3.29(1H×2,m),2.73(1H×2,m)
, http://www.100md.com
168.8(CO×2),159.2
(C×2),133.1(CH×2),128.8(CH×2),117.6
(C×2),58.9(CH×2),41.9(CH2×2)
18
White
powder
54.6
228~228.5
-
262[M]+
(49)
, 百拇医药
262.0805
(262.0810)
8.10(NH,s),4.32(1H×2,m),2.15(2H×2,m),2.20
(2H×2),1.90(3H×2,s)
169.9(CO×2),60.3
(C×2),31.0(CH2×2),30.1(CH2×2),16.9(CH3×2)
*联系人现址:国家医药管理局上海医药工业研究院新药研究室,上海 200437。Tel:(021)65442731-22, Fax:(021)62791715,E-mail:ychwang45@hotmail.com
, 百拇医药
参考文献
1 中华人民共和国卫生部药典.英文版.广州:广东科技出版社,1992∶82
2 Takeya T, Yamaki S, Itoh T, et al. A general synthesis of (±)-dibenzocyclooctadiene. Chem Pharm Bull, 1996,44∶909
3 秦文娟,孔庆芬,范志同,等.掌叶半夏化学成分的研究(III).
中草药,1984,15∶490
4 Kimura Y, Tani K, Kojima A, et al. Cyclo-(L-tryptophyl-
phenylalanyl), a new plant growth regulator from the fungus
, 百拇医药
Penicillium sp.. Phytochemistry, 1996,41∶665
5 Massharu K. Cyclic dipeptides for stress resistance in
plants. Jpn Kokai Tokkyo Koho JP 05 43, 408, 1993(CA 1993,119∶
295,133454y)
6 Ueda T, Saito M, Kato T, et al. Facile synthesis of cyclic
dipeptides and detection of racemization. Bull Chem Soc Jpn,1983,56∶568
, 百拇医药
7 Cook B, Hill RR, Jeffs GE. Efficient one-step synthesis of
diastereoisomeric cyclic dipeptides from amino acids: Three
diastereoisomers of cyclo-L-isoleucyl-L-isoleucine. J Chem Soc
Perkin Trans, 1992,10∶1199
8 Vicar J, Smolikova J, Blaha K. Amino acids and peptides.
CIX. Synthesis and infrared spectroscopy of 2,5-piperazinediones
, 百拇医药
derived from proline and pipecolic acid, Collect Czech Chem
Commun, 1972,37∶864
9 Nitecti DE, Halpern B, Westley JW. A simple route to
sterically pure diketopiperazines. J Org Chem, 1968,33∶864
10 Suzuki K, Sasaki Y, Endo N, et al. Acetic acid-catalyzed
diketopiperazine synthesis. Chem Pharm Bull, 1981,29∶233
11 Evzen K, Jiri K, Josef S, et al. 2,5-Dioxopiperazine
derivatives. Czech CS, 232,319,1986
收稿日期: 1997-10-13, 百拇医药