CD8+细胞免疫亲合柱的研制及条件探讨①
作者:王郡甫 田志刚 张彩 刘金生 张建华 许晓群 孙 张捷
单位:王郡甫(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062);田志刚(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062) ;张 彩(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062);刘金生(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062)
关键词:免疫亲合柱;CD8+细胞;细胞纯化;流式细胞仪
中国免疫学杂志000208 摘 要:目的:建立一种利用免疫亲合柱纯化细胞的方法。方法: 将亲合素交联于聚丙烯酰胺凝胶Bio-Gel上,制成免疫亲合柱;将外周血单个核细胞与生物素化抗CD8单克隆抗体作用后,加到该免疫亲合柱上进行纯化,CD8+细胞即吸附于柱上,洗去其他细胞后,得到纯化的CD8+细胞。结果:纯化后CD8+细胞纯度达56%~7l%,细胞回收率为39%~66%,台盼蓝染色法显示活细胞达98%。 结论:利用免疫亲合柱纯化细胞具有纯度高,回收率高,细胞活性好等优点,是一种方便有效的细胞纯化方法。
, http://www.100md.com
分类号:R392-33
The preparation of immunoaffinity column and the purification of CD8+ cells
WANG Jun-Fu
(Shandong Academy of Medical Sciences,Jinan 250062)
TIAN Zhi-Gang
(Shandong Academy of Medical Sciences,Jinan 250062)
ZHANG Cai
(Shandong Academy of Medical Sciences,Jinan 250062)
, 百拇医药
Abstract:Objective:To prepare immunoaffinity column for cell separation. Methods: Avidin was attached to Bio-Gel and columns packed with Avidin-conjugated Bio-Gel was prepared. Cells from human peripheral blood were incubated with biotinylated anti-CD8 monoclonal antibody and then applied to the column;Biotin-labeled target cells are captured on Avidin coated Bio-Gel beads and non-target cells were washed off .Bounded target cells were then released by gentle agitation. Results: CD8+cells were enriched with a purity of 56%~71% and a recovery of 39%~66%;the percent of viable CD8+ cells were proved to be 98% by Trypan Blue Staining. Conclusion: With an high purity and recovery,the immunoaffinity column can be used as an efficient method for cell isolation.
, 百拇医药
Key words:Immunoaffinity column CD8+ cells Cell separation Flow cytometry▲
有效地分离造血及免疫细胞(如造血干细胞,NK细胞等),是深入研究其发育,分化及功能的先决条件,同时也是进一步开发新型生物治疗方案的需要。为此,国外建立了免疫亲合柱纯化细胞的方法,其基本原理是利用亲合素交联的凝胶捕获生物素化单抗阳性细胞,去除非目的细胞。此方法不仅细胞纯度高,回收率好,且操作简便易行[1]。而国内尚未建立类似的技术。本文参考国外相关文献制备了免疫亲合柱,并利用该柱进行了CD8+细胞的纯化,获得较满意的结果。
1 材料与方法
1.1 主要试剂及仪器 亲合素(Avidin,12 U/mg),生物素化N-羟基琥珀酰亚氨酯,碳二亚胺盐酸盐(EDC-HCl),均购自Sigma公司;Bio-Gel P-30,购自BIO-RAD公司;抗CD8单克隆抗体由本实验室自行制备,并经DEAE离子交换色谱纯化,双扩活性l:64,纯度大于90%;标准抗CD8单克隆抗体,为Pharmingen公司产品;羊抗小鼠IgG-FITC购自北京挚诚生物研究所;生物素标记辣根过氧化物酶由华美公司提供; Avidin-FITC由山东省农科院生物技术中心提供;流式细胞仪FACScan为Becton Dickinson公司产品; Olympus荧光显微镜。
, 百拇医药
1.2 外周血单个核细胞(PBMNC)的分离 用淋巴细胞分离液(Ficoll-Hypaque)常规分离。
1.3 生物素化抗CD8单克隆抗体的制备 参考文献[2]进行,制备后于4℃保存。
1.4 生物素化抗CD8单克隆抗体用于FACS检测 取PBMNC各100 μl ,一份加入10 μl本文制备的生物素化抗CD8单克隆抗体,于4℃作用30 min后,用PBS洗2次,加入FACS配备的荧光二抗,进行流式细胞术分析;另一份采用标准抗CD8单克隆抗体和FACS配备的荧光二抗进行CD8+细胞检测,比较两种处理方法的结果,以鉴定本文制备的生物素化抗CD8单克隆抗体的效果。
1.5 生物素与抗CD8单克隆抗体交联效果鉴定 取PBMNC各100 μl,分别加入10 μl本文制备的生物素化抗CD8单克隆抗体,洗涤后一份加入GAMIgG-FITC,另一份加入Avidin-FITC,在荧光显微镜下观察CD8+细胞比例,以鉴定生物素与抗CD8单克隆抗体交联效果。
, 百拇医药
1.6 亲合素与Bio-Gel的交联反应 按文献[3]进行,交联后于4℃保存备用。
1.7 Avidin与Bio-Gel交联效果判定 将100 μl已交联的Avidin-Bio-Gel用PBS洗涤5次,然后加入生物素标记辣根过氧化物酶(l:25稀释),4℃作用1 h(此间轻轻震荡混匀1次),用PBS洗5次,用饱和联苯胺/H2O2显色,以相同处理的Bio-Gel作为阴性对照,显色方法见文献[4]。
1.8 用免疫亲合柱纯化细胞 将PBMNC调整细胞浓度为5×107~2×108 ml-1,加入约l/10体积的生物素化抗CD8单克隆抗体,4℃冰箱中作用30~120 min(在此过程中轻轻震荡1次)。用含1%BSA的PBS洗细胞2次,并将细胞悬于适量的5%BSA中。将Avidin-Bio-Gel装于10 ml层析柱内,用PBS充分冲洗后,用5%BSA平衡柱子加细胞于柱上,使细胞缓缓流入凝胶内,静置约3~5 min。先以5%BSA洗去未吸附的细胞,再以PBS洗去BSA,用吸管轻轻吹打凝胶,CD8+细胞即与凝胶脱离,随PBS流出柱子,收集CD8+细胞进行检测。
, 百拇医药
1.9 CD8+细胞纯度及回收率测定 分别将未经柱分离的PBMNC上柱,用5%BSA洗下的未吸附细胞以及柱分离得到的CD8+细胞,采用单克隆抗体直接免疫荧光法,用FACS检测细胞表面CD8抗原表达百分率,计算出CD8+细胞纯度和回收率。
1.10 细胞活力测定 采用常规台盼蓝染色法计算经过纯化的活细胞数。
2 结果
2.1 生物素化抗CD8单克隆抗体用于FACS检测结果 利用本文制备的生物素化抗CD8单克隆抗体作为一抗,加入FACS配备的荧光二抗进行流式细胞术分析,结果与采用标准抗CD8单克隆抗体作为一抗进行流式细胞术分析的结果基本相同,说明本文采用的抗CD8单抗的效果令人满意,同时也证实生物素化未影响该单抗的活性。
2.2 生物素与抗CD8单克隆抗体交联效果鉴定 在荧光显微镜下观察发现,用生物素化抗CD8单克隆抗体处理的细胞,在分别用荧光二抗或Avidin-FITC作用后,CD8+细胞含量基本相同,表明生物素与抗CD8单克隆抗体交联效果良好。
, 百拇医药
2.3 Avidin与Bio-Gel交联效果的鉴定 采用生物素化辣根过氧化物酶鉴定Avidin与Bio-Gel交联效果,结果显示未交联的Bio-Gel经生物素标记辣根过氧化物酶处理后,加入底物溶液联苯胺/H2O2后无颜色变化,而已交联了Avidin的Bio-Gel经同样处理后呈肉眼可见的棕褐色,应用显微镜也可以观察到凝胶颗粒表面有棕褐色微晶沉着(见图1)。说明交联介质表面已有Avidin结合上去。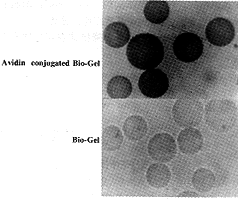
图1 Avidin与Bio-Gel交联效果(×100)
Fig.l Conjugation effects of Avidin to Bio-Gel(×100)
2.4 CD8+细胞纯化结果 利用本文设计的免疫亲合柱对CD8+细胞进行初步纯化,表1所列为5个样品的分离结果,表明本方法每次可处理约7×106~9×106个细胞,用5%BSA洗掉的未吸附细胞中CD8+细胞含量低于2%,而从亲合柱上解离后收集的细胞中CD8+细胞达56%~71%,回收率约39%~66%,纯化了近3倍。用台盼蓝染色分析CD8+活细胞数超过98%。
, 百拇医药
表1 CD8+细胞纯化结果
Tab.1 Results of CD8+ cell purification
Starting cell population
Cells collected from CD8 column
Expt
Total cells per column(×106)
Percent CD8+(%)
Total cells collected
, http://www.100md.com
Percent CD8+(%)
Percent yield (%)
1
96.0
25.7
24.0
62.1
60
2
7.0
33.6
1.5
, http://www.100md.com
73.3
47
3
76.0
22.0
11.5
56.7
39
4
76.0
22.0
19.8
57.3
, 百拇医药
68
5
76.0
22.0
15.4
71.8
66
3 讨论
细胞分离是基础医学和临床医学研究中常用的基本技术之一。早期的方法如密度梯度离心法,其回收率及细胞纯度均不理想,用尼龙毛柱分离只能去除B细胞和单核细胞。后来发展的利用细胞表面抗原与其抗体结合分离细胞的方法,如免疫Panning法,免疫磁珠法和免疫亲合柱法,分离效果大大提高。其中免疫亲合柱纯化法由于分离效果可靠,操作简便易行等特点已在国外实验室受到较为广泛的重视[1]。这种方法不需特殊设备,成本较低。由于利用Avidin和Biotin之间特异而强烈的亲合作用,本方法对靶细胞捕获能力强,特异性好,回收率高。所用介质对细胞的非特异吸附低,易于去除非靶细胞。由于Bio-Gel具有良好的亲水性和柔性,因而对细胞的损伤作用小,整个分离过程大约需要2 h。本方法处理量较大,分离规模易于放大。由于柱子是通用的,只需更换不同的生物素标记抗细胞表面抗原的单抗,也可用于其他细胞的分离。
, 百拇医药
实验中发现,抗CD8单克隆抗体在与生物素交联前后双扩活性均达l:64,说明生物素化并未影响CD8单克隆抗体的活性。每毫升介质交联100~1 000 μg Avidin均能获得较好的分离,但由于Avidin价格昂贵,所以交联量也不宜过高。样品上样速度、洗脱速度过慢,会在一定程度上增加非特异吸附,使细胞纯度下降,但是过快的流速又导致回收率降低,本实验认为3~5 ml/min 的流速比较理想。细胞与单抗作用时间在30~120 min内均能得到较好结果,但加入单抗的量不宜过多,以免增加细胞对单抗的非特异吸附而导致细胞纯度偏低。另外,单抗与细胞的亲合力也会对结果有一定影响,最好使用亲合力较高的单抗。■
①本课题受国家自然科学基金资助(39870729)
作者简介:王郡甫,男,34岁,硕士,助理研究员,主要研究免疫化学;
田志刚,男,42岁,研究员,博士生导师,主要从事分子免疫学研究
, 百拇医药
作者单位: 张建华(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062); 许晓群(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062); 孙 (山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062); 张 捷(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062)
(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062); 张 捷(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062)
参考文献:
[1] Johnson R J ,Owen R G ,Smith G M et al.Peripheral blood stem cell transplantion in myeloma using CD34 selected cells.Bone Marrow Transplant,1996;17(5):723
[2]王浩丹,周 申.生物医学标记示踪技术.北京:人民卫生出版社,1995:135
[3] Inman J K,Dintzis H M.Affinity techniques:covalent linkage of groups,ligands,and proteins to polyacrylamide beads.Vol 34.New York:Academic Press,1974:30
[4]李成文.免疫酶技术.济南:山东科学技术出版社,1983:94
收稿日期:1999-03-08
修回日期:1999-10-22, http://www.100md.com
单位:王郡甫(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062);田志刚(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062) ;张 彩(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062);刘金生(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062)
关键词:免疫亲合柱;CD8+细胞;细胞纯化;流式细胞仪
中国免疫学杂志000208 摘 要:目的:建立一种利用免疫亲合柱纯化细胞的方法。方法: 将亲合素交联于聚丙烯酰胺凝胶Bio-Gel上,制成免疫亲合柱;将外周血单个核细胞与生物素化抗CD8单克隆抗体作用后,加到该免疫亲合柱上进行纯化,CD8+细胞即吸附于柱上,洗去其他细胞后,得到纯化的CD8+细胞。结果:纯化后CD8+细胞纯度达56%~7l%,细胞回收率为39%~66%,台盼蓝染色法显示活细胞达98%。 结论:利用免疫亲合柱纯化细胞具有纯度高,回收率高,细胞活性好等优点,是一种方便有效的细胞纯化方法。
, http://www.100md.com
分类号:R392-33
The preparation of immunoaffinity column and the purification of CD8+ cells
WANG Jun-Fu
(Shandong Academy of Medical Sciences,Jinan 250062)
TIAN Zhi-Gang
(Shandong Academy of Medical Sciences,Jinan 250062)
ZHANG Cai
(Shandong Academy of Medical Sciences,Jinan 250062)
, 百拇医药
Abstract:Objective:To prepare immunoaffinity column for cell separation. Methods: Avidin was attached to Bio-Gel and columns packed with Avidin-conjugated Bio-Gel was prepared. Cells from human peripheral blood were incubated with biotinylated anti-CD8 monoclonal antibody and then applied to the column;Biotin-labeled target cells are captured on Avidin coated Bio-Gel beads and non-target cells were washed off .Bounded target cells were then released by gentle agitation. Results: CD8+cells were enriched with a purity of 56%~71% and a recovery of 39%~66%;the percent of viable CD8+ cells were proved to be 98% by Trypan Blue Staining. Conclusion: With an high purity and recovery,the immunoaffinity column can be used as an efficient method for cell isolation.
, 百拇医药
Key words:Immunoaffinity column CD8+ cells Cell separation Flow cytometry▲
有效地分离造血及免疫细胞(如造血干细胞,NK细胞等),是深入研究其发育,分化及功能的先决条件,同时也是进一步开发新型生物治疗方案的需要。为此,国外建立了免疫亲合柱纯化细胞的方法,其基本原理是利用亲合素交联的凝胶捕获生物素化单抗阳性细胞,去除非目的细胞。此方法不仅细胞纯度高,回收率好,且操作简便易行[1]。而国内尚未建立类似的技术。本文参考国外相关文献制备了免疫亲合柱,并利用该柱进行了CD8+细胞的纯化,获得较满意的结果。
1 材料与方法
1.1 主要试剂及仪器 亲合素(Avidin,12 U/mg),生物素化N-羟基琥珀酰亚氨酯,碳二亚胺盐酸盐(EDC-HCl),均购自Sigma公司;Bio-Gel P-30,购自BIO-RAD公司;抗CD8单克隆抗体由本实验室自行制备,并经DEAE离子交换色谱纯化,双扩活性l:64,纯度大于90%;标准抗CD8单克隆抗体,为Pharmingen公司产品;羊抗小鼠IgG-FITC购自北京挚诚生物研究所;生物素标记辣根过氧化物酶由华美公司提供; Avidin-FITC由山东省农科院生物技术中心提供;流式细胞仪FACScan为Becton Dickinson公司产品; Olympus荧光显微镜。
, 百拇医药
1.2 外周血单个核细胞(PBMNC)的分离 用淋巴细胞分离液(Ficoll-Hypaque)常规分离。
1.3 生物素化抗CD8单克隆抗体的制备 参考文献[2]进行,制备后于4℃保存。
1.4 生物素化抗CD8单克隆抗体用于FACS检测 取PBMNC各100 μl ,一份加入10 μl本文制备的生物素化抗CD8单克隆抗体,于4℃作用30 min后,用PBS洗2次,加入FACS配备的荧光二抗,进行流式细胞术分析;另一份采用标准抗CD8单克隆抗体和FACS配备的荧光二抗进行CD8+细胞检测,比较两种处理方法的结果,以鉴定本文制备的生物素化抗CD8单克隆抗体的效果。
1.5 生物素与抗CD8单克隆抗体交联效果鉴定 取PBMNC各100 μl,分别加入10 μl本文制备的生物素化抗CD8单克隆抗体,洗涤后一份加入GAMIgG-FITC,另一份加入Avidin-FITC,在荧光显微镜下观察CD8+细胞比例,以鉴定生物素与抗CD8单克隆抗体交联效果。
, 百拇医药
1.6 亲合素与Bio-Gel的交联反应 按文献[3]进行,交联后于4℃保存备用。
1.7 Avidin与Bio-Gel交联效果判定 将100 μl已交联的Avidin-Bio-Gel用PBS洗涤5次,然后加入生物素标记辣根过氧化物酶(l:25稀释),4℃作用1 h(此间轻轻震荡混匀1次),用PBS洗5次,用饱和联苯胺/H2O2显色,以相同处理的Bio-Gel作为阴性对照,显色方法见文献[4]。
1.8 用免疫亲合柱纯化细胞 将PBMNC调整细胞浓度为5×107~2×108 ml-1,加入约l/10体积的生物素化抗CD8单克隆抗体,4℃冰箱中作用30~120 min(在此过程中轻轻震荡1次)。用含1%BSA的PBS洗细胞2次,并将细胞悬于适量的5%BSA中。将Avidin-Bio-Gel装于10 ml层析柱内,用PBS充分冲洗后,用5%BSA平衡柱子加细胞于柱上,使细胞缓缓流入凝胶内,静置约3~5 min。先以5%BSA洗去未吸附的细胞,再以PBS洗去BSA,用吸管轻轻吹打凝胶,CD8+细胞即与凝胶脱离,随PBS流出柱子,收集CD8+细胞进行检测。
, 百拇医药
1.9 CD8+细胞纯度及回收率测定 分别将未经柱分离的PBMNC上柱,用5%BSA洗下的未吸附细胞以及柱分离得到的CD8+细胞,采用单克隆抗体直接免疫荧光法,用FACS检测细胞表面CD8抗原表达百分率,计算出CD8+细胞纯度和回收率。
1.10 细胞活力测定 采用常规台盼蓝染色法计算经过纯化的活细胞数。
2 结果
2.1 生物素化抗CD8单克隆抗体用于FACS检测结果 利用本文制备的生物素化抗CD8单克隆抗体作为一抗,加入FACS配备的荧光二抗进行流式细胞术分析,结果与采用标准抗CD8单克隆抗体作为一抗进行流式细胞术分析的结果基本相同,说明本文采用的抗CD8单抗的效果令人满意,同时也证实生物素化未影响该单抗的活性。
2.2 生物素与抗CD8单克隆抗体交联效果鉴定 在荧光显微镜下观察发现,用生物素化抗CD8单克隆抗体处理的细胞,在分别用荧光二抗或Avidin-FITC作用后,CD8+细胞含量基本相同,表明生物素与抗CD8单克隆抗体交联效果良好。
, 百拇医药
2.3 Avidin与Bio-Gel交联效果的鉴定 采用生物素化辣根过氧化物酶鉴定Avidin与Bio-Gel交联效果,结果显示未交联的Bio-Gel经生物素标记辣根过氧化物酶处理后,加入底物溶液联苯胺/H2O2后无颜色变化,而已交联了Avidin的Bio-Gel经同样处理后呈肉眼可见的棕褐色,应用显微镜也可以观察到凝胶颗粒表面有棕褐色微晶沉着(见图1)。说明交联介质表面已有Avidin结合上去。

图1 Avidin与Bio-Gel交联效果(×100)
Fig.l Conjugation effects of Avidin to Bio-Gel(×100)
2.4 CD8+细胞纯化结果 利用本文设计的免疫亲合柱对CD8+细胞进行初步纯化,表1所列为5个样品的分离结果,表明本方法每次可处理约7×106~9×106个细胞,用5%BSA洗掉的未吸附细胞中CD8+细胞含量低于2%,而从亲合柱上解离后收集的细胞中CD8+细胞达56%~71%,回收率约39%~66%,纯化了近3倍。用台盼蓝染色分析CD8+活细胞数超过98%。
, 百拇医药
表1 CD8+细胞纯化结果
Tab.1 Results of CD8+ cell purification
Starting cell population
Cells collected from CD8 column
Expt
Total cells per column(×106)
Percent CD8+(%)
Total cells collected
, http://www.100md.com
Percent CD8+(%)
Percent yield (%)
1
96.0
25.7
24.0
62.1
60
2
7.0
33.6
1.5
, http://www.100md.com
73.3
47
3
76.0
22.0
11.5
56.7
39
4
76.0
22.0
19.8
57.3
, 百拇医药
68
5
76.0
22.0
15.4
71.8
66
3 讨论
细胞分离是基础医学和临床医学研究中常用的基本技术之一。早期的方法如密度梯度离心法,其回收率及细胞纯度均不理想,用尼龙毛柱分离只能去除B细胞和单核细胞。后来发展的利用细胞表面抗原与其抗体结合分离细胞的方法,如免疫Panning法,免疫磁珠法和免疫亲合柱法,分离效果大大提高。其中免疫亲合柱纯化法由于分离效果可靠,操作简便易行等特点已在国外实验室受到较为广泛的重视[1]。这种方法不需特殊设备,成本较低。由于利用Avidin和Biotin之间特异而强烈的亲合作用,本方法对靶细胞捕获能力强,特异性好,回收率高。所用介质对细胞的非特异吸附低,易于去除非靶细胞。由于Bio-Gel具有良好的亲水性和柔性,因而对细胞的损伤作用小,整个分离过程大约需要2 h。本方法处理量较大,分离规模易于放大。由于柱子是通用的,只需更换不同的生物素标记抗细胞表面抗原的单抗,也可用于其他细胞的分离。
, 百拇医药
实验中发现,抗CD8单克隆抗体在与生物素交联前后双扩活性均达l:64,说明生物素化并未影响CD8单克隆抗体的活性。每毫升介质交联100~1 000 μg Avidin均能获得较好的分离,但由于Avidin价格昂贵,所以交联量也不宜过高。样品上样速度、洗脱速度过慢,会在一定程度上增加非特异吸附,使细胞纯度下降,但是过快的流速又导致回收率降低,本实验认为3~5 ml/min 的流速比较理想。细胞与单抗作用时间在30~120 min内均能得到较好结果,但加入单抗的量不宜过多,以免增加细胞对单抗的非特异吸附而导致细胞纯度偏低。另外,单抗与细胞的亲合力也会对结果有一定影响,最好使用亲合力较高的单抗。■
①本课题受国家自然科学基金资助(39870729)
作者简介:王郡甫,男,34岁,硕士,助理研究员,主要研究免疫化学;
田志刚,男,42岁,研究员,博士生导师,主要从事分子免疫学研究
, 百拇医药
作者单位: 张建华(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062); 许晓群(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062); 孙
 (山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062); 张 捷(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062)
(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062); 张 捷(山东省医科院基础医学研究所山东省肿瘤生物治疗研究中心 济南 250062)参考文献:
[1] Johnson R J ,Owen R G ,Smith G M et al.Peripheral blood stem cell transplantion in myeloma using CD34 selected cells.Bone Marrow Transplant,1996;17(5):723
[2]王浩丹,周 申.生物医学标记示踪技术.北京:人民卫生出版社,1995:135
[3] Inman J K,Dintzis H M.Affinity techniques:covalent linkage of groups,ligands,and proteins to polyacrylamide beads.Vol 34.New York:Academic Press,1974:30
[4]李成文.免疫酶技术.济南:山东科学技术出版社,1983:94
收稿日期:1999-03-08
修回日期:1999-10-22, http://www.100md.com