PET与脑科学
作者:马云川
单位:首都医科大学宣武医院核医学科,北京PET中心,北京100053
关键词:
基础医学与临床990603 Abstract The carcinogenesis and development is a progress of multi-gene alterations in the human gastric cancer (HGC).In order to determine the relation between the aberration of these genes and gastric cancer,we chose c-met (7q31)、hMLH1 (3p21)、E-cadherin (16q22.1) and HLA loci DQA1、DR2、DR3、DR4、DR7、DR9 and detected their changes in 32 tumor specimens of intestinal type HGC and 4 cell lines of gastric cancer by performing analysis of SSP/PCR、PCR/SSCP and MSI technigues.Our data show that none point mutation was detected in c-met gene.We examined two microsatellites loci D3S1298 and D3S1561 in hMLH1 gene and detected that 6 cases retain MSI (Microsatellite Instability) and 2 cases of LOH (Loss of Heterozygosity) at D3S1298 and 2 cases of MSI at D3S1561.We also examined E-cadherin gene at two microsatellites loci D16S3083 and D16S3095 close to the gene and detected that 5 cases retain MSI and 1 case of LOH at D16S3083 and no change at D16S3095.The point mutation incidence of HLA-DR4 loci is 9/20 (45%),higher than the other loci in HLA-Ⅱ.High frequent deletion,expression deregulation and methylation of mts1/p16 gene were detected in cell lines and solid tumors from human gastric cancer patients.
, 百拇医药
Our data showed that the point mutation of c-met gene is not the main pattern of alteration in intestinal type HGC that is consistent with the previous results.E-cadherin and hMLH1 are related to intestinal type HGC but whether they are susceptibility gene still need further study.The point mutation of the HLA-Ⅱ loci DR4 is closely related to intestinal type HGC.Methylation of mts1/p16 gene 5 CpG island might be plays an important role in the carcinogenesis in HGC.
, 百拇医药
Key words Gastric cancer Mismatch repair genes Susceptibility Methylation p16 HLA-DR4
1 引言
人类经过一百多年的努力,通过对肿瘤遗传家系分析、流行病学以及大量的动物实验研究证明了肿瘤的发生受遗传因素的影响,特别是近二十年来,已进一步明确肿瘤是一种环境因素与遗传因素相互作用导致的一类疾病。大多数的环境致病因素如饮食、病毒、化学物质、射线的致癌作用都是通过影响遗传基因使遗传物质发生一系列的变化而致。目前研究的结果已表明肿瘤是细胞中多种基因突变累积的结果,突变主要发生在三类细胞基因,即癌基因、肿瘤抑制基因和DNA修复基因。通常这些基因在细胞中行使正常的生物学功能,对细胞的增殖和分化过程起重要调控作用。在某些致病因素作用下这些基因发生点突变、扩增、重排、缺失或甲基化状态的改变。目前的研究结果表明在大多数肿瘤中可以检测到这三类基因的变异,这些基因的变异有可能受机体遗传易感性的影响。为了进一步明确肿瘤的遗传易感性,鉴定和克隆与肿瘤相关的易感基因已成为肿瘤研究领域的一个重要科学问题。
, 百拇医药
2 肿瘤的遗传易感性和肿瘤易感基因
有某些遗传缺陷或疾病的个体会表现出易患某些肿瘤的倾向,这就是一种对肿瘤的遗传易感性。机体的性状是遗传与环境相互作用的结果。某一地区有肿瘤家族聚集现象,这一方面与不良的环境因素有关,同时也取决于不同人群对肿瘤易感性的差异。遗传易感性就是遗传变异对环境致癌因素的敏感程度。肿瘤的易感性除涉及到癌基因、抑癌基因、DNA修复基因等与肿瘤发生密切相关的基因的变化以外,还涉及到免疫缺陷、代谢酶系统改变和DNA-染色体的不稳定性等。遗传易感性是致癌物在某些遗传素质下,通过体内代谢活化而致癌,而体内代谢酶系统的差异是直接影响肿瘤易感性的基础。染色体脆性部位(fraglesite,fra)是染色体上随机的断裂点,它表示了染色体的不稳定性,许多研究提示染色体脆性位点与肿瘤易感性密切相关,这些不稳定的染色体和染色体上存在的脆性位点也和基因一样可以遗传,有些脆性位点是致癌剂作用敏感点及癌基因同位点,肿瘤细胞的染色体缺失和重排往往发生在这些脆性部位,在多种因素作用下,脆性位点变得十分敏感,不稳定性升高,导致染色体DNA发生断裂、丢失、重排和突变,从而导致细胞内重要基因(癌基因、抑癌基因和DNA修复基因)的变异,最终导致细胞癌变和肿瘤发生。在对肠型胃癌的研究中已知有多种癌基因(如ras、met、erbB2、akt2)、抑癌基因(P16、P53、APC)、转移抑制基因nm23等以不同变异方式(如点突变、过量表达、缺失、扩增)参与了不同阶段的发病。这些基因中有哪些基因对胃癌发病真正易感或者还有哪些未被发现的基因与此病易感现在仍不十分清楚。Guilford等[1]在对三个大的家族性胃癌的家系的研究中发现E-cadherin基因与弥漫性胃癌的发病密切相关。HNPCC(遗传性非息肉性结直肠癌)是西方国家的多发肿瘤,有明显的家族遗传史,研究发现与这种疾病密切相关的是一组错配修复基因。不同种族不同个体对疾病的易感性的差异有很大程度上是由遗传因素决定的,HLA是第一个被发现与疾病有明确联系的遗传系统,HLA基因的多态性与疾病的易感性有关,是研究肿瘤易感基因的一个热点问题。
, http://www.100md.com
3 肠型胃癌发病过程中癌基因与抑癌基因改变的规律和特点
原癌基因是一类编码关键性调控蛋白质的正常细胞基因。它编码的蛋白质几乎存在于细胞的各个部位包括细胞核、细胞质和细胞膜,其主要的功能是调节细胞的增殖与分化,在细胞生长方面起着重要的调节功能,原癌基因只有当其发生突变导致正常结构和功能发生改变时才具有致癌作用。癌基因突变在肿瘤发生过程中起促进作用。与此相反抑癌基因是一类可以抑制细胞增殖并能潜在抑制癌变的基因。癌基因的激活和抑癌基因的失活究其原因是因为在一些物理、化学和生物等因素作用下促发了某些遗传的不稳定因素而引发的结果。
根据组织结构、生物学行为及流行病学特征,Lauren将胃癌分为肠型胃癌和弥漫型胃癌[2]。其中肠型胃癌被确定是一个从慢性萎缩性胃炎→肠上皮化生→异型增生I、Ⅱ、Ⅲ级→胃癌的演变过程。在对肠型胃癌的发病规律以及细胞癌变及肿瘤发生发展过程中基因变异规律的研究中已经确定胃癌的发生、发展是多基因变异累积的结果(见图1)[3]。胃癌高发区的研究显示,当地的胃粘膜疾病的发病率很高,这可能是胃癌高发的主要原因。同时调查还发现在当地的部分家庭中有胃癌的家族聚居现象。这进一步说明了胃癌的发生发展是一个多因素多阶段的逐步演变过程,并受遗传因素的影响,其发生过程可能包含着复杂的病理机制。因此只有从分子水平上充分了解和阐明慢性胃粘膜疾病癌变过程中不同基因结构和表达异常的规律,特别是寻找一组与胃癌相关的肿瘤易感基因才是从根本上提高胃癌早期诊治水平的关键。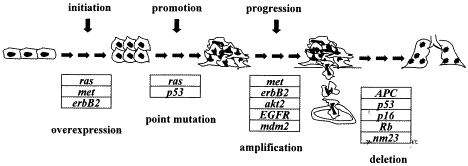
, 百拇医药
图1 基因变异方式和数量与胃癌了生发展的关系
Fig1 Accumulation of multiple gene changes in human gastric carcinogenesis
针对胃癌发生、发展过程中多基因变异的特性,以几类与肿瘤相关的基因为对象,鉴定这些基因变异在胃癌中的改变,进一步探讨与肿瘤易感性的关系。选择c-met原癌基因、错配修复基因hMLH1、E-cadherin基因以及HLA-Ⅱ类分子的(DQA1、DR2、DR3、DR4、DR7、DR9)6个基因位点,采用PCR系列技术(PCR/SSP、PCR/SSCP和MSI)对32例肠型胃癌标本和4个胃癌细胞系进行检测以确定上述基因在肠型胃癌中的变异情况。研究结果表明:经过对c-met基因突变热点的第17、18和19外显子的SSCP分析,未检测到点突变。对错配修复基因hMLH1的D3S1298和D3S1561两个位点进行微卫星不稳定性(Microsatellite Instability,MSI)检测,其中在D3S1298位点检测到6例MSI(19.4%),2例杂和性缺失(Loss of Heterozygosity,LOH),D3S1561位点有2例检测到MSI。在E-cadherin基因附近选择两个微卫星位点D16S3083和D16S3095进行MSI检测,D16S3083位点有5例检测到MSI(16%),1例有LOH,D16S3095位点未检测到异常带型。HLA-Ⅱ类基因区6个基因位点基因型在个体中存在着明显多态性,PCR-SSCP结果显示DR4基因位点点突变频率为45%,明显高于其它几个基因位点。
, http://www.100md.com
上述结果表明:c-met原癌基因在胃癌中的变化方式不是以点突变为主,符合以往的研究结果。hMLH1、E-cadherin基因均与肠型胃癌的发生有关,其相关性大小有待于进一步研究。HLA-Ⅱ类基因区DR4基因的突变可能与胃癌发生的易感性有关。
4 弥漫性胃癌中E-cadherin基因的改变
弥漫性胃癌有明显的家族聚集性,为了鉴定哪些基因与弥漫性胃癌易感, Guilford等对一个来自新西兰的大的弥漫型胃癌家系作一描述,用基因连锁分析通过微卫星标记在与肿瘤易感的侯选位点进行筛查,侯选基因之一为E-cadherin基因[1]。此基因位于16q22.1区,对于维持上皮组织的细胞与细胞之间的粘附有重要作用。它的功能的丧失对一些实体性肿瘤的永生性、侵袭性或恶性程度起促进作用[4]。根据体外实验和临床观察资料认为它是一种侵袭抑制基因[5],也有人认为它是一个抑癌基因。E-cadherin gene的失活性突变在胃癌细胞系[6]、原发性胃癌[7]、妇科肿瘤[8]、肺癌细胞系[9]和原发性肺癌[10]中均见报道。
, http://www.100md.com
E-cadherin在肿瘤中失活的机制可能通过突变、启动子甲基化和转录下游调节等发生[11]。了解其失活的机制可以指导治疗,恢复其表达。Yoshiura等在E-cadherin基因负性表达肿瘤细胞系中发现有高甲基化状态[5],而且对E-cadherin 基因表达阴性肿瘤细胞系用去甲基化物质5-azacytidine处理,结果使此基因重新表达并且使梭形细胞向上皮形细胞转化,重新获得细胞之间同源粘附作用。
不仅弥漫型胃癌的发病具有家族聚集性,据流行病学调查肠型胃癌的发病也有家族聚集性。肠型胃癌的发生是一个多阶段、多基因参与的过程,为了说明在这个过程中是否有E-cadherin基因的改变,我们选择了这个基因附近的与弥漫型胃癌显著相关的两个微卫星位点对肠型胃癌的32例标本和四个胃癌细胞系进行检测,结果发现D16S3083有6例异常带型,其中1例肿瘤比正常少一条带,属杂合性缺失LOH。其余5例肿瘤比正常多一至二条带,属于微卫星的不稳定性(Microsatellite Instebility,MSI),D16S3095未检测出异常带型。微卫星的不稳定代表了附近基因的改变,这两个微卫星位点与E-cadherin基因密切连锁,说明此基因在肠型胃癌中也有改变。E-cadherin基因的变化和功能的丧失与弥漫性胃癌的发病高度易感,在许多其他类型的散发型肿瘤中此基因高频率失活又提示此基因也与其他肿瘤的易感性也有关。因此利用MSI只能初步说明此基因在肠型胃癌中有改变,但具体变异方式需进行深入研究。
, http://www.100md.com
5 错配修复基因与细胞癌变的关系
现在越来越多的证据表明另一类重要的肿瘤易感基因―DNA修复基因与癌基因和抑癌基因一样在致瘤过程中起关键性作用,与抑癌基因不同之处在于一些抑癌基因是通过影响抑制细胞增殖或分化的信号而调节细胞生长,另一些是在DNA损伤或细胞周期受干扰的情况下阻断细胞生长或引起细胞凋亡。而DNA损伤修复基因在控制细胞生长过程中起被动的作用,这种基因突变导致的生物学功能并不直接改变细胞的生长状态,但是这种基因的失活可能增加受损伤细胞中癌基因和抑癌基因的突变频率。DNA的主要损伤为硷基损伤与DNA链的断裂。DNA的损伤是环境致癌因素作用于靶分子的结果,与肿瘤的发生有密切关系,但是并不是受环境致癌因素作用就一定要患癌。在生物体内有多种修复DNA损伤的途径,细胞的修复功能使生物体能在一定限度内克服环境因素对机体造成的不利作用,使机体免于产生疾病。目前在肿瘤研究方面DNA损伤修复基因之所以引起人们极大重视在很大程度上是对遗传性非息肉性结直肠癌(Hereditary Nonpolyposis Colorectal Cancer,HNPCC)的研究。
, 百拇医药
5.1 错配修复基因的生物学意义
错配修复基因是一组高度保守的看家基因,在原核真核细胞中都具有高度同源的序列。核苷酸错配可发生于三种情况,即DNA的物理损伤、DNA复制过程中核苷酸的错误掺入和基因重组,当错配发生时细胞内特异性酶系统即错配修复系统开始启动对错配碱基进行修复。目前在人类中发现的错配修复基因主要有四个成员分别为hMSH2、hMLH1、hPMS1、hPMS2。这几个基因在染色体上的位置、结构以及在HNPCC中的作用方式已经研究的比较清楚(见表1)。
表1 人类错配修复基因及其与HNPCC的关系*
Table1 Correlation between HNPCC and DNA Mismatch repair gene
Genes
, http://www.100md.com
Chromosome
lication
Homologue
Relevance ratio
in HNPCC
Changes in HNPCC
Bacteria
Yeast
hMSH2
2p16
mutS
MSH2
, http://www.100md.com
50%~60%
codon622(Pro-Leu)
GTBP
2p16
mutS
MSH2
frame shift(HCT-15)
hMLH1
3p21
mutL
MLH1
30%
, 百拇医药
codon 578-622(LOH)
codon 519(T insertion)
homzygosity deletion (H6)
hPMS1
2q31-33
mutL
PMS1
5%
codon 195 -233(deletion in frame)
codon 233(Gln-termination codon)
, 百拇医药
hPMS2
7p22
mutL
PMS2
5%
codon 268-269(deletion in frame)
*引自邓锡云、曹亚.国外医学遗传学分册,1997,20(1).
5.2 错配修复基因缺陷与细胞癌变和肿瘤的发生、发展
在研究HNPCC的过程中相继发现了hMSH2、hMLH、hPMS1和hPMS2等四个人类错配修复基因。HNPCC是西方国家常见的肿瘤易感性症侯群,每200人中就有1人受累,受累的个体在50岁以前常发生结直肠癌、子宫内膜癌、卵巢癌、胃癌以及其他一些脏器的肿瘤,通过研究发现部分HNPCC患者存在微卫星的不稳定性(Microsatelite Instability,MSI)。芬兰学者Peltomaki[12]等选择了两个HNPCC家系用微卫星标记对上述两家系的整个基因组DNA进行筛选,对2号染色体上HNPCC基因进一步研究第一次找到了与细菌错配修复基因MutS同源的hMSH基因。随后又分别得到hMLH1,hPMS1和hPMS2基因。
, http://www.100md.com
随着错配修复缺陷在HNPCC及其他肿瘤中的发现,它与肿瘤的关系越来越受到广泛的重视。目前在许多肿瘤细胞里都发现有微卫星序列不稳定现象,在这些肿瘤细胞中证实有错配修复功能的缺陷。许多实验也表明错配修复对于维持微卫星序列稳定性有重要作用,人们推测错配修复功能缺陷导致肿瘤可能是由于错配修复功能缺陷使基因突变事件不断放大、积累,使大量错误信息遍布于整个基因组所致。错配修复基因作为从细菌到人类都存在的高度保守的看家基因,对于DNA错配的修复、维持DNA复制的保真度起到极其重要的作用,对其机制的深入研究将有利于揭示肿瘤的发生机制。
研究发现人的3p21区不仅在肺癌、乳腺癌、肾癌、恶性间皮瘤等多种肿瘤中有变异,而且在胃癌中也有明显异常。错配修复基因的成员之一hMLH1基因就定位于3p21.3,与DNA的损伤修复有关。我们在此基因内选择了两个微卫星位点D3S1298和D3S1561对32例肠型胃癌和四个胃癌细胞系进行检测。结果在D3S1298位点有一例标本PCR扩增阴性,同样在另一微卫星位点D3S1561有一例标本和一个胃癌细胞系PAMC82其PCR扩增阴性,说明这个微卫星位点的侧翼序列有改变,也就是这个基因本身在这些肿瘤组织中有变化。另外在D3S1298位点PCR扩增阳性的31例标本中有8例出现异常带型,其中两例有LOH,6例有MSI。在D3S1561位点有2例异常带型,均为MSI。以上结果表明在肠型胃癌发病中错配修复基因hMLH1可能由于结构的改变导致功能的丧失。根据这些微卫星位点检测中存在的不稳定现象推测在胃癌的发病过程中当核酸发生错误的时候一些错配修复基因、p53等的具有监视功能的基因发生了变异未能起到监视和修复的作用,使胃粘膜在由正常到肿瘤的过程中基因突变事件不断放大、积累,使大量错误信息遍布于整个基因组所致。明确了胃癌中错配修复基因有改变以后,就要深入研究它的变异方式以及导致其改变的根本原因,确定其是否与胃癌发病真正易感。
, http://www.100md.com
6 HLA基因的多态性与肿瘤的易感性
6.1 HLA区基因结构特征
人类主要组织相容性复合物(Major histocompatibility complex,MHC)基因组编码HLA抗原(Human leukocyte antigene),其基因组存在于6p21.3区,长度约为3600~4000kb占全部人类基因组区域的0.1%。HLA区是人类MHC基因组中基因密度极高的区域之一。该区包括100多个基因座,633个等位基因[13],每个基因编码一个特异性抗原。
6.2 HLA基因的多态性决定疾病的易感性
HLA系统是已知人类最复杂的显性多态遗传系统,其多态性是指随机婚配的群体中同一基因位点可以存在两种以上的基因型。基因的多态性并不一定影响基因的功能,但可以作为区别个体的标志。目前已知HLA的各位点上等位基因的总数为633个,不同群体和地区各等位基因频率不尽相同,可编码出大量不同的HLA分子。即使在同一个个体中,由于HLA两条单倍型的两位点等位基因编码的α、β链可按顺式和反式不同方式组合形成不同的杂合二聚体,而且不同种族的两位点基因编码的α、β链也可以组合形成如DRα-DRβ这样的族间分子,因此大大增加了体细胞表面的HLA分子的多样性。HLA的多态性决定着免疫应答和疾病易感性的个体差异。HLA与疾病的相关性归纳起来有以下两种情况:第一,HLA决定着对特定自身或非自身抗原发生免疫逃逸或免疫应答的个体差异,而这种差异直接决定着人群对疾病的易感性。第二,和HLA密切连锁的HLA之外的致病基因存在着和特定HLA等位基因的连锁不平衡性。
, 百拇医药
不同个体对疾病的易感性的差异在很大程度上是由遗传因素所决定的,HLA是第一个被发现与疾病有明确联系的遗传系统。迄今已发现60余种疾病与HLA相关。近年来开展的多种疾病与HLA区微卫星标记的相关性有助于我们更好地定位疾病易感基因,更进一步确定涉及肿瘤遗传易感性的基因。最终有助于阐明某些疾病的发病机制,并在此基础上制定新的肿瘤防治措施。
6.3 HLA与肿瘤
HLAⅠ类或Ⅱ类基因在肿瘤细胞中表达的变化与肿瘤生长和转移有密切的相关性。已有的研究表明在人的肿瘤细胞HLA-Ⅰ类抗原表达丧失与肿瘤的分化程度、转移能力有关[14]。恶性黑色素瘤的进展阶段有HLA-DR抗原的表达,此抗原的表达可能提示恶性黑色素瘤的预后不好[15]。但是在结肠癌和喉癌中却有相反的情况,即HLA-DR的表达预示着这类肿瘤的预后较好[16]。
胃癌是一个多因素参与的疾病,已知胃癌的发病机制与某些基因的改变有关。在MHC基因的表达与人的胃癌关系的研究中有报道HLA-Ⅱ类基因DQB1*0301在白种人中与胃癌的发病密切相关[17]。M.Ohmori等在研究HLA基因在日本人中与胃癌的关系结果发现相关性不是很大[18]。可能的解释就是环境因素例如饮食等在导致日本人胃癌的基因变化方面所起的不可忽视的作用。另有报道[19]在低分化型的胃腺癌HLA-DR4抗原的表达与淋巴结转移有高度相关性。我们选择了DQA1、DR2、DR3、DR4、DR7、DR9等六对引物对32例肠型胃癌及癌旁组织进行SSP-PCR扩增,对基因型阳性病例又作SSCP点突变检测,结果发现HLA-DR4基因位点点突变频率很高,说明此基因位点的改变与胃癌发病易感性有关。SSCP带型显示这些基因位点明显的多态性。有纯合互补两条带型、杂合四链型、异源双链和变性不彻底的两条带型等等。国外在对HLA与胃癌的相关性研究方面作过几篇报道:其中Lee等[7]的研究结果表明HLA-Ⅱ基因DQB1-0301在白种人中与胃癌的发病密切相关。Oyoshi等[10]的研究结果表明,在低分化的胃腺癌中HLA-DR4抗原表达与淋巴结转移之间存在着密切的关系,有淋巴结转移的病人HLA-DR4抗原表达阳性率高。这些发现进一步提示人的肿瘤的组织相容性抗原在影响免疫应答和免疫逃逸机制方面的重要作用。
, http://www.100md.com
7 小结
肿瘤已成为一类严重危害人类健康的疾病,其发病的主要原因是遗传和环境因素相互作用的结果,特别是在环境致病条件的作用下,使机体内的某些基因发生改变,从而导致细胞增殖与分化的平衡失调,使细胞发生癌变。人们已经逐渐认识到晚期恶性肿瘤由于多种基因、多种变异方式的累积给治疗带来了极大的困难,按人类目前的知识水平在较短时间内攻克晚期恶性肿瘤是难以达到目标,因此对肿瘤进行预防和早期诊治,就要从研究肿瘤的遗传易感性和易感基因入手。我们的研究提示c-met基因在肠型胃癌中的变化方式不是以点突变为主。与以往的研究结果相符:c-met基因在胃癌中的变化是以过表达和基因扩增为主,在癌变早期以过表达为主,基因扩增与肿瘤的快速生长有关。E-cadherin基因不仅是弥漫型胃癌发生的易感基因而且与肠型胃癌的发病也有相关性。错配修复基因hMLH1与肠型胃癌的发病相关,但是胃癌发生的易感基因仍有待于进一步证实。HLA-DR4基因位点的点突变与肠型胃癌的易感性有关。HLA区域基因位点的突变使与HLA某等位基因连锁的某些致病基因发生了变化,这可能是导致疾病发生的更为重要的原因。
, 百拇医药
参考文献
1 Guiford P,Hopkins J,Harraway J,et al.Nature,1998,392(26):402
2 Lauren P.Acta Pathol Microbiol Scand A,1965,64:34
3 吕有勇.中华医学杂志,1997,77(11):85
4 Hiraguri S,Godfrey T,Nakamura H,et al.Cancer Research,1998,58:1972
5 Yoshiura K,Yaekanai,Ochiai A,et al.Proc Natl Acad Sci USA,1995,92:7416
, http://www.100md.com 6 Oda T,Kanai Y,Oyama T,et al.Proc Natl Acad Sci USA,1994,91:1858
7 Becker K F,Atkinson M J,Reich H,et al.Cancer Res,1994,54:3845
8 Risinger JI,Berchuck A,Kohler MF,et al.Nat Genet,1994,7:98
9 Pierceall W,Woodard A,Morrow J,et al.Oncogene,1995,11:1319
10 Berx G,Cleton-Jansen A M,Strumane K,et al.Oncogene,1996,13:1919
11 Bussemakers M G,Giroldi L A,Vanibokhoven A,et al.Biochem Biophys Res Commun,1994,203:1284
, 百拇医药
12 Peltomaki P,Aaltonen L,Sistonen P,et al.Scinece,1993,260(5107):810
13 Bodmer JG,Marsh SGE,Albert ED,et al.Tissue Antigens,1996,49:297
14 Momburg F,Degener T,Baccbus L,et al.Internationnal Journal of Cancer,1986,37:179
15 Broker EB,Suter L,Bruggen J,et al.International Journal of Cancer,1985,36:29
16 Gutierrez J,Lopez Nevot MA,Cabrera,et al.Experimental and Clinical Immunogenetics,1987,4:44
17 Lee JE,Lowyam,Thompson WA,et al.Gastroenterology,1996,111:426
18 Mohmori S,Yasunaga Y,Machara K,et al.Tissue Antigens,1997,50:277
19 Ogoshi K,Tajima T,Mitomi T,et al.Cancer,1994,73(9):2250, 百拇医药
单位:首都医科大学宣武医院核医学科,北京PET中心,北京100053
关键词:
基础医学与临床990603 Abstract The carcinogenesis and development is a progress of multi-gene alterations in the human gastric cancer (HGC).In order to determine the relation between the aberration of these genes and gastric cancer,we chose c-met (7q31)、hMLH1 (3p21)、E-cadherin (16q22.1) and HLA loci DQA1、DR2、DR3、DR4、DR7、DR9 and detected their changes in 32 tumor specimens of intestinal type HGC and 4 cell lines of gastric cancer by performing analysis of SSP/PCR、PCR/SSCP and MSI technigues.Our data show that none point mutation was detected in c-met gene.We examined two microsatellites loci D3S1298 and D3S1561 in hMLH1 gene and detected that 6 cases retain MSI (Microsatellite Instability) and 2 cases of LOH (Loss of Heterozygosity) at D3S1298 and 2 cases of MSI at D3S1561.We also examined E-cadherin gene at two microsatellites loci D16S3083 and D16S3095 close to the gene and detected that 5 cases retain MSI and 1 case of LOH at D16S3083 and no change at D16S3095.The point mutation incidence of HLA-DR4 loci is 9/20 (45%),higher than the other loci in HLA-Ⅱ.High frequent deletion,expression deregulation and methylation of mts1/p16 gene were detected in cell lines and solid tumors from human gastric cancer patients.
, 百拇医药
Our data showed that the point mutation of c-met gene is not the main pattern of alteration in intestinal type HGC that is consistent with the previous results.E-cadherin and hMLH1 are related to intestinal type HGC but whether they are susceptibility gene still need further study.The point mutation of the HLA-Ⅱ loci DR4 is closely related to intestinal type HGC.Methylation of mts1/p16 gene 5 CpG island might be plays an important role in the carcinogenesis in HGC.
, 百拇医药
Key words Gastric cancer Mismatch repair genes Susceptibility Methylation p16 HLA-DR4
1 引言
人类经过一百多年的努力,通过对肿瘤遗传家系分析、流行病学以及大量的动物实验研究证明了肿瘤的发生受遗传因素的影响,特别是近二十年来,已进一步明确肿瘤是一种环境因素与遗传因素相互作用导致的一类疾病。大多数的环境致病因素如饮食、病毒、化学物质、射线的致癌作用都是通过影响遗传基因使遗传物质发生一系列的变化而致。目前研究的结果已表明肿瘤是细胞中多种基因突变累积的结果,突变主要发生在三类细胞基因,即癌基因、肿瘤抑制基因和DNA修复基因。通常这些基因在细胞中行使正常的生物学功能,对细胞的增殖和分化过程起重要调控作用。在某些致病因素作用下这些基因发生点突变、扩增、重排、缺失或甲基化状态的改变。目前的研究结果表明在大多数肿瘤中可以检测到这三类基因的变异,这些基因的变异有可能受机体遗传易感性的影响。为了进一步明确肿瘤的遗传易感性,鉴定和克隆与肿瘤相关的易感基因已成为肿瘤研究领域的一个重要科学问题。
, 百拇医药
2 肿瘤的遗传易感性和肿瘤易感基因
有某些遗传缺陷或疾病的个体会表现出易患某些肿瘤的倾向,这就是一种对肿瘤的遗传易感性。机体的性状是遗传与环境相互作用的结果。某一地区有肿瘤家族聚集现象,这一方面与不良的环境因素有关,同时也取决于不同人群对肿瘤易感性的差异。遗传易感性就是遗传变异对环境致癌因素的敏感程度。肿瘤的易感性除涉及到癌基因、抑癌基因、DNA修复基因等与肿瘤发生密切相关的基因的变化以外,还涉及到免疫缺陷、代谢酶系统改变和DNA-染色体的不稳定性等。遗传易感性是致癌物在某些遗传素质下,通过体内代谢活化而致癌,而体内代谢酶系统的差异是直接影响肿瘤易感性的基础。染色体脆性部位(fraglesite,fra)是染色体上随机的断裂点,它表示了染色体的不稳定性,许多研究提示染色体脆性位点与肿瘤易感性密切相关,这些不稳定的染色体和染色体上存在的脆性位点也和基因一样可以遗传,有些脆性位点是致癌剂作用敏感点及癌基因同位点,肿瘤细胞的染色体缺失和重排往往发生在这些脆性部位,在多种因素作用下,脆性位点变得十分敏感,不稳定性升高,导致染色体DNA发生断裂、丢失、重排和突变,从而导致细胞内重要基因(癌基因、抑癌基因和DNA修复基因)的变异,最终导致细胞癌变和肿瘤发生。在对肠型胃癌的研究中已知有多种癌基因(如ras、met、erbB2、akt2)、抑癌基因(P16、P53、APC)、转移抑制基因nm23等以不同变异方式(如点突变、过量表达、缺失、扩增)参与了不同阶段的发病。这些基因中有哪些基因对胃癌发病真正易感或者还有哪些未被发现的基因与此病易感现在仍不十分清楚。Guilford等[1]在对三个大的家族性胃癌的家系的研究中发现E-cadherin基因与弥漫性胃癌的发病密切相关。HNPCC(遗传性非息肉性结直肠癌)是西方国家的多发肿瘤,有明显的家族遗传史,研究发现与这种疾病密切相关的是一组错配修复基因。不同种族不同个体对疾病的易感性的差异有很大程度上是由遗传因素决定的,HLA是第一个被发现与疾病有明确联系的遗传系统,HLA基因的多态性与疾病的易感性有关,是研究肿瘤易感基因的一个热点问题。
, http://www.100md.com
3 肠型胃癌发病过程中癌基因与抑癌基因改变的规律和特点
原癌基因是一类编码关键性调控蛋白质的正常细胞基因。它编码的蛋白质几乎存在于细胞的各个部位包括细胞核、细胞质和细胞膜,其主要的功能是调节细胞的增殖与分化,在细胞生长方面起着重要的调节功能,原癌基因只有当其发生突变导致正常结构和功能发生改变时才具有致癌作用。癌基因突变在肿瘤发生过程中起促进作用。与此相反抑癌基因是一类可以抑制细胞增殖并能潜在抑制癌变的基因。癌基因的激活和抑癌基因的失活究其原因是因为在一些物理、化学和生物等因素作用下促发了某些遗传的不稳定因素而引发的结果。
根据组织结构、生物学行为及流行病学特征,Lauren将胃癌分为肠型胃癌和弥漫型胃癌[2]。其中肠型胃癌被确定是一个从慢性萎缩性胃炎→肠上皮化生→异型增生I、Ⅱ、Ⅲ级→胃癌的演变过程。在对肠型胃癌的发病规律以及细胞癌变及肿瘤发生发展过程中基因变异规律的研究中已经确定胃癌的发生、发展是多基因变异累积的结果(见图1)[3]。胃癌高发区的研究显示,当地的胃粘膜疾病的发病率很高,这可能是胃癌高发的主要原因。同时调查还发现在当地的部分家庭中有胃癌的家族聚居现象。这进一步说明了胃癌的发生发展是一个多因素多阶段的逐步演变过程,并受遗传因素的影响,其发生过程可能包含着复杂的病理机制。因此只有从分子水平上充分了解和阐明慢性胃粘膜疾病癌变过程中不同基因结构和表达异常的规律,特别是寻找一组与胃癌相关的肿瘤易感基因才是从根本上提高胃癌早期诊治水平的关键。

, 百拇医药
图1 基因变异方式和数量与胃癌了生发展的关系
Fig1 Accumulation of multiple gene changes in human gastric carcinogenesis
针对胃癌发生、发展过程中多基因变异的特性,以几类与肿瘤相关的基因为对象,鉴定这些基因变异在胃癌中的改变,进一步探讨与肿瘤易感性的关系。选择c-met原癌基因、错配修复基因hMLH1、E-cadherin基因以及HLA-Ⅱ类分子的(DQA1、DR2、DR3、DR4、DR7、DR9)6个基因位点,采用PCR系列技术(PCR/SSP、PCR/SSCP和MSI)对32例肠型胃癌标本和4个胃癌细胞系进行检测以确定上述基因在肠型胃癌中的变异情况。研究结果表明:经过对c-met基因突变热点的第17、18和19外显子的SSCP分析,未检测到点突变。对错配修复基因hMLH1的D3S1298和D3S1561两个位点进行微卫星不稳定性(Microsatellite Instability,MSI)检测,其中在D3S1298位点检测到6例MSI(19.4%),2例杂和性缺失(Loss of Heterozygosity,LOH),D3S1561位点有2例检测到MSI。在E-cadherin基因附近选择两个微卫星位点D16S3083和D16S3095进行MSI检测,D16S3083位点有5例检测到MSI(16%),1例有LOH,D16S3095位点未检测到异常带型。HLA-Ⅱ类基因区6个基因位点基因型在个体中存在着明显多态性,PCR-SSCP结果显示DR4基因位点点突变频率为45%,明显高于其它几个基因位点。
, http://www.100md.com
上述结果表明:c-met原癌基因在胃癌中的变化方式不是以点突变为主,符合以往的研究结果。hMLH1、E-cadherin基因均与肠型胃癌的发生有关,其相关性大小有待于进一步研究。HLA-Ⅱ类基因区DR4基因的突变可能与胃癌发生的易感性有关。
4 弥漫性胃癌中E-cadherin基因的改变
弥漫性胃癌有明显的家族聚集性,为了鉴定哪些基因与弥漫性胃癌易感, Guilford等对一个来自新西兰的大的弥漫型胃癌家系作一描述,用基因连锁分析通过微卫星标记在与肿瘤易感的侯选位点进行筛查,侯选基因之一为E-cadherin基因[1]。此基因位于16q22.1区,对于维持上皮组织的细胞与细胞之间的粘附有重要作用。它的功能的丧失对一些实体性肿瘤的永生性、侵袭性或恶性程度起促进作用[4]。根据体外实验和临床观察资料认为它是一种侵袭抑制基因[5],也有人认为它是一个抑癌基因。E-cadherin gene的失活性突变在胃癌细胞系[6]、原发性胃癌[7]、妇科肿瘤[8]、肺癌细胞系[9]和原发性肺癌[10]中均见报道。
, http://www.100md.com
E-cadherin在肿瘤中失活的机制可能通过突变、启动子甲基化和转录下游调节等发生[11]。了解其失活的机制可以指导治疗,恢复其表达。Yoshiura等在E-cadherin基因负性表达肿瘤细胞系中发现有高甲基化状态[5],而且对E-cadherin 基因表达阴性肿瘤细胞系用去甲基化物质5-azacytidine处理,结果使此基因重新表达并且使梭形细胞向上皮形细胞转化,重新获得细胞之间同源粘附作用。
不仅弥漫型胃癌的发病具有家族聚集性,据流行病学调查肠型胃癌的发病也有家族聚集性。肠型胃癌的发生是一个多阶段、多基因参与的过程,为了说明在这个过程中是否有E-cadherin基因的改变,我们选择了这个基因附近的与弥漫型胃癌显著相关的两个微卫星位点对肠型胃癌的32例标本和四个胃癌细胞系进行检测,结果发现D16S3083有6例异常带型,其中1例肿瘤比正常少一条带,属杂合性缺失LOH。其余5例肿瘤比正常多一至二条带,属于微卫星的不稳定性(Microsatellite Instebility,MSI),D16S3095未检测出异常带型。微卫星的不稳定代表了附近基因的改变,这两个微卫星位点与E-cadherin基因密切连锁,说明此基因在肠型胃癌中也有改变。E-cadherin基因的变化和功能的丧失与弥漫性胃癌的发病高度易感,在许多其他类型的散发型肿瘤中此基因高频率失活又提示此基因也与其他肿瘤的易感性也有关。因此利用MSI只能初步说明此基因在肠型胃癌中有改变,但具体变异方式需进行深入研究。
, http://www.100md.com
5 错配修复基因与细胞癌变的关系
现在越来越多的证据表明另一类重要的肿瘤易感基因―DNA修复基因与癌基因和抑癌基因一样在致瘤过程中起关键性作用,与抑癌基因不同之处在于一些抑癌基因是通过影响抑制细胞增殖或分化的信号而调节细胞生长,另一些是在DNA损伤或细胞周期受干扰的情况下阻断细胞生长或引起细胞凋亡。而DNA损伤修复基因在控制细胞生长过程中起被动的作用,这种基因突变导致的生物学功能并不直接改变细胞的生长状态,但是这种基因的失活可能增加受损伤细胞中癌基因和抑癌基因的突变频率。DNA的主要损伤为硷基损伤与DNA链的断裂。DNA的损伤是环境致癌因素作用于靶分子的结果,与肿瘤的发生有密切关系,但是并不是受环境致癌因素作用就一定要患癌。在生物体内有多种修复DNA损伤的途径,细胞的修复功能使生物体能在一定限度内克服环境因素对机体造成的不利作用,使机体免于产生疾病。目前在肿瘤研究方面DNA损伤修复基因之所以引起人们极大重视在很大程度上是对遗传性非息肉性结直肠癌(Hereditary Nonpolyposis Colorectal Cancer,HNPCC)的研究。
, 百拇医药
5.1 错配修复基因的生物学意义
错配修复基因是一组高度保守的看家基因,在原核真核细胞中都具有高度同源的序列。核苷酸错配可发生于三种情况,即DNA的物理损伤、DNA复制过程中核苷酸的错误掺入和基因重组,当错配发生时细胞内特异性酶系统即错配修复系统开始启动对错配碱基进行修复。目前在人类中发现的错配修复基因主要有四个成员分别为hMSH2、hMLH1、hPMS1、hPMS2。这几个基因在染色体上的位置、结构以及在HNPCC中的作用方式已经研究的比较清楚(见表1)。
表1 人类错配修复基因及其与HNPCC的关系*
Table1 Correlation between HNPCC and DNA Mismatch repair gene
Genes
, http://www.100md.com
Chromosome
lication
Homologue
Relevance ratio
in HNPCC
Changes in HNPCC
Bacteria
Yeast
hMSH2
2p16
mutS
MSH2
, http://www.100md.com
50%~60%
codon622(Pro-Leu)
GTBP
2p16
mutS
MSH2
frame shift(HCT-15)
hMLH1
3p21
mutL
MLH1
30%
, 百拇医药
codon 578-622(LOH)
codon 519(T insertion)
homzygosity deletion (H6)
hPMS1
2q31-33
mutL
PMS1
5%
codon 195 -233(deletion in frame)
codon 233(Gln-termination codon)
, 百拇医药
hPMS2
7p22
mutL
PMS2
5%
codon 268-269(deletion in frame)
*引自邓锡云、曹亚.国外医学遗传学分册,1997,20(1).
5.2 错配修复基因缺陷与细胞癌变和肿瘤的发生、发展
在研究HNPCC的过程中相继发现了hMSH2、hMLH、hPMS1和hPMS2等四个人类错配修复基因。HNPCC是西方国家常见的肿瘤易感性症侯群,每200人中就有1人受累,受累的个体在50岁以前常发生结直肠癌、子宫内膜癌、卵巢癌、胃癌以及其他一些脏器的肿瘤,通过研究发现部分HNPCC患者存在微卫星的不稳定性(Microsatelite Instability,MSI)。芬兰学者Peltomaki[12]等选择了两个HNPCC家系用微卫星标记对上述两家系的整个基因组DNA进行筛选,对2号染色体上HNPCC基因进一步研究第一次找到了与细菌错配修复基因MutS同源的hMSH基因。随后又分别得到hMLH1,hPMS1和hPMS2基因。
, http://www.100md.com
随着错配修复缺陷在HNPCC及其他肿瘤中的发现,它与肿瘤的关系越来越受到广泛的重视。目前在许多肿瘤细胞里都发现有微卫星序列不稳定现象,在这些肿瘤细胞中证实有错配修复功能的缺陷。许多实验也表明错配修复对于维持微卫星序列稳定性有重要作用,人们推测错配修复功能缺陷导致肿瘤可能是由于错配修复功能缺陷使基因突变事件不断放大、积累,使大量错误信息遍布于整个基因组所致。错配修复基因作为从细菌到人类都存在的高度保守的看家基因,对于DNA错配的修复、维持DNA复制的保真度起到极其重要的作用,对其机制的深入研究将有利于揭示肿瘤的发生机制。
研究发现人的3p21区不仅在肺癌、乳腺癌、肾癌、恶性间皮瘤等多种肿瘤中有变异,而且在胃癌中也有明显异常。错配修复基因的成员之一hMLH1基因就定位于3p21.3,与DNA的损伤修复有关。我们在此基因内选择了两个微卫星位点D3S1298和D3S1561对32例肠型胃癌和四个胃癌细胞系进行检测。结果在D3S1298位点有一例标本PCR扩增阴性,同样在另一微卫星位点D3S1561有一例标本和一个胃癌细胞系PAMC82其PCR扩增阴性,说明这个微卫星位点的侧翼序列有改变,也就是这个基因本身在这些肿瘤组织中有变化。另外在D3S1298位点PCR扩增阳性的31例标本中有8例出现异常带型,其中两例有LOH,6例有MSI。在D3S1561位点有2例异常带型,均为MSI。以上结果表明在肠型胃癌发病中错配修复基因hMLH1可能由于结构的改变导致功能的丧失。根据这些微卫星位点检测中存在的不稳定现象推测在胃癌的发病过程中当核酸发生错误的时候一些错配修复基因、p53等的具有监视功能的基因发生了变异未能起到监视和修复的作用,使胃粘膜在由正常到肿瘤的过程中基因突变事件不断放大、积累,使大量错误信息遍布于整个基因组所致。明确了胃癌中错配修复基因有改变以后,就要深入研究它的变异方式以及导致其改变的根本原因,确定其是否与胃癌发病真正易感。
, http://www.100md.com
6 HLA基因的多态性与肿瘤的易感性
6.1 HLA区基因结构特征
人类主要组织相容性复合物(Major histocompatibility complex,MHC)基因组编码HLA抗原(Human leukocyte antigene),其基因组存在于6p21.3区,长度约为3600~4000kb占全部人类基因组区域的0.1%。HLA区是人类MHC基因组中基因密度极高的区域之一。该区包括100多个基因座,633个等位基因[13],每个基因编码一个特异性抗原。
6.2 HLA基因的多态性决定疾病的易感性
HLA系统是已知人类最复杂的显性多态遗传系统,其多态性是指随机婚配的群体中同一基因位点可以存在两种以上的基因型。基因的多态性并不一定影响基因的功能,但可以作为区别个体的标志。目前已知HLA的各位点上等位基因的总数为633个,不同群体和地区各等位基因频率不尽相同,可编码出大量不同的HLA分子。即使在同一个个体中,由于HLA两条单倍型的两位点等位基因编码的α、β链可按顺式和反式不同方式组合形成不同的杂合二聚体,而且不同种族的两位点基因编码的α、β链也可以组合形成如DRα-DRβ这样的族间分子,因此大大增加了体细胞表面的HLA分子的多样性。HLA的多态性决定着免疫应答和疾病易感性的个体差异。HLA与疾病的相关性归纳起来有以下两种情况:第一,HLA决定着对特定自身或非自身抗原发生免疫逃逸或免疫应答的个体差异,而这种差异直接决定着人群对疾病的易感性。第二,和HLA密切连锁的HLA之外的致病基因存在着和特定HLA等位基因的连锁不平衡性。
, 百拇医药
不同个体对疾病的易感性的差异在很大程度上是由遗传因素所决定的,HLA是第一个被发现与疾病有明确联系的遗传系统。迄今已发现60余种疾病与HLA相关。近年来开展的多种疾病与HLA区微卫星标记的相关性有助于我们更好地定位疾病易感基因,更进一步确定涉及肿瘤遗传易感性的基因。最终有助于阐明某些疾病的发病机制,并在此基础上制定新的肿瘤防治措施。
6.3 HLA与肿瘤
HLAⅠ类或Ⅱ类基因在肿瘤细胞中表达的变化与肿瘤生长和转移有密切的相关性。已有的研究表明在人的肿瘤细胞HLA-Ⅰ类抗原表达丧失与肿瘤的分化程度、转移能力有关[14]。恶性黑色素瘤的进展阶段有HLA-DR抗原的表达,此抗原的表达可能提示恶性黑色素瘤的预后不好[15]。但是在结肠癌和喉癌中却有相反的情况,即HLA-DR的表达预示着这类肿瘤的预后较好[16]。
胃癌是一个多因素参与的疾病,已知胃癌的发病机制与某些基因的改变有关。在MHC基因的表达与人的胃癌关系的研究中有报道HLA-Ⅱ类基因DQB1*0301在白种人中与胃癌的发病密切相关[17]。M.Ohmori等在研究HLA基因在日本人中与胃癌的关系结果发现相关性不是很大[18]。可能的解释就是环境因素例如饮食等在导致日本人胃癌的基因变化方面所起的不可忽视的作用。另有报道[19]在低分化型的胃腺癌HLA-DR4抗原的表达与淋巴结转移有高度相关性。我们选择了DQA1、DR2、DR3、DR4、DR7、DR9等六对引物对32例肠型胃癌及癌旁组织进行SSP-PCR扩增,对基因型阳性病例又作SSCP点突变检测,结果发现HLA-DR4基因位点点突变频率很高,说明此基因位点的改变与胃癌发病易感性有关。SSCP带型显示这些基因位点明显的多态性。有纯合互补两条带型、杂合四链型、异源双链和变性不彻底的两条带型等等。国外在对HLA与胃癌的相关性研究方面作过几篇报道:其中Lee等[7]的研究结果表明HLA-Ⅱ基因DQB1-0301在白种人中与胃癌的发病密切相关。Oyoshi等[10]的研究结果表明,在低分化的胃腺癌中HLA-DR4抗原表达与淋巴结转移之间存在着密切的关系,有淋巴结转移的病人HLA-DR4抗原表达阳性率高。这些发现进一步提示人的肿瘤的组织相容性抗原在影响免疫应答和免疫逃逸机制方面的重要作用。
, http://www.100md.com
7 小结
肿瘤已成为一类严重危害人类健康的疾病,其发病的主要原因是遗传和环境因素相互作用的结果,特别是在环境致病条件的作用下,使机体内的某些基因发生改变,从而导致细胞增殖与分化的平衡失调,使细胞发生癌变。人们已经逐渐认识到晚期恶性肿瘤由于多种基因、多种变异方式的累积给治疗带来了极大的困难,按人类目前的知识水平在较短时间内攻克晚期恶性肿瘤是难以达到目标,因此对肿瘤进行预防和早期诊治,就要从研究肿瘤的遗传易感性和易感基因入手。我们的研究提示c-met基因在肠型胃癌中的变化方式不是以点突变为主。与以往的研究结果相符:c-met基因在胃癌中的变化是以过表达和基因扩增为主,在癌变早期以过表达为主,基因扩增与肿瘤的快速生长有关。E-cadherin基因不仅是弥漫型胃癌发生的易感基因而且与肠型胃癌的发病也有相关性。错配修复基因hMLH1与肠型胃癌的发病相关,但是胃癌发生的易感基因仍有待于进一步证实。HLA-DR4基因位点的点突变与肠型胃癌的易感性有关。HLA区域基因位点的突变使与HLA某等位基因连锁的某些致病基因发生了变化,这可能是导致疾病发生的更为重要的原因。
, 百拇医药
参考文献
1 Guiford P,Hopkins J,Harraway J,et al.Nature,1998,392(26):402
2 Lauren P.Acta Pathol Microbiol Scand A,1965,64:34
3 吕有勇.中华医学杂志,1997,77(11):85
4 Hiraguri S,Godfrey T,Nakamura H,et al.Cancer Research,1998,58:1972
5 Yoshiura K,Yaekanai,Ochiai A,et al.Proc Natl Acad Sci USA,1995,92:7416
, http://www.100md.com 6 Oda T,Kanai Y,Oyama T,et al.Proc Natl Acad Sci USA,1994,91:1858
7 Becker K F,Atkinson M J,Reich H,et al.Cancer Res,1994,54:3845
8 Risinger JI,Berchuck A,Kohler MF,et al.Nat Genet,1994,7:98
9 Pierceall W,Woodard A,Morrow J,et al.Oncogene,1995,11:1319
10 Berx G,Cleton-Jansen A M,Strumane K,et al.Oncogene,1996,13:1919
11 Bussemakers M G,Giroldi L A,Vanibokhoven A,et al.Biochem Biophys Res Commun,1994,203:1284
, 百拇医药
12 Peltomaki P,Aaltonen L,Sistonen P,et al.Scinece,1993,260(5107):810
13 Bodmer JG,Marsh SGE,Albert ED,et al.Tissue Antigens,1996,49:297
14 Momburg F,Degener T,Baccbus L,et al.Internationnal Journal of Cancer,1986,37:179
15 Broker EB,Suter L,Bruggen J,et al.International Journal of Cancer,1985,36:29
16 Gutierrez J,Lopez Nevot MA,Cabrera,et al.Experimental and Clinical Immunogenetics,1987,4:44
17 Lee JE,Lowyam,Thompson WA,et al.Gastroenterology,1996,111:426
18 Mohmori S,Yasunaga Y,Machara K,et al.Tissue Antigens,1997,50:277
19 Ogoshi K,Tajima T,Mitomi T,et al.Cancer,1994,73(9):2250, 百拇医药