水中臭氧的快速测定
作者:宋钰 蔡士林 张卫强
单位:中国预防医学科学院环境卫生监测所,北京 100021
关键词:臭氧;硫酸-4-氨基-N,N-二乙基苯胺;分光光度法
卫生研究000310 摘要:建立了水中臭氧的KI-硫酸-4-氨基-N,N-二乙基苯胺(DPD)分光光度测定法。此方法是在pH3.35条件下,根据臭氧与碘化钾的定量反应:O3+2I-+2H+→O2+I2+H2O,生成的I2与DPD反应显粉红色,在510nm处用分光光度计测定,直接测定的线型范围为0~1.00mg/L,最低检测浓度为0.01 mg/L,相对标准偏差为1.2%~2.7%(n=10),回收率在98.6%~106.6%之间。应用此方法对各种水样进行了测定并和碘量法做了比较,结果基本相符。该方法实用、可靠,用于实际水样中臭氧的测定,结果满意。
, 百拇医药
中图分类号:R123.1 文献标识码:B
文章编号:1000-8020(2000)03-0151-03
Rapid determination of the ozone in water
Song Yu, Cai Shilin, Zhang Weiqiang
(Institute of Environment Health Monitoring, Chinese Academy of Preventive Medicine, Beijing 100021,China)
Abstract:A new potassium iodide-N, N-diethy1-1,4-phenylen-ediammonium sulfate(DPD) spectrophotometry method for the determination of the ozone in water was established. The method was based on the quantitative reaction between the ozone and potassium iodide in buffered solution(pH 3.35):O3+2I-+2H+→O2+I2+H2O.Iodine could react with DPD regent and produce pink color. Its absorption was determined at 510nm with spectrophotometer. The range of direct determination was 0―1.00mg/L. Beer's law was obeyed in this range. The detection limit was 0.01mg/L. The relative standard deviations were from 1.2% to 2.7%(n=10). The recoveries were from 98.6% to 106.6%.Water samples were determined with both this method and iodimetry. The results were comparable. The method was applied to the determination of the ozone in water sample with satisfactory results. It was practical and reliable.
, 百拇医药
Key words:ozone, N, N-diethy1-1,4-phenylen-ediammonium sulfate, spectrophotometry
臭氧是一种强氧化剂,能破坏使水产生臭和味的有机化合物和有色的有机物,能将亚铁和亚锰氧化为高价氧化物,然后通过沉淀过滤除去;臭氧还是一种强杀菌剂,对杀灭细菌和病毒等微生物有显著的效果。
目前水中臭氧的测定方法主要有碘量法、靛蓝比色法、尿素法、铬酸紫钾(ACVK)法和连续自动测定法等。国内常用的是碘量法[1],但此法操作复杂,需要气源,难以实现现场快速测定的要求。本文针对水中的臭氧提出了一种KI-硫酸-4-氨基-N,N-二乙基苯胺(DPD)分光光度测定方法。此法是通过臭氧氧化碘化钾生成碘,碘再与DPD作用显粉红色这一机理,在510nm处用分光光度计测定,用EDTA-2Na消除Ca2+、Fe3+、SO2-4和HCO-3的干扰,而EDTA-2Na的加入和用量对吸光度无影响。经选择各种水样进行测定,都得到较为满意的结果,并且此方法操作简单,适用于现场测定,在测定高浓度臭氧时,采用直接稀释后测定,同时也可消除干扰物的影响。
, http://www.100md.com
1 材料与方法
1.1 仪器
722型分光光度计(上海第三分析仪器厂);BX4型臭氧发生器(北京环境科学保护研究所);Mettler天平。
1.2 试剂
臭氧标准使用液(用碘配制): 称取13.0g碘和20.0g碘化钾于乳钵中,加少许纯水(本文中纯水均为离子交换法制备的去离子水,25℃时电阻率大于5×105Ω.cm)研磨使碘溶解,加纯水稀释定容于100ml容量瓶中,用玻璃砂芯漏斗过滤,贮于棕色瓶中,用0.1mol/L的硫代硫酸钠溶液标定,该碘液的浓度为0.1014mol/L。移取0.1014mol/L的碘液38.66ml用纯水稀释定容于1000ml的容量瓶中,该碘液的浓度为1000mg/L,移取该碘液5.29ml用纯水稀释定容于100ml容量瓶中,得到52.90mg/L的碘使用液,该碘液相当于臭氧标准使用液5.00mg/L。
, http://www.100md.com
碘化钾溶液(20g/L):称取2g分析纯的碘化钾,用新煮沸并冷却至室温的纯水溶解并定容于100ml的容量瓶中,贮于棕色瓶中。
DPD溶液(1g/L):称取1gDPD,溶于含0.8ml 1+3硫酸溶液及0.2gEDTA-2Na的无氯纯水(在无氯纯水中加入少量氯水或漂白粉精溶液,使水中总余氯浓度约为0.5mg/L,加热煮沸除氯,冷却后备用)中,并稀释定容至1000ml的容量瓶中。用棕色瓶在冷暗处保存,贮存中如溶液颜色变红(在510nm处试剂空白的吸光度超过0.002)即应重配。
EDTA-2Na溶液(4g/L):称取4g分析纯的EDTA-2Na用纯水溶解并定容于1000ml的容量瓶中。
缓冲溶液(pH3.35):称取8.28g分析纯的柠檬酸和5.40g柠檬酸三钠用纯水溶解并定容于1000ml的容量瓶中。
1.3 实验方法
, 百拇医药
水中臭氧的测定:向10ml的具塞比色管中加入pH3.35的缓冲溶液1.0ml,EDTA-2Na溶液1.0ml,KI溶液1.0ml,DPD溶液1.0ml,加纯水至9.0ml,混匀后加入1.0ml臭氧水,颠倒混匀,3分钟后在722型分光光度计上用1cm的比色皿,于波长510nm处,以纯水为参比,测定溶液的吸光度,然后在以相同方法测定得到的臭氧标准溶液的工作曲线上查得相应的臭氧浓度,再乘以稀释倍数(10)既为水中臭氧的浓度(在测定臭氧浓度时,可以根据臭氧的实际浓度调整臭氧水与纯水的加入量,使臭氧在测定时的浓度在0~1.00mg/L之间,计算臭氧的实际浓度时再乘以稀释倍数即可)。
2 结果
2.1 吸收曲线
分别测定低、中、高3个臭氧浓度的样品显色后在不同波长下的吸光度,由实验结果可知,该反应的吸收曲线分别在510nm和550nm处有2个吸收峰,最后确定峰形较缓的510nm为该方法的测定波长。
, http://www.100md.com
2.2 酸度的影响
2.2.1 DPD与I2反应的最佳pH 在不同pH的缓冲溶液中只加入DPD溶液,以纯水为参比测定溶液的吸光度A1(试剂空白),同时在不同pH的缓冲溶液中加入DPD溶液和碘标准使用液,以试剂空白为参比测定溶液的吸光度A2,实验结果如图1。因pH大于2.86时,溶液有稳定的吸光度,而pH大于5.10时试剂空白的吸光度明显增加,因此DPD与I2反应的最佳pH值在2.86~5.10之间。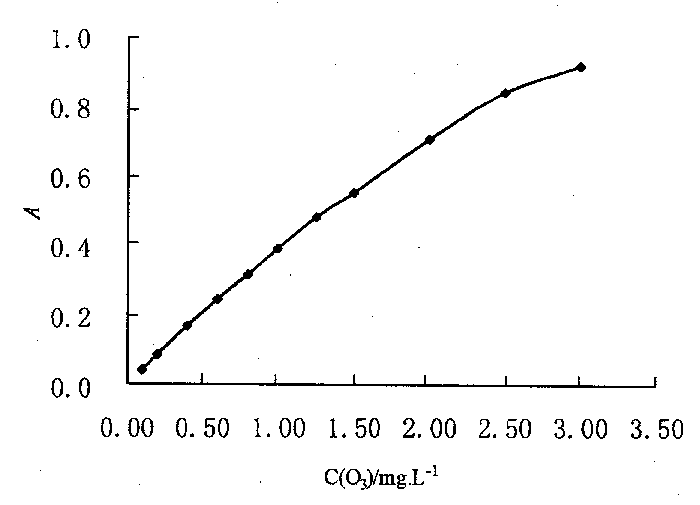
图1 DPD与I2反应的最佳pH
2.2.2 O3氧化I-转化为I2的最佳pH 取不同pH的缓冲溶液5ml代替碘量法中的硫酸溶液对臭氧水样进行滴定,测定结果记为C1,测定每个样品的同时用碘量法作对比滴定,测定结果记为C2,然后计算该组测定结果的相对误差,即(C1-C2)×100%/C2。再做速测法和碘量法测定同一水样臭氧浓度的实验,也计算该组测定结果的相对误差,即(C速测法-C碘量法)×100%/C碘量法。实验结果如附表所示。2组实验均显示,溶液的pH应在3.13~3.81之间,2组实验结果的差别才能控制在±5.0%内。
, http://www.100md.com
附表 O3氧化I-转化为I2的最佳pH 编号
pH
(C1-C2)
×100%/C2
(C速测法-C碘量法)
×100%/C碘量法
1
2.85
-4.5
/
, http://www.100md.com
2
3.13
0.9
-5.4
3
3.35
3.9
3.3
4
3.58
0
2.8
5
, 百拇医药 3.81
-3.1
-2.3
6
4.02
-11.9
-9.6
综合实验2.2.1和2.2.2的结果可以看出,控制溶液的pH在3.13~3.81之间,O3氧化I-转化为I2有较好的转化率,并且生成的I2可与DPD充分反应。该方法选用pH3.35的缓冲溶液,可将溶液的pH值较好的控制在所需范围内。
2.3 显色时间的影响
, http://www.100md.com
测定反应后不同时间溶液的吸光度,由实验结果可知吸光度在3分钟后即可达到稳定,10分钟后吸光度略有下降,因此确定显色后3分钟立即测定吸光度。
2.4 显色温度的影响
测定不同环境温度下,同一臭氧溶液显色后的吸光度,由实验结果可知,环境温度在0~30℃之间对该反应无影响。
2.5 碘化钾用量对吸光度的影响
测定不同KI加入量时显色后溶液的吸光度,由实验结果可知,KI用量0.4~6.4mg/ml对吸光度无影响,因此确定用2.0mg/ml(相当于20g/L的KI溶液1.0ml)作为实际测定条件。
2.6 DPD用量对吸光度的影响
测定不同DPD加入量时显色后溶液的吸光度,由实验结果可知,DPD的用量在0.08~0.50mg/ml之间对吸光度无影响,因此确定用0.10mg/ml(相当于1g/L的DPD溶液1.0ml)作为实际测定条件。
, 百拇医药
2.7 干扰离子的影响及消除
同时测定含有干扰离子(实际测定时的浓度相当于饮水卫生标准最高限量的10倍)和不含干扰离子的溶液的吸光度,比色管中均不加入EDTA-2Na溶液,由实验结果可知,干扰离子Mn2+、Cu2+、Zn2+、Mg2+、NO3-N、Cl-、F-、SiO2对该反应无影响,Fe3+、SO2-4、Ca2+、HCO-3对该反应有影响。比色管中若加入4 g/L的EDTA-2Na溶液1.0ml,即能很好的消除SO2-4、Ca2+、Fe3+和HCO-3的干扰,而EDTA-2Na的加入和用量对吸光度无影响。
, 百拇医药
2.8 水样的测定
2.8.1 工作曲线依1.3实验方法所得结果作工作曲线。实验结果如图2,由实验结果可知,臭氧浓度在0~1.00mg/L的范围内符合比耳定律,最低检测浓度为0.01mg/L,此时溶液的吸光度为0.02。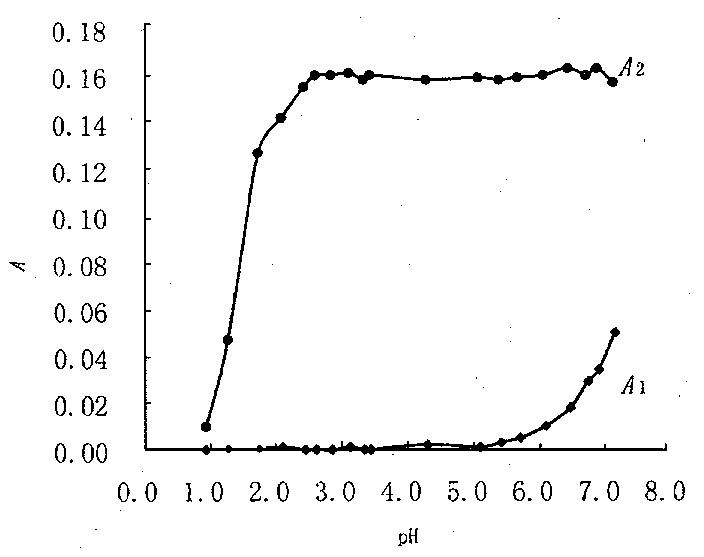
图2 工作曲线
经计算,臭氧浓度在0~1.00mg/L时,n=6,r=0.99954,b=0.382,a=0.0122。
2.8.2 方法的精密度 分别测定低、中、高(浓度分别为0.12、0.25、0.32mg/L)3个样品中臭氧的含量,每个样品测定10个结果,3组实验的相对标准偏差分别为2.7%、1.7%和1.2%。由实验结果可以看出,该方法具有较好的精密度。
, http://www.100md.com
2.8.3 方法的准确度 用速测法和碘量法同时测定8份水样(4份去离子水,3份矿泉水,1份湖泊水)的臭氧含量,然后进行比较,速测法与碘量法测定结果的相对误差在-1.3%~6.0%,说明该方法具有较好的准确度。
2.8.4 方法的回收实验 在反应液中预先加入标准碘使用液,再进行测定,与不加入标准碘使用液的测定结果进行比较,该方法的回收率为98.6%~106.6%,说明该方法有较好的回收率。
本法适宜经臭氧消毒的生活饮用水、矿泉水中臭氧浓度的测定。相当于饮水卫生标准10倍的Mn2+、Cu2+、Zn2+、Mg2+、NO3-N、Cl-、F-、SiO2、SO2-4、Ca2+、Fe3+、HCO-3对该反应无影响。
, 百拇医药
该反应的pH值对I-转化为I2及I2与DPD的反应影响很大,因此采用pH3.35柠檬酸盐缓冲液,将反应的pH控制在3.13~3.81之间,柠檬酸还能与金属离子络和,具有抗金属离子干扰的作用。
该方法的各种固体试剂按测定时的使用量成比例地混匀,再加入稀释剂制粒压成片剂后,试剂的稳定性更好。片剂溶解后即可供现场测定臭氧使用,尤其适用于低浓度臭氧的测定,操作简单、准确,易于掌握。
作者简介:宋钰,女,本科,实习研究员
参考文献
1,张宏陶.水质分析大全.重庆:科学技术出版社重庆分社,1989
2,吴辛友,袁盛铨,翟金铣.分析试剂的提纯与配制.北京:冶金工业出版社,1989
3,常文保,李克安.简明分析化学手册.北京:北京大学出版社,1981
4,楼书聪.化学试剂配制手册.南京:江苏科学技术出版社,1993
(1999-10-27收稿), 百拇医药
单位:中国预防医学科学院环境卫生监测所,北京 100021
关键词:臭氧;硫酸-4-氨基-N,N-二乙基苯胺;分光光度法
卫生研究000310 摘要:建立了水中臭氧的KI-硫酸-4-氨基-N,N-二乙基苯胺(DPD)分光光度测定法。此方法是在pH3.35条件下,根据臭氧与碘化钾的定量反应:O3+2I-+2H+→O2+I2+H2O,生成的I2与DPD反应显粉红色,在510nm处用分光光度计测定,直接测定的线型范围为0~1.00mg/L,最低检测浓度为0.01 mg/L,相对标准偏差为1.2%~2.7%(n=10),回收率在98.6%~106.6%之间。应用此方法对各种水样进行了测定并和碘量法做了比较,结果基本相符。该方法实用、可靠,用于实际水样中臭氧的测定,结果满意。
, 百拇医药
中图分类号:R123.1 文献标识码:B
文章编号:1000-8020(2000)03-0151-03
Rapid determination of the ozone in water
Song Yu, Cai Shilin, Zhang Weiqiang
(Institute of Environment Health Monitoring, Chinese Academy of Preventive Medicine, Beijing 100021,China)
Abstract:A new potassium iodide-N, N-diethy1-1,4-phenylen-ediammonium sulfate(DPD) spectrophotometry method for the determination of the ozone in water was established. The method was based on the quantitative reaction between the ozone and potassium iodide in buffered solution(pH 3.35):O3+2I-+2H+→O2+I2+H2O.Iodine could react with DPD regent and produce pink color. Its absorption was determined at 510nm with spectrophotometer. The range of direct determination was 0―1.00mg/L. Beer's law was obeyed in this range. The detection limit was 0.01mg/L. The relative standard deviations were from 1.2% to 2.7%(n=10). The recoveries were from 98.6% to 106.6%.Water samples were determined with both this method and iodimetry. The results were comparable. The method was applied to the determination of the ozone in water sample with satisfactory results. It was practical and reliable.
, 百拇医药
Key words:ozone, N, N-diethy1-1,4-phenylen-ediammonium sulfate, spectrophotometry
臭氧是一种强氧化剂,能破坏使水产生臭和味的有机化合物和有色的有机物,能将亚铁和亚锰氧化为高价氧化物,然后通过沉淀过滤除去;臭氧还是一种强杀菌剂,对杀灭细菌和病毒等微生物有显著的效果。
目前水中臭氧的测定方法主要有碘量法、靛蓝比色法、尿素法、铬酸紫钾(ACVK)法和连续自动测定法等。国内常用的是碘量法[1],但此法操作复杂,需要气源,难以实现现场快速测定的要求。本文针对水中的臭氧提出了一种KI-硫酸-4-氨基-N,N-二乙基苯胺(DPD)分光光度测定方法。此法是通过臭氧氧化碘化钾生成碘,碘再与DPD作用显粉红色这一机理,在510nm处用分光光度计测定,用EDTA-2Na消除Ca2+、Fe3+、SO2-4和HCO-3的干扰,而EDTA-2Na的加入和用量对吸光度无影响。经选择各种水样进行测定,都得到较为满意的结果,并且此方法操作简单,适用于现场测定,在测定高浓度臭氧时,采用直接稀释后测定,同时也可消除干扰物的影响。
, http://www.100md.com
1 材料与方法
1.1 仪器
722型分光光度计(上海第三分析仪器厂);BX4型臭氧发生器(北京环境科学保护研究所);Mettler天平。
1.2 试剂
臭氧标准使用液(用碘配制): 称取13.0g碘和20.0g碘化钾于乳钵中,加少许纯水(本文中纯水均为离子交换法制备的去离子水,25℃时电阻率大于5×105Ω.cm)研磨使碘溶解,加纯水稀释定容于100ml容量瓶中,用玻璃砂芯漏斗过滤,贮于棕色瓶中,用0.1mol/L的硫代硫酸钠溶液标定,该碘液的浓度为0.1014mol/L。移取0.1014mol/L的碘液38.66ml用纯水稀释定容于1000ml的容量瓶中,该碘液的浓度为1000mg/L,移取该碘液5.29ml用纯水稀释定容于100ml容量瓶中,得到52.90mg/L的碘使用液,该碘液相当于臭氧标准使用液5.00mg/L。
, http://www.100md.com
碘化钾溶液(20g/L):称取2g分析纯的碘化钾,用新煮沸并冷却至室温的纯水溶解并定容于100ml的容量瓶中,贮于棕色瓶中。
DPD溶液(1g/L):称取1gDPD,溶于含0.8ml 1+3硫酸溶液及0.2gEDTA-2Na的无氯纯水(在无氯纯水中加入少量氯水或漂白粉精溶液,使水中总余氯浓度约为0.5mg/L,加热煮沸除氯,冷却后备用)中,并稀释定容至1000ml的容量瓶中。用棕色瓶在冷暗处保存,贮存中如溶液颜色变红(在510nm处试剂空白的吸光度超过0.002)即应重配。
EDTA-2Na溶液(4g/L):称取4g分析纯的EDTA-2Na用纯水溶解并定容于1000ml的容量瓶中。
缓冲溶液(pH3.35):称取8.28g分析纯的柠檬酸和5.40g柠檬酸三钠用纯水溶解并定容于1000ml的容量瓶中。
1.3 实验方法
, 百拇医药
水中臭氧的测定:向10ml的具塞比色管中加入pH3.35的缓冲溶液1.0ml,EDTA-2Na溶液1.0ml,KI溶液1.0ml,DPD溶液1.0ml,加纯水至9.0ml,混匀后加入1.0ml臭氧水,颠倒混匀,3分钟后在722型分光光度计上用1cm的比色皿,于波长510nm处,以纯水为参比,测定溶液的吸光度,然后在以相同方法测定得到的臭氧标准溶液的工作曲线上查得相应的臭氧浓度,再乘以稀释倍数(10)既为水中臭氧的浓度(在测定臭氧浓度时,可以根据臭氧的实际浓度调整臭氧水与纯水的加入量,使臭氧在测定时的浓度在0~1.00mg/L之间,计算臭氧的实际浓度时再乘以稀释倍数即可)。
2 结果
2.1 吸收曲线
分别测定低、中、高3个臭氧浓度的样品显色后在不同波长下的吸光度,由实验结果可知,该反应的吸收曲线分别在510nm和550nm处有2个吸收峰,最后确定峰形较缓的510nm为该方法的测定波长。
, http://www.100md.com
2.2 酸度的影响
2.2.1 DPD与I2反应的最佳pH 在不同pH的缓冲溶液中只加入DPD溶液,以纯水为参比测定溶液的吸光度A1(试剂空白),同时在不同pH的缓冲溶液中加入DPD溶液和碘标准使用液,以试剂空白为参比测定溶液的吸光度A2,实验结果如图1。因pH大于2.86时,溶液有稳定的吸光度,而pH大于5.10时试剂空白的吸光度明显增加,因此DPD与I2反应的最佳pH值在2.86~5.10之间。

图1 DPD与I2反应的最佳pH
2.2.2 O3氧化I-转化为I2的最佳pH 取不同pH的缓冲溶液5ml代替碘量法中的硫酸溶液对臭氧水样进行滴定,测定结果记为C1,测定每个样品的同时用碘量法作对比滴定,测定结果记为C2,然后计算该组测定结果的相对误差,即(C1-C2)×100%/C2。再做速测法和碘量法测定同一水样臭氧浓度的实验,也计算该组测定结果的相对误差,即(C速测法-C碘量法)×100%/C碘量法。实验结果如附表所示。2组实验均显示,溶液的pH应在3.13~3.81之间,2组实验结果的差别才能控制在±5.0%内。
, http://www.100md.com
附表 O3氧化I-转化为I2的最佳pH 编号
pH
(C1-C2)
×100%/C2
(C速测法-C碘量法)
×100%/C碘量法
1
2.85
-4.5
/
, http://www.100md.com
2
3.13
0.9
-5.4
3
3.35
3.9
3.3
4
3.58
0
2.8
5
, 百拇医药 3.81
-3.1
-2.3
6
4.02
-11.9
-9.6
综合实验2.2.1和2.2.2的结果可以看出,控制溶液的pH在3.13~3.81之间,O3氧化I-转化为I2有较好的转化率,并且生成的I2可与DPD充分反应。该方法选用pH3.35的缓冲溶液,可将溶液的pH值较好的控制在所需范围内。
2.3 显色时间的影响
, http://www.100md.com
测定反应后不同时间溶液的吸光度,由实验结果可知吸光度在3分钟后即可达到稳定,10分钟后吸光度略有下降,因此确定显色后3分钟立即测定吸光度。
2.4 显色温度的影响
测定不同环境温度下,同一臭氧溶液显色后的吸光度,由实验结果可知,环境温度在0~30℃之间对该反应无影响。
2.5 碘化钾用量对吸光度的影响
测定不同KI加入量时显色后溶液的吸光度,由实验结果可知,KI用量0.4~6.4mg/ml对吸光度无影响,因此确定用2.0mg/ml(相当于20g/L的KI溶液1.0ml)作为实际测定条件。
2.6 DPD用量对吸光度的影响
测定不同DPD加入量时显色后溶液的吸光度,由实验结果可知,DPD的用量在0.08~0.50mg/ml之间对吸光度无影响,因此确定用0.10mg/ml(相当于1g/L的DPD溶液1.0ml)作为实际测定条件。
, 百拇医药
2.7 干扰离子的影响及消除
同时测定含有干扰离子(实际测定时的浓度相当于饮水卫生标准最高限量的10倍)和不含干扰离子的溶液的吸光度,比色管中均不加入EDTA-2Na溶液,由实验结果可知,干扰离子Mn2+、Cu2+、Zn2+、Mg2+、NO3-N、Cl-、F-、SiO2对该反应无影响,Fe3+、SO2-4、Ca2+、HCO-3对该反应有影响。比色管中若加入4 g/L的EDTA-2Na溶液1.0ml,即能很好的消除SO2-4、Ca2+、Fe3+和HCO-3的干扰,而EDTA-2Na的加入和用量对吸光度无影响。
, 百拇医药
2.8 水样的测定
2.8.1 工作曲线依1.3实验方法所得结果作工作曲线。实验结果如图2,由实验结果可知,臭氧浓度在0~1.00mg/L的范围内符合比耳定律,最低检测浓度为0.01mg/L,此时溶液的吸光度为0.02。

图2 工作曲线
经计算,臭氧浓度在0~1.00mg/L时,n=6,r=0.99954,b=0.382,a=0.0122。
2.8.2 方法的精密度 分别测定低、中、高(浓度分别为0.12、0.25、0.32mg/L)3个样品中臭氧的含量,每个样品测定10个结果,3组实验的相对标准偏差分别为2.7%、1.7%和1.2%。由实验结果可以看出,该方法具有较好的精密度。
, http://www.100md.com
2.8.3 方法的准确度 用速测法和碘量法同时测定8份水样(4份去离子水,3份矿泉水,1份湖泊水)的臭氧含量,然后进行比较,速测法与碘量法测定结果的相对误差在-1.3%~6.0%,说明该方法具有较好的准确度。
2.8.4 方法的回收实验 在反应液中预先加入标准碘使用液,再进行测定,与不加入标准碘使用液的测定结果进行比较,该方法的回收率为98.6%~106.6%,说明该方法有较好的回收率。
本法适宜经臭氧消毒的生活饮用水、矿泉水中臭氧浓度的测定。相当于饮水卫生标准10倍的Mn2+、Cu2+、Zn2+、Mg2+、NO3-N、Cl-、F-、SiO2、SO2-4、Ca2+、Fe3+、HCO-3对该反应无影响。
, 百拇医药
该反应的pH值对I-转化为I2及I2与DPD的反应影响很大,因此采用pH3.35柠檬酸盐缓冲液,将反应的pH控制在3.13~3.81之间,柠檬酸还能与金属离子络和,具有抗金属离子干扰的作用。
该方法的各种固体试剂按测定时的使用量成比例地混匀,再加入稀释剂制粒压成片剂后,试剂的稳定性更好。片剂溶解后即可供现场测定臭氧使用,尤其适用于低浓度臭氧的测定,操作简单、准确,易于掌握。
作者简介:宋钰,女,本科,实习研究员
参考文献
1,张宏陶.水质分析大全.重庆:科学技术出版社重庆分社,1989
2,吴辛友,袁盛铨,翟金铣.分析试剂的提纯与配制.北京:冶金工业出版社,1989
3,常文保,李克安.简明分析化学手册.北京:北京大学出版社,1981
4,楼书聪.化学试剂配制手册.南京:江苏科学技术出版社,1993
(1999-10-27收稿), 百拇医药