霉菌性鼻窦炎的临床、病理及CT影像研究
作者:黄明刚 杨萍 王茁
单位:黄明刚(陕西省人民医院CT室,陕西 西安 710068);杨萍(陕西省人民医院CT室,陕西 西安 710068);王茁(陕西省人民医院病理科,陕西 西安 710068)
关键词:
中国医学影像技术000811[中图分类号] R445.3 R322.3+1 [文献标识码] A
[文章编号] 1003-3289(2000)08-0637-02
本文搜集经病理证实的21例霉菌性鼻窦炎,对比分析其临床、病理及CT表现并探讨其发病机理及鉴别诊断。
1 资料与方法
搜集1989年至1999年在我院诊治、有完整资料的21例霉菌性鼻窦炎,男6例,女15例。年龄37~70岁,平均48.2岁,病史半年至20余年。全部病例均有术前CT检查,采用西门子SOMATOM DR3及岛津4800TF CT扫描机,层厚和间隔5mm,轴位和/或冠状扫描。1例病人同时行MR检查。观察内容:①临床:病史,症状,鼻腔检查及预后;②病理:常规HE染色,观察指标为霉菌菌丝,黏膜血管浸润及钙化;③霉菌培养:手术切除组织或分泌物的微生物培养并分类;④CT影像:病变位置、形态、范围、密度、骨质破坏,单窦、多窦及有无周围结构的侵犯,鼻腔及副窦结构。
, 百拇医药
分型:根据病变有无侵入黏膜动脉和鼻窦黏膜及骨壁坏死,将霉菌性鼻窦炎分为侵袭型和非侵袭型两型。
2 结果
2.1 临床表现 21例中侵袭型9例,非侵袭型12例,男6例,女15例,男女比例为1∶2.5。单侧20例,双侧1例。病史在0.5~1年的14例,1~2年的6例,20余年有1例。症状:脓涕,鼻阻伴头痛12例,涕中带血或间断性鼻衄8例,面颊部肿痛、张口困难1例,伴眼突2例,1例失明,发热、头痛、呕吐及嗅觉减退1例。5例合并有慢性鼻炎史,3例伴鼻息肉,1例合并糖尿病,1例患白血病,1例有风湿性心脏病。鼻腔专科检查情况:鼻中隔偏曲12例,鼻甲肥大6例,鼻黏膜充血14例,鼻息肉3例,鼻腔检查正常6例。预后:经过手术切除及抗霉菌治疗,1~2年后复查,18例无复发,1例复发,2例死亡。
2.2 CT表现 单窦病变16例(上颌窦15例,筛窦1例,累及多窦5例,窦外侵犯2例;病变形态呈片状破棉絮样10例,呈充满窦腔型6例,呈肿块型5例;病变密度不均匀,16例可见斑点状高密度影,中央分布11例,边缘分布2例,散在分布3例,平均CT值为(143.4±11.8)HU。7例有骨质破坏,以上颌窦内侧壁为主,5例上颌窦前壁增厚硬化,2例侵犯眼眶,1例并侵入颅内海绵窦、颞叶,出现多区域骨质破坏。合并鼻腔鼻旁窦结构异常14例,其中鼻中隔偏曲12例,鼻甲肥大6例,钩突弯曲3例,1例鼻中甲气化。合并鼻息肉3例。此外1例做MR检查,鼻腔内软组织阴影在T1WI上呈与脑实质信号相似的肿块影,T2WI呈明显低信号强度改变(图1,2)。
, 百拇医药
2.3 病理 浸润型光镜下见被覆复层纤毛柱状上皮黏膜组织中有大量炎性细胞、渗出物、细胞碎片及浆细胞和多核细胞浸润,在坏死组织中有大量浓密缠结的有隔菌丝,黏膜血管受侵。非浸润型则表现为肉芽组织内成团的霉菌菌丝,无黏膜血管受侵及组织坏死。18例HE染色见有斑片状钙化灶。
2.4 霉菌培养 12例经过培养检见霉菌,其中烟曲菌11例,黑曲菌1例,9例培养未检见真菌。
3 讨论
3.1 发病机制 霉菌性鼻窦炎的病理生理过程是各种原因导致鼻窦口狭窄或阻塞,造成窦腔内环境异常,包括分泌物的潴留,低氧状态,pH值下降,糖含量上升和黏稠度增加等,为病原微生物创造了适应的生长环境,在一定诱因下致人发病。造成鼻窦口狭窄的局部因素有鼻腔、鼻窦解剖畸形,局部黏膜病变,鼻息肉,鼻窦黏膜囊肿及异物等。诱因主要为人体免疫功能异常、机体抵抗力下降(如患有消耗性、代谢性疾病,长期使用抗生素、类固醇激素的患者)。近年来许多学者提出鼻腔鼻窦解剖畸形致鼻道复合体异常与鼻窦炎有密切关系。本组资料中,鼻腔、鼻窦结构异常者占66.7%(14/21),包括鼻中隔偏曲,鼻甲肥大气化及钩突变异等,23.8%(5/21)有慢性鼻炎史,合并鼻息肉14.3%(3/21),合并糖尿病、白血病等疾病有14.3%(3/21)。由此我们认为除环境因素、宿主因素外,鼻道复合体异常在鼻窦炎(包括特异性和非特异性)的发病原因中也占有重要的作用。
, http://www.100md.com
3.2 临床特点与病理 传统上将霉菌性鼻窦炎分为非侵袭型和侵袭型,前者又包括变应型和霉菌球,后者包括慢性无痛型和急性爆发型,本文主要为霉菌球型和慢性无痛型。本病多见于中年人,女性多于男性(2.5∶1),单侧发病为主,本组占95.2%,病程长短不一,短者数月,长者可达10余年,本文1例达20余年,临床症状主要有脓涕、鼻阻伴头痛或涕中带血或患侧鼻窦区压痛、面部肿胀,同慢性鼻窦炎比较症状较单一,各鼻窦中上颌窦发病率最高,达90.5%。有时临床表现与慢性鼻窦炎相似。此外不同分型具有不同的病理改变,其临床表现也有差异,非侵袭型常局限于窦内黏膜下产生黏膜水肿及化脓性炎症,形成炎性肉芽肿,对黏膜及骨无侵袭力,临床可无症状或有鼻塞、脓涕或血涕,预后良好,而侵袭型常侵犯窦腔黏膜动脉,导致血栓形成,鼻窦黏膜及骨壁坏死,侵犯眼眶可造成眼球突出,侵犯颅内可产生相应的神经系统症状,急性暴发型发展更为迅速,有时类似于恶性肿瘤、Wegener肉芽肿、骨髓炎等,预后较差,严重者可造成死亡。本文1例因眼眶、颅内广泛侵犯而死亡,另1例合并有白血病。尽管非侵袭型霉菌炎预后佳,但若不及时诊断治疗,也有转化为侵袭型的可能。Hartwick报告有28%的变应型霉菌性鼻窦炎可见窦腔扩大骨质破坏。因此早期诊断具有重要的临床意义。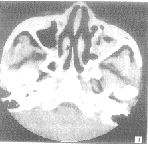
, 百拇医药
图1 上颌窦内霉菌球,片状破棉絮样,散在钙化,局限于黏膜下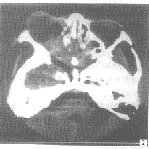
图2 侵袭型霉菌
性鼻窦炎侵犯眼眶,致右眼球突出、失明,局部广泛骨质破坏
3.3 CT影像表现及其病理基础 霉菌性鼻窦炎的CT表现较具特征性,主要有:①单侧为主;②鼻窦内片状破棉絮样或充满型或肿块状软组织阴影;③窦内软组织阴影中有斑点状高密度影,且多为中央性分布;④骨质破坏;⑤常伴有鼻腔鼻窦结构畸形。霉菌性鼻窦炎的病理组织学表现2/3属于增殖型,由炎性细胞浸润、炎性肉芽组织及大量菌丝增殖而成,因此CT影像上主要表现为软组织密度阴影或肿物,仅10%属于渗出型,影像上呈液性阴影。窦内软组织中斑点状高密度影,通过与病理染色对照提示为钙盐类物质,本组18例镜下显示伴紫染之钙化,较影像发现略多。关于窦内高密度影的原因目前有二种学说:其一为空气源性学说,此观点认为空气中曲霉菌孢子被吸入鼻窦,霉菌代谢产物或霉菌球钙化而造成影像上的高密度影,其主要成分是磷酸钙或硫酸钙;另一种为牙源性学说,认为是医源性牙髓充填材料沉积于上颌窦内所致,因为牙髓材料中含氧化锌等重金属,而烟曲霉菌在繁殖与代谢过程中需要氧化锌,此外重金属沉积不易被变性的呼吸道上皮清除,成为霉菌孢子的隐身地,为霉菌孢子致病提供了条件。Lenglinger报告霉菌性上颌窦炎窦内高密度影平均CT值2868HU(187~3070HU),非霉菌性平均仅778HU(228~2644HU),牙根填充材料平均CT值2866HU(2156~3070HU)。本文资料统计窦内高密度影CT值平均为143.4±11.8HU,与文献出入较大,我们同意空气源性学说。此外钙化的分布,我们统计中央性分布占68.8%,边缘分布12.5%,散在分布18.7%,与文献一致。
, 百拇医药
1例侵袭型霉菌性上颌窦炎同时行MR检查,T1WI及T2WI表现通过与病理对照并参考文献认为窦内无信号区相当于肉芽内霉菌团(尚需病例论证)。
3.4 鉴别诊断 霉菌性鼻窦炎的增生软组织内斑点状高密度钙化为与一般炎症的良好鉴别点,但若病变组织中无高密度钙化灶则与慢性鼻窦炎不易鉴别,主要依靠临床、霉菌培养及病理检查。慢性鼻窦炎病程较长,临床症状多而复杂,全身症状重,且常为多发性(多窦,双侧),窦腔内黏膜增厚,有时可见液气平,少见钙化,文献报道非霉菌性鼻窦炎的钙化率仅有3%,并以周围性分布为主,且形态多呈圆形或蛋壳样钙化,与霉菌性鼻窦炎的中央型斑点样分布不同。窦壁以见增生硬化为主,而侵袭型霉菌性鼻窦炎多见有骨质破坏改变。
少数侵袭型霉菌炎呈肿瘤样表现,与鼻窦恶性肿瘤较易混淆,后者侵袭力更强,破坏范围广泛,可出现瘤组织坏死液化,钙化不常见,侵入鼻腔可见菜花状肿物,侵犯牙槽突可使牙齿松脱,肿瘤有强化效应,MRT2加权像有不同表现(霉菌性病变T2呈很低信号强度),最终诊断依靠病理,若软组织内发现菌丝孢子而未见瘤细胞即可排除肿瘤。
, http://www.100md.com
CT还有助于非侵袭型和侵袭型霉菌性鼻窦炎的鉴别,非侵袭型常局限于单个鼻窦内,主要为上颌窦,而累及多个鼻窦或侵入邻近结构即提示为侵袭型霉菌性鼻窦炎。
作者简介:黄明刚(1964―),男,西安人,学士,主治医师。
[参考文献]
[1] DeCarpentier JP,Ramamurthy L,Denning DW,et al.An algorithmic approach to asper-gillus sinusitis[J].J Laryngol Otol,1994,108:314-318.
[2] Hartwick RW,Batsakis JG.Pathology consultation sinus aspergillosis and allergic fungal sinusitis[J].Ann Otol Rhinnol Laryngol,1991,100:427-430.
, http://www.100md.com
[3] Reilly JS.The sinusitis cycle[J].Otolaryngol Head Neck Surg,1990,103:856-862.
[4] 刘湘燕,韩德民,周兵.鼻鼻窦解剖变异与慢性鼻窦炎的关系[J].中华耳鼻咽喉科杂志,1998,33(3):149-152.
[5] Min YG,Kim HS,Kang MK,et al.Aspergillus sinusitis:Clnical aspects and treatment outcomes[J].Otolaryngol Head Neck Surg,1996,115(1):49-52.
[6] Krennmair G,Lenglinger F.Maxillary sinus aspergillosis:diagnosis and differentiatiation of the pathogenesis based on computed tomography densitometry of sinus concretions[J].J Oral Maxillofac Surg,1995,53(6):657-563.
[7] Yoon JH,Na DG,Byun HS,et al.Calcification in chronic maxillary sinusitis:comparison of CT findings with histopathologic results[J].Am J Neuroradiol,1999,20(4):571-574.
收稿日期:2000-04-02, http://www.100md.com
单位:黄明刚(陕西省人民医院CT室,陕西 西安 710068);杨萍(陕西省人民医院CT室,陕西 西安 710068);王茁(陕西省人民医院病理科,陕西 西安 710068)
关键词:
中国医学影像技术000811[中图分类号] R445.3 R322.3+1 [文献标识码] A
[文章编号] 1003-3289(2000)08-0637-02
本文搜集经病理证实的21例霉菌性鼻窦炎,对比分析其临床、病理及CT表现并探讨其发病机理及鉴别诊断。
1 资料与方法
搜集1989年至1999年在我院诊治、有完整资料的21例霉菌性鼻窦炎,男6例,女15例。年龄37~70岁,平均48.2岁,病史半年至20余年。全部病例均有术前CT检查,采用西门子SOMATOM DR3及岛津4800TF CT扫描机,层厚和间隔5mm,轴位和/或冠状扫描。1例病人同时行MR检查。观察内容:①临床:病史,症状,鼻腔检查及预后;②病理:常规HE染色,观察指标为霉菌菌丝,黏膜血管浸润及钙化;③霉菌培养:手术切除组织或分泌物的微生物培养并分类;④CT影像:病变位置、形态、范围、密度、骨质破坏,单窦、多窦及有无周围结构的侵犯,鼻腔及副窦结构。
, 百拇医药
分型:根据病变有无侵入黏膜动脉和鼻窦黏膜及骨壁坏死,将霉菌性鼻窦炎分为侵袭型和非侵袭型两型。
2 结果
2.1 临床表现 21例中侵袭型9例,非侵袭型12例,男6例,女15例,男女比例为1∶2.5。单侧20例,双侧1例。病史在0.5~1年的14例,1~2年的6例,20余年有1例。症状:脓涕,鼻阻伴头痛12例,涕中带血或间断性鼻衄8例,面颊部肿痛、张口困难1例,伴眼突2例,1例失明,发热、头痛、呕吐及嗅觉减退1例。5例合并有慢性鼻炎史,3例伴鼻息肉,1例合并糖尿病,1例患白血病,1例有风湿性心脏病。鼻腔专科检查情况:鼻中隔偏曲12例,鼻甲肥大6例,鼻黏膜充血14例,鼻息肉3例,鼻腔检查正常6例。预后:经过手术切除及抗霉菌治疗,1~2年后复查,18例无复发,1例复发,2例死亡。
2.2 CT表现 单窦病变16例(上颌窦15例,筛窦1例,累及多窦5例,窦外侵犯2例;病变形态呈片状破棉絮样10例,呈充满窦腔型6例,呈肿块型5例;病变密度不均匀,16例可见斑点状高密度影,中央分布11例,边缘分布2例,散在分布3例,平均CT值为(143.4±11.8)HU。7例有骨质破坏,以上颌窦内侧壁为主,5例上颌窦前壁增厚硬化,2例侵犯眼眶,1例并侵入颅内海绵窦、颞叶,出现多区域骨质破坏。合并鼻腔鼻旁窦结构异常14例,其中鼻中隔偏曲12例,鼻甲肥大6例,钩突弯曲3例,1例鼻中甲气化。合并鼻息肉3例。此外1例做MR检查,鼻腔内软组织阴影在T1WI上呈与脑实质信号相似的肿块影,T2WI呈明显低信号强度改变(图1,2)。
, 百拇医药
2.3 病理 浸润型光镜下见被覆复层纤毛柱状上皮黏膜组织中有大量炎性细胞、渗出物、细胞碎片及浆细胞和多核细胞浸润,在坏死组织中有大量浓密缠结的有隔菌丝,黏膜血管受侵。非浸润型则表现为肉芽组织内成团的霉菌菌丝,无黏膜血管受侵及组织坏死。18例HE染色见有斑片状钙化灶。
2.4 霉菌培养 12例经过培养检见霉菌,其中烟曲菌11例,黑曲菌1例,9例培养未检见真菌。
3 讨论
3.1 发病机制 霉菌性鼻窦炎的病理生理过程是各种原因导致鼻窦口狭窄或阻塞,造成窦腔内环境异常,包括分泌物的潴留,低氧状态,pH值下降,糖含量上升和黏稠度增加等,为病原微生物创造了适应的生长环境,在一定诱因下致人发病。造成鼻窦口狭窄的局部因素有鼻腔、鼻窦解剖畸形,局部黏膜病变,鼻息肉,鼻窦黏膜囊肿及异物等。诱因主要为人体免疫功能异常、机体抵抗力下降(如患有消耗性、代谢性疾病,长期使用抗生素、类固醇激素的患者)。近年来许多学者提出鼻腔鼻窦解剖畸形致鼻道复合体异常与鼻窦炎有密切关系。本组资料中,鼻腔、鼻窦结构异常者占66.7%(14/21),包括鼻中隔偏曲,鼻甲肥大气化及钩突变异等,23.8%(5/21)有慢性鼻炎史,合并鼻息肉14.3%(3/21),合并糖尿病、白血病等疾病有14.3%(3/21)。由此我们认为除环境因素、宿主因素外,鼻道复合体异常在鼻窦炎(包括特异性和非特异性)的发病原因中也占有重要的作用。
, http://www.100md.com
3.2 临床特点与病理 传统上将霉菌性鼻窦炎分为非侵袭型和侵袭型,前者又包括变应型和霉菌球,后者包括慢性无痛型和急性爆发型,本文主要为霉菌球型和慢性无痛型。本病多见于中年人,女性多于男性(2.5∶1),单侧发病为主,本组占95.2%,病程长短不一,短者数月,长者可达10余年,本文1例达20余年,临床症状主要有脓涕、鼻阻伴头痛或涕中带血或患侧鼻窦区压痛、面部肿胀,同慢性鼻窦炎比较症状较单一,各鼻窦中上颌窦发病率最高,达90.5%。有时临床表现与慢性鼻窦炎相似。此外不同分型具有不同的病理改变,其临床表现也有差异,非侵袭型常局限于窦内黏膜下产生黏膜水肿及化脓性炎症,形成炎性肉芽肿,对黏膜及骨无侵袭力,临床可无症状或有鼻塞、脓涕或血涕,预后良好,而侵袭型常侵犯窦腔黏膜动脉,导致血栓形成,鼻窦黏膜及骨壁坏死,侵犯眼眶可造成眼球突出,侵犯颅内可产生相应的神经系统症状,急性暴发型发展更为迅速,有时类似于恶性肿瘤、Wegener肉芽肿、骨髓炎等,预后较差,严重者可造成死亡。本文1例因眼眶、颅内广泛侵犯而死亡,另1例合并有白血病。尽管非侵袭型霉菌炎预后佳,但若不及时诊断治疗,也有转化为侵袭型的可能。Hartwick报告有28%的变应型霉菌性鼻窦炎可见窦腔扩大骨质破坏。因此早期诊断具有重要的临床意义。

, 百拇医药
图1 上颌窦内霉菌球,片状破棉絮样,散在钙化,局限于黏膜下

图2 侵袭型霉菌
性鼻窦炎侵犯眼眶,致右眼球突出、失明,局部广泛骨质破坏
3.3 CT影像表现及其病理基础 霉菌性鼻窦炎的CT表现较具特征性,主要有:①单侧为主;②鼻窦内片状破棉絮样或充满型或肿块状软组织阴影;③窦内软组织阴影中有斑点状高密度影,且多为中央性分布;④骨质破坏;⑤常伴有鼻腔鼻窦结构畸形。霉菌性鼻窦炎的病理组织学表现2/3属于增殖型,由炎性细胞浸润、炎性肉芽组织及大量菌丝增殖而成,因此CT影像上主要表现为软组织密度阴影或肿物,仅10%属于渗出型,影像上呈液性阴影。窦内软组织中斑点状高密度影,通过与病理染色对照提示为钙盐类物质,本组18例镜下显示伴紫染之钙化,较影像发现略多。关于窦内高密度影的原因目前有二种学说:其一为空气源性学说,此观点认为空气中曲霉菌孢子被吸入鼻窦,霉菌代谢产物或霉菌球钙化而造成影像上的高密度影,其主要成分是磷酸钙或硫酸钙;另一种为牙源性学说,认为是医源性牙髓充填材料沉积于上颌窦内所致,因为牙髓材料中含氧化锌等重金属,而烟曲霉菌在繁殖与代谢过程中需要氧化锌,此外重金属沉积不易被变性的呼吸道上皮清除,成为霉菌孢子的隐身地,为霉菌孢子致病提供了条件。Lenglinger报告霉菌性上颌窦炎窦内高密度影平均CT值2868HU(187~3070HU),非霉菌性平均仅778HU(228~2644HU),牙根填充材料平均CT值2866HU(2156~3070HU)。本文资料统计窦内高密度影CT值平均为143.4±11.8HU,与文献出入较大,我们同意空气源性学说。此外钙化的分布,我们统计中央性分布占68.8%,边缘分布12.5%,散在分布18.7%,与文献一致。
, 百拇医药
1例侵袭型霉菌性上颌窦炎同时行MR检查,T1WI及T2WI表现通过与病理对照并参考文献认为窦内无信号区相当于肉芽内霉菌团(尚需病例论证)。
3.4 鉴别诊断 霉菌性鼻窦炎的增生软组织内斑点状高密度钙化为与一般炎症的良好鉴别点,但若病变组织中无高密度钙化灶则与慢性鼻窦炎不易鉴别,主要依靠临床、霉菌培养及病理检查。慢性鼻窦炎病程较长,临床症状多而复杂,全身症状重,且常为多发性(多窦,双侧),窦腔内黏膜增厚,有时可见液气平,少见钙化,文献报道非霉菌性鼻窦炎的钙化率仅有3%,并以周围性分布为主,且形态多呈圆形或蛋壳样钙化,与霉菌性鼻窦炎的中央型斑点样分布不同。窦壁以见增生硬化为主,而侵袭型霉菌性鼻窦炎多见有骨质破坏改变。
少数侵袭型霉菌炎呈肿瘤样表现,与鼻窦恶性肿瘤较易混淆,后者侵袭力更强,破坏范围广泛,可出现瘤组织坏死液化,钙化不常见,侵入鼻腔可见菜花状肿物,侵犯牙槽突可使牙齿松脱,肿瘤有强化效应,MRT2加权像有不同表现(霉菌性病变T2呈很低信号强度),最终诊断依靠病理,若软组织内发现菌丝孢子而未见瘤细胞即可排除肿瘤。
, http://www.100md.com
CT还有助于非侵袭型和侵袭型霉菌性鼻窦炎的鉴别,非侵袭型常局限于单个鼻窦内,主要为上颌窦,而累及多个鼻窦或侵入邻近结构即提示为侵袭型霉菌性鼻窦炎。
作者简介:黄明刚(1964―),男,西安人,学士,主治医师。
[参考文献]
[1] DeCarpentier JP,Ramamurthy L,Denning DW,et al.An algorithmic approach to asper-gillus sinusitis[J].J Laryngol Otol,1994,108:314-318.
[2] Hartwick RW,Batsakis JG.Pathology consultation sinus aspergillosis and allergic fungal sinusitis[J].Ann Otol Rhinnol Laryngol,1991,100:427-430.
, http://www.100md.com
[3] Reilly JS.The sinusitis cycle[J].Otolaryngol Head Neck Surg,1990,103:856-862.
[4] 刘湘燕,韩德民,周兵.鼻鼻窦解剖变异与慢性鼻窦炎的关系[J].中华耳鼻咽喉科杂志,1998,33(3):149-152.
[5] Min YG,Kim HS,Kang MK,et al.Aspergillus sinusitis:Clnical aspects and treatment outcomes[J].Otolaryngol Head Neck Surg,1996,115(1):49-52.
[6] Krennmair G,Lenglinger F.Maxillary sinus aspergillosis:diagnosis and differentiatiation of the pathogenesis based on computed tomography densitometry of sinus concretions[J].J Oral Maxillofac Surg,1995,53(6):657-563.
[7] Yoon JH,Na DG,Byun HS,et al.Calcification in chronic maxillary sinusitis:comparison of CT findings with histopathologic results[J].Am J Neuroradiol,1999,20(4):571-574.
收稿日期:2000-04-02, http://www.100md.com