ΦΉΜ«Υα»ΞΧζΑΖΩΙ«λ¥σΟΙΥΊΕζΕΨ–‘Ής”ΟΦΑΜζάμ―–ΨΩ
Ής’ΏΘΚ≥¬―τ ΆθΫθΝα ΜΤΈ§Ιζ ««άρ ΝθΥ≥άϊ Μϋœή…ζ
ΒΞΈΜΘΚΜϋœή…ζΘ§ΜυΫπΑύ―–ΨΩ…ζ ΈςΑ≤ ΒΎΥΡΨϋ“Ϋ¥σ―ßΗΫ τΈςΨ©“Ϋ‘ΚΕ汫― ΚμΩΤ 710032
ΙΊΦϋ¥ ΘΚ«λ¥σΟΙΥΊάύΘΜΘΜ»ΞΧζΑΖΘΜΘΜ“©ΈοœύΜΞΉς”ΟΘΜΘΜ÷–ΕΨΘΜΘΜΧΐΝΠ’œΑ≠
÷–ΜΣΕ汫― ΚμΩΤ‘”÷Ψ990308 ΓΨ’Σ“ΣΓΩ ΡΩΒΡ ΧΫΧ÷ΧζρϋΚœΦΝΦΉΜ«Υα»ΞΧζΑΖ(deferoxamine mesylate, DFO)Ε‘ΩΙ«λ¥σΟΙΥΊ(gentamicinΘ§GM)ΕζΕΨ–‘Ής”ΟΦΑΤδΜζάμΓΘΖΫΖ® κύ σΥφΜζΖ÷ΈΣGMΉι(17÷Μ)ΓΔDFOΉι(8÷Μ)ΓΔGM+DFOΉι(17÷Μ)ΦΑΕ‘’’Ήι(8÷Μ)Θ§≤…”ΟΧΐ–‘Ρ‘Η…Ζ¥”Π(acoustic brainstem responseΘ§ABR)ΓΔΕζΈœΤΧΤ§ΦΑΆΗ…δΒγΨΒΦΦ θΘ§Ιέ≤λ”Ο“©«ΑΚσΧΐΖ¥”Πψ–ΦΑ–ΈΧ§―ß±δΜ·Θ§Φλ≤β―Σ«εΡρΥΊΒΣΓΔΦΓή’“‘ΦΑGM≈®Ε»Θ§Ά§ ±≤βΕ®ΕζΈœΚΆ…ωΤΛ÷ Ήι÷·÷–±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζάκΉ”Κ§ΝΩΓΘΫαΙϊ GMΉι8 kHz ABRψ–“ΤΈΣ40ΓΪ60 dBΘΜGM+DFOΉιψ–“ΤΈΣ15ΓΪ25 dBΘ§≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘ–ΈΧ§―ßΗΡ±δ”κΧΐΝΠ±δΜ·“Μ÷¬ΓΘDFOΕ‘GM―Σ“©≈®Ε»ΟΜ”–”ΑœλΓΘGMΉι…ωΙΠΟςœ‘Υπ…Υ,ΒΪ…ωΤΛ÷ ±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζάκΉ”±δΜ·≤ν“λΈόœ‘÷χ–‘(P>0.05)Θ§GM+DFOΉιΕζΈœΉι÷·±ϊΕΰ»©ΚΆΧζάκΉ”Κ§ΝΩΫœGMΉιΟςœ‘Φθ…Ό(P<0.05)Θ§≥§―θΜ·ΈοΤγΜ·ΟΗΚ§ΝΩΟςœ‘ΗΏ”ΎGMΉι(P<0.05)ΓΘΫα¬έ Ή‘”…ΜυΚΆΧζάκΉ”‘ΎGMΒΡΕζΕΨ–‘÷–Τπ÷Ί“ΣΉς”ΟΘ§DFOΡή”––ßΦθ«αGMΒΡΕζΕΨ–‘Ής”ΟΘ§Ω…Ρή≥…ΈΣ”–œΘΆϊΒΡ‘ΛΖά“©ΈοΓΘ
, ΑΌΡ¥“Ϋ“©
Deferoxamine protects against gentamicin ototoxicity
CHEN Yang, WANG Jinling,HUANG Weiguo,et al. Department of Otorhinolaryngology, XiJing Hospital, Fourth Military Medical University, XiΓ·an 710032
ΓΨAbstractΓΩ Objective To study the prevention of gentamicin(GM) ototoxicity by deferoxamine(DFO) in the guinea pig. Methods Guinea pigs were randomly assigned to three experimental groups (GM-treated alone, DFO-treated alone, GM and DFO in combination) and one control group. Acoustic brainstem response (ABR), the surface preparation and transmission electron microscopy were utilized to evaluate the hearing thresholds and the cochlear morphology. To explore the mechanism associated with deferoxamine protection, serum levels of GM, BUN and Cr, together with concentration of MDA, SOD and iron in cochlear and renal tissues were measured. Results The GM group developed up to 40 ΓΪ60 dB of the threshold shifts at 8 kHz while the GM+DFO group developed only 15 ΓΪ25 dB of the threshold shifts (P<0.05). Morphological changes were consistent with functional changes. DFO did not alter serum levels of GM. Renal function of GM group was damaged obviously. However, changes of MDA, SOD and iron were not significant (P>0.05). MDA and iron concentrations in cochlear tissue of the GM+DFO group were significantly lower than those in the GM group (P<0.05) while SOD level was much higher than that in GM group. Conclusion This study suggests that free radical and iron involve in GM ototoxicity and DFO may become a promising therapeutic agent that can be used to reduce gentamicin ototoxicity.
, ΑΌΡ¥“Ϋ“©
ΓΨKey wordsΓΩ Gentamicins Poisoning Hearing disorders Deferoxamine Drug interactions
PriuskaΒ»[1]Χα≥ω«λ¥σΟΙΥΊ(gentamicinΘ§GM)ΕζΕΨ–‘Ω…Ρή «”…”ΎGM‘ΎΧεΡΎ–Έ≥…GM-ΧζΗ¥ΚœΈοΘ§¥ΏΜ·≤ζ…ζΉ‘”…ΜυΕχΥπ…ΥΟΪœΗΑϊΓΘΉ‘”…Μυ«ε≥ΐΦΝΚΆΧζρϋΚœΦΝΩ…“‘Φθ«αGM “ΐΤπΒΡΧΐΝΠΥπΚΠ[2]ΓΘ±Ψ Β―ιΆ®ΙΐABRΦλ≤βΓΔΕζΈœΤΧΤ§ΦΑΆΗ…δΒγΨΒΦΦ θΘ§Ιέ≤λκύ σ”Ο“©«ΑΚσΧΐΖ¥”Πψ–ΦΑΕζΈœΟΪœΗΑϊΓΔ―ΣΙήΈΤΒΡΗΡ±δΘ§Ιέ≤λΧζρϋΚœΦΝΦΉΜ«Υα»ΞΧζΑΖ(deferoxamine mesylate,DFO)Ε‘ΩΙGMΕζΕΨ–‘ΒΡΉς”ΟΘΜΆ§ ±Φλ≤βΕζΈœΚΆ…ωΤΛ÷ Ήι÷·±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζάκΉ”ΒΡΚ§ΝΩΘ§≤βΕ®―Σ«εGMΚΆΡρΥΊΒΣΓΔΦΓή’Υ°ΤΫΘ§“‘ΧΫΧ÷ΤδΩ…ΡήΒΡΉς”ΟΜζάμΦΑΤδ”κ…ωΕΨ–‘ΒΡΙΊœΒΓΘ
≤ΡΝœΦΑΖΫΖ®
1. Β―ιΕ·ΈοΘΚΕζάΣΖ¥…δ’ΐ≥ΘΒΡΫΓΩΒ–έ–‘‘”…Ϊκύ σ50÷ΜΘ§Χε÷Ί250ΓΪ350 gΘ§ΥφΜζΖ÷≥…4ΉιΓΘ GMΉι17÷ΜΘΚΝρΥα«λ¥σΟΙΥΊ(Ές±±ΒΎΕΰΚœ≥…“©≥ß…ζ≤ζΘ§≈ζΚ≈970818) 120 mg/kgΤΛœ¬ΉΔ…δΘ§ΟΩΧλ1¥ΈΘ§Ν§–χ19 dΘΜDFOΉι8÷ΜΘΚDFO(SigmaΙΪΥΨΘ§ΟάΙζΘ§ΟήΈςΗυ¥σ―ß“Ϋ―ß÷––ΡKresgeΧΐΝΠ―–ΨΩΥυΧαΙ©) ΟΩ¥Έ100 mg/kgΤΛœ¬ΉΔ…δΘ§ΟΩΧλ2¥Έ(ΦδΗτ4 h)Θ§Ν§–χ19 dΘΜGM+DFOΉι17÷ΜΘΚGMΚΆDFOΆ§ ±ΉΔ…δΘ§4 hΚσΉΔ…δDFOΘ§ΦΝΝΩΆ§…œΘΜΕ‘’’Ήι 8÷ΜΘΚ…ζάμ―ΈΥ°Β»ΝΩΤΛœ¬ΉΔ…δΘ§ΟΩΧλ1¥ΈΘ§Ν§–χ19 dΓΘ Ε·Έο Β―ιΤΎΦδΟΩΧλ≥”Χε÷Ί“‘Βς’ϊ“©ΝΩΓΘ
, ΑΌΡ¥“Ϋ“©
2.ABRΦλ≤βΧΐΖ¥”Πψ–ΘΚ”Ο“©«ΑΦΑ”Ο“©ΚσΒΎ9ΚΆ19 dΓΔΒΎ28ΚΆ42 d÷ήΦλ≤βΥΪΕζABRΓΘΕ·Έο‘ΎΈλΑΆ±»ΆΉΡΤ 40 mg/kg ΗΙ«ΜΉΔ…δ¬ιΉμΚσΘ§’κ–ΆΦ«¬ΦΒγΦΪ÷Ο«ΑΕν’ΐ÷–ΤΛœ¬Θ§≤ΈΩΦΒγΦΪ÷Ο≤β ‘ΕζΆβΕζΒάΩΎΚσ…œΤΛœ¬Θ§±«ΦβΫ”ΒΊΓΘ”ΟSS-1–Ά…υ¥ΧΦΛΤςΘ§286ΦΤΥψΜζΉ‘Ε·≤…―υΘ§≤…”ΟΕΧ…υ(click)1ΓΔ2ΓΔ4ΓΔ8 kHz¥ΧΦΛΘ§ΦδΗτ75 msΘ§…®Οη ±Φδ20 msΘ§ΒΰΦ”256¥ΈΘ§¥χΆ®¬Υ≤®80ΓΪ1 500 HzΘ§‘ΎΤΝ±ΈΗτ…υ “ΡΎ≥ΘΙφ≤β ‘ΓΘ
3.ΆΗ…δΒγΨΒ±ξ±Ψ÷Τ±ΗΘΚΆΘ“©ΚσΒΎ2 dΦλ≤βABRΚσΗςΉιΥφΜζ»Γ4 ÷ΜΕ·ΈοΕœΆΖ¥ΠΥάΘ§ΟΩ÷ΜΕ·ΈοΗς»Γ1ΕζΘ§Χΐ≈ί÷Ο2.5%ΈλΕΰ»©ΡΎΘ§ΫβΤ œ‘ΈΔΨΒœ¬’Σ≥ΐοκΙ«Θ§¥ΧΤΤ‘≤¥ΑΘ§ΧτΩΣΈœΕΞΘ§ΙύΝςΙΧΕ®ΚσΫΰΉ’ΙΧΕ®24 hΘ§ΝΉΥαΜΚ≥ε“ΚΤ·œ¥ΚσΫβΤ ±ξ±ΨΘ§»Γ≥ωΗςΜΊΜυΒΉΡΛΦΑ―ΣΙήΈΤΘ§1%οΑΥαΚσΙΧΕ®Θ§±ϊΆΣΆ―Υ°Θ§ΜΖ―θ ς÷§Αϋ¬ώΘ§≥§±Γ«–Τ§Θ§”Υ«Π»Ψ…ΪΓΘ
4.ΕζΈœ”≤ΤΧΤ§±ξ±Ψ÷Τ±ΗΘΚ»Γ≤Ρ ±ΦδΆ§…œΘ§Νμ1ΕζΧΐ≈ίœθΥα“χ»Ψ…ΪΖ®≥ΘΙφ÷Τ±Η[3]ΓΘ
, ΑΌΡ¥“Ϋ“©
5.ΈΔ…ζΈο÷ΫΤ§ά©…ΔΖ®≤βΕ®«λ¥σΟΙΥΊ―Σ“©≈®Ε»[4]ΘΚGMΉιΚΆGM+DFOΉιΕ·ΈοΒΎ9ΚΆ19 dΉΔ…δ«λ¥σΟΙΥΊΚσ 1 hΦτΉΠ»Γ―ΣΘ§≤βΕ®―Σ«ε“÷ΨζΜΖ÷±ΨΕΘ§‘Ό≤ι±ξΉΦ«ζœΏΆΦΘ§ΒΟ≥ω―Σ«ε«λ¥σΟΙΥΊ≈®Ε»ΓΘ
6.Φλ≤β…ωΙΠΘΚ»Γ―υ ±ΦδΚΆΖΫΖ®Ά§…œΘ§»ΪΉ‘Ε·…ζΜ·Φλ≤β“«(»’ΝΔΙΪΥΨ, »’±Ψ)≤βΕ®―Σ«εΡρΥΊΒΣΚΆΦΓή’ΓΘ
7.Φλ≤βΕζΈœΚΆ…ωΤΛ÷ ΒΡ±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζΘΚGMΉιΚΆGM+DFOΉιΒΎ9ΚΆ19 dΗς»Γ3÷ΜΕ·ΈοΜν…±Θ§―ΗΥΌ»Γ≥ωΕζΈœΘ§ΥΪΕζΚœΈΣ1Ζί±ξ±Ψ÷Τ≥…‘»Ϋ§Θ§4 000 r/minάκ–Ρ10 minΘ§»Γ…œ«ε“Κ-20 ΓφΕ≥¥φΓΘ≤…”ΟΡœΨ©Ϋ®≥……ζΈο―–ΨΩΥυΒΡ±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΩΦ¬μΥΙΝΝάΕΒΑΑΉ≤βΕ® ‘ΦΝΚ–Θ§Α¥ΥΒΟς≤ΌΉςΦλ≤βΘΜ‘≠Ή”Έϋ ’Ζ÷ΙβΙβΕ»ΦΤ(ΧλΫρΒΎ“Μ“ΫΝΤΤς≤Ρ…η±Η≥ß)Φλ≤βΧζΒΡΚ§ΝΩΓΘΆ≥ΦΤ―ß¥Πάμ”ΟΖΫ≤νΖ÷ΈωΓΘ
ΫαΙϊ
1. Β―ι÷–GMΉι3÷ΜΕ·ΈοΖ÷±π”Ύ”Ο“©ΒΎ11ΓΔ18ΚΆ19 dΥάΆωΘ§Υά«ΑΨυœϊ ίΓΔΈόΝΠΓΔΕζάΣΖ¥…δœϊ ßΘ§Τδ”ύΗςΉιΈόΥάΆωΓΘΒΎ19 dΕ‘’’ΉιΤΫΨυ‘ω≥Λ35 gΘ§ΕχGMΉιΕ·ΈοΧε÷ΊΤΫΨυΦθ…Ό2 g, ≤ν“λ”–œ‘÷χ–‘(P<0.05)ΘΜΆΘ“©ΚσGMΉιΕ·ΈοΜ÷Η¥Χε÷Ί‘ω≥ΛΓΘGM+DFOΉιΓΔDFOΉιΒΎ19 dΧε÷ΊΤΫΨυ‘ω≥Λ33gΚΆ31gΘ§ΚΆΕ‘’’Ήι÷°Φδ±»Ϋœ≤ν“λΈόœ‘÷χ–‘(P>0.05)ΓΘ
, ΑΌΡ¥“Ϋ“©
2.ABRΦλ≤βΘΚκύ σΒΡABR“‘Δσ≤®Ήν÷χΘ§“ρ¥Υ“‘Δσ≤®≈–ΕœABRΖ¥”Πψ–(dB SPL)Θ§”Ο“©ΚσΗςΉιΕ·ΈοABRΤΫΨυΖ¥”Πψ–“ΤΦϊΆΦ1ΓΘΥδ»Μ Β―ιΕ·ΈοΕ‘“©ΈοΒΡΖ¥”ΠΨΏ”–ΗωΧε≤ν“λΘ§ΒΪGM+DFOΉιΖ¥”Πψ–ΥπΚΠΫœGMΉιΟςœ‘Φθ«αΓΘ”Ο“©ΚσΒΎ4÷ήΘ§GMΉι4 kHzΦΑ8 kHzΖ¥”Πψ–ΤΫΨυ(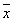 ΓάsΘ§œ¬Ά§)…ΐΗΏ(44Γά18)dBΦΑ(60Γά17)dBΘ§ΕχGM+DFOΉι‘ρΖ÷±πΈΣ(16Γά5)dBΦΑ(21Γά5)dBΘ§ΝΫΉι≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘΥπ…ΥΨΏ”–ΤΒ¬ ≤ν“λΘ§ΗΏΤΒΥπ…ΥΟςœ‘±»ΒΆΤΒΥπ…Υ―œ÷Ί(P<0.01)ΓΘDFOΉιΚΆΕ‘’’ΉιΖ¥”Πψ–±δΜ·≤ΜΟςœ‘(P>0.05)ΓΘ
ΓάsΘ§œ¬Ά§)…ΐΗΏ(44Γά18)dBΦΑ(60Γά17)dBΘ§ΕχGM+DFOΉι‘ρΖ÷±πΈΣ(16Γά5)dBΦΑ(21Γά5)dBΘ§ΝΫΉι≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘΥπ…ΥΨΏ”–ΤΒ¬ ≤ν“λΘ§ΗΏΤΒΥπ…ΥΟςœ‘±»ΒΆΤΒΥπ…Υ―œ÷Ί(P<0.01)ΓΘDFOΉιΚΆΕ‘’’ΉιΖ¥”Πψ–±δΜ·≤ΜΟςœ‘(P>0.05)ΓΘ 
ΆΦ1 ”Ο“©ΚσΗςΉιΕ·Έο≤ΜΆ§ΤΒ¬ ΕΧ…υ¥ΧΦΛΒΡABRΤΫΨυψ–“Τ
3.ΕζΈœΤΧΤ§ΦΑΆΗ…δΒγΨΒΥυΦϊΘΚΕζΈœΤΧΤ§œ‘ ΨGMΉι”Ο“©Κσ3≈≈ΆβΟΪœΗΑϊΥπ…ΥΟςœ‘±»GM+DFOΉι÷Ί(ΆΦ2,3)Θ§«“¥”ΕΞΜΊ÷ΝΒΉΜΊ÷πΫΞΦ”÷ΊΘ§ΆβΟΪœΗΑϊΥπ…ΥΫœΡΎΟΪœΗΑϊ÷ΊΓΘΆΗ…δΒγΨΒΦϊGMΉιΕζΈœΟΪœΗΑϊΑϊΫ§œΗΑϊΤςΦθ…ΌΘ§≥ Ω’≈ί±δ–‘(ΆΦ4)ΘΜGM+DFOΉι‘ρœ‘ ΨΥπ…ΥΫœ«αΘ§œΏΝΘΧεΆξ’ϊΘ§≥ωœ÷“Μ–©Εύ≈ίΧεΫαΙΙ(ΆΦ5)ΓΘGMΉιΜΙΩ…ΦϊΕζΈœ¥Ϊ»κ…ώΨ≠ΆΜ¥ΞœΏΝΘΧεΩ’Μ·Θ§―ΣΙήΈΤ±Ώ‘ΒœΗΑϊΆΜΤπ÷–ΒΡ…Ό ΐœΏΝΘΧε“ύ≥ωœ÷α’Φθ…ΌΓΔΩ’Μ·ΓΘDFOΉι”κΕ‘’’Ήι”Ο“©«ΑΚσΕζΈœΤΧΤ§ΦΑΆΗ…δΒγΨΒΗΡ±δ≤ΜΟςœ‘ΓΘ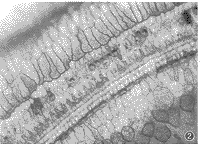
, ΑΌΡ¥“Ϋ“©
ΆΦ2 ΕζΈœΤΧΤ§ΦϊGMΉιΒΎΕΰΜΊΆβΟΪœΗΑϊΥπ…ΥΟςœ‘Θ§Ϋω”–…Ό ΐ≤–ΝτΘ§ΡΎΟΪœΗΑϊ“ύΦϊΥπ…ΥΓΘΓΝ400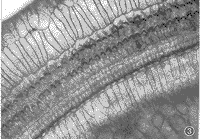
ΆΦ3 ΕζΈœΤΧΤ§ΦϊGM+DFOΉιΒΎΕΰΜΊΆβΟΪœΗΑϊΥπ…ΥΫœ«αΘ§ΡΎΟΪœΗΑϊΈό»± ßΓΘΓΝ400
ΆΦ4 ΆΗ…δΒγΨΒΙέ≤λGMΉιΟΪœΗΑϊΑϊΫ§œΓ η≥ Ω’≈ί±δ–‘Θ§ΑϊΚΥ≈®ΥθΓΘΓΝ6000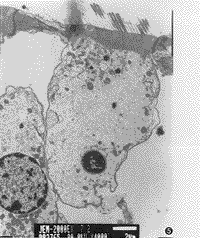
ΆΦ5 ΆΗ…δΒγΨΒΙέ≤λGM+DFOΉιΟΪœΗΑϊΑϊΫ§ΖαΗΜΘ§”–ΕύΗωΕύ≈ίΧε–Έ≥…ΓΘΓΝ4000
4.―Σ«εΦλ≤βΘΚGMΉιΚΆGM+DFOΉιΕ·ΈοΒΡ―Σ«εGM≈®Ε»≤ν“λΈόœ‘÷χ–‘(P>0.05)ΓΘΒΎ9 d≤βΕ®÷Β(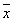 ΓάsΘ§œ¬Ά§)Ζ÷±πΈΣ(75Γά12) mg/LΚΆ(80Γά9) mg/LΘ§ΒΎ19d≤βΕ®÷ΒΖ÷±πΈΣ(110Γά12) mg/LΚΆ(114Γά9) mg/LΓΘGMΉιΒΎ19 d―Σ«εΡρΥΊΒΣΚΆΦΓή’Ζ÷±πΈΣ(28.34Γά4.3)mmol/LΚΆ(93.39Γά15.8)mmol/LΘ§GM+DFOΉιΖ÷±πΈΣ (11.48Γά5.6) mmol/LΚΆ(45.47Γά12.8) mmol/LΘ§ΝΫΉιΦδ≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘ
ΓάsΘ§œ¬Ά§)Ζ÷±πΈΣ(75Γά12) mg/LΚΆ(80Γά9) mg/LΘ§ΒΎ19d≤βΕ®÷ΒΖ÷±πΈΣ(110Γά12) mg/LΚΆ(114Γά9) mg/LΓΘGMΉιΒΎ19 d―Σ«εΡρΥΊΒΣΚΆΦΓή’Ζ÷±πΈΣ(28.34Γά4.3)mmol/LΚΆ(93.39Γά15.8)mmol/LΘ§GM+DFOΉιΖ÷±πΈΣ (11.48Γά5.6) mmol/LΚΆ(45.47Γά12.8) mmol/LΘ§ΝΫΉιΦδ≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘ
, ΑΌΡ¥“Ϋ“©
5. ΕζΈœΚΆ…ωΤΛ÷ ΒΡ±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζΦλ≤βΘΚ GM+DFOΉιΕζΈœΉι÷·ΒΎ9ΚΆ19 dΒΡΧζάκΉ”ΤΫΨυΚ§ΝΩΈΣ5.01ΠΧmol/LΚΆ5.21ΠΧmol/LΘ§ΒΆ”ΎGMΉι9.70ΠΧmol/LΚΆ8.21ΠΧmol/LΘ§≤ν“λΨυ”–œ‘÷χ–‘(P<0.05)ΘΜGM+DFOΉιΕζΈœΉι÷·Ά§ΤΎΒΡ±ϊΕΰ»©ΤΫΨυΚ§ΝΩΈΣ2.43ΚΆ2.83 mmol/mgΒΑΑΉΘ§ΒΆ”ΎGMΉι3.83ΚΆ4.78 mmol/mgΒΑΑΉΘ§≤ν“λ”–œ‘÷χ–‘(P<0.05)ΘΜGM+DFOΉιΒΎ9 d≥§―θΜ·ΈοΤγΜ·ΟΗΚ§ΝΩ‘ρœ‘÷χΗΏ”ΎGMΉι(P<0.05)Θ§Ζ÷±πΈΣ4 351ΚΆ2 480 U/mgΒΑΑΉ(nitris unit)ΓΘΝΫΉι…ωΤΛ÷ Ήι÷·±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζΚ§ΝΩ≤ν“λΈόœ‘÷χ–‘(P>0.05)ΓΘ¥ΥΆβΘ§ΒΎ19 dΩ…ΦϊGMΉι3÷ΜΕ·ΈοΒΡ…ω‘ύ÷Ή¥σ»γ«ρΉ¥Θ§≥ ΝΝΜΤ…ΪΓΘ
Χ÷¬έ
DFO «“Μ÷÷ρϋΚœΦΝΘ§÷ς“Σ”κΧζάκΉ”ΚΆ»ΐΦέ¬ΝάκΉ”–Έ≥…Η¥ΚœΈοΘ§ΤδΗ¥ΚœΈο–Έ≥…≥Θ ΐΖ÷±πΈΣ1031ΚΆ1025ΓΘ’βΝΫ÷÷Η¥ΚœΈοΆ®ΙΐΒ®÷≠ΚΆΡρΩ…Άξ»Ϊ≈≈–ΙΘ§“ρ¥ΥΕχΦθ…ΌΧζΜρ¬Ν‘ΎΤςΙΌΒΡ≤Γάμ–‘≥ΝΜΐΓΘΝΌ¥≤”Ο”Ύ÷ΈΝΤ δ―ΣΥυ÷¬ΒΡΚ§Χζ―ΣΜΤΥΊ≥ΝΉ≈≤ΓΚΆΒΊ÷–ΚΘΤΕ―ΣΒ»Φ±ΓΔ¬ΐ–‘Χζ÷–ΕΨ[5] ΓΘΝΌ¥≤‘χ±®ΒάDFOΉς≥ΛΤΎ÷ΈΝΤ ±Θ§”»ΤδΥυ”ΟΦΝΝΩ≥§ΙΐΆΤΦωΦΝΝΩΚΆ/ΜρΤδΦΝΝΩΈ¥Α¥ΒΆ―Σ«εΧζΒΑΑΉΜρ―Σ«ε¬Ν≈®Ε»ΕχΒς’ϊ ±Θ§Ω…“ΐΤπ ”ΝΠΓΔΧΐΝΠ’œΑ≠ΓΘ“≤”–―–ΨΩ÷ΛΟςΤδ≥ΛΤΎΖΰ”ΟΒΡΑ≤»Ϊ–‘[6]ΓΘ±Ψ Β―ιΥυ”Ο«λ¥σΟΙΥΊΈΣΝΌ¥≤”Π”ΟΒΡ20±ΕΘ§ΕχDFO÷Μ «ΝΌ¥≤ΦΝΝΩΒΡ2ΓΪ4±ΕΘ§DFOΉιΧΐΖ¥”Πψ–‘Ύ’ϊΗω Β―ιΙΐ≥Χ÷–±Θ≥÷Έ»Ε®Θ§±μΟςΤδΑ≤»ΪΈόΕΨ–‘ΓΘΆΘ“©Κσ1÷ήΧΐΝΠΥπΚΠ¥οΒΫΕΞΖεΘ§GM+DFOΉι8 kHzΧΐΖ¥”Πψ–ΤΫΨυΫœGMΉιΫΒΒΆ31.5 dBΘ§1 kHz“≤ΫΒΒΆΝΥ11 dB(P<0.05) Θ§ΕζΈœΟΪœΗΑϊΒΡ–ΈΧ§―ßΥπ…Υ”κΧΐΖ¥”Πψ–…ΐΗΏΒΡ≥ΧΕ»œύΤΫ––ΓΘ’β”κSongΒ»[7]ΒΡΫαΙϊ“Μ÷¬Θ§ΥΒΟςDFOΡή”––ßΦθ«αGMΒΡΕζΕΨΉς”ΟΘ§≥…ΈΣ”–œΘΆϊΒΡ‘ΛΖά“©ΈοΓΘΕχ«“’β÷÷±ΘΜΛΉς”Ο≤Μ”ΑœλGMΒΡ―Σ“©≈®Ε»Θ§»‘Ρή±Θ≥÷GMΒΡΩΙΨζ–ßΝΠΓΘ”κ“‘ΆυΒΡ±®ΒάœύΆ§Θ§GMΒΡΧΐΝΠΥπΚΠ“‘ΗΏΤΒ”»ΈΣΟτΗ–Θ§8 kHz Ήœ»≥ωœ÷Ζ¥”Πψ–…ΐΗΏΘ§«“Υπ ßΫœ÷–ΓΔΒΆΤΒΈΣ…θ(P<0.01)ΓΘ“ρ¥ΥΘ§ΗΏΤΒΧΐΖ¥”Πψ–ΒΡ…ΐΗΏΩ…‘γΤΎ‘Λ ΨGMΒΡΕζΕΨ–‘ΓΘ
, http://www.100md.com
”–ΙΊΑ±ΜυΧ«ΏΑάύΩΙ…ζΥΊΒΡΕζΕΨ–‘ΜζάμΒΡ―ßΥΒΚήΕύΘ§…–Έ¥Άξ»ΪΟςΝΥΘ§Τδ÷–÷°“ΜΈΣΉ‘”…Μυ―ßΥΒΓΘ1981ΡξPiersonΒ»[8]±®ΒάΉ‘”…Μυ«ε≥ΐΦΝWR2721Ω…―”ΜΚΩ®Ρ«ΟΙΥΊΕζ÷–ΕΨΒΡΖΔ…ζΘ§≤ΔΦθ«αΧΐΝΠΥπ ß≥ΧΕ»ΓΘΒΪΥφΚσΗςΦ“ Β―ιΒΡΫαΙϊ≤Μœύ“Μ÷¬Θ§≤ΜΆ§ΒΡΉ‘”…Μυ«ε≥ΐΦΝ÷ΈΝΤΒΟΒΫ≤ΜΆ§ΒΡΫαΙϊΓΘGaretsΒ»[9]ΚΆLautermannΒ»[10]ΕΦ÷Λ ΒΙ»Α±θΘΑΖΩ…Φθ«α«λ¥σΟΙΥΊΕζΕΨ–‘Θ§ΒΪΫωΕ‘Φ≤≤ΓΉ¥Χ§œ¬Μρ”Σ―χ»±ΖΠΒΡΕ·Έο”––ßΓΘ’β±μΟς”Π”ΟΉ‘”…Μυ«ε≥ΐΦΝΖάΜΛ«λ¥σΟΙΥΊΕζΕΨ–‘Ής”ΟΒΡ≤Μ»ΖΕ®–‘ΓΘΜζΧεΡΎΒΡ―θΉ‘”…Μυ”…ΟΗœΒΆ≥ΚΆΖ«ΟΗœΒΆ≥≤ζ…ζΡ≥–©Η¥ΚœΈο¥ΏΜ·ΒΡHaber-WeissΖ¥”ΠΘ§”…ΧζάκΉ”ΧαΙ©ΒγΉ”≤ζ…ζτ«Ή‘”…Μυ «Τδ÷–“ΜΧθ÷Ί“ΣΆΨΨΕΓΘPriuskaΒ»[1]Χα≥ωGMΒΡΕζΕΨΉς”Ο «Ά®Ιΐ”κ”ΈάκΧζάκΉ”–Έ≥…Η¥ΚœΈοΘ§¥ΏΜ·≤ζ…ζΉ‘”…ΜυΒΡΖ¥”ΠΕχΖΔΜ”ΕζΕΨ–‘Ής”ΟΓΘΉ‘”…ΜυΩ…Ά®Ιΐ…ζΈοΡΛ÷–≤Μ±ΞΚΆ÷§ΖΨΥαΒΡΙΐ―θΜ·“ΐΤπœΗΑϊΥπ…ΥΘ§≤Δ“ρ¥Υ–Έ≥…÷§÷ Ιΐ―θΜ·ΈοΘ§»γΘΚ»©Μυ(±ϊΕΰ»©)ΓΔΆΣΜυΓΔτ«ΜυΓΔτ ΜυΒ»ΓΘ“ρΕχ≤β ‘±ϊΕΰ»©Κ§ΝΩ≥ΘΩ…Ζ¥”≥ΜζΧεΡΎ÷§÷ Ιΐ―θΜ·ΒΡ≥ΧΕ»Θ§ΦδΫ”ΒΊΖ¥”≥≥ωœΗΑϊΥπ…ΥΒΡ≥ΧΕ»ΓΘ
, ΑΌΡ¥“Ϋ“©
±Ψ Β―ιΫαΙϊ÷Λ ΒΧζρϋΚœΦΝDFOΡήΟςœ‘Φθ«αGMΕ‘κύ σΒΡΧΐΝΠΥπΚΠΓΘDFO+GMΉιΒΡΕζΈœΉι÷·±ϊΕΰ»©ΚΆΧζάκΉ”Κ§ΝΩΕΦœ‘÷χΒΆ”ΎGMΉιΘ§ΥΒΟς±ϊΕΰ»©ΚΆΧζάκΉ”Ω…Ρή‘ΎGMΕζΕΨΜζάμ÷–Τπ÷Ί“ΣΉς”ΟΓΘDFO+GMΉιΒΡΕζΈœΉι÷·≥§―θΜ·ΈοΤγΜ·ΟΗΚ§ΝΩœ‘÷χΗΏ”ΎGMΉι(P<0.05)Θ§ ΦδΫ”Ζ¥”≥ΝΥDFOΒΡ±ΘΜΛΉς”Ο”κΉ‘”…Μυ”–ΙΊΓΘ Β―ιΫαΙϊGMΉι…ωΙΠ”–Οςœ‘Υπ…ΥΘ§ΕχΝΫΉι…ωΤΛ÷ Ήι÷·±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζάκΉ”Κ§ΝΩ≤ν“λΈόœ‘÷χ–‘(P>0.05)Θ§±μΟςGMΒΡ…ωΕΨ–‘Ω…ΡήΜΙ”–ΗϋΗ¥‘”ΒΡΉς”ΟΜζάμΘ§”–¥ΐΫχ“Μ≤Ϋ―–ΨΩΓΘ
≤ΈΩΦΈΡœΉ
1 Priuska EM, Schacht J.Formation of free radicals by gentamicin and iron and evidence for an iron/gentamicin complex. Biochem Pharmacol, 1995,50:1749-1752.
2 Song BB, Schacht J.Variable efficacy of radical scavengers and iron chelators to attenuate gentamicin ototoxicity in guinea pig in vivo. Hear Res, 1996,94:87-93.
, http://www.100md.com
3 ΝθΥ≥άϊ,ΆθΫθΝα.÷Τ±ΗΕζΈœ”≤ΤΧΤ§“χΫΰ±ξ±ΨΒΡΧεΜα.ΒΎΥΡΨϋ“Ϋ¥σ―ß―ß±®,1985,6:353-354.
4 Sabath LD, Matsen JM.Assay of antimicrobial agents. In: Lennethe EH, Spaulding EH, Truant JP, eds. Manual of clinical microbiology. 2ed. Washington:American Society for Microbiology,1974.428-430.
5 Hershko C.Iron chelators in medicine. Mol Aspects Med, 1992,13:113-165.
6 Shirane M, Harrison RV.The effects of deferoxamine mesylate and hypoxia on the cochlea.Acta Otolaryngol,1987,16:334-339.
, ΑΌΡ¥“Ϋ“©
7 Song BB, Anderson DJ, Schacht J.Protection from gentamicin ototoxicity by iron chelators in guinea pig in vivo. J Pharmacol Exp Ther, 1997,282:369-377.
8 Pierson MG, Moller AR.Prophylaxis of kanamycin-induced ototoxicity by a radioprotectant. Hear Res, 1981,4:79-87.
9 Garets SL,Altschuler RA,Schacht J.Attenuation of gentamicin ototoxicity by glutathione in the guinea pig in vivo.Hear Res,1994,77:81-87.
10 Lautermann J,McLaren J ,Schacht J.Glutathione protection against gentamicin ototoxicity depends on nutritional status.Hear Res,1995,86:15-24.
( ’ΗεΘΚ1998-11-06 –όΜΊΘΚ1999-03-02), http://www.100md.com
ΒΞΈΜΘΚΜϋœή…ζΘ§ΜυΫπΑύ―–ΨΩ…ζ ΈςΑ≤ ΒΎΥΡΨϋ“Ϋ¥σ―ßΗΫ τΈςΨ©“Ϋ‘ΚΕ汫― ΚμΩΤ 710032
ΙΊΦϋ¥ ΘΚ«λ¥σΟΙΥΊάύΘΜΘΜ»ΞΧζΑΖΘΜΘΜ“©ΈοœύΜΞΉς”ΟΘΜΘΜ÷–ΕΨΘΜΘΜΧΐΝΠ’œΑ≠
÷–ΜΣΕ汫― ΚμΩΤ‘”÷Ψ990308 ΓΨ’Σ“ΣΓΩ ΡΩΒΡ ΧΫΧ÷ΧζρϋΚœΦΝΦΉΜ«Υα»ΞΧζΑΖ(deferoxamine mesylate, DFO)Ε‘ΩΙ«λ¥σΟΙΥΊ(gentamicinΘ§GM)ΕζΕΨ–‘Ής”ΟΦΑΤδΜζάμΓΘΖΫΖ® κύ σΥφΜζΖ÷ΈΣGMΉι(17÷Μ)ΓΔDFOΉι(8÷Μ)ΓΔGM+DFOΉι(17÷Μ)ΦΑΕ‘’’Ήι(8÷Μ)Θ§≤…”ΟΧΐ–‘Ρ‘Η…Ζ¥”Π(acoustic brainstem responseΘ§ABR)ΓΔΕζΈœΤΧΤ§ΦΑΆΗ…δΒγΨΒΦΦ θΘ§Ιέ≤λ”Ο“©«ΑΚσΧΐΖ¥”Πψ–ΦΑ–ΈΧ§―ß±δΜ·Θ§Φλ≤β―Σ«εΡρΥΊΒΣΓΔΦΓή’“‘ΦΑGM≈®Ε»Θ§Ά§ ±≤βΕ®ΕζΈœΚΆ…ωΤΛ÷ Ήι÷·÷–±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζάκΉ”Κ§ΝΩΓΘΫαΙϊ GMΉι8 kHz ABRψ–“ΤΈΣ40ΓΪ60 dBΘΜGM+DFOΉιψ–“ΤΈΣ15ΓΪ25 dBΘ§≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘ–ΈΧ§―ßΗΡ±δ”κΧΐΝΠ±δΜ·“Μ÷¬ΓΘDFOΕ‘GM―Σ“©≈®Ε»ΟΜ”–”ΑœλΓΘGMΉι…ωΙΠΟςœ‘Υπ…Υ,ΒΪ…ωΤΛ÷ ±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζάκΉ”±δΜ·≤ν“λΈόœ‘÷χ–‘(P>0.05)Θ§GM+DFOΉιΕζΈœΉι÷·±ϊΕΰ»©ΚΆΧζάκΉ”Κ§ΝΩΫœGMΉιΟςœ‘Φθ…Ό(P<0.05)Θ§≥§―θΜ·ΈοΤγΜ·ΟΗΚ§ΝΩΟςœ‘ΗΏ”ΎGMΉι(P<0.05)ΓΘΫα¬έ Ή‘”…ΜυΚΆΧζάκΉ”‘ΎGMΒΡΕζΕΨ–‘÷–Τπ÷Ί“ΣΉς”ΟΘ§DFOΡή”––ßΦθ«αGMΒΡΕζΕΨ–‘Ής”ΟΘ§Ω…Ρή≥…ΈΣ”–œΘΆϊΒΡ‘ΛΖά“©ΈοΓΘ
, ΑΌΡ¥“Ϋ“©
Deferoxamine protects against gentamicin ototoxicity
CHEN Yang, WANG Jinling,HUANG Weiguo,et al. Department of Otorhinolaryngology, XiJing Hospital, Fourth Military Medical University, XiΓ·an 710032
ΓΨAbstractΓΩ Objective To study the prevention of gentamicin(GM) ototoxicity by deferoxamine(DFO) in the guinea pig. Methods Guinea pigs were randomly assigned to three experimental groups (GM-treated alone, DFO-treated alone, GM and DFO in combination) and one control group. Acoustic brainstem response (ABR), the surface preparation and transmission electron microscopy were utilized to evaluate the hearing thresholds and the cochlear morphology. To explore the mechanism associated with deferoxamine protection, serum levels of GM, BUN and Cr, together with concentration of MDA, SOD and iron in cochlear and renal tissues were measured. Results The GM group developed up to 40 ΓΪ60 dB of the threshold shifts at 8 kHz while the GM+DFO group developed only 15 ΓΪ25 dB of the threshold shifts (P<0.05). Morphological changes were consistent with functional changes. DFO did not alter serum levels of GM. Renal function of GM group was damaged obviously. However, changes of MDA, SOD and iron were not significant (P>0.05). MDA and iron concentrations in cochlear tissue of the GM+DFO group were significantly lower than those in the GM group (P<0.05) while SOD level was much higher than that in GM group. Conclusion This study suggests that free radical and iron involve in GM ototoxicity and DFO may become a promising therapeutic agent that can be used to reduce gentamicin ototoxicity.
, ΑΌΡ¥“Ϋ“©
ΓΨKey wordsΓΩ Gentamicins Poisoning Hearing disorders Deferoxamine Drug interactions
PriuskaΒ»[1]Χα≥ω«λ¥σΟΙΥΊ(gentamicinΘ§GM)ΕζΕΨ–‘Ω…Ρή «”…”ΎGM‘ΎΧεΡΎ–Έ≥…GM-ΧζΗ¥ΚœΈοΘ§¥ΏΜ·≤ζ…ζΉ‘”…ΜυΕχΥπ…ΥΟΪœΗΑϊΓΘΉ‘”…Μυ«ε≥ΐΦΝΚΆΧζρϋΚœΦΝΩ…“‘Φθ«αGM “ΐΤπΒΡΧΐΝΠΥπΚΠ[2]ΓΘ±Ψ Β―ιΆ®ΙΐABRΦλ≤βΓΔΕζΈœΤΧΤ§ΦΑΆΗ…δΒγΨΒΦΦ θΘ§Ιέ≤λκύ σ”Ο“©«ΑΚσΧΐΖ¥”Πψ–ΦΑΕζΈœΟΪœΗΑϊΓΔ―ΣΙήΈΤΒΡΗΡ±δΘ§Ιέ≤λΧζρϋΚœΦΝΦΉΜ«Υα»ΞΧζΑΖ(deferoxamine mesylate,DFO)Ε‘ΩΙGMΕζΕΨ–‘ΒΡΉς”ΟΘΜΆ§ ±Φλ≤βΕζΈœΚΆ…ωΤΛ÷ Ήι÷·±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζάκΉ”ΒΡΚ§ΝΩΘ§≤βΕ®―Σ«εGMΚΆΡρΥΊΒΣΓΔΦΓή’Υ°ΤΫΘ§“‘ΧΫΧ÷ΤδΩ…ΡήΒΡΉς”ΟΜζάμΦΑΤδ”κ…ωΕΨ–‘ΒΡΙΊœΒΓΘ
≤ΡΝœΦΑΖΫΖ®
1. Β―ιΕ·ΈοΘΚΕζάΣΖ¥…δ’ΐ≥ΘΒΡΫΓΩΒ–έ–‘‘”…Ϊκύ σ50÷ΜΘ§Χε÷Ί250ΓΪ350 gΘ§ΥφΜζΖ÷≥…4ΉιΓΘ GMΉι17÷ΜΘΚΝρΥα«λ¥σΟΙΥΊ(Ές±±ΒΎΕΰΚœ≥…“©≥ß…ζ≤ζΘ§≈ζΚ≈970818) 120 mg/kgΤΛœ¬ΉΔ…δΘ§ΟΩΧλ1¥ΈΘ§Ν§–χ19 dΘΜDFOΉι8÷ΜΘΚDFO(SigmaΙΪΥΨΘ§ΟάΙζΘ§ΟήΈςΗυ¥σ―ß“Ϋ―ß÷––ΡKresgeΧΐΝΠ―–ΨΩΥυΧαΙ©) ΟΩ¥Έ100 mg/kgΤΛœ¬ΉΔ…δΘ§ΟΩΧλ2¥Έ(ΦδΗτ4 h)Θ§Ν§–χ19 dΘΜGM+DFOΉι17÷ΜΘΚGMΚΆDFOΆ§ ±ΉΔ…δΘ§4 hΚσΉΔ…δDFOΘ§ΦΝΝΩΆ§…œΘΜΕ‘’’Ήι 8÷ΜΘΚ…ζάμ―ΈΥ°Β»ΝΩΤΛœ¬ΉΔ…δΘ§ΟΩΧλ1¥ΈΘ§Ν§–χ19 dΓΘ Ε·Έο Β―ιΤΎΦδΟΩΧλ≥”Χε÷Ί“‘Βς’ϊ“©ΝΩΓΘ
, ΑΌΡ¥“Ϋ“©
2.ABRΦλ≤βΧΐΖ¥”Πψ–ΘΚ”Ο“©«ΑΦΑ”Ο“©ΚσΒΎ9ΚΆ19 dΓΔΒΎ28ΚΆ42 d÷ήΦλ≤βΥΪΕζABRΓΘΕ·Έο‘ΎΈλΑΆ±»ΆΉΡΤ 40 mg/kg ΗΙ«ΜΉΔ…δ¬ιΉμΚσΘ§’κ–ΆΦ«¬ΦΒγΦΪ÷Ο«ΑΕν’ΐ÷–ΤΛœ¬Θ§≤ΈΩΦΒγΦΪ÷Ο≤β ‘ΕζΆβΕζΒάΩΎΚσ…œΤΛœ¬Θ§±«ΦβΫ”ΒΊΓΘ”ΟSS-1–Ά…υ¥ΧΦΛΤςΘ§286ΦΤΥψΜζΉ‘Ε·≤…―υΘ§≤…”ΟΕΧ…υ(click)1ΓΔ2ΓΔ4ΓΔ8 kHz¥ΧΦΛΘ§ΦδΗτ75 msΘ§…®Οη ±Φδ20 msΘ§ΒΰΦ”256¥ΈΘ§¥χΆ®¬Υ≤®80ΓΪ1 500 HzΘ§‘ΎΤΝ±ΈΗτ…υ “ΡΎ≥ΘΙφ≤β ‘ΓΘ
3.ΆΗ…δΒγΨΒ±ξ±Ψ÷Τ±ΗΘΚΆΘ“©ΚσΒΎ2 dΦλ≤βABRΚσΗςΉιΥφΜζ»Γ4 ÷ΜΕ·ΈοΕœΆΖ¥ΠΥάΘ§ΟΩ÷ΜΕ·ΈοΗς»Γ1ΕζΘ§Χΐ≈ί÷Ο2.5%ΈλΕΰ»©ΡΎΘ§ΫβΤ œ‘ΈΔΨΒœ¬’Σ≥ΐοκΙ«Θ§¥ΧΤΤ‘≤¥ΑΘ§ΧτΩΣΈœΕΞΘ§ΙύΝςΙΧΕ®ΚσΫΰΉ’ΙΧΕ®24 hΘ§ΝΉΥαΜΚ≥ε“ΚΤ·œ¥ΚσΫβΤ ±ξ±ΨΘ§»Γ≥ωΗςΜΊΜυΒΉΡΛΦΑ―ΣΙήΈΤΘ§1%οΑΥαΚσΙΧΕ®Θ§±ϊΆΣΆ―Υ°Θ§ΜΖ―θ ς÷§Αϋ¬ώΘ§≥§±Γ«–Τ§Θ§”Υ«Π»Ψ…ΪΓΘ
4.ΕζΈœ”≤ΤΧΤ§±ξ±Ψ÷Τ±ΗΘΚ»Γ≤Ρ ±ΦδΆ§…œΘ§Νμ1ΕζΧΐ≈ίœθΥα“χ»Ψ…ΪΖ®≥ΘΙφ÷Τ±Η[3]ΓΘ
, ΑΌΡ¥“Ϋ“©
5.ΈΔ…ζΈο÷ΫΤ§ά©…ΔΖ®≤βΕ®«λ¥σΟΙΥΊ―Σ“©≈®Ε»[4]ΘΚGMΉιΚΆGM+DFOΉιΕ·ΈοΒΎ9ΚΆ19 dΉΔ…δ«λ¥σΟΙΥΊΚσ 1 hΦτΉΠ»Γ―ΣΘ§≤βΕ®―Σ«ε“÷ΨζΜΖ÷±ΨΕΘ§‘Ό≤ι±ξΉΦ«ζœΏΆΦΘ§ΒΟ≥ω―Σ«ε«λ¥σΟΙΥΊ≈®Ε»ΓΘ
6.Φλ≤β…ωΙΠΘΚ»Γ―υ ±ΦδΚΆΖΫΖ®Ά§…œΘ§»ΪΉ‘Ε·…ζΜ·Φλ≤β“«(»’ΝΔΙΪΥΨ, »’±Ψ)≤βΕ®―Σ«εΡρΥΊΒΣΚΆΦΓή’ΓΘ
7.Φλ≤βΕζΈœΚΆ…ωΤΛ÷ ΒΡ±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζΘΚGMΉιΚΆGM+DFOΉιΒΎ9ΚΆ19 dΗς»Γ3÷ΜΕ·ΈοΜν…±Θ§―ΗΥΌ»Γ≥ωΕζΈœΘ§ΥΪΕζΚœΈΣ1Ζί±ξ±Ψ÷Τ≥…‘»Ϋ§Θ§4 000 r/minάκ–Ρ10 minΘ§»Γ…œ«ε“Κ-20 ΓφΕ≥¥φΓΘ≤…”ΟΡœΨ©Ϋ®≥……ζΈο―–ΨΩΥυΒΡ±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΩΦ¬μΥΙΝΝάΕΒΑΑΉ≤βΕ® ‘ΦΝΚ–Θ§Α¥ΥΒΟς≤ΌΉςΦλ≤βΘΜ‘≠Ή”Έϋ ’Ζ÷ΙβΙβΕ»ΦΤ(ΧλΫρΒΎ“Μ“ΫΝΤΤς≤Ρ…η±Η≥ß)Φλ≤βΧζΒΡΚ§ΝΩΓΘΆ≥ΦΤ―ß¥Πάμ”ΟΖΫ≤νΖ÷ΈωΓΘ
ΫαΙϊ
1. Β―ι÷–GMΉι3÷ΜΕ·ΈοΖ÷±π”Ύ”Ο“©ΒΎ11ΓΔ18ΚΆ19 dΥάΆωΘ§Υά«ΑΨυœϊ ίΓΔΈόΝΠΓΔΕζάΣΖ¥…δœϊ ßΘ§Τδ”ύΗςΉιΈόΥάΆωΓΘΒΎ19 dΕ‘’’ΉιΤΫΨυ‘ω≥Λ35 gΘ§ΕχGMΉιΕ·ΈοΧε÷ΊΤΫΨυΦθ…Ό2 g, ≤ν“λ”–œ‘÷χ–‘(P<0.05)ΘΜΆΘ“©ΚσGMΉιΕ·ΈοΜ÷Η¥Χε÷Ί‘ω≥ΛΓΘGM+DFOΉιΓΔDFOΉιΒΎ19 dΧε÷ΊΤΫΨυ‘ω≥Λ33gΚΆ31gΘ§ΚΆΕ‘’’Ήι÷°Φδ±»Ϋœ≤ν“λΈόœ‘÷χ–‘(P>0.05)ΓΘ
, ΑΌΡ¥“Ϋ“©
2.ABRΦλ≤βΘΚκύ σΒΡABR“‘Δσ≤®Ήν÷χΘ§“ρ¥Υ“‘Δσ≤®≈–ΕœABRΖ¥”Πψ–(dB SPL)Θ§”Ο“©ΚσΗςΉιΕ·ΈοABRΤΫΨυΖ¥”Πψ–“ΤΦϊΆΦ1ΓΘΥδ»Μ Β―ιΕ·ΈοΕ‘“©ΈοΒΡΖ¥”ΠΨΏ”–ΗωΧε≤ν“λΘ§ΒΪGM+DFOΉιΖ¥”Πψ–ΥπΚΠΫœGMΉιΟςœ‘Φθ«αΓΘ”Ο“©ΚσΒΎ4÷ήΘ§GMΉι4 kHzΦΑ8 kHzΖ¥”Πψ–ΤΫΨυ(
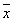 ΓάsΘ§œ¬Ά§)…ΐΗΏ(44Γά18)dBΦΑ(60Γά17)dBΘ§ΕχGM+DFOΉι‘ρΖ÷±πΈΣ(16Γά5)dBΦΑ(21Γά5)dBΘ§ΝΫΉι≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘΥπ…ΥΨΏ”–ΤΒ¬ ≤ν“λΘ§ΗΏΤΒΥπ…ΥΟςœ‘±»ΒΆΤΒΥπ…Υ―œ÷Ί(P<0.01)ΓΘDFOΉιΚΆΕ‘’’ΉιΖ¥”Πψ–±δΜ·≤ΜΟςœ‘(P>0.05)ΓΘ
ΓάsΘ§œ¬Ά§)…ΐΗΏ(44Γά18)dBΦΑ(60Γά17)dBΘ§ΕχGM+DFOΉι‘ρΖ÷±πΈΣ(16Γά5)dBΦΑ(21Γά5)dBΘ§ΝΫΉι≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘΥπ…ΥΨΏ”–ΤΒ¬ ≤ν“λΘ§ΗΏΤΒΥπ…ΥΟςœ‘±»ΒΆΤΒΥπ…Υ―œ÷Ί(P<0.01)ΓΘDFOΉιΚΆΕ‘’’ΉιΖ¥”Πψ–±δΜ·≤ΜΟςœ‘(P>0.05)ΓΘ 
ΆΦ1 ”Ο“©ΚσΗςΉιΕ·Έο≤ΜΆ§ΤΒ¬ ΕΧ…υ¥ΧΦΛΒΡABRΤΫΨυψ–“Τ
3.ΕζΈœΤΧΤ§ΦΑΆΗ…δΒγΨΒΥυΦϊΘΚΕζΈœΤΧΤ§œ‘ ΨGMΉι”Ο“©Κσ3≈≈ΆβΟΪœΗΑϊΥπ…ΥΟςœ‘±»GM+DFOΉι÷Ί(ΆΦ2,3)Θ§«“¥”ΕΞΜΊ÷ΝΒΉΜΊ÷πΫΞΦ”÷ΊΘ§ΆβΟΪœΗΑϊΥπ…ΥΫœΡΎΟΪœΗΑϊ÷ΊΓΘΆΗ…δΒγΨΒΦϊGMΉιΕζΈœΟΪœΗΑϊΑϊΫ§œΗΑϊΤςΦθ…ΌΘ§≥ Ω’≈ί±δ–‘(ΆΦ4)ΘΜGM+DFOΉι‘ρœ‘ ΨΥπ…ΥΫœ«αΘ§œΏΝΘΧεΆξ’ϊΘ§≥ωœ÷“Μ–©Εύ≈ίΧεΫαΙΙ(ΆΦ5)ΓΘGMΉιΜΙΩ…ΦϊΕζΈœ¥Ϊ»κ…ώΨ≠ΆΜ¥ΞœΏΝΘΧεΩ’Μ·Θ§―ΣΙήΈΤ±Ώ‘ΒœΗΑϊΆΜΤπ÷–ΒΡ…Ό ΐœΏΝΘΧε“ύ≥ωœ÷α’Φθ…ΌΓΔΩ’Μ·ΓΘDFOΉι”κΕ‘’’Ήι”Ο“©«ΑΚσΕζΈœΤΧΤ§ΦΑΆΗ…δΒγΨΒΗΡ±δ≤ΜΟςœ‘ΓΘ

, ΑΌΡ¥“Ϋ“©
ΆΦ2 ΕζΈœΤΧΤ§ΦϊGMΉιΒΎΕΰΜΊΆβΟΪœΗΑϊΥπ…ΥΟςœ‘Θ§Ϋω”–…Ό ΐ≤–ΝτΘ§ΡΎΟΪœΗΑϊ“ύΦϊΥπ…ΥΓΘΓΝ400

ΆΦ3 ΕζΈœΤΧΤ§ΦϊGM+DFOΉιΒΎΕΰΜΊΆβΟΪœΗΑϊΥπ…ΥΫœ«αΘ§ΡΎΟΪœΗΑϊΈό»± ßΓΘΓΝ400

ΆΦ4 ΆΗ…δΒγΨΒΙέ≤λGMΉιΟΪœΗΑϊΑϊΫ§œΓ η≥ Ω’≈ί±δ–‘Θ§ΑϊΚΥ≈®ΥθΓΘΓΝ6000

ΆΦ5 ΆΗ…δΒγΨΒΙέ≤λGM+DFOΉιΟΪœΗΑϊΑϊΫ§ΖαΗΜΘ§”–ΕύΗωΕύ≈ίΧε–Έ≥…ΓΘΓΝ4000
4.―Σ«εΦλ≤βΘΚGMΉιΚΆGM+DFOΉιΕ·ΈοΒΡ―Σ«εGM≈®Ε»≤ν“λΈόœ‘÷χ–‘(P>0.05)ΓΘΒΎ9 d≤βΕ®÷Β(
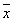 ΓάsΘ§œ¬Ά§)Ζ÷±πΈΣ(75Γά12) mg/LΚΆ(80Γά9) mg/LΘ§ΒΎ19d≤βΕ®÷ΒΖ÷±πΈΣ(110Γά12) mg/LΚΆ(114Γά9) mg/LΓΘGMΉιΒΎ19 d―Σ«εΡρΥΊΒΣΚΆΦΓή’Ζ÷±πΈΣ(28.34Γά4.3)mmol/LΚΆ(93.39Γά15.8)mmol/LΘ§GM+DFOΉιΖ÷±πΈΣ (11.48Γά5.6) mmol/LΚΆ(45.47Γά12.8) mmol/LΘ§ΝΫΉιΦδ≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘ
ΓάsΘ§œ¬Ά§)Ζ÷±πΈΣ(75Γά12) mg/LΚΆ(80Γά9) mg/LΘ§ΒΎ19d≤βΕ®÷ΒΖ÷±πΈΣ(110Γά12) mg/LΚΆ(114Γά9) mg/LΓΘGMΉιΒΎ19 d―Σ«εΡρΥΊΒΣΚΆΦΓή’Ζ÷±πΈΣ(28.34Γά4.3)mmol/LΚΆ(93.39Γά15.8)mmol/LΘ§GM+DFOΉιΖ÷±πΈΣ (11.48Γά5.6) mmol/LΚΆ(45.47Γά12.8) mmol/LΘ§ΝΫΉιΦδ≤ν“λ”–œ‘÷χ–‘(P<0.05)ΓΘ, ΑΌΡ¥“Ϋ“©
5. ΕζΈœΚΆ…ωΤΛ÷ ΒΡ±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζΦλ≤βΘΚ GM+DFOΉιΕζΈœΉι÷·ΒΎ9ΚΆ19 dΒΡΧζάκΉ”ΤΫΨυΚ§ΝΩΈΣ5.01ΠΧmol/LΚΆ5.21ΠΧmol/LΘ§ΒΆ”ΎGMΉι9.70ΠΧmol/LΚΆ8.21ΠΧmol/LΘ§≤ν“λΨυ”–œ‘÷χ–‘(P<0.05)ΘΜGM+DFOΉιΕζΈœΉι÷·Ά§ΤΎΒΡ±ϊΕΰ»©ΤΫΨυΚ§ΝΩΈΣ2.43ΚΆ2.83 mmol/mgΒΑΑΉΘ§ΒΆ”ΎGMΉι3.83ΚΆ4.78 mmol/mgΒΑΑΉΘ§≤ν“λ”–œ‘÷χ–‘(P<0.05)ΘΜGM+DFOΉιΒΎ9 d≥§―θΜ·ΈοΤγΜ·ΟΗΚ§ΝΩ‘ρœ‘÷χΗΏ”ΎGMΉι(P<0.05)Θ§Ζ÷±πΈΣ4 351ΚΆ2 480 U/mgΒΑΑΉ(nitris unit)ΓΘΝΫΉι…ωΤΛ÷ Ήι÷·±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζΚ§ΝΩ≤ν“λΈόœ‘÷χ–‘(P>0.05)ΓΘ¥ΥΆβΘ§ΒΎ19 dΩ…ΦϊGMΉι3÷ΜΕ·ΈοΒΡ…ω‘ύ÷Ή¥σ»γ«ρΉ¥Θ§≥ ΝΝΜΤ…ΪΓΘ
Χ÷¬έ
DFO «“Μ÷÷ρϋΚœΦΝΘ§÷ς“Σ”κΧζάκΉ”ΚΆ»ΐΦέ¬ΝάκΉ”–Έ≥…Η¥ΚœΈοΘ§ΤδΗ¥ΚœΈο–Έ≥…≥Θ ΐΖ÷±πΈΣ1031ΚΆ1025ΓΘ’βΝΫ÷÷Η¥ΚœΈοΆ®ΙΐΒ®÷≠ΚΆΡρΩ…Άξ»Ϊ≈≈–ΙΘ§“ρ¥ΥΕχΦθ…ΌΧζΜρ¬Ν‘ΎΤςΙΌΒΡ≤Γάμ–‘≥ΝΜΐΓΘΝΌ¥≤”Ο”Ύ÷ΈΝΤ δ―ΣΥυ÷¬ΒΡΚ§Χζ―ΣΜΤΥΊ≥ΝΉ≈≤ΓΚΆΒΊ÷–ΚΘΤΕ―ΣΒ»Φ±ΓΔ¬ΐ–‘Χζ÷–ΕΨ[5] ΓΘΝΌ¥≤‘χ±®ΒάDFOΉς≥ΛΤΎ÷ΈΝΤ ±Θ§”»ΤδΥυ”ΟΦΝΝΩ≥§ΙΐΆΤΦωΦΝΝΩΚΆ/ΜρΤδΦΝΝΩΈ¥Α¥ΒΆ―Σ«εΧζΒΑΑΉΜρ―Σ«ε¬Ν≈®Ε»ΕχΒς’ϊ ±Θ§Ω…“ΐΤπ ”ΝΠΓΔΧΐΝΠ’œΑ≠ΓΘ“≤”–―–ΨΩ÷ΛΟςΤδ≥ΛΤΎΖΰ”ΟΒΡΑ≤»Ϊ–‘[6]ΓΘ±Ψ Β―ιΥυ”Ο«λ¥σΟΙΥΊΈΣΝΌ¥≤”Π”ΟΒΡ20±ΕΘ§ΕχDFO÷Μ «ΝΌ¥≤ΦΝΝΩΒΡ2ΓΪ4±ΕΘ§DFOΉιΧΐΖ¥”Πψ–‘Ύ’ϊΗω Β―ιΙΐ≥Χ÷–±Θ≥÷Έ»Ε®Θ§±μΟςΤδΑ≤»ΪΈόΕΨ–‘ΓΘΆΘ“©Κσ1÷ήΧΐΝΠΥπΚΠ¥οΒΫΕΞΖεΘ§GM+DFOΉι8 kHzΧΐΖ¥”Πψ–ΤΫΨυΫœGMΉιΫΒΒΆ31.5 dBΘ§1 kHz“≤ΫΒΒΆΝΥ11 dB(P<0.05) Θ§ΕζΈœΟΪœΗΑϊΒΡ–ΈΧ§―ßΥπ…Υ”κΧΐΖ¥”Πψ–…ΐΗΏΒΡ≥ΧΕ»œύΤΫ––ΓΘ’β”κSongΒ»[7]ΒΡΫαΙϊ“Μ÷¬Θ§ΥΒΟςDFOΡή”––ßΦθ«αGMΒΡΕζΕΨΉς”ΟΘ§≥…ΈΣ”–œΘΆϊΒΡ‘ΛΖά“©ΈοΓΘΕχ«“’β÷÷±ΘΜΛΉς”Ο≤Μ”ΑœλGMΒΡ―Σ“©≈®Ε»Θ§»‘Ρή±Θ≥÷GMΒΡΩΙΨζ–ßΝΠΓΘ”κ“‘ΆυΒΡ±®ΒάœύΆ§Θ§GMΒΡΧΐΝΠΥπΚΠ“‘ΗΏΤΒ”»ΈΣΟτΗ–Θ§8 kHz Ήœ»≥ωœ÷Ζ¥”Πψ–…ΐΗΏΘ§«“Υπ ßΫœ÷–ΓΔΒΆΤΒΈΣ…θ(P<0.01)ΓΘ“ρ¥ΥΘ§ΗΏΤΒΧΐΖ¥”Πψ–ΒΡ…ΐΗΏΩ…‘γΤΎ‘Λ ΨGMΒΡΕζΕΨ–‘ΓΘ
, http://www.100md.com
”–ΙΊΑ±ΜυΧ«ΏΑάύΩΙ…ζΥΊΒΡΕζΕΨ–‘ΜζάμΒΡ―ßΥΒΚήΕύΘ§…–Έ¥Άξ»ΪΟςΝΥΘ§Τδ÷–÷°“ΜΈΣΉ‘”…Μυ―ßΥΒΓΘ1981ΡξPiersonΒ»[8]±®ΒάΉ‘”…Μυ«ε≥ΐΦΝWR2721Ω…―”ΜΚΩ®Ρ«ΟΙΥΊΕζ÷–ΕΨΒΡΖΔ…ζΘ§≤ΔΦθ«αΧΐΝΠΥπ ß≥ΧΕ»ΓΘΒΪΥφΚσΗςΦ“ Β―ιΒΡΫαΙϊ≤Μœύ“Μ÷¬Θ§≤ΜΆ§ΒΡΉ‘”…Μυ«ε≥ΐΦΝ÷ΈΝΤΒΟΒΫ≤ΜΆ§ΒΡΫαΙϊΓΘGaretsΒ»[9]ΚΆLautermannΒ»[10]ΕΦ÷Λ ΒΙ»Α±θΘΑΖΩ…Φθ«α«λ¥σΟΙΥΊΕζΕΨ–‘Θ§ΒΪΫωΕ‘Φ≤≤ΓΉ¥Χ§œ¬Μρ”Σ―χ»±ΖΠΒΡΕ·Έο”––ßΓΘ’β±μΟς”Π”ΟΉ‘”…Μυ«ε≥ΐΦΝΖάΜΛ«λ¥σΟΙΥΊΕζΕΨ–‘Ής”ΟΒΡ≤Μ»ΖΕ®–‘ΓΘΜζΧεΡΎΒΡ―θΉ‘”…Μυ”…ΟΗœΒΆ≥ΚΆΖ«ΟΗœΒΆ≥≤ζ…ζΡ≥–©Η¥ΚœΈο¥ΏΜ·ΒΡHaber-WeissΖ¥”ΠΘ§”…ΧζάκΉ”ΧαΙ©ΒγΉ”≤ζ…ζτ«Ή‘”…Μυ «Τδ÷–“ΜΧθ÷Ί“ΣΆΨΨΕΓΘPriuskaΒ»[1]Χα≥ωGMΒΡΕζΕΨΉς”Ο «Ά®Ιΐ”κ”ΈάκΧζάκΉ”–Έ≥…Η¥ΚœΈοΘ§¥ΏΜ·≤ζ…ζΉ‘”…ΜυΒΡΖ¥”ΠΕχΖΔΜ”ΕζΕΨ–‘Ής”ΟΓΘΉ‘”…ΜυΩ…Ά®Ιΐ…ζΈοΡΛ÷–≤Μ±ΞΚΆ÷§ΖΨΥαΒΡΙΐ―θΜ·“ΐΤπœΗΑϊΥπ…ΥΘ§≤Δ“ρ¥Υ–Έ≥…÷§÷ Ιΐ―θΜ·ΈοΘ§»γΘΚ»©Μυ(±ϊΕΰ»©)ΓΔΆΣΜυΓΔτ«ΜυΓΔτ ΜυΒ»ΓΘ“ρΕχ≤β ‘±ϊΕΰ»©Κ§ΝΩ≥ΘΩ…Ζ¥”≥ΜζΧεΡΎ÷§÷ Ιΐ―θΜ·ΒΡ≥ΧΕ»Θ§ΦδΫ”ΒΊΖ¥”≥≥ωœΗΑϊΥπ…ΥΒΡ≥ΧΕ»ΓΘ
, ΑΌΡ¥“Ϋ“©
±Ψ Β―ιΫαΙϊ÷Λ ΒΧζρϋΚœΦΝDFOΡήΟςœ‘Φθ«αGMΕ‘κύ σΒΡΧΐΝΠΥπΚΠΓΘDFO+GMΉιΒΡΕζΈœΉι÷·±ϊΕΰ»©ΚΆΧζάκΉ”Κ§ΝΩΕΦœ‘÷χΒΆ”ΎGMΉιΘ§ΥΒΟς±ϊΕΰ»©ΚΆΧζάκΉ”Ω…Ρή‘ΎGMΕζΕΨΜζάμ÷–Τπ÷Ί“ΣΉς”ΟΓΘDFO+GMΉιΒΡΕζΈœΉι÷·≥§―θΜ·ΈοΤγΜ·ΟΗΚ§ΝΩœ‘÷χΗΏ”ΎGMΉι(P<0.05)Θ§ ΦδΫ”Ζ¥”≥ΝΥDFOΒΡ±ΘΜΛΉς”Ο”κΉ‘”…Μυ”–ΙΊΓΘ Β―ιΫαΙϊGMΉι…ωΙΠ”–Οςœ‘Υπ…ΥΘ§ΕχΝΫΉι…ωΤΛ÷ Ήι÷·±ϊΕΰ»©ΓΔ≥§―θΜ·ΈοΤγΜ·ΟΗΚΆΧζάκΉ”Κ§ΝΩ≤ν“λΈόœ‘÷χ–‘(P>0.05)Θ§±μΟςGMΒΡ…ωΕΨ–‘Ω…ΡήΜΙ”–ΗϋΗ¥‘”ΒΡΉς”ΟΜζάμΘ§”–¥ΐΫχ“Μ≤Ϋ―–ΨΩΓΘ
≤ΈΩΦΈΡœΉ
1 Priuska EM, Schacht J.Formation of free radicals by gentamicin and iron and evidence for an iron/gentamicin complex. Biochem Pharmacol, 1995,50:1749-1752.
2 Song BB, Schacht J.Variable efficacy of radical scavengers and iron chelators to attenuate gentamicin ototoxicity in guinea pig in vivo. Hear Res, 1996,94:87-93.
, http://www.100md.com
3 ΝθΥ≥άϊ,ΆθΫθΝα.÷Τ±ΗΕζΈœ”≤ΤΧΤ§“χΫΰ±ξ±ΨΒΡΧεΜα.ΒΎΥΡΨϋ“Ϋ¥σ―ß―ß±®,1985,6:353-354.
4 Sabath LD, Matsen JM.Assay of antimicrobial agents. In: Lennethe EH, Spaulding EH, Truant JP, eds. Manual of clinical microbiology. 2ed. Washington:American Society for Microbiology,1974.428-430.
5 Hershko C.Iron chelators in medicine. Mol Aspects Med, 1992,13:113-165.
6 Shirane M, Harrison RV.The effects of deferoxamine mesylate and hypoxia on the cochlea.Acta Otolaryngol,1987,16:334-339.
, ΑΌΡ¥“Ϋ“©
7 Song BB, Anderson DJ, Schacht J.Protection from gentamicin ototoxicity by iron chelators in guinea pig in vivo. J Pharmacol Exp Ther, 1997,282:369-377.
8 Pierson MG, Moller AR.Prophylaxis of kanamycin-induced ototoxicity by a radioprotectant. Hear Res, 1981,4:79-87.
9 Garets SL,Altschuler RA,Schacht J.Attenuation of gentamicin ototoxicity by glutathione in the guinea pig in vivo.Hear Res,1994,77:81-87.
10 Lautermann J,McLaren J ,Schacht J.Glutathione protection against gentamicin ototoxicity depends on nutritional status.Hear Res,1995,86:15-24.
( ’ΗεΘΚ1998-11-06 –όΜΊΘΚ1999-03-02), http://www.100md.com