羟基磷灰石+骨形成蛋白+纤维蛋白粘合剂复合物增高牙槽嵴的新骨形成反应
作者:陈松龄 王大章
单位:陈松龄(中山医科大学附属第一医院口腔科, 广东 广州 510080);王大章(华西医科大学口腔医学院, 四川 成都)
关键词:骨和骨组织;纤维蛋白组织粘着剂;牙槽嵴增强术
中国病理生理杂志000720
[摘 要] 目的:观察羟基磷灰石+骨形成蛋白+纤维蛋白粘合剂(HA+BMP+FS)复合物增高牙槽嵴的新骨形成反应。方法:从小牛长骨中提取骨形成蛋白(BMP),首次采用羟基磷灰石(HA)与纤维蛋白粘合剂(FS)以及具有高效骨诱导性的BMP三者复合,形成一种功能互补的新的人工骨材料,用以进行增高犬的无牙颌牙槽嵴,术后3、6、12、24周动物处死取标本作大体、组织学观察、组织学新骨形成量计算、四环素荧光标记显微法、扫描电镜形貌观察、背反射电子图象和X线能谱分析法等检查。结果:发现:(1)实验组术后3周起出现编织骨,6周新骨增加,12~24周有成熟的骨组织相互连结,布满HA微粒间隙。对照组术后3周未见新骨,6周个别HA微粒与基骨接触,12~24周少许新骨长入。(2)新骨组织与HA直接结合,钙磷元素与HA和基骨接近。结论:HA+BMP+FS复合材料可显著地促进HA-基骨界面骨性结合,加快再建牙槽嵴的新骨形成,增加新骨形成量,从形态和功能上大大提高再建牙槽嵴的质量。
, 百拇医药
[中图分类号] R782.2 [文献标识码] A
[文章编号] 1000-4718(2000)07-0650-05
Bone formation of alveolar augmentation with hydroxylapatite,bone morphogenetic protein and fibrin sealant composite
CHEN Song-ling, WANG Da-zhang
(Dept. of Stomatology, First Affiliated Hospital, SUMS, Guangzhou 510080, China)
Abstract AIM: To investigate new bone formation of alveolar augmentation with hydroxylapatite(HA)+bone morphogenetic protein(BMP)+fibrin sealant FS(HA+BMP+FS) composite.METHODS:Bone morphogenetic protein was extracted from bovine cortical bone. Hydroxylapatite particles were combined with fibrin sealant and BMP, which is of high efficient osteoinduction, forming a new complex material. The alveolar augmentation was made with this composite. The samples were investigated 3, 6,12 and 24 weeks postoperatively, with gross observation, microscope, calculation of new bone formation, tetracycline fluorescent microscope, scanning electron microscope, backscattered electron image and X-ray energy analysis.RESULTS: 1. In experimental group, weave bone had been seen since 3 weeks postoperatively and more new bone 6 weeks postoperatively; remolded bones united and distributed to all spaces of HA particles 12~24 weeks postoperatively. In control group, no new bone appeared 3 weeks postoperatively, only some HA particles contacted base bone 6 weeks postoperatively, a little of new bone grew into HA spaces 12~24 weeks postoperatively. 2. New bone directly incorporated with HA. The quantity of calcium and phosphate are similar to HA and base bone. CONCLUSION:This composite in alveolar augmentation obviously promotes incorporation HA with base bone, speeds formation of new bone and adds amount of new bone, reconstructing a bony alveolar ridge.
, 百拇医药
MeSH Bone and bones; Fibrin tissue adhesive; Alveolar ridge augmentation
牙槽嵴处于特殊的位置,具有独特的解剖生理功能。增高的牙槽嵴要求达到承受托牙和咀嚼等功能所需的高度、外形和足够的生物力学强度。现已广泛用于增高牙槽嵴的羟基磷灰石(hydroxylapatite, HA)微粒使牙槽嵴增高术进入了一个新的发展阶段。但是,HA微粒存在早期移位和新骨形成少这两个缺点,严重地影响增高牙槽嵴的形态、功能及其临床效果。HA微粒与粘合剂复合应用,可控制微粒早期移位,却不能增加新骨形成[1]。骨形成蛋白(bone morphogenetic protein, BMP),是一种高效的骨诱导性物质,自1986年开始了临床应用研究。此后的研究表明,BMP是一种可与其他材料配合用于修复骨缺损的生物材料。针对用HA增高牙槽嵴的上述主要问题,本研究旨在利用致密HA微粒与BMP以及纤维蛋白粘合剂(fibrin sealant, FS)的各自优点,形成以HA微粒为支架的复合人工骨材料,用以进行增高牙槽嵴的实验研究,探讨其植入后的结局与规律,为临床改善增高的牙槽嵴形态和功能提供实验依据。
, 百拇医药
材 料 和 方 法
一、骨形成蛋白的提取和纯化
取新鲜1岁公牛管状骨,参考杨连甲等方法[2]提取和纯化得牛骨形成蛋白(bBMP)。
二、种植复合材料准备
致密HA微粒/bBMP/FS复合材料可在术中即时准备:
1 g HA微粒:30 mg bBMP:适当的FS。3种材料按上比例混合成块状,牙槽嵴骨区准备好后即行植入。
三、动物分组和手术方法
12只成年犬,体重10~14 kg,雌雄兼有。手术方法:拔除双侧下颌后牙形成双侧下颌后牙区无牙颌模型和3个月后牙槽嵴增高术采用牙槽嵴顶部骨膜下隧道微粒型HA植入方法。一侧(实验组)牙槽嵴增高术材料采用HA+BMP+FS复合物,对侧(对照组)用HA+FS。术后3、6、12和24周分别处死3只动物,切取双侧下颌标本,作下列检查。
, http://www.100md.com
四、观察方法
(一)大体观察 肉眼观察再建牙槽嵴的形态、高度和牢固度。
(二)组织学检查 将下颌骨标本(包括基骨、种植体和少量的周围软组织)分切,10%福尔马林固定。脱钙、包埋、腊块切片,HE和三色染色,光镜下观察。其中12周、24周标本切片计分评价新骨形成量。按下列标准计分(参考Block评分方法):
[0]再建牙槽嵴无新骨生成。
[1]再建牙槽嵴新骨生成高度为0.5~1.5 mm,并包绕基骨骨皮质附近的HA微粒。
[2]新骨生成高度2~3 mm。
[3]新骨生成高度3.5~4.5 mm,未达种植体全层。
, 百拇医药 [4]新骨长入HA微粒种植体全层,接触种植体顶部。
(三)四环素荧光标记显微观察 12、24周部分标本分切酒精固定后,磨片,荧光显微镜下观察。
(四)扫描电镜背反射电子图象检查 12、24周部分标本2.5%戊二醛固定,金刚砂片分切,低温切面磨平,酒精逐级脱水,临界点干燥,在扫描电子显微镜(AMRAY-1000BSEM)作背反射电子图象检查,并同时作X线能谱分析。
(五)扫描电镜形貌观察 主要观察新骨形态以及新骨与HA结合的界面关系。
五、数据处理
实验数据以 ±s表示,组间差异显著性用t检验判定。
±s表示,组间差异显著性用t检验判定。
, http://www.100md.com 结 果
一、形态学观察所见
(一)大体观察 术后3周,对照组和实验组两组增高的牙槽嵴指压均有轻微的压痕。用牙科金刚片转动切割增高牙槽嵴标本,HA微粒易于脱落。剖面观察,HA微粒与周围组织结合疏松。术后6周,两组增高的牙槽嵴硬度增加,指压呈骨样硬度感。金刚砂片转动切割,微粒较少脱落。剖面观察,对照组HA种植体为白色,基骨呈暗黄色,界线清楚;实验组HA微粒间有暗黄色骨样物质存在,HA-基骨界限不清,微粒之间结合较对照组紧密。术后12周,两组增高的牙槽外形圆滑,不易推动,金刚砂片切割,对照组增高的牙槽嵴易于切入,手指用力沿剖面推压,可见HA微粒脱落,实验组增高的牙槽嵴切入阻力大,剖面见HA微粒间有较多暗黄色骨样组织长入,手指沿剖面推压,微粒未见脱落。术后24周,对照组:用金刚砂片切割增高的牙槽嵴,感觉稍较术后12周对照组样品硬,但仍易切入。剖面观察,HA微粒间见少许的暗黄色骨样组织自界面长入。沿剖面推压仍见微粒脱出。实验组:金刚砂片切面阻力大,与切割骨皮质的阻力相近。剖面HA微粒间有大量的暗黄色骨样组织长入,HA微粒紧嵌在骨组织中,与骨组织相互结合紧密,形成一坚硬的整体即使沿剖面在磨石表面推磨,也只见微粒部份磨损,未见微粒脱出。
, http://www.100md.com
(二)组织学观察
1.对照组 术后3周再建牙槽嵴HA微粒间纤维组织长入。6周起,种植体和基骨之间界面骨性结合。12~24周,种植体内只见少量的新生骨形成,包绕基骨皮质附近的微粒,种植体其他区域大都为纤维组织分布,其间见新生的毛细血管。
2.实验组 术后3周有大量的纤维组织长入种植体,其间见许多未分化的间充质细胞,梭形、圆形、钩形,排列不规则,聚集分布。已见软骨和骨样组织。未成熟的编织骨在某一区域已相互连成片,种植体-基质界面已见骨性结合。炎症细胞浸润已基本消退。术后6周,HA微粒间纤维组织分化成类骨样组织,细胞核大,多为卵圆形,向成骨细胞分化。这时期,已见明显的更加成熟的新骨组织出现,新骨组织相互连接,但尚不能成熟为板状骨,细胞成份多,基质较少。新骨不仅仅出现在HA-基骨界面区域,而且在种植体中部也已经见到。术后12周种植体与基质界面融合,难分清界线。HA微粒间见大量的新骨组织,大都已形成板状骨。在板状骨的基础上可见更新的骨组织形成。可见软骨成骨、编织骨、钙化灶等多样成骨反应。骨形成明显较同期的对照组活跃、丰富,可达种植体全层。新形成骨细胞体大,胞浆丰富、核大,埋于骨基质之中。哈佛氏系统清楚地出现。三色染色显示新形成的板状骨和基骨染成红色一片,分不清界限。许多毛细血管存在。术后24周,新骨改建更加成熟,较多的哈佛氏系统已明显可见(图1~2)。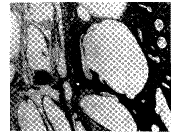
, http://www.100md.com
Fig 1 In control group, 24 weeks after operation, a little of new bone grew into HA spaces (HE 4×10)
图1 对照组标本,术后24周,新骨少量长入
Fig 2 In experimental group, 24 weeks after operation, new bone grew into all spaces of HA (HE 4×10)
图2 实验组标本,术后24周,新骨长入所有HA间隙
二、新骨形成量的计算
表1 术后12~24周再建牙槽嵴新骨高度及评分比较
, 百拇医药
Tab 1 Comparison of height and grade of new bone in alveolar
augmentation 12~24 weeks after operation ( ±s,n=12)
±s,n=12)
Control group
Experimental group
Height of new bone (mm)
0.893±0.318
4.610±0.725*
Grade of new bone
, http://www.100md.com
0.916±0.204
3.670±0.516*
*P<0.05, vs control group
三、四环素荧光标记显微法
术后12周的对照组标本见HA种植体底部少量的新骨生成,术后24周新骨形成增加。术后12周的实验组,新骨形成活跃,荧光不仅出现于HA-基骨界面区域,而且分布在HA微粒种植体的中央,有些可达种植体顶层,有些磨片荧光虽未达到顶层,但荧光物质继续沉积增加。术后24周,HA微粒大部分由荧光带包绕,多数磨片中,荧光带可达种植体顶层。可见HA微粒间新骨更加成熟,出现哈佛氏系统圆形、椭圆形荧光环,与其下基骨哈佛氏系统荧光环相似。HA微粒间荧光和基骨荧光连成一片。
四、背反射电子图象检查
, http://www.100md.com
背反射电子图象中,HA材料显示为白色,新骨组织为灰白色,软组织为黑色。对照组术后12周,HA种植体基底有少许新骨,24周新骨继续增加。术后12周实验组标本,新骨形成活跃,分布于大部分HA微粒间,有些标本,可见达顶层,但新骨不够成熟,呈暗灰白色,术后24周新骨更加成熟,较术后12周的新骨颜色白,接近基骨。可见新骨布满整个HA种植体,HA微粒间隙变大(图3)。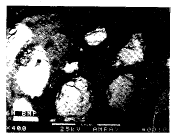
Fig 3 The backscattered electron image showed in experimental group, 24 weeks after operation, new bone distributed to all spaces of HA (×40)
图3 背反射电子图象显示实验组标本,术后24周,新骨长入所有HA间隙
, 百拇医药
五、扫描电镜形貌观察
对照组:术后12周标本HA种植体基底见少许新骨生成,其余大部分微粒由纤维组织包绕。术后24周标本,新骨形成增加。实验组:术后12周标本,HA微粒间见较多的新骨形成,新骨不仅出现在HA复合种植体基底区,也见出现在中部,或种植体的2/3高度,个别标本可见新骨达种植体顶层。新骨沉积于纤维组织间,与HA微粒直接结合,但新骨不够致密。术后24周标本新骨组织致密呈板状,形态与基骨相似,与HA直接结合,大部分HA微粒间新骨形成,新骨可达顶部。
六、X线能谱分析
对照组HA微粒间组织钙磷含量低,显示较高的有机组织能谱,实验组HA微粒间新骨钙磷含量较高,接近基骨。
讨 论
1965年,Urist发现脱矿骨植入皮下组织可刺激新骨生长,提出了骨诱导的理论。骨诱导的细胞分化过程,是从未分化的间充质细胞转变为软骨或骨母细胞。Sampath和Reddi进一步的研究揭示了骨诱导的主要因子是小于50 kD的物质,且在人、猴、牛和兔不同种属中有同源性[3]。自此以后,许多学者已从可诱导骨形成的骨基质上提取许多活性因子,如骨形成蛋白和转移生长因子-β等。骨形成蛋白是迄今最为肯定的高效骨诱导性物质,分子量为18~22 kD,在动物的骨皮质中BMP含量小,而且与其他蛋白质成份结合成一个复杂的厌水性聚合物。本实验用小公牛管状骨提取的bBMP证明具有骨诱导能力,骨组织形成的诱导过程与Urist、杨连甲等报道相似[2,4]。
, 百拇医药
本研究采用了HA+BMP+FS作为再建牙槽嵴的复合人工骨材料,其中HA是种植材料的主体成分,它构成再造牙槽嵴的骨性支架。种植体HA微粒可与基骨骨性结合,引导新骨长入,可是新骨形成量少,时间长,难以在较短的时间范围内形成一个骨性的再造牙槽嵴。所以,设计HA与BMP复合以求迅速地增加再建牙槽嵴的新骨形成量。致密HA微粒无孔性结构,面积小,溶解BMP与之复合需经一系列过程(溶解、透析、冻干、再消毒),且这种直接复合方式必须术前就完成。过程复杂、费时,且得不到满意的复合效果[5]。本研究用纤维蛋白作为BMP载体,能定量地将BMP混合种植体中,可在术中即时进行,简便易行。纤维蛋白作为种植体的一种成份,可发挥以下功能:(1)限制术后微粒的早期移位;(2)促进纤维组织长入,有利于种植材料固位、成形和速硬,促进BMP在计划区域内发挥骨诱导作用;(3)作为BMP的载体,建立一个BMP浓度梯度,改善BMP与周围细胞的接触,增加BMP诱导的新骨量;(4)纤维蛋白粘合剂使种植材料易于成形,方便手术操作。3种材料组成一种功能互补的种植复合物,能使再造牙槽嵴获得较理想的效果。
, http://www.100md.com
以HA复合BMP再造牙槽嵴的目的是增加新骨形成。以HA复合其他骨诱导性物质也是同样的目的,Block等[6]实验表明:HA复合自体骨再造牙槽嵴术后12周,便观察到相互连结的新骨组织。用HA+脱矿骨,则12周只见少许的新骨形成,部份区域新骨连成片。26周才见相互连接的板状骨成片布满全层[7]。但与自体骨复合则必需自体取骨,而复合脱矿骨成骨较慢。本研究发现HA+BMP+FS复合材料再建牙槽嵴,所得结果与复合自体骨、脱矿骨相比,HA复合BMP免除了自体骨移植的缺点,新骨形成早,增加了新骨形成量,而且未发现局部异物反应。
多种方法较客观地显示BMP诱导的新骨组织与HA直接结合,新骨钙磷含量与HA和基骨相近。表明这些新骨组织与HA的结合完全可以构成一个骨性的再建牙槽嵴。
致密HA在体内不吸收,HA+BMP复合种植同时具有骨诱导和骨引导作用。本研究发现新骨形成主要自基骨界面开始,与这种双重作用有关。
, http://www.100md.com
[基金项目]:卫生部青年基金(93064)和广东省科委基金(97016)资助
[参 考 文 献]
[1] Meijer HJ, Steen WH, Bosman F, et al. Radiographic evaluation of mandibular augmentation with prefabricated hydroxylapatite/fibrin glue implants[J]. J Oral Maxillofac Surg, 1997, 55(2): 138~144.
[2] 杨连甲,金岩.骨形成蛋白(BMP)的实验研究[J].实用口腔医学杂志,1987, 3(2): 78~80.
[3] Sampath TK, Reddi AH. Homology of bone-inductive proteins from human, monkey, bovine, and rat extra-cellular matrix[J]. Proc Natl Acad Aci USA, 1983, 80(21): 6591~6595.
, 百拇医药
[4] Urist MR, Lietze A, Mizuatani H, et al. A bovine low molecular weight bone morphogenetic protein (BMP) fraction[J]. Clin Orthop, 1982, 162: 219~232.
[5] Sato T, Kawamura Ⅲ, Sato K, et al. Bone morphogenesis of rabbit bone morphogenetic protein-bound hydroxylapatite-fibrin composite[J]. Clin Othop, 1991, 263: 254~262.
[6] Block MS, Kent JN. Healing of mandibular ridge augmentations using hydroxylapatite with and without autogenous bone in dogs[J]. J Oral Maxillofac Surg, 1985, 43(1): 3~7.
[7] Block MS, Kent JN, Ardoin RC, et al. Mandibular augmentation in dogs with hydroxylapatite combined with demineralized bone[J]. J Oral Maxillofac Surg, 1987, 45(5): 412~420.
[收稿日期] 2000-01-10
[修回日期] 2000-04-12, http://www.100md.com
单位:陈松龄(中山医科大学附属第一医院口腔科, 广东 广州 510080);王大章(华西医科大学口腔医学院, 四川 成都)
关键词:骨和骨组织;纤维蛋白组织粘着剂;牙槽嵴增强术
中国病理生理杂志000720
[摘 要] 目的:观察羟基磷灰石+骨形成蛋白+纤维蛋白粘合剂(HA+BMP+FS)复合物增高牙槽嵴的新骨形成反应。方法:从小牛长骨中提取骨形成蛋白(BMP),首次采用羟基磷灰石(HA)与纤维蛋白粘合剂(FS)以及具有高效骨诱导性的BMP三者复合,形成一种功能互补的新的人工骨材料,用以进行增高犬的无牙颌牙槽嵴,术后3、6、12、24周动物处死取标本作大体、组织学观察、组织学新骨形成量计算、四环素荧光标记显微法、扫描电镜形貌观察、背反射电子图象和X线能谱分析法等检查。结果:发现:(1)实验组术后3周起出现编织骨,6周新骨增加,12~24周有成熟的骨组织相互连结,布满HA微粒间隙。对照组术后3周未见新骨,6周个别HA微粒与基骨接触,12~24周少许新骨长入。(2)新骨组织与HA直接结合,钙磷元素与HA和基骨接近。结论:HA+BMP+FS复合材料可显著地促进HA-基骨界面骨性结合,加快再建牙槽嵴的新骨形成,增加新骨形成量,从形态和功能上大大提高再建牙槽嵴的质量。
, 百拇医药
[中图分类号] R782.2 [文献标识码] A
[文章编号] 1000-4718(2000)07-0650-05
Bone formation of alveolar augmentation with hydroxylapatite,bone morphogenetic protein and fibrin sealant composite
CHEN Song-ling, WANG Da-zhang
(Dept. of Stomatology, First Affiliated Hospital, SUMS, Guangzhou 510080, China)
Abstract AIM: To investigate new bone formation of alveolar augmentation with hydroxylapatite(HA)+bone morphogenetic protein(BMP)+fibrin sealant FS(HA+BMP+FS) composite.METHODS:Bone morphogenetic protein was extracted from bovine cortical bone. Hydroxylapatite particles were combined with fibrin sealant and BMP, which is of high efficient osteoinduction, forming a new complex material. The alveolar augmentation was made with this composite. The samples were investigated 3, 6,12 and 24 weeks postoperatively, with gross observation, microscope, calculation of new bone formation, tetracycline fluorescent microscope, scanning electron microscope, backscattered electron image and X-ray energy analysis.RESULTS: 1. In experimental group, weave bone had been seen since 3 weeks postoperatively and more new bone 6 weeks postoperatively; remolded bones united and distributed to all spaces of HA particles 12~24 weeks postoperatively. In control group, no new bone appeared 3 weeks postoperatively, only some HA particles contacted base bone 6 weeks postoperatively, a little of new bone grew into HA spaces 12~24 weeks postoperatively. 2. New bone directly incorporated with HA. The quantity of calcium and phosphate are similar to HA and base bone. CONCLUSION:This composite in alveolar augmentation obviously promotes incorporation HA with base bone, speeds formation of new bone and adds amount of new bone, reconstructing a bony alveolar ridge.
, 百拇医药
MeSH Bone and bones; Fibrin tissue adhesive; Alveolar ridge augmentation
牙槽嵴处于特殊的位置,具有独特的解剖生理功能。增高的牙槽嵴要求达到承受托牙和咀嚼等功能所需的高度、外形和足够的生物力学强度。现已广泛用于增高牙槽嵴的羟基磷灰石(hydroxylapatite, HA)微粒使牙槽嵴增高术进入了一个新的发展阶段。但是,HA微粒存在早期移位和新骨形成少这两个缺点,严重地影响增高牙槽嵴的形态、功能及其临床效果。HA微粒与粘合剂复合应用,可控制微粒早期移位,却不能增加新骨形成[1]。骨形成蛋白(bone morphogenetic protein, BMP),是一种高效的骨诱导性物质,自1986年开始了临床应用研究。此后的研究表明,BMP是一种可与其他材料配合用于修复骨缺损的生物材料。针对用HA增高牙槽嵴的上述主要问题,本研究旨在利用致密HA微粒与BMP以及纤维蛋白粘合剂(fibrin sealant, FS)的各自优点,形成以HA微粒为支架的复合人工骨材料,用以进行增高牙槽嵴的实验研究,探讨其植入后的结局与规律,为临床改善增高的牙槽嵴形态和功能提供实验依据。
, 百拇医药
材 料 和 方 法
一、骨形成蛋白的提取和纯化
取新鲜1岁公牛管状骨,参考杨连甲等方法[2]提取和纯化得牛骨形成蛋白(bBMP)。
二、种植复合材料准备
致密HA微粒/bBMP/FS复合材料可在术中即时准备:
1 g HA微粒:30 mg bBMP:适当的FS。3种材料按上比例混合成块状,牙槽嵴骨区准备好后即行植入。
三、动物分组和手术方法
12只成年犬,体重10~14 kg,雌雄兼有。手术方法:拔除双侧下颌后牙形成双侧下颌后牙区无牙颌模型和3个月后牙槽嵴增高术采用牙槽嵴顶部骨膜下隧道微粒型HA植入方法。一侧(实验组)牙槽嵴增高术材料采用HA+BMP+FS复合物,对侧(对照组)用HA+FS。术后3、6、12和24周分别处死3只动物,切取双侧下颌标本,作下列检查。
, http://www.100md.com
四、观察方法
(一)大体观察 肉眼观察再建牙槽嵴的形态、高度和牢固度。
(二)组织学检查 将下颌骨标本(包括基骨、种植体和少量的周围软组织)分切,10%福尔马林固定。脱钙、包埋、腊块切片,HE和三色染色,光镜下观察。其中12周、24周标本切片计分评价新骨形成量。按下列标准计分(参考Block评分方法):
[0]再建牙槽嵴无新骨生成。
[1]再建牙槽嵴新骨生成高度为0.5~1.5 mm,并包绕基骨骨皮质附近的HA微粒。
[2]新骨生成高度2~3 mm。
[3]新骨生成高度3.5~4.5 mm,未达种植体全层。
, 百拇医药 [4]新骨长入HA微粒种植体全层,接触种植体顶部。
(三)四环素荧光标记显微观察 12、24周部分标本分切酒精固定后,磨片,荧光显微镜下观察。
(四)扫描电镜背反射电子图象检查 12、24周部分标本2.5%戊二醛固定,金刚砂片分切,低温切面磨平,酒精逐级脱水,临界点干燥,在扫描电子显微镜(AMRAY-1000BSEM)作背反射电子图象检查,并同时作X线能谱分析。
(五)扫描电镜形貌观察 主要观察新骨形态以及新骨与HA结合的界面关系。
五、数据处理
实验数据以
 ±s表示,组间差异显著性用t检验判定。
±s表示,组间差异显著性用t检验判定。, http://www.100md.com 结 果
一、形态学观察所见
(一)大体观察 术后3周,对照组和实验组两组增高的牙槽嵴指压均有轻微的压痕。用牙科金刚片转动切割增高牙槽嵴标本,HA微粒易于脱落。剖面观察,HA微粒与周围组织结合疏松。术后6周,两组增高的牙槽嵴硬度增加,指压呈骨样硬度感。金刚砂片转动切割,微粒较少脱落。剖面观察,对照组HA种植体为白色,基骨呈暗黄色,界线清楚;实验组HA微粒间有暗黄色骨样物质存在,HA-基骨界限不清,微粒之间结合较对照组紧密。术后12周,两组增高的牙槽外形圆滑,不易推动,金刚砂片切割,对照组增高的牙槽嵴易于切入,手指用力沿剖面推压,可见HA微粒脱落,实验组增高的牙槽嵴切入阻力大,剖面见HA微粒间有较多暗黄色骨样组织长入,手指沿剖面推压,微粒未见脱落。术后24周,对照组:用金刚砂片切割增高的牙槽嵴,感觉稍较术后12周对照组样品硬,但仍易切入。剖面观察,HA微粒间见少许的暗黄色骨样组织自界面长入。沿剖面推压仍见微粒脱出。实验组:金刚砂片切面阻力大,与切割骨皮质的阻力相近。剖面HA微粒间有大量的暗黄色骨样组织长入,HA微粒紧嵌在骨组织中,与骨组织相互结合紧密,形成一坚硬的整体即使沿剖面在磨石表面推磨,也只见微粒部份磨损,未见微粒脱出。
, http://www.100md.com
(二)组织学观察
1.对照组 术后3周再建牙槽嵴HA微粒间纤维组织长入。6周起,种植体和基骨之间界面骨性结合。12~24周,种植体内只见少量的新生骨形成,包绕基骨皮质附近的微粒,种植体其他区域大都为纤维组织分布,其间见新生的毛细血管。
2.实验组 术后3周有大量的纤维组织长入种植体,其间见许多未分化的间充质细胞,梭形、圆形、钩形,排列不规则,聚集分布。已见软骨和骨样组织。未成熟的编织骨在某一区域已相互连成片,种植体-基质界面已见骨性结合。炎症细胞浸润已基本消退。术后6周,HA微粒间纤维组织分化成类骨样组织,细胞核大,多为卵圆形,向成骨细胞分化。这时期,已见明显的更加成熟的新骨组织出现,新骨组织相互连接,但尚不能成熟为板状骨,细胞成份多,基质较少。新骨不仅仅出现在HA-基骨界面区域,而且在种植体中部也已经见到。术后12周种植体与基质界面融合,难分清界线。HA微粒间见大量的新骨组织,大都已形成板状骨。在板状骨的基础上可见更新的骨组织形成。可见软骨成骨、编织骨、钙化灶等多样成骨反应。骨形成明显较同期的对照组活跃、丰富,可达种植体全层。新形成骨细胞体大,胞浆丰富、核大,埋于骨基质之中。哈佛氏系统清楚地出现。三色染色显示新形成的板状骨和基骨染成红色一片,分不清界限。许多毛细血管存在。术后24周,新骨改建更加成熟,较多的哈佛氏系统已明显可见(图1~2)。

, http://www.100md.com
Fig 1 In control group, 24 weeks after operation, a little of new bone grew into HA spaces (HE 4×10)
图1 对照组标本,术后24周,新骨少量长入

Fig 2 In experimental group, 24 weeks after operation, new bone grew into all spaces of HA (HE 4×10)
图2 实验组标本,术后24周,新骨长入所有HA间隙
二、新骨形成量的计算
表1 术后12~24周再建牙槽嵴新骨高度及评分比较
, 百拇医药
Tab 1 Comparison of height and grade of new bone in alveolar
augmentation 12~24 weeks after operation (
 ±s,n=12)
±s,n=12)Control group
Experimental group
Height of new bone (mm)
0.893±0.318
4.610±0.725*
Grade of new bone
, http://www.100md.com
0.916±0.204
3.670±0.516*
*P<0.05, vs control group
三、四环素荧光标记显微法
术后12周的对照组标本见HA种植体底部少量的新骨生成,术后24周新骨形成增加。术后12周的实验组,新骨形成活跃,荧光不仅出现于HA-基骨界面区域,而且分布在HA微粒种植体的中央,有些可达种植体顶层,有些磨片荧光虽未达到顶层,但荧光物质继续沉积增加。术后24周,HA微粒大部分由荧光带包绕,多数磨片中,荧光带可达种植体顶层。可见HA微粒间新骨更加成熟,出现哈佛氏系统圆形、椭圆形荧光环,与其下基骨哈佛氏系统荧光环相似。HA微粒间荧光和基骨荧光连成一片。
四、背反射电子图象检查
, http://www.100md.com
背反射电子图象中,HA材料显示为白色,新骨组织为灰白色,软组织为黑色。对照组术后12周,HA种植体基底有少许新骨,24周新骨继续增加。术后12周实验组标本,新骨形成活跃,分布于大部分HA微粒间,有些标本,可见达顶层,但新骨不够成熟,呈暗灰白色,术后24周新骨更加成熟,较术后12周的新骨颜色白,接近基骨。可见新骨布满整个HA种植体,HA微粒间隙变大(图3)。

Fig 3 The backscattered electron image showed in experimental group, 24 weeks after operation, new bone distributed to all spaces of HA (×40)
图3 背反射电子图象显示实验组标本,术后24周,新骨长入所有HA间隙
, 百拇医药
五、扫描电镜形貌观察
对照组:术后12周标本HA种植体基底见少许新骨生成,其余大部分微粒由纤维组织包绕。术后24周标本,新骨形成增加。实验组:术后12周标本,HA微粒间见较多的新骨形成,新骨不仅出现在HA复合种植体基底区,也见出现在中部,或种植体的2/3高度,个别标本可见新骨达种植体顶层。新骨沉积于纤维组织间,与HA微粒直接结合,但新骨不够致密。术后24周标本新骨组织致密呈板状,形态与基骨相似,与HA直接结合,大部分HA微粒间新骨形成,新骨可达顶部。
六、X线能谱分析
对照组HA微粒间组织钙磷含量低,显示较高的有机组织能谱,实验组HA微粒间新骨钙磷含量较高,接近基骨。
讨 论
1965年,Urist发现脱矿骨植入皮下组织可刺激新骨生长,提出了骨诱导的理论。骨诱导的细胞分化过程,是从未分化的间充质细胞转变为软骨或骨母细胞。Sampath和Reddi进一步的研究揭示了骨诱导的主要因子是小于50 kD的物质,且在人、猴、牛和兔不同种属中有同源性[3]。自此以后,许多学者已从可诱导骨形成的骨基质上提取许多活性因子,如骨形成蛋白和转移生长因子-β等。骨形成蛋白是迄今最为肯定的高效骨诱导性物质,分子量为18~22 kD,在动物的骨皮质中BMP含量小,而且与其他蛋白质成份结合成一个复杂的厌水性聚合物。本实验用小公牛管状骨提取的bBMP证明具有骨诱导能力,骨组织形成的诱导过程与Urist、杨连甲等报道相似[2,4]。
, 百拇医药
本研究采用了HA+BMP+FS作为再建牙槽嵴的复合人工骨材料,其中HA是种植材料的主体成分,它构成再造牙槽嵴的骨性支架。种植体HA微粒可与基骨骨性结合,引导新骨长入,可是新骨形成量少,时间长,难以在较短的时间范围内形成一个骨性的再造牙槽嵴。所以,设计HA与BMP复合以求迅速地增加再建牙槽嵴的新骨形成量。致密HA微粒无孔性结构,面积小,溶解BMP与之复合需经一系列过程(溶解、透析、冻干、再消毒),且这种直接复合方式必须术前就完成。过程复杂、费时,且得不到满意的复合效果[5]。本研究用纤维蛋白作为BMP载体,能定量地将BMP混合种植体中,可在术中即时进行,简便易行。纤维蛋白作为种植体的一种成份,可发挥以下功能:(1)限制术后微粒的早期移位;(2)促进纤维组织长入,有利于种植材料固位、成形和速硬,促进BMP在计划区域内发挥骨诱导作用;(3)作为BMP的载体,建立一个BMP浓度梯度,改善BMP与周围细胞的接触,增加BMP诱导的新骨量;(4)纤维蛋白粘合剂使种植材料易于成形,方便手术操作。3种材料组成一种功能互补的种植复合物,能使再造牙槽嵴获得较理想的效果。
, http://www.100md.com
以HA复合BMP再造牙槽嵴的目的是增加新骨形成。以HA复合其他骨诱导性物质也是同样的目的,Block等[6]实验表明:HA复合自体骨再造牙槽嵴术后12周,便观察到相互连结的新骨组织。用HA+脱矿骨,则12周只见少许的新骨形成,部份区域新骨连成片。26周才见相互连接的板状骨成片布满全层[7]。但与自体骨复合则必需自体取骨,而复合脱矿骨成骨较慢。本研究发现HA+BMP+FS复合材料再建牙槽嵴,所得结果与复合自体骨、脱矿骨相比,HA复合BMP免除了自体骨移植的缺点,新骨形成早,增加了新骨形成量,而且未发现局部异物反应。
多种方法较客观地显示BMP诱导的新骨组织与HA直接结合,新骨钙磷含量与HA和基骨相近。表明这些新骨组织与HA的结合完全可以构成一个骨性的再建牙槽嵴。
致密HA在体内不吸收,HA+BMP复合种植同时具有骨诱导和骨引导作用。本研究发现新骨形成主要自基骨界面开始,与这种双重作用有关。
, http://www.100md.com
[基金项目]:卫生部青年基金(93064)和广东省科委基金(97016)资助
[参 考 文 献]
[1] Meijer HJ, Steen WH, Bosman F, et al. Radiographic evaluation of mandibular augmentation with prefabricated hydroxylapatite/fibrin glue implants[J]. J Oral Maxillofac Surg, 1997, 55(2): 138~144.
[2] 杨连甲,金岩.骨形成蛋白(BMP)的实验研究[J].实用口腔医学杂志,1987, 3(2): 78~80.
[3] Sampath TK, Reddi AH. Homology of bone-inductive proteins from human, monkey, bovine, and rat extra-cellular matrix[J]. Proc Natl Acad Aci USA, 1983, 80(21): 6591~6595.
, 百拇医药
[4] Urist MR, Lietze A, Mizuatani H, et al. A bovine low molecular weight bone morphogenetic protein (BMP) fraction[J]. Clin Orthop, 1982, 162: 219~232.
[5] Sato T, Kawamura Ⅲ, Sato K, et al. Bone morphogenesis of rabbit bone morphogenetic protein-bound hydroxylapatite-fibrin composite[J]. Clin Othop, 1991, 263: 254~262.
[6] Block MS, Kent JN. Healing of mandibular ridge augmentations using hydroxylapatite with and without autogenous bone in dogs[J]. J Oral Maxillofac Surg, 1985, 43(1): 3~7.
[7] Block MS, Kent JN, Ardoin RC, et al. Mandibular augmentation in dogs with hydroxylapatite combined with demineralized bone[J]. J Oral Maxillofac Surg, 1987, 45(5): 412~420.
[收稿日期] 2000-01-10
[修回日期] 2000-04-12, http://www.100md.com