过氧亚硝基阴离子致大鼠肺微血管壁通透性增高的研究
作者:谷振勇 凌亦凌 丛斌 朱铁年
单位:(河北医科大学病理生理教研室, 河北 石家庄 050017)
关键词:一氧化氮;肺;内皮
中国病理生理杂志000718
[摘 要] 目的:探讨过氧亚硝基阴离子(ONOO-)对肺微血管内皮屏障功能的影响和在急性肺损伤发生中的意义。方法:向SD大鼠气管内推注不同浓度的ONOO-、分解 ONOO-或溶剂2 h后,检测肺微血管壁通透性变化和肺组织病理学变化,并检测ONOO-引起正常肺匀浆MDA含量变化。结果:ONOO-推入气管后,肺系数、肺湿干重比以及肺含水量和伊文思兰含量明显增高呈现剂量效应关系;并可导致肺泡明显萎陷、肺泡壁毛细血管明显扩张充血及局灶性出血,内皮细胞肿胀、核深染及脱落。ONOO-造成正常肺匀浆MDA含量增加。结论:外源性ONOO-气管推注后可导致明显的肺微血管内皮屏障功能障碍,提示肺内源性ONOO-生成增多时可能参与介导急性肺损伤的发生。
, 百拇医药
[中图分类号] R563 [文献标识码] A
[文章编号] 1000-4718(2000)07-0643-04
Study on peroxynitrite-induced increase in microvascular
permeability in rat lungs
GU Zhen-yong, LING Yi-ling, CONG Bin, ZHU Tie-nian
(Department of Pathophysiology, Hebei Medical University, Shijiazhuang 050017, China)
[Abstract] AIM: To explore the effect of peroxynitrite (ONOO-) on pulmonary microvascular endothelial barrier and roles of ONOO- in the pathogenesis of acute lung injury in vivo. METHODS: SD rats in different groups were insufflated with various concentrations of ONOO-, decomposed ONOO- or vehicle (alkaline normal saline), respectively. Then permeability changes in pulmonary microvascular walls were detected and the pathological alterations of pulmonary tissue were examined under light microscope. Malondialdehyde(MDA) contents were measured in normal lung homogenate pretreated with various concentration of ONOO-. RESULTS: Intratracheal insufflation of ONOO- resulted in dose-dependent increase in lung coefficient, lung wet/dry ratio, lung water contents and Evans blue contents, together with significant pulmonary pathological changes such as diffuse alveolar collapse, capillary congestion, focal hemorrhage, and endothelial swollen. In addition, ONOO- can also elicit increase in MDA contents in normal lung homogenate. CONCLUSION: ONOO- may induce dysfunctions of pulmonary microvascular endothelial barriers, it is suggested that enhanced endogenous ONOO- generation may take part in the pathogenesis of acute lung injury.
, 百拇医药
[MeSH] Nitric oxide; Lung; Endothelium
肺微血管壁通透性增高是内毒素引起急性肺损伤(acute lung injury, ALI)的特征性病理变化,其发生机理迄今尚未完全阐明。研究显示,肺内生成增多的一氧化氮(nitric oxide, NO)参与内毒素引起的ALI[1],NO的衍生物过氧亚硝基阴离子(peroxynitrite, ONOO-)介导了NO的细胞毒效应[2],而且ONOO-可能是导致机体氧化应激的新物质[2,3]。ONOO-可否引起ALI迄今尚无报道。本实验采用向大鼠气管内吹注入ONOO-的方法,观察ONOO-对肺微血管内皮屏障功能变化的影响,以探讨其在ALI发病中的意义。
材 料 和 方 法
, http://www.100md.com
一、 ONOO-的制备
采用淬灭流动反应方法合成[3]。0.6 mol/L HCl+0.7 mol/L H2O2与0.6 mol/L NaNO2经Y形玻璃管上口灌入混匀,1.5 mol/L NaOH由底部灌流,以淬灭前两种溶液的反应。3种溶液使用前4℃预冷,其灌流量与速度相同(30 mL,26 mL/min)。反应后溶液用MnO2 4 g处理1 min,以清除残存的微量H2O2,在负压下过滤后,置于-20℃过夜。上层析出分离的亮黄色溶液即为ONOO-储备液。采用
紫外色谱分析方法(ε 302=1 670 mol-1*cm-1,UV-2201型津岛紫外分光光度计)进行鉴定和浓度定量,证实在302 nm波长下呈吸收峰。另将部分ONOO-溶液置于100℃水中温育10 min,该吸收峰消失,表明ONOO-已彻底分解,此溶液降温后备用。
, http://www.100md.com
二、体内实验
(一)实验动物 SD大鼠40只,雌雄不拘,体重(172±9) g。实验前禁食18 h,自由饮水。由本校实验动物中心提供。
(二)实验程序 大鼠随机分组,0.2 mmol/L ONOO-组(n=8)、1.0 mmol/L ONOO-组(n=8)、2.5 mmol/L ONOO-组(n=8)、2.5 mmol/L分解的(dec)ONOO-组(n=7)和溶剂对照组(n=9)。ONOO-溶液于-20℃环境中保存,用生理盐水稀释。溶剂为与2.5 mmol/L ONOO-溶液酸碱度相同的碱化生理盐水。大鼠用2%戊巴比妥钠(02.mL/100 g ? b.w. ip)麻醉后,行颈部手术分离暴露气管。舌下静脉注入伊文思蓝(Evans blue, EB)30 mg/kg b.w.。5 min后,不同实验组动物在直视下往气管内分别推入ONOO-、dec ONOO-或溶剂200 μL。推入时动物取头高尾低位,推入后随即轻摇大鼠,以使药物均匀分布于两肺。2 h后剪断两侧颈动脉放血处死,联合取出心肺,剪开右心室以尽量放出肺血管内的残血。全肺湿重和肺组织干、湿重用分析天平(上海天平四厂)称重,肺组织湿重称量后,置肺组织于95℃烤箱至恒重;体重用一般天平称重,以麻醉后的重量为准。
, 百拇医药
(三)反映微血管壁通透性的指标 肺系数(lung coefficient, LC):全肺湿重(g)/体重(kg);肺湿干重比(W/D);肺含水量(%):用[(肺湿重-肺干重)/肺湿重]×100%计算;肺组织EB含量:精确称取肺组织适量,用甲酰胺(2 mL/100 mg湿肺)提取EB,1 000 r/min离心5 min,吸取上清液于620 nm波长下检测吸光度(722型分光光度计)。根据已知EB量溶液吸光度,计算回归方程。EB含量用ng/mg表示。
(四)肺组织学改变 各组另取大鼠3只,除不向静脉注射EB外,其余处理同前。大鼠处死后,剪取右肺中叶组织小块,10%缓冲福尔马林固定,常规制备石蜡切片,HE染色后,光镜下观察。
三、体外实验
(一)肺组织匀浆的制备 SD大鼠2只,麻醉后开胸取肺。分析天平称重后,两肺用预冷的1.15% KCl轻轻漂洗去除残血,用玻璃组织匀浆器制备10%肺组织匀浆(W/D)。
, http://www.100md.com
(二)分组及ONOO-预处理 将肺组织匀浆分为5组,ONOO- 50 μmol/L组(n=9)、ONOO- 200 μmol/L组(n=9)、ONOO- 500 μmol/L组(n=9)、dec ONOO- 500 μmol/L组(n=9)和溶剂对照组(n=9)。ONOO-剂量均为终浓度,容积约6 μL,溶剂为等量生理盐水。把ONOO-加至试管内匀浆上缘,迅速混匀。混合后匀浆pH=7.0,于室温下静置1 h,3 500 r/min离心20 min。
(三)丙二醛(malondialdehyde, MDA)含量检测 吸取上清液0.12 mL,用比色法检测肺组织匀浆脂质过氧化产物MDA含量(MDA试剂盒购于南京建成生物工程研究所)。
四、统计分析
, http://www.100md.com
数据均用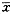 ±s表示。差异显著性检验用PSI统计软件包进行非配对t检验。
±s表示。差异显著性检验用PSI统计软件包进行非配对t检验。
结 果
一、 ONOO-引起肺微血管壁通透性的变化
表1显示, ONOO-可剂量依赖性引起大鼠肺系数、肺湿干重比、肺含水量和EB含量明显高于溶剂对照组和分解 ONOO-组。与0.2 mmol/L ONOO-组相比,2.5 mmol/L ONOO-组的肺系数、肺湿干重比和肺含水量也有明显增高(P<0.05或0.01),而肺EB含量未见显著变化。
表1 ONOO-对肺系数、肺湿干重比、肺含水量和伊文思蓝含量的影响
, http://www.100md.com
Tab 1 Effects of peroxynitrite insufflation on lung coefficient, lung W/D ratio, water and Evans blue contents(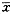 ±s) Group
±s) Group
n
LC
W/D ratio
Water contents
EB contents (ng/mg lung)
Vehicle control
9
, 百拇医药
4.94±0.26
4.30±0.27
76.69±1.51
280.26± 61.42
dec ONOO- 2.5 mmol/L
7
5.55±0.31
4.40±0.26
77.22±1.38
301.77± 15.95
ONOO- 0.2 mmol/L
, http://www.100md.com
8
6.18±0.43* *##
4.82±0.33* * #
79.16±1.43* *##
344.43± 51.16*
ONOO- 1.0 mmol/L
8
7.44±0.87* * ##
5.24±0.84* * #
, 百拇医药
80.56±2.57* * ##
390.98±109.02*#
ONOO- 2.5 mmol/L
8
7.48±0.77* * ##
5.20±0.07* * ##
80.77±0.38* * ##
413.80±81.79* * #
* P<0.05, * * P<0.01, * * P<0.001,vs vehicle group; # P<0.05, ## P<0.01, vs dec ONOO- group
, 百拇医药
二、肺组织的病理变化
溶剂对照组肺泡腔大,肺泡壁薄,毛细血管轻度淤血,接近正常肺组织。分解ONOO-组有轻度肺泡萎陷。ONOO- 0.2 mmol/L组肺泡腔变小,肺泡壁略增厚,间质毛细血管充血,有局灶性出血。ONOO- 1.0 mmol/L和ONOO- 2.5 mmol/L组肺组织弥漫性萎陷,肺泡腔明显窄小,丧失了环形结构,有处实变,肺泡壁增厚,出现褶皱;毛细血管明显扩张淤血伴少量局灶性出血,内皮细胞肿胀、核深染;细支气管粘膜上皮变性脱落。上述变化以2.5 mmol/L组为著。
三、肺组织MDA含量变化
表2 ONOO-引起肺组织匀浆MDA含量的变化
Tab 2 Changes of MDA contents induced by peroxynitrite
, http://www.100md.com
in lung homogenate(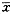 ±s,n=9) Group
±s,n=9) Group
MDA (nmol/mL)
Vehicle control
117.49±21.04
dec ONOO- 500 μmol/L
123.11±13.34
ONOO- 50 μmol/L
128.52±12.42
ONOO- 200 μmol/L
, 百拇医药
131.82± 9.02
ONOO- 500 μmol/L
140.28± 6.81*
* P<0.05, vs vehicle, dec ONOO- 500 μmol/L and ONOO- 50 μmol/L groups
表2显示,50 μmol/L和200 μmol/L ONOO-可导致肺组织MDA含量增高(P>0.05), 500 μmol/L ONOO-引起MDA显著升高。讨 论
ONOO-是NO与超氧阴离子(superoxide,O-2)的快速反应产物[3],该反应速度接近弥散的速率极限,是超氧化物歧化酶歧化O2速度的3倍,而比NO与血红素蛋白结合的速度快数百倍。与NO或NO2相比,ONOO-具有更强的氧化性,并能很快衍生多种其它的氧化剂或硝基化因子。因此,在NO与O2同时生成增多的病理过程中,ONOO-可能是导致损伤的关键物质。Haddad等[4]报道,大鼠吸入纯氧6h后和儿童肺炎尸检病例的肺脏发现有ONOO-生成。最近我们采用免疫组化方法也检测到,内毒素休克大鼠的肺脏有ONOO-形成的标志物。然而,由于目前尚未发现或研制出ONOO-的特异性清除剂,这不利于确切评估内源性ONOO-在ALI发生中的意义。本实验首次观察了ONOO-对肺脏微血管壁通透性变化的影响。结果显示,气管推注不同浓度的ONOO- 2 h后,大鼠肺系数、肺湿干重比、肺含水量和EB含量明显增高,并呈现出量效关系。这与ONOO-皮下注射诱导[125I]-白蛋白渗出增多以及直肠腔内注射ONOO-导致肠粘膜肿胀的情况一致[5,6]。而气管推注分解的ONOO-后,上述指标仅轻微增高,与溶剂组无明显差异。表明ONOO-溶液的其它成分对肺微血管壁通透性影响不大,证实气管推注ONOO-确实可以造成肺微血管壁通透性增高。
, 百拇医药
ONOO-的作用机制可能与其干扰了肺泡呼吸膜不同成分的功能有关。①ONOO-可能损伤肺毛细血管内皮功能。ONOO-具有跨膜弥散能力[7],当吸入肺泡后可透过肺泡壁至血管内皮,并引起氧化损伤。ONOO-可致肺匀浆MDA含量增高为此观点提供间接依据,而肺间质小血管明显扩张充血可能恰恰是对ONOO-损伤作用的反应。②ONOO-干扰肺泡上皮能量代谢、灭活钠通道[8],破坏肺泡表面活性物质[9],妨碍它们对肺泡水含量的调节作用,从而促进肺微血管壁通透性增加。ONOO-引起弥漫性肺泡萎陷支持这一认识。
[基金项目] 国家自然科学基金资助 (No. 39870317)
Tel: 0311-6044121转5645或5602
, 百拇医药
[参 考 文 献]
[1] 万 梅,凌亦凌,谷振勇,等. 内源性一氧化氮在内毒素引起肺动脉高压及肺损伤中的作用[J]. 生理学报, 1999, 51(1):80~86.
[2] 谷振勇,凌亦凌,黄善生. NO: ONOO- ……,氧化应激的新通路[J]. 国外医学创伤与外科基本问题分册, 1999, 20(2):83~86.
[3] Beckman JS, Beckman TW, Chen J, et al. Apparent hydroxyl radical production by peroxynitrite: implication for endothelial injury from nitric oxide and superoxide[J]. Proc Natl Acad Sci USA, 1990, 87:1820~1824.
, http://www.100md.com
[4] Haddad IY, Pataki G, Hu P, et al. Quantitation of nitrotyrosine levels in lung sections of patients and animal with acute lung injury[J]. J Clin Invest, 1994, 94:2407~2413.
[5] Ridger VC, Greenacre SAB, Handy RIC, et al. Effect of peroxynitrite on plasma extravasation, microvascular blood flow and nociception in the rat[J]. Br J Pharmacol, 1997, 122:1083~1088.
[6] Rachmilewitz D, Stamler JS, Karmeli F, et al. Peroxynitrite-induced rat colitise—a new model of colonic inflammation[J]. Gastroenterology, 1993, 105:1681~1688.
, 百拇医药
[7] Denicola A, Souza JM, Radi R. Diffusion of peroxynitrite across erythrocyte membrane[J]. Proc Natl Acad Sci USA, 1998, 95:3566~3571.
[8] Haddad IY, Ischiropoulos H, Holm BA, et al. Mechanism of peroxynitrite-induced injury to pulmonary surfactants[J]. Am J Physiol, 1993, 265:L555~L564.
[9] Hu P, Ischiropoulos H, Beckman JS, et al. Peroxynitrite inhibition of oxygen consumption and sodium transport in alveolar Ⅱ type cells[J]. Am J Physiol, 1994, 266:L628~L634.
[收稿日期] 1999-05-10
[修回日期] 1999-10-18, 百拇医药
单位:(河北医科大学病理生理教研室, 河北 石家庄 050017)
关键词:一氧化氮;肺;内皮
中国病理生理杂志000718
[摘 要] 目的:探讨过氧亚硝基阴离子(ONOO-)对肺微血管内皮屏障功能的影响和在急性肺损伤发生中的意义。方法:向SD大鼠气管内推注不同浓度的ONOO-、分解 ONOO-或溶剂2 h后,检测肺微血管壁通透性变化和肺组织病理学变化,并检测ONOO-引起正常肺匀浆MDA含量变化。结果:ONOO-推入气管后,肺系数、肺湿干重比以及肺含水量和伊文思兰含量明显增高呈现剂量效应关系;并可导致肺泡明显萎陷、肺泡壁毛细血管明显扩张充血及局灶性出血,内皮细胞肿胀、核深染及脱落。ONOO-造成正常肺匀浆MDA含量增加。结论:外源性ONOO-气管推注后可导致明显的肺微血管内皮屏障功能障碍,提示肺内源性ONOO-生成增多时可能参与介导急性肺损伤的发生。
, 百拇医药
[中图分类号] R563 [文献标识码] A
[文章编号] 1000-4718(2000)07-0643-04
Study on peroxynitrite-induced increase in microvascular
permeability in rat lungs
GU Zhen-yong, LING Yi-ling, CONG Bin, ZHU Tie-nian
(Department of Pathophysiology, Hebei Medical University, Shijiazhuang 050017, China)
[Abstract] AIM: To explore the effect of peroxynitrite (ONOO-) on pulmonary microvascular endothelial barrier and roles of ONOO- in the pathogenesis of acute lung injury in vivo. METHODS: SD rats in different groups were insufflated with various concentrations of ONOO-, decomposed ONOO- or vehicle (alkaline normal saline), respectively. Then permeability changes in pulmonary microvascular walls were detected and the pathological alterations of pulmonary tissue were examined under light microscope. Malondialdehyde(MDA) contents were measured in normal lung homogenate pretreated with various concentration of ONOO-. RESULTS: Intratracheal insufflation of ONOO- resulted in dose-dependent increase in lung coefficient, lung wet/dry ratio, lung water contents and Evans blue contents, together with significant pulmonary pathological changes such as diffuse alveolar collapse, capillary congestion, focal hemorrhage, and endothelial swollen. In addition, ONOO- can also elicit increase in MDA contents in normal lung homogenate. CONCLUSION: ONOO- may induce dysfunctions of pulmonary microvascular endothelial barriers, it is suggested that enhanced endogenous ONOO- generation may take part in the pathogenesis of acute lung injury.
, 百拇医药
[MeSH] Nitric oxide; Lung; Endothelium
肺微血管壁通透性增高是内毒素引起急性肺损伤(acute lung injury, ALI)的特征性病理变化,其发生机理迄今尚未完全阐明。研究显示,肺内生成增多的一氧化氮(nitric oxide, NO)参与内毒素引起的ALI[1],NO的衍生物过氧亚硝基阴离子(peroxynitrite, ONOO-)介导了NO的细胞毒效应[2],而且ONOO-可能是导致机体氧化应激的新物质[2,3]。ONOO-可否引起ALI迄今尚无报道。本实验采用向大鼠气管内吹注入ONOO-的方法,观察ONOO-对肺微血管内皮屏障功能变化的影响,以探讨其在ALI发病中的意义。
材 料 和 方 法
, http://www.100md.com
一、 ONOO-的制备
采用淬灭流动反应方法合成[3]。0.6 mol/L HCl+0.7 mol/L H2O2与0.6 mol/L NaNO2经Y形玻璃管上口灌入混匀,1.5 mol/L NaOH由底部灌流,以淬灭前两种溶液的反应。3种溶液使用前4℃预冷,其灌流量与速度相同(30 mL,26 mL/min)。反应后溶液用MnO2 4 g处理1 min,以清除残存的微量H2O2,在负压下过滤后,置于-20℃过夜。上层析出分离的亮黄色溶液即为ONOO-储备液。采用
紫外色谱分析方法(ε 302=1 670 mol-1*cm-1,UV-2201型津岛紫外分光光度计)进行鉴定和浓度定量,证实在302 nm波长下呈吸收峰。另将部分ONOO-溶液置于100℃水中温育10 min,该吸收峰消失,表明ONOO-已彻底分解,此溶液降温后备用。
, http://www.100md.com
二、体内实验
(一)实验动物 SD大鼠40只,雌雄不拘,体重(172±9) g。实验前禁食18 h,自由饮水。由本校实验动物中心提供。
(二)实验程序 大鼠随机分组,0.2 mmol/L ONOO-组(n=8)、1.0 mmol/L ONOO-组(n=8)、2.5 mmol/L ONOO-组(n=8)、2.5 mmol/L分解的(dec)ONOO-组(n=7)和溶剂对照组(n=9)。ONOO-溶液于-20℃环境中保存,用生理盐水稀释。溶剂为与2.5 mmol/L ONOO-溶液酸碱度相同的碱化生理盐水。大鼠用2%戊巴比妥钠(02.mL/100 g ? b.w. ip)麻醉后,行颈部手术分离暴露气管。舌下静脉注入伊文思蓝(Evans blue, EB)30 mg/kg b.w.。5 min后,不同实验组动物在直视下往气管内分别推入ONOO-、dec ONOO-或溶剂200 μL。推入时动物取头高尾低位,推入后随即轻摇大鼠,以使药物均匀分布于两肺。2 h后剪断两侧颈动脉放血处死,联合取出心肺,剪开右心室以尽量放出肺血管内的残血。全肺湿重和肺组织干、湿重用分析天平(上海天平四厂)称重,肺组织湿重称量后,置肺组织于95℃烤箱至恒重;体重用一般天平称重,以麻醉后的重量为准。
, 百拇医药
(三)反映微血管壁通透性的指标 肺系数(lung coefficient, LC):全肺湿重(g)/体重(kg);肺湿干重比(W/D);肺含水量(%):用[(肺湿重-肺干重)/肺湿重]×100%计算;肺组织EB含量:精确称取肺组织适量,用甲酰胺(2 mL/100 mg湿肺)提取EB,1 000 r/min离心5 min,吸取上清液于620 nm波长下检测吸光度(722型分光光度计)。根据已知EB量溶液吸光度,计算回归方程。EB含量用ng/mg表示。
(四)肺组织学改变 各组另取大鼠3只,除不向静脉注射EB外,其余处理同前。大鼠处死后,剪取右肺中叶组织小块,10%缓冲福尔马林固定,常规制备石蜡切片,HE染色后,光镜下观察。
三、体外实验
(一)肺组织匀浆的制备 SD大鼠2只,麻醉后开胸取肺。分析天平称重后,两肺用预冷的1.15% KCl轻轻漂洗去除残血,用玻璃组织匀浆器制备10%肺组织匀浆(W/D)。
, http://www.100md.com
(二)分组及ONOO-预处理 将肺组织匀浆分为5组,ONOO- 50 μmol/L组(n=9)、ONOO- 200 μmol/L组(n=9)、ONOO- 500 μmol/L组(n=9)、dec ONOO- 500 μmol/L组(n=9)和溶剂对照组(n=9)。ONOO-剂量均为终浓度,容积约6 μL,溶剂为等量生理盐水。把ONOO-加至试管内匀浆上缘,迅速混匀。混合后匀浆pH=7.0,于室温下静置1 h,3 500 r/min离心20 min。
(三)丙二醛(malondialdehyde, MDA)含量检测 吸取上清液0.12 mL,用比色法检测肺组织匀浆脂质过氧化产物MDA含量(MDA试剂盒购于南京建成生物工程研究所)。
四、统计分析
, http://www.100md.com
数据均用
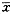 ±s表示。差异显著性检验用PSI统计软件包进行非配对t检验。
±s表示。差异显著性检验用PSI统计软件包进行非配对t检验。结 果
一、 ONOO-引起肺微血管壁通透性的变化
表1显示, ONOO-可剂量依赖性引起大鼠肺系数、肺湿干重比、肺含水量和EB含量明显高于溶剂对照组和分解 ONOO-组。与0.2 mmol/L ONOO-组相比,2.5 mmol/L ONOO-组的肺系数、肺湿干重比和肺含水量也有明显增高(P<0.05或0.01),而肺EB含量未见显著变化。
表1 ONOO-对肺系数、肺湿干重比、肺含水量和伊文思蓝含量的影响
, http://www.100md.com
Tab 1 Effects of peroxynitrite insufflation on lung coefficient, lung W/D ratio, water and Evans blue contents(
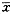 ±s) Group
±s) Groupn
LC
W/D ratio
Water contents
EB contents (ng/mg lung)
Vehicle control
9
, 百拇医药
4.94±0.26
4.30±0.27
76.69±1.51
280.26± 61.42
dec ONOO- 2.5 mmol/L
7
5.55±0.31
4.40±0.26
77.22±1.38
301.77± 15.95
ONOO- 0.2 mmol/L
, http://www.100md.com
8
6.18±0.43* *##
4.82±0.33* * #
79.16±1.43* *##
344.43± 51.16*
ONOO- 1.0 mmol/L
8
7.44±0.87* * ##
5.24±0.84* * #
, 百拇医药
80.56±2.57* * ##
390.98±109.02*#
ONOO- 2.5 mmol/L
8
7.48±0.77* * ##
5.20±0.07* * ##
80.77±0.38* * ##
413.80±81.79* * #
* P<0.05, * * P<0.01, * * P<0.001,vs vehicle group; # P<0.05, ## P<0.01, vs dec ONOO- group
, 百拇医药
二、肺组织的病理变化
溶剂对照组肺泡腔大,肺泡壁薄,毛细血管轻度淤血,接近正常肺组织。分解ONOO-组有轻度肺泡萎陷。ONOO- 0.2 mmol/L组肺泡腔变小,肺泡壁略增厚,间质毛细血管充血,有局灶性出血。ONOO- 1.0 mmol/L和ONOO- 2.5 mmol/L组肺组织弥漫性萎陷,肺泡腔明显窄小,丧失了环形结构,有处实变,肺泡壁增厚,出现褶皱;毛细血管明显扩张淤血伴少量局灶性出血,内皮细胞肿胀、核深染;细支气管粘膜上皮变性脱落。上述变化以2.5 mmol/L组为著。
三、肺组织MDA含量变化
表2 ONOO-引起肺组织匀浆MDA含量的变化
Tab 2 Changes of MDA contents induced by peroxynitrite
, http://www.100md.com
in lung homogenate(
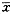 ±s,n=9) Group
±s,n=9) GroupMDA (nmol/mL)
Vehicle control
117.49±21.04
dec ONOO- 500 μmol/L
123.11±13.34
ONOO- 50 μmol/L
128.52±12.42
ONOO- 200 μmol/L
, 百拇医药
131.82± 9.02
ONOO- 500 μmol/L
140.28± 6.81*
* P<0.05, vs vehicle, dec ONOO- 500 μmol/L and ONOO- 50 μmol/L groups
表2显示,50 μmol/L和200 μmol/L ONOO-可导致肺组织MDA含量增高(P>0.05), 500 μmol/L ONOO-引起MDA显著升高。讨 论
ONOO-是NO与超氧阴离子(superoxide,O-2)的快速反应产物[3],该反应速度接近弥散的速率极限,是超氧化物歧化酶歧化O2速度的3倍,而比NO与血红素蛋白结合的速度快数百倍。与NO或NO2相比,ONOO-具有更强的氧化性,并能很快衍生多种其它的氧化剂或硝基化因子。因此,在NO与O2同时生成增多的病理过程中,ONOO-可能是导致损伤的关键物质。Haddad等[4]报道,大鼠吸入纯氧6h后和儿童肺炎尸检病例的肺脏发现有ONOO-生成。最近我们采用免疫组化方法也检测到,内毒素休克大鼠的肺脏有ONOO-形成的标志物。然而,由于目前尚未发现或研制出ONOO-的特异性清除剂,这不利于确切评估内源性ONOO-在ALI发生中的意义。本实验首次观察了ONOO-对肺脏微血管壁通透性变化的影响。结果显示,气管推注不同浓度的ONOO- 2 h后,大鼠肺系数、肺湿干重比、肺含水量和EB含量明显增高,并呈现出量效关系。这与ONOO-皮下注射诱导[125I]-白蛋白渗出增多以及直肠腔内注射ONOO-导致肠粘膜肿胀的情况一致[5,6]。而气管推注分解的ONOO-后,上述指标仅轻微增高,与溶剂组无明显差异。表明ONOO-溶液的其它成分对肺微血管壁通透性影响不大,证实气管推注ONOO-确实可以造成肺微血管壁通透性增高。
, 百拇医药
ONOO-的作用机制可能与其干扰了肺泡呼吸膜不同成分的功能有关。①ONOO-可能损伤肺毛细血管内皮功能。ONOO-具有跨膜弥散能力[7],当吸入肺泡后可透过肺泡壁至血管内皮,并引起氧化损伤。ONOO-可致肺匀浆MDA含量增高为此观点提供间接依据,而肺间质小血管明显扩张充血可能恰恰是对ONOO-损伤作用的反应。②ONOO-干扰肺泡上皮能量代谢、灭活钠通道[8],破坏肺泡表面活性物质[9],妨碍它们对肺泡水含量的调节作用,从而促进肺微血管壁通透性增加。ONOO-引起弥漫性肺泡萎陷支持这一认识。
[基金项目] 国家自然科学基金资助 (No. 39870317)
Tel: 0311-6044121转5645或5602
, 百拇医药
[参 考 文 献]
[1] 万 梅,凌亦凌,谷振勇,等. 内源性一氧化氮在内毒素引起肺动脉高压及肺损伤中的作用[J]. 生理学报, 1999, 51(1):80~86.
[2] 谷振勇,凌亦凌,黄善生. NO: ONOO- ……,氧化应激的新通路[J]. 国外医学创伤与外科基本问题分册, 1999, 20(2):83~86.
[3] Beckman JS, Beckman TW, Chen J, et al. Apparent hydroxyl radical production by peroxynitrite: implication for endothelial injury from nitric oxide and superoxide[J]. Proc Natl Acad Sci USA, 1990, 87:1820~1824.
, http://www.100md.com
[4] Haddad IY, Pataki G, Hu P, et al. Quantitation of nitrotyrosine levels in lung sections of patients and animal with acute lung injury[J]. J Clin Invest, 1994, 94:2407~2413.
[5] Ridger VC, Greenacre SAB, Handy RIC, et al. Effect of peroxynitrite on plasma extravasation, microvascular blood flow and nociception in the rat[J]. Br J Pharmacol, 1997, 122:1083~1088.
[6] Rachmilewitz D, Stamler JS, Karmeli F, et al. Peroxynitrite-induced rat colitise—a new model of colonic inflammation[J]. Gastroenterology, 1993, 105:1681~1688.
, 百拇医药
[7] Denicola A, Souza JM, Radi R. Diffusion of peroxynitrite across erythrocyte membrane[J]. Proc Natl Acad Sci USA, 1998, 95:3566~3571.
[8] Haddad IY, Ischiropoulos H, Holm BA, et al. Mechanism of peroxynitrite-induced injury to pulmonary surfactants[J]. Am J Physiol, 1993, 265:L555~L564.
[9] Hu P, Ischiropoulos H, Beckman JS, et al. Peroxynitrite inhibition of oxygen consumption and sodium transport in alveolar Ⅱ type cells[J]. Am J Physiol, 1994, 266:L628~L634.
[收稿日期] 1999-05-10
[修回日期] 1999-10-18, 百拇医药