大鼠拟“血管性痴呆”模型的改进
作者:王蕊 杨秦飞 唐一鹏 房良敏 胡京红 贾绪东 洪庆涛
单位:王蕊 杨秦飞 房良敏(北京中医药大学中西医结合研究所 生理室);唐一鹏 胡京红 贾绪东 洪庆涛(病理室, 北京 100029)
关键词:脑缺血;暂时性;大鼠;痴呆;血管性
中国病理生理杂志001012
[中图分类号] R743.31 [文献标识码] A
[文章编号] 1000-4718(2000)10-0914-03
[MeSH] Cerebral ischemia, transient; Rats; Dementia, vascular
随着社会进入老龄化,作为老年病的脑血管病,已成为人类三大死亡原因之一。近年来由于医疗水平的提高和防治知识的深入,脑血管病死亡率有所下降,而脑血管病造成的各种功能和智力障碍却有增高的趋势。血管性痴呆的防治日益受到人们的关注。目前虽建立了数种脑缺血动物模型,但脑缺血晚期学习记忆功能障碍的动物模型较少并不够完善,在一定程度上影响了对其机理及治疗的研究。本工作在前人实验的基础上加以改进,建立了一种拟“血管性痴呆”的动物模型,为研究脑缺血后学习、记忆功能障碍的发生机理及防治提供实验基础。
, http://www.100md.com
材 料 和 方 法
一、模型的复制
成年Wistar雄性大鼠,体重200-250 g,由本校实验动物室提供。18只动物随机分为假手术对照组(n=9)及脑缺血模型组(n=9)。将大鼠用10%的水合氯醛(350 mg/kg, i.p)麻醉后,仰卧固定在手术台上,常规消毒,颈正中切口,分离双侧颈总动脉(common carotid arteries, CCA),模型组在夹闭双侧CCA之前,腹腔注射硝普钠(sodium nitroprusside, 北京制药工业研究所实验药厂;2.5 mg/kg, 用无菌蒸馏水溶解),随即用无创动脉夹夹闭双侧CCA,10 min后,再通10 min,再夹闭10 min(I10-R10-I10),再通后缝合伤口,放回笼中保温饲养。假手术组麻醉及手术过程与模型组相同,但不阻断CCA及注射硝普钠。在全部造模过程中保持动物直肠温度在37℃左右,以防止低温对脑缺血损伤的保护作用。
, 百拇医药
二、行为学测试
(一)跳台实验(step-down avoidance test) 跳台实验装置为被动回避反应箱,底板设有铜栅,可通交流电,电压40V。铜栅的一角放置一个橡胶圆台作为安全区,动物可停留在圆台上回避电击。造模后第7 d开始进行学习训练。训练前先将动物放入箱中自由活动3 min,熟悉环境,然后接通铜栅电源,持续5 min,记录动物首次找到安全区所需时间(潜伏期,latency),错误次数(动物跳下圆台次数,number of error)及受电击总时间(潜伏期与错误时间之和,the sum of latency and error time),作为学习测试成绩。24 h后重复上述实验,作为记忆测试成绩。
(二)水迷宫试验(water maze test) 水迷宫试验装置为一约1 m见方的棕色有机玻璃槽,槽的一端有一阶梯,动物可顺其爬上。槽内为迷宫状,有多处盲端,只有一条通路可到达阶梯。实验时,槽内充水,水深20 cm,水温(25±2)℃,动物不能看到阶梯。造模后7 d,训练4次,训练时如大鼠进入盲端,则将其诱入路径。第5次记录其游完全程的时间(swimming time),进入盲端的次数(number of error)及进入盲端的时间(error time)作为学习成绩。若在3 min时仍未找到阶梯,则定为不能完成学习训练,即有明显的学习能力低下。24 h后重复测试上述指标作为记忆成绩。
, http://www.100md.com
三、形态学观察
行为学测试完成后,在10%的水合氯醛(350 mg/kg,i.p)麻醉下,断头处死动物,取脑组织浸入10%福尔马林溶液内固定,取视交叉后4 mm处至小脑前的脑组织,常规石蜡包埋、切片,HE、Nissl染色,光镜观察海马细胞形态变化。细胞计数方法计数1 mm长度(×50)海马CA1区中段正常细胞数,取双侧海马细胞计数的均值。
四、统计学处理
采用t检验判断均数差异显著性。数据用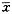 ±s表示。
±s表示。
结 果
一、行为学实验
脑缺血再灌注后,大鼠发生了明显的学习记忆障碍,表现为:跳台实验记忆成绩中,模型组之潜伏期、受电击总时间明显长于假手术对照组,错误次数较多。统计学上有显著性差异,P<0.05,P<0.01。水迷宫实验中,学习及记忆成绩,模型组大鼠游完全程时间、进入盲端次数及时间均明显高于假手术组,P<0.05(见表1,2)。
, 百拇医药
表1 各组大鼠跳台实验的学习和记忆成绩比较
Tab 1 The results of rats' learning and memory in step-down avoidance test (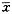 ±s. n=9)
±s. n=9)
Learning
Memory
Latency
(min)
Number of
error (time)
The sum of latency
, http://www.100md.com
and time of error
(min)
Latency
(min)
Number of
error (time)
The sum of latency
and time of error
(min)
Sham-operated
0.57±0.60
, 百拇医药
1.56±1.67
0.89±0.72
0.50±0.69
0.67±1.66
0.56±0.68
Postischemia
1.13±0.60
2.56±2.51
1.54±0.88
1.75±1.94#
3.44±4.13#
, http://www.100md.com
2.04±1.79##
# P<0.05,##P<0.01 vs sham-operated.表2 各组大鼠水迷宫实验的学习和记忆成绩比较
Tab 2 The results of rats' learning and memory in in water maze test (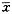 ±s. n=9)
±s. n=9)
Learning
Memory
Swimming
time (min)
, http://www.100md.com
Number of
error (time)
Time of
error(min)
Swimming
time (min)
Number of
error (time)
Time of
error(min)
Sham-operated
, 百拇医药 0.41±0.17
1.33±0.87
0.10±0.08
0.23±0.16
0.44±0.73
0.01±0.02
Postischemia
3.68±1.64#
4.33±1.58#
1.93±1.38#
2.76±1.04#
, http://www.100md.com
4.56±1.51#
1.37±0.84#
# P<0.05 vs sham-operated.
二、形态学观察
低倍镜下,假手术组大鼠海马锥体细胞层结构紧密,层次丰富。模型组CA1、CA4区细胞排列稀疏,细胞线变得不清晰,尤以CA1区明显(图1,2)。
Fig 1 Region of hippocampal CA1 that exhibits clear line and rich layer of pyramidal cell.
, 百拇医药
Sham-operated control, Nissl stain×150.
图1 假手术组海马CA1区,锥体细胞排列紧密,层次丰富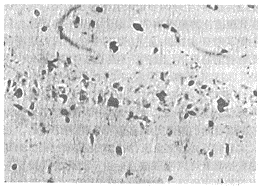
Fig 2 Region of hippocampal CA1 that exhibits unclear pyramidal cell line and notable loss of neurons.
Ischemia injury, Nissl stain×150.
图2 模型组海马CA1区,细胞线模糊, 锥体细胞缺失
高倍镜下,假手术组锥体细胞核大,染色浅,细胞质丰富,细胞排列紧密,Nissl染色显示胞浆内尼氏体丰富。模型组CA1区形态正常的细胞数明显较少,许多细胞结构变得不完整,细胞周围出现间隙,细胞核固缩,有的形成碎片。尼氏体染色细胞质内尼氏体少,CA4区亦有细胞排列稀疏及形态异常,但远不如CA1区明显。
, 百拇医药
表3 短暂脑缺血后海马CA1区细胞计数的变化
Tab 3 Changes of the number of neurons in CA1 region after
transient global ischemia (cells/mm.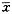 ±s. n=4) Group
±s. n=4) Group
Number of neuron
Sham-operated control
146.25±18.45
Postischemia
67.00±27.99*
, 百拇医药
*P<0.05 vs sham-operated.
由表3可见,模型组海马CA1区细胞数明显少于假手术组,差异有高度显著性,表明海马CA1区有明显的细胞缺失。
讨 论
目前被常用于研究血管性痴呆的动物模型主要有四血管阻断(4VO)[1]和两血管阻断(2VO)模型[2,3]。有报道称,较严重的不完全性脑缺血动物的脑损伤较相同时间完全脑缺血的动物恢复差[4]。贾健民等采用4VO制造全脑反复缺血再灌模型,认为其可作为“血管性痴呆”模型使用[5]。我们对上述方法进行了改良,采用大鼠双侧颈总动脉反复夹闭并再通,同时腹腔注射硝普钠降低血压的方法复制模型。硝普钠的剂量用急性颈总动脉插管接压力传感器,生理四导记录监测血压确定。我们观察到腹腔注射硝普钠(2.5 mg/kg)后平均动脉血压立即下降至6.7 kPa左右,然后在30 min内逐渐回到给药前的水平。给硝普钠后血压一般不低于5.3 kPa。随着给药剂量的增加,其血压恢复的时间亦延长,稳定性较好,超过5 mg/kg,血压下降将不易恢复,造成动物死亡。因此在一定程度上可以通过控制硝普钠的剂量达到控制降压时间的目的。正式实验时不必监测血压,从而简化实验过程。采用硝普钠降压可以克服放血后由于机体的代偿反应引起的血压回升。跳台和水迷宫试验发现,手术后7 d模型组大鼠出现了明显的学习记忆功能障碍,空间定位、识别能力损伤较为严重。形态学观察可见明显的CA1区锥体细胞的变性、死亡、甚至丢失,而CA3区神经元无明显异常,这一变化印证了行为学的结果。而且动物没有明显的运动系统损伤表现,存活率较高。可重复性、稳定性较好,其优点为手术操作简单,对动物创伤较小,易于恢复,尤其是以学习记忆能力低下为主等特点,与临床“血管性痴呆”的发病过程相似,笔者认为可作为拟“血管性痴呆”的动物模型使用,适用于研究血管性痴呆的病理生理机制和评价药物的作用。由于造模时间较短,尤其适用于大批实验。值得注意的是:(1)在阻断双侧CCA的过程中,血压的变化对损伤程度影响较大,本模型是通过腹腔注射硝普钠降压的,因此,剂量的准确和注射的可靠性就显得十分重要,若剂量不准或药物未注射入腹腔,均会对血压造成影响进而影响造模的效果。(2)硝普钠的降压原理是直接扩张外周血管,而环境温度对外周血管的舒缩状态影响很大,因此环境温度变化较大时,应适当调整药物的剂量。
, 百拇医药
[基金项目] 国家九五攻关课题资助(No. 96-906-09-03)
参 考 文 献
[1] Pulsinelli WA, Brierley JB. A new model of bilateral hemispheric ischemia in the unanesthetized rat[J]. Stroke, 1979, 10(3): 267-272.
[2] Nordstrom CH, Siesjo BK. Effects of phenobarbital in cerebral ischemia. Prat I: Cerebral energy metabolism during incomplete ischemia[J]. Stroke, 1978, 9:327-335.
[3] Smith ML, Bendek G, Dahlgren N, et al. Models for studying long-term recovery following forebrain ischemia in the rat. 2.A2-vessel occlusion model[J]. Acta Neurol Scand, 1984, 69: 385-401.
, 百拇医药
[4] 李 巍, 严徽瑾. 脑缺血性学习记忆障碍模型[M].见:方福德, 周 吕, 丁 濂, 等. 主编. 现代医学实验技巧全书(下册). 第1版. 北京:北京医科大学协和医科大学联合出版社,1995. 248-251.
[5] 贾健民,贾健平,张 昱,等. Wistar Rat全脑反复缺血再灌流动物模型及行为学研究[J]. 中风与神经疾病杂志, 1992, 9(2):71-73.
[收稿日期]1999-07-23
[修回日期]2000-05-23
, http://www.100md.com
单位:王蕊 杨秦飞 房良敏(北京中医药大学中西医结合研究所 生理室);唐一鹏 胡京红 贾绪东 洪庆涛(病理室, 北京 100029)
关键词:脑缺血;暂时性;大鼠;痴呆;血管性
中国病理生理杂志001012
[中图分类号] R743.31 [文献标识码] A
[文章编号] 1000-4718(2000)10-0914-03
[MeSH] Cerebral ischemia, transient; Rats; Dementia, vascular
随着社会进入老龄化,作为老年病的脑血管病,已成为人类三大死亡原因之一。近年来由于医疗水平的提高和防治知识的深入,脑血管病死亡率有所下降,而脑血管病造成的各种功能和智力障碍却有增高的趋势。血管性痴呆的防治日益受到人们的关注。目前虽建立了数种脑缺血动物模型,但脑缺血晚期学习记忆功能障碍的动物模型较少并不够完善,在一定程度上影响了对其机理及治疗的研究。本工作在前人实验的基础上加以改进,建立了一种拟“血管性痴呆”的动物模型,为研究脑缺血后学习、记忆功能障碍的发生机理及防治提供实验基础。
, http://www.100md.com
材 料 和 方 法
一、模型的复制
成年Wistar雄性大鼠,体重200-250 g,由本校实验动物室提供。18只动物随机分为假手术对照组(n=9)及脑缺血模型组(n=9)。将大鼠用10%的水合氯醛(350 mg/kg, i.p)麻醉后,仰卧固定在手术台上,常规消毒,颈正中切口,分离双侧颈总动脉(common carotid arteries, CCA),模型组在夹闭双侧CCA之前,腹腔注射硝普钠(sodium nitroprusside, 北京制药工业研究所实验药厂;2.5 mg/kg, 用无菌蒸馏水溶解),随即用无创动脉夹夹闭双侧CCA,10 min后,再通10 min,再夹闭10 min(I10-R10-I10),再通后缝合伤口,放回笼中保温饲养。假手术组麻醉及手术过程与模型组相同,但不阻断CCA及注射硝普钠。在全部造模过程中保持动物直肠温度在37℃左右,以防止低温对脑缺血损伤的保护作用。
, 百拇医药
二、行为学测试
(一)跳台实验(step-down avoidance test) 跳台实验装置为被动回避反应箱,底板设有铜栅,可通交流电,电压40V。铜栅的一角放置一个橡胶圆台作为安全区,动物可停留在圆台上回避电击。造模后第7 d开始进行学习训练。训练前先将动物放入箱中自由活动3 min,熟悉环境,然后接通铜栅电源,持续5 min,记录动物首次找到安全区所需时间(潜伏期,latency),错误次数(动物跳下圆台次数,number of error)及受电击总时间(潜伏期与错误时间之和,the sum of latency and error time),作为学习测试成绩。24 h后重复上述实验,作为记忆测试成绩。
(二)水迷宫试验(water maze test) 水迷宫试验装置为一约1 m见方的棕色有机玻璃槽,槽的一端有一阶梯,动物可顺其爬上。槽内为迷宫状,有多处盲端,只有一条通路可到达阶梯。实验时,槽内充水,水深20 cm,水温(25±2)℃,动物不能看到阶梯。造模后7 d,训练4次,训练时如大鼠进入盲端,则将其诱入路径。第5次记录其游完全程的时间(swimming time),进入盲端的次数(number of error)及进入盲端的时间(error time)作为学习成绩。若在3 min时仍未找到阶梯,则定为不能完成学习训练,即有明显的学习能力低下。24 h后重复测试上述指标作为记忆成绩。
, http://www.100md.com
三、形态学观察
行为学测试完成后,在10%的水合氯醛(350 mg/kg,i.p)麻醉下,断头处死动物,取脑组织浸入10%福尔马林溶液内固定,取视交叉后4 mm处至小脑前的脑组织,常规石蜡包埋、切片,HE、Nissl染色,光镜观察海马细胞形态变化。细胞计数方法计数1 mm长度(×50)海马CA1区中段正常细胞数,取双侧海马细胞计数的均值。
四、统计学处理
采用t检验判断均数差异显著性。数据用
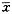 ±s表示。
±s表示。结 果
一、行为学实验
脑缺血再灌注后,大鼠发生了明显的学习记忆障碍,表现为:跳台实验记忆成绩中,模型组之潜伏期、受电击总时间明显长于假手术对照组,错误次数较多。统计学上有显著性差异,P<0.05,P<0.01。水迷宫实验中,学习及记忆成绩,模型组大鼠游完全程时间、进入盲端次数及时间均明显高于假手术组,P<0.05(见表1,2)。
, 百拇医药
表1 各组大鼠跳台实验的学习和记忆成绩比较
Tab 1 The results of rats' learning and memory in step-down avoidance test (
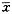 ±s. n=9)
±s. n=9)Learning
Memory
Latency
(min)
Number of
error (time)
The sum of latency
, http://www.100md.com
and time of error
(min)
Latency
(min)
Number of
error (time)
The sum of latency
and time of error
(min)
Sham-operated
0.57±0.60
, 百拇医药
1.56±1.67
0.89±0.72
0.50±0.69
0.67±1.66
0.56±0.68
Postischemia
1.13±0.60
2.56±2.51
1.54±0.88
1.75±1.94#
3.44±4.13#
, http://www.100md.com
2.04±1.79##
# P<0.05,##P<0.01 vs sham-operated.表2 各组大鼠水迷宫实验的学习和记忆成绩比较
Tab 2 The results of rats' learning and memory in in water maze test (
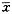 ±s. n=9)
±s. n=9)Learning
Memory
Swimming
time (min)
, http://www.100md.com
Number of
error (time)
Time of
error(min)
Swimming
time (min)
Number of
error (time)
Time of
error(min)
Sham-operated
, 百拇医药 0.41±0.17
1.33±0.87
0.10±0.08
0.23±0.16
0.44±0.73
0.01±0.02
Postischemia
3.68±1.64#
4.33±1.58#
1.93±1.38#
2.76±1.04#
, http://www.100md.com
4.56±1.51#
1.37±0.84#
# P<0.05 vs sham-operated.
二、形态学观察
低倍镜下,假手术组大鼠海马锥体细胞层结构紧密,层次丰富。模型组CA1、CA4区细胞排列稀疏,细胞线变得不清晰,尤以CA1区明显(图1,2)。

Fig 1 Region of hippocampal CA1 that exhibits clear line and rich layer of pyramidal cell.
, 百拇医药
Sham-operated control, Nissl stain×150.
图1 假手术组海马CA1区,锥体细胞排列紧密,层次丰富

Fig 2 Region of hippocampal CA1 that exhibits unclear pyramidal cell line and notable loss of neurons.
Ischemia injury, Nissl stain×150.
图2 模型组海马CA1区,细胞线模糊, 锥体细胞缺失
高倍镜下,假手术组锥体细胞核大,染色浅,细胞质丰富,细胞排列紧密,Nissl染色显示胞浆内尼氏体丰富。模型组CA1区形态正常的细胞数明显较少,许多细胞结构变得不完整,细胞周围出现间隙,细胞核固缩,有的形成碎片。尼氏体染色细胞质内尼氏体少,CA4区亦有细胞排列稀疏及形态异常,但远不如CA1区明显。
, 百拇医药
表3 短暂脑缺血后海马CA1区细胞计数的变化
Tab 3 Changes of the number of neurons in CA1 region after
transient global ischemia (cells/mm.
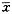 ±s. n=4) Group
±s. n=4) GroupNumber of neuron
Sham-operated control
146.25±18.45
Postischemia
67.00±27.99*
, 百拇医药
*P<0.05 vs sham-operated.
由表3可见,模型组海马CA1区细胞数明显少于假手术组,差异有高度显著性,表明海马CA1区有明显的细胞缺失。
讨 论
目前被常用于研究血管性痴呆的动物模型主要有四血管阻断(4VO)[1]和两血管阻断(2VO)模型[2,3]。有报道称,较严重的不完全性脑缺血动物的脑损伤较相同时间完全脑缺血的动物恢复差[4]。贾健民等采用4VO制造全脑反复缺血再灌模型,认为其可作为“血管性痴呆”模型使用[5]。我们对上述方法进行了改良,采用大鼠双侧颈总动脉反复夹闭并再通,同时腹腔注射硝普钠降低血压的方法复制模型。硝普钠的剂量用急性颈总动脉插管接压力传感器,生理四导记录监测血压确定。我们观察到腹腔注射硝普钠(2.5 mg/kg)后平均动脉血压立即下降至6.7 kPa左右,然后在30 min内逐渐回到给药前的水平。给硝普钠后血压一般不低于5.3 kPa。随着给药剂量的增加,其血压恢复的时间亦延长,稳定性较好,超过5 mg/kg,血压下降将不易恢复,造成动物死亡。因此在一定程度上可以通过控制硝普钠的剂量达到控制降压时间的目的。正式实验时不必监测血压,从而简化实验过程。采用硝普钠降压可以克服放血后由于机体的代偿反应引起的血压回升。跳台和水迷宫试验发现,手术后7 d模型组大鼠出现了明显的学习记忆功能障碍,空间定位、识别能力损伤较为严重。形态学观察可见明显的CA1区锥体细胞的变性、死亡、甚至丢失,而CA3区神经元无明显异常,这一变化印证了行为学的结果。而且动物没有明显的运动系统损伤表现,存活率较高。可重复性、稳定性较好,其优点为手术操作简单,对动物创伤较小,易于恢复,尤其是以学习记忆能力低下为主等特点,与临床“血管性痴呆”的发病过程相似,笔者认为可作为拟“血管性痴呆”的动物模型使用,适用于研究血管性痴呆的病理生理机制和评价药物的作用。由于造模时间较短,尤其适用于大批实验。值得注意的是:(1)在阻断双侧CCA的过程中,血压的变化对损伤程度影响较大,本模型是通过腹腔注射硝普钠降压的,因此,剂量的准确和注射的可靠性就显得十分重要,若剂量不准或药物未注射入腹腔,均会对血压造成影响进而影响造模的效果。(2)硝普钠的降压原理是直接扩张外周血管,而环境温度对外周血管的舒缩状态影响很大,因此环境温度变化较大时,应适当调整药物的剂量。
, 百拇医药
[基金项目] 国家九五攻关课题资助(No. 96-906-09-03)
参 考 文 献
[1] Pulsinelli WA, Brierley JB. A new model of bilateral hemispheric ischemia in the unanesthetized rat[J]. Stroke, 1979, 10(3): 267-272.
[2] Nordstrom CH, Siesjo BK. Effects of phenobarbital in cerebral ischemia. Prat I: Cerebral energy metabolism during incomplete ischemia[J]. Stroke, 1978, 9:327-335.
[3] Smith ML, Bendek G, Dahlgren N, et al. Models for studying long-term recovery following forebrain ischemia in the rat. 2.A2-vessel occlusion model[J]. Acta Neurol Scand, 1984, 69: 385-401.
, 百拇医药
[4] 李 巍, 严徽瑾. 脑缺血性学习记忆障碍模型[M].见:方福德, 周 吕, 丁 濂, 等. 主编. 现代医学实验技巧全书(下册). 第1版. 北京:北京医科大学协和医科大学联合出版社,1995. 248-251.
[5] 贾健民,贾健平,张 昱,等. Wistar Rat全脑反复缺血再灌流动物模型及行为学研究[J]. 中风与神经疾病杂志, 1992, 9(2):71-73.
[收稿日期]1999-07-23
[修回日期]2000-05-23
, http://www.100md.com