“»ΒΚΥΊΕ‘Χ«Ρρ≤Γ¥σ σΡΎΤΛΥΊΥθ―ΣΙήΉς”ΟΒΡ”Αœλ
Ής’ΏΘΚΕΓβυ ΆθΦ“ΗΜ ΝθΆ§Οά ΕΈΈΡΉΩ ΥΈ–ψφ¬ Ι§Ϋ®Να
ΒΞΈΜΘΚΈΪΖΜ“Ϋ―ß‘Κ≤Γάμ…ζάμΫΧ―– “Θ§ …ΫΕΪ ΈΪΖΜ 261042
ΙΊΦϋ¥ ΘΚ“»ΒΚΥΊΘΜΡΎΤΛΥθ―ΣΙήκΡάύΘΜ÷ςΕ·¬ωΘΜΗΏ―ΣΧ«÷Δ
÷–Ιζ≤Γάμ…ζάμ‘”÷Ψ001006
[’Σ “Σ] ΡΩΒΡΘΚ ―–ΨΩΗΏΧ«―Σ÷Δ ±“»ΒΚΥΊΕ‘ΡΎΤΛΥΊ-1(ET-1)Υθ―ΣΙήΉς”ΟΒΡ”ΑœλΓΘΖΫΖ®ΘΚ Η¥÷ΤΗΏΧ«―Σ÷Δ¥σ σΡΘ–ΆΘΜΫΪΗΏΧ«¥σ σΚΆ’ΐ≥Θ¥σ σΒΡάκΧε÷ςΕ·¬ω―ΣΙήΜΖ÷Ο”ΎΈό“»ΒΚΥΊΚΆΗΏ”Ύ…ζάμ≈®Ε»(40 mIU/L)“»ΒΚΥΊΒΡKH“Κ÷–Θ§Ιέ≤λΝΫΉι¥σ σ―ΣΙήΕ‘10-9 mol/L ET-1ΒΡΖ¥”ΠΓΘΫαΙϊΘΚ ΗΏΧ«¥σ σ―ΣΙήΕ‘ET-1ΒΡΖ¥”ΠΟςœ‘»θ”Ύ’ΐ≥Θ¥σ σ(P<0.01)ΘΜΗΏ≈®Ε»“»ΒΚΥΊΩ…Φθ»θET-1Ε‘’ΐ≥Θ¥σ σ―ΣΙήΒΡ ’ΥθΉς”Ο(P<0.01)ΘΜ“»ΒΚΥΊ≤ΜΡήΦθ»θET-1Ε‘ΗΏΧ«¥σ σ―ΣΙήΒΡ ’ΥθΉς”ΟΓΘΫα¬έΘΚ (1)≥ΛΤΎΗΏΧ«―Σ÷Δ Ι―ΣΙήΕ‘ET-1ΒΡΖ¥”ΠΫΒΒΆΘΜ(2)“»ΒΚΥΊΩ…Φθ»θET-1Ε‘’ΐ≥Θ¥σ σ―ΣΙήΒΡ ’ΥθΉς”ΟΘΜ(3)≥ΛΤΎΗΏΧ«―Σ÷Δ Ι“»ΒΚΥΊΕ‘ET-1Υθ―ΣΙήΜν–‘ΒΡ”ΑœλΦθ–ΓΓΘ
, http://www.100md.com
[÷–ΆΦΖ÷άύΚ≈] R587.1ΘΜQ578 [ΈΡœΉ±ξ Ε¬κ] A
[ΈΡ’¬±ύΚ≈] 1000-4718(2000)10-0894-03
Insulin influences the vasoconstriction caused by
endothelin-1 in the hyperglycemic rat
DING Yi WANG Jia-fu LIU Tong-mei DUAN Wen-zuo SONG Xiu-yuan GONG Jian-ling
(Department of Pathophysiolgy, Weifang Medical College, Weifang 261042, China)
, ΑΌΡ¥“Ϋ“©
[Abstract] AIMΘΚ To investigate the effects of insulin on aortic constriction caused by endothelin-1(ET-1) in normal and hyperglycemic rats. METHODSΘΚ Hyperglycemic rat models were prepared. Two aortic rings were immersed in the Krebs-Hensleit fluid with and without insulin (40 mIU/L) and the responses of rings to 10-9mol/L ET-1 were observed. RESULTSΘΚET-1 induced more obvious aortic ring constriction in normal rats than those in hyperglycemic rats (P<0.01). Rings constriction caused by ET-1 were attenuated in normal rats if the rings were immersed in the KH fluid with insulin (P<0.01), but no obvious changes were found in hyperglycemic rats. CONCLUSIONΘΚ (1) the vasoconstriction of aortic rings caused by ET-1 can be reduced by hyperglycemia. (2) Insulin can attenuate the aortic response to ET-1. (3) Insulin can not attenuate the vasoconstriction caused by ET-1 in hyperglycemic rats. These results suggest that insulin may affect vasoconstriction caused by ET-1, which may be involved in the pathogenesis of vascular complication in diabetic or insulin resistance condition.
, http://www.100md.com
[MeSH] Insulin; Endothelins; Aorta; Hyperglycemia
ΡΎΤΛΥΊ(endothelin, ET)÷ς“Σ”…―ΣΙήΡΎΤΛœΗΑϊ≤ζ…ζΘ§―ΣΙήΤΫΜ§ΦΓœΗΑϊ“≤Ω…≤ζ…ζET-1Θ§“ρ¥Υ―ΣΙήΤΫΜ§ΦΓœΗΑϊΦ» «ET-1ΒΡά¥‘¥”÷ «÷ς“ΣΒΡΑ–ΤςΙΌΓΘET-1ΚΆΈΜ”Ύ―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡETA ήΧεΫαΚœΕχΖΔΜ”«Ω¥σΒΡΥθ―ΣΙήΉς”ΟΓΘET-1ΒΡΝμ“Μ ήΧεETB‘ρ÷ς“ΣΈΜ”Ύ―ΣΙήΡΎΤΛœΗΑϊΘ§»œΈΣΩ…Ρή”κΡΎΤΛ φ’≈“ρΉ”ΚΆ«ΑΝ–ΜΖΥΊΒΡ ΆΖ≈”–ΙΊΓΘ
Χ«Ρρ≤Γ≤ΔΖΔ―ΣΙήΦ≤≤Γ «Χ«Ρρ≤Γ≤Γ»ΥΥάΆωΒΡ÷ς“Σ‘≠“ρΓΘΡΩ«Α―–ΨΩ»œΈΣΗΏ“»ΒΚΥΊ―Σ÷ΔΦΑ“»ΒΚΥΊΒ÷ΩΙΩ…Ρή «ΒΦ÷¬―ΣΙή≤ΔΖΔ÷ΔΒΡ÷Ί“Σ“ρΥΊΘ§Εχ≥ΛΤΎΗΏΧ«―Σ÷Δ”÷ΆυΆυΒΦ÷¬ΗΏ“»ΒΚΥΊ―Σ÷ΔΓΘ“ρ¥ΥΘ§ΗΏΧ«―Σ÷ΔΦ» «Χ«Ρρ≤ΓΒΡ≤Γ±δΧΊ’ςΘ§”÷ «ΒΦ÷¬Χ«Ρρ≤Γ―ΣΙή≤ΔΖΔ÷ΔΒΡ÷ς“Σ‘≠“ρΘ§ΒΪΨΏΧεΜζ÷Τ≤Μ«εΓΘ”–―–ΨΩΖΔœ÷Χ«Ρρ≤Γ≤Γ»ΥΧεΡΎET-1ΒΡ≈®Ε»‘ωΦ”Θ§≤Δ”κ–Ρ―ΣΙήΒΡΥπΚΠ≥ΧΕ»Οή«–œύΙΊ[1]ΓΘ“‘…œΉ ΝœΧα Ψ“»ΒΚΥΊΓΔET-1‘ΎΧ«Ρρ≤Γ―ΣΙή≤ΔΖΔ÷ΔΒΡΖΔ≤Γ÷–ΖΔΜ”÷Ί“ΣΉς”ΟΘ§ΒΪΥϋΟ«‘ΎΖΔ≤Γ÷–ΒΡΙΊœΒΡΩ«Α…–≤Μ«ε≥ΰΓΘ±Ψ Β―ι÷Φ‘ΎΧΫΧ÷ΗΏ”Ύ…ζάμ≈®Ε»ΒΡ“»ΒΚΥΊΕ‘ET-1Υθ―ΣΙήΉς”ΟΒΡ”Αœλ“‘ΦΑ≥ΛΤΎΗΏΧ«―Σ÷Δ ±¥Υ”Αœλ”–ΈόΗΡ±δΓΘ
, ΑΌΡ¥“Ϋ“©
≤Ρ Νœ ΚΆ ΖΫ Ζ®
“ΜΓΔ ≤ΡΝœ
ET-1(SigmaΙΪΥΨ)Θ§“»ΒΚΥΊ(–λ÷ί…ζΈοΜ·―ß÷Τ“©≥ß)Θ§Krebs-Hensleit“Κ(KH“Κ)ΒΡΉι≥…»γœ¬(mmol/L)ΘΚNaCl 11.5, CaCl2 1.8, MgSO4 1.2, NaHCO3 25.0, Glu 11.0, NaH2PO4 1.2, KCl 5.8ΓΘ’≈ΝΠΜΜΡήΤς(ΚΫΧλΙΛ“Β≤Ω¥ΪΗ–Τς―–ΨΩΥυ)Θ§ΝΩ≥ΧΈΣ10 gΓΘΕΰΒά…ζάμΦ«¬Φ“«(≥…ΕΦ“«Τς≥ß)Θ§Φ«¬Φ÷ΫΥΌ1 mm/minΓΘ
ΕΰΓΔ Β―ιΕ·ΈοΒΡΉΦ±Η
―Γ»ΓΫΓΩΒ≥…ΡξWistar¥σ σ(…ΫΕΪ“ΫΩΤ¥σ―ß Β―ιΕ·Έο÷––ΡΧαΙ©)12÷ΜΘ§–έ–‘Θ§Χε÷Ί200-250 gΓΘΥφΜζΖ÷ΈΣΝΫΉιΘ§ΟΩΉι6÷ΜΘ§Τδ÷–“ΜΉιΗχ”ηΗΏΧ«“ϊ ≥ΈΣΗΏΧ«ΉιΘΜΝμ“ΜΉιΈΣΕ‘’’ΉιΓΘ12÷ήΚσΘ§≤βΒΟΗΏΧ«Ήι¥σ σΒΡ―ΣΧ«(10.73Γά1.27) mmol/LΚΆ―Σ«ε“»ΒΚΥΊ(24.57Γά5.79) mIU/LΨυΟςœ‘ΗΏ”ΎΕ‘’’Ήι[(7.54Γά0.78) mmol/L, P<0.05]ΚΆ[(15.68Γά1.69) mIU/LΘ§ P<0.05]ΓΘ
, http://www.100md.com
»ΐΓΔ άκΧε―ΣΙήΜΖΒΡ÷Τ±Η
≤…”Ο≈δΕ‘ΒΡΝΫΉι¥σ σΘ§““Ο―¬ιΉμœ¬Θ§ΩΣ–Ί―ΗΥΌ»Γ≥ω–Ί÷ςΕ·¬ωΘ§‘Ύ Δ”–37ΓφΓΔ―θΚœKH“ΚΒΡΤΫΟσ÷–Ή–œΗΖ÷άκ―ΣΙή÷ήΈßΒΡ÷§ΖΨΚΆΫαΒόΉι÷·ΚσΘ§ΫΪΤδΦτ≥… ΐΕΈ2-3 mmΒΡΕ·¬ωΜΖΘ§―Γ»Γ÷–ΦδΈΜ÷ΟΒΡΕ·¬ωΜΖ±Η”ΟΓΘ
ΥΡΓΔ ―ΣΙήΙύΝς
ΫΪΝΫ÷Μ¥σ σΕ·¬ωΜΖΖ÷±π”ΟΝΫΗυL–ΈΗ÷’κ¥Ι÷±–ϋΙ“”ΎΉΑ”–KH“ΚΒΡΆ§“Μ‘ΓΗΉΒΡΆ§“ΜΥ°ΤΫ(37 ΓφΘ§pH 7.35-7.45)Θ§“‘95% O2-5% CO2Έ§≥÷―θΖ÷―Ι‘Ύ10.9 kPa,Μυ¥Γ’≈ΝΠΈΣ2 gΘ§ΤΫΚβ ±ΦδΈΣ90 minΘ§ΤΎΦδ”Ο30 mmol/LΒΡKCl ’Υθ“Μ¥ΈΘ§»ΜΚσ”ΟKH“Κœ¥Ά―÷ΝΜυœΏΘ§¥ΐ”ΟΓΘ
œ»”Ο≤ΜΚ§“»ΒΚΥΊΒΡKH“ΚΤΫΚβΚσΘ§Φ”»κET-1(10-9mol/L)÷ΝΉν¥σΖ¥”ΠΘ§”ΟKH“Κœ¥Ά―÷ΝΜυœΏΘΜ‘Ό“‘Κ§“»ΒΚΥΊ(40 mIU/L)ΒΡKH“Κ÷Ί–¬ΤΫΚβΘ§Φ”»κET-1(10-9 mol/L)÷ΝΉν¥σΖ¥”ΠΓΘ
, http://www.100md.com
ΈεΓΔ Ά≥ΦΤ¥Πάμ
ΉιΡΎ±»Ϋœ≤…”Ο≈δΕ‘±»ΫœΒΡtΦλ―ιΘ§ΉιΦδ±»Ϋœ≤…”ΟΝΫΨυ ΐ±»ΫœΒΡtΦλ―ιΓΘ ΐΨί”Ο Γάs±μ ΨΓΘ
Γάs±μ ΨΓΘ
Ϋα Ιϊ
ΗΏΧ«¥σ σ―ΣΙή”κΕ‘’’¥σ σ―ΣΙή±»ΫœΘ§“»ΒΚΥΊΖθ”ΐ«ΑΚΆ“»ΒΚΥΊΖθ”ΐΚσΕ‘ET-1ΒΡΖ¥”ΠΕΦ”–Οςœ‘ΒΡ≤ν“λ(Tab 1)ΓΘ“»ΒΚΥΊΖθ”ΐ«ΑΘ§ΗΏΧ«¥σ σ―ΣΙήΕ‘ET-1 (10-9 mol/L)ΒΡΉν¥σΖ¥”ΠΟςœ‘»θ”ΎΕ‘’’¥σ σ―ΣΙή(P<0.01)Θ§Εχ‘Ύ“»ΒΚΥΊΖθ”ΐΚσΕ‘ET-1ΒΡΖ¥”ΠΟςœ‘«Ω”ΎΕ‘’’¥σ σ―ΣΙή(P<0.01Θ§Fig 1)ΓΘΕ‘’’¥σ σ―ΣΙή‘Ύ“»ΒΚΥΊΖθ”ΐ«ΑΓΔΚσΕ‘ET-1ΒΡΖ¥”Π”–œ‘÷χ–‘≤ν“λΘ§Ψ≠“»ΒΚΥΊΖθ”ΐΚσ―ΣΙήΕ‘ET-1(10-9 mol/L)“ΐΤπΒΡ ’ΥθΖ¥”ΠΫœ“»ΒΚΥΊΦ”»κ«ΑΟςœ‘Φθ»θ(P<0.01Θ§Fig 2)ΓΘΕχΗΏΧ«¥σ σ―ΣΙή‘Ύ“»ΒΚΥΊΖθ”ΐ«ΑΚσΕ‘ET-1ΒΡΖ¥”ΠΈόΟςœ‘≤ν“λ(P>0.05)ΓΘ
, ΑΌΡ¥“Ϋ“©
±μ1 10-9 mol/L ET-1 Ε‘÷ςΕ·¬ω―ΣΙήΜΖΉν¥σ’≈ΝΠΒΡ”Αœλ
Tab 1 Effects of ET-1 (10-9mol/L) on Maximum Tension
of Aortic Rings ( Γάs) Group
Γάs) Group
Maximum Tension(mg)
Before Insulin
After Insulin
Control
108.04Γά7.32
, http://www.100md.com
37.95Γά10.97* *
Experiment
77.95Γά15.66*
94.02Γά20.91*
*P<0.01 vs control;* *P<0.01 vs before insulin.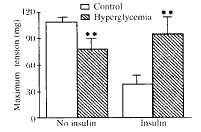
Fig 1 Effects of constriction of aortic rings caused by ET-1 (10-9 mol/L) in normal and hyperglycemic rats before and after insulin (40 mIU/L) immersion. n=6. Γάs.* *P<0.01 vs control.
Γάs.* *P<0.01 vs control.
, ΑΌΡ¥“Ϋ“©
ΆΦ1 ’ΐ≥Θ¥σ σΚΆΗΏΧ«¥σ σ―ΣΙή‘Ύ40 mIU/L“»ΒΚΥΊΖθ”ΐ«ΑΓΔΚσΕ‘10-9 mol/L ET-1Ζ¥”ΠΒΡ±»Ϋœ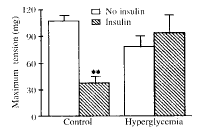
Fig 2 Effects of 40 mIU/L insulin on constriction of aortic rings caused by 10-9 mol/L ET-1 in normal and hyperglycemic rats. n=6.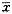 Γάs.* * P<0.01 vs NO insulin.
Γάs.* * P<0.01 vs NO insulin.
Χ÷ ¬έ
ΗΏΧ«―Σ÷Δ «Χ«Ρρ≤ΓΒΡ÷ς“Σ≤Γ±δΧΊ’ςΘ§Εχ≥ΛΤΎΗΏΧ«―Σ÷ΔΆυΆυΒΦ÷¬ΗΏ“»ΒΚΥΊ―Σ÷ΔΒΡ≥ωœ÷Θ§≤Δ«“ΖΔœ÷Χ«Ρρ≤ΓΚΆ“»ΒΚΥΊΒ÷ΩΙ(insulin resistance, IR) ±ΗΏΧ«―Σ÷ΔΚœ≤ΔΗΏ“»ΒΚΥΊ―Σ÷ΔΩ…Φ”ΥΌ–Ρ―ΣΙήΦ≤≤ΓΒΡΖΔ…ζΓΘHealyΖΔœ÷ΗΏΥ°ΤΫ“»ΒΚΥΊΩ…¥ΧΦΛ―ΣΙήΡΎΤΛœΗΑϊΚœ≥…ΚΆ ΆΖ≈ET-1[2]Θ§«“Χ«Ρρ≤Γ≤Γ»Υ―ΣΫ§ET-1≈®Ε»‘ωΦ””κ–Ρ―ΣΙήΒΡΥπΚΠ≥ΧΕ»Οή«–œύΙΊΓΘ
, http://www.100md.com
±Ψ Β―ιΖΔœ÷Θ§10-9 mol/L ET-1Φ¥Ρή Ι’ΐ≥Θ¥σ σ―ΣΙήΟςœ‘ ’ΥθΘ§’β”κ“‘ΆυΒΡ±®Βά“Μ÷¬ΓΘET-1«Ω¥σΕχ≥÷ΨΟΒΡΥθ―ΣΙήΉς”Ο÷ς“Σ «Ά®Ιΐ”κ―ΣΙήΤΫΜ§ΦΓœΗΑϊ…œΒΡETA ήΧεΫαΚœΘ§ΦΛΜν―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡCa2+Ά®ΒάΘ§ Ι[Ca2+]i‘ωΦ”Εχ Βœ÷ΒΡΓΘΈ“Ο«ΖΔœ÷‘Ύ“»ΒΚΥΊΖθ”ΐ«ΑΘ§ΗΏΧ«¥σ σ―ΣΙήΕ‘10-9 mol/L ET-1ΒΡΖ¥”ΠΟςœ‘ΒΆ”ΎΕ‘’’ΓΘ“ΜΖΫΟφΩ…Ρή «”…”Ύ≥ΛΤΎΗΏΧ«―Σ÷Δ Ι―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡ±μ–ΆΖΔ…ζΗΡ±δΘ§”… ’Υθ±μ–ΆΉΣ±δΈΣΚœ≥…±μ–ΆΘ§ΕχΒΦ÷¬Τδ ’ΥθΡήΝΠΫΒΒΆΓΘΝμ“ΜΖΫΟφΩ…Ρή «ΗΏΧ«―Σ÷Δ¥ΧΦΛΡΎΤΛœΗΑϊΚœ≥…ΚΆ ΆΖ≈ET-1Θ§―ΣΫ§ET-1ΒΡ≈®Ε»‘ωΦ” ΙETA ήΧεœ¬ΒςΘ§¥”Εχ Ι―ΣΙήΕ‘ET-1ΒΡΟτΗ––‘ΫΒΒΆΘ§Ζ¥”ΠΦθ»θΓΘ»Ζ«–Μζ÷Τ”–¥ΐΫχ“Μ≤ΫΧΫΧ÷ΓΘΨί±®ΒάΘ§ΩΎΖΰ¥σΝΩΤœΧ―Χ«Κσ―ΣΫ§ET-1‘ωΦ”ΓΘΧεΆβ Β―ι“≤÷ΛΟςΗΏΥ°ΤΫΤœΧ―Χ«Ω…¥ΧΦΛ―ΣΙήΡΎΤΛœΗΑϊ ΆΖ≈ET-1[3]ΓΘ
±Ψ Β―ιΫαΙϊœ‘ ΨΘ§ΗΏ”Ύ…ζάμΥ°ΤΫΒΡ“»ΒΚΥΊΩ… Ι’ΐ≥Θ¥σ σ―ΣΙήΕ‘ET-1ΒΡΖ¥”ΠΟςœ‘Φθ»θΓΘ“»ΒΚΥΊΩ…ΡήΆ®Ιΐ(1)Φ”«ΩET-1Ε‘ΡΎΤΛœΗΑϊΒΡ¥ΧΦΛΘ§ Ι φ―ΣΙήΈο÷ ΒΡ ΆΖ≈‘ωΦ”ΘΜ(2)”Αœλ―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡΤœΧ―Χ«…ψ»ΓΚΆάκΉ”ΉΣ‘ΥΕχ Βœ÷ΒΡΓΘ»ΜΕχ“»ΒΚΥΊ≤ΜΡή”ΑœλΗΏΧ«―Σ÷Δ¥σ σ―ΣΙήΕ‘ET-1ΒΡΖ¥”ΠΓΘ’βΩ…Ρή «”…”Ύ≥ΛΤΎΗΏΧ«―Σ÷Δ ΙΜζΧε≤ζ…ζIRΘ§“»ΒΚΥΊ≤ΜΡήΖΔΜ”Τδ’ΐ≥ΘΒΡ…ζάμΙΠΡήΘ§Φ”÷°Θ§≥ΛΤΎΗΏΧ«―Σ÷ΔΩ…ΡήΆ®Ιΐ(1)ΗΏ≈®Ε»ΤœΧ―Χ«ΒΡ÷±Ϋ”ΕΨ–‘Ής”ΟΓΔ(2)Χ«ΜυΜ·÷’≤ζΈοΒΡΜΐάέΓΔ(3)ΤΤΜΒœΗΑϊΡΎ–≈Κ≈¥ΪΒίœΒΆ≥ΦΑ‘λ≥…ΦΌ»±―θΓΔ(4)Φ”ΥΌΉ‘”…ΜυΒΡ≤ζ…ζΒ»ΆΨΨΕ Ι―ΣΙήΡΎΤΛ ήΥπΘ§ΙΠΡή≥ωœ÷“λ≥ΘΘ§ φ―ΣΙήΈο÷ (»γ―ΣΙή φ’≈“ρΉ”ΓΔΗΈΥΊΒ»)ΒΡ ΆΖ≈Φθ…ΌΥυ÷¬ΓΘKanameΒ»»œΈΣΡΎΤΛ «ΉηΒ≤“»ΒΚΥΊΒΡΤΝ’œ[4]Θ§―ΣΫ§÷–ΒΡ“»ΒΚΥΊΡήΖώ’ΐ≥ΘΖΔΜ”Ής”ΟΒΡΨωΕ®“ρΥΊ «“»ΒΚΥΊΒΡΩγΡΛΉΣ‘Υ[5]ΓΘ“―”–―–ΨΩ÷ΛΟςΩ…άϊ”ΟΡΎΤΛΟφΜΐΒΡΦθ…ΌΚΆΙΠΡή“λ≥Θ «ΒΦ÷¬―ΣΙήΉι÷·ΖΔ…ζIRΒΡ÷ς“Σ‘≠“ρΓΘ≥ΛΤΎΗΏΧ«―Σ÷Δ…œ―ΣΙήΡΎΤΛ ήΥπΘ§“»ΒΚΥΊ“ρΕχ≤ΜΡήΖΔΜ”’ΐ≥ΘΉς”ΟΓΘΨΏΧεΜζ÷Τ”–¥ΐΫχ“Μ≤ΫΧΫΧ÷ΓΘ
, ΑΌΡ¥“Ϋ“©
Ήέ…œΥυ ωΘ§≥ΛΤΎΗΏΧ«―Σ÷ΔΩ…ΡήΆ®Ιΐ―ΣΙήΡΎΤΛΥπ…ΥΘ§―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡΙΐΕ»‘ω÷≥“‘ΦΑ≤ζ…ζIRΘ§¥”Εχ Ι―ΣΙήΕ‘Υθ―ΣΙήΈο÷ ΒΡΖ¥”Π‘ω«ΩΘ§―ΣΙή’≈ΝΠ‘ωΦ”Θ§’β–©ΗΡ±δΕΦ”–÷ζ”ΎΧ«Ρρ≤Γ―ΣΙή≤ΔΖΔ÷ΔΒΡΖΔ…ζΚΆΖΔ’ΙΓΘ
[ΜυΫπœνΡΩ] …ΫΕΪ ΓΫΧΈ·Ή ÷ζΩΈΧβ
Tel: 0536-8290829
[≤Έ ΩΦ ΈΡ œΉ]
[1] Masafumi Takahashi. Involvement of adhesion molecules in human monocyte adhesion to and transmigration through endothelial cells in vitro[J]. Atherosclerosis, 1994, 10: 73-81.
[2] Healy B. Endothelial cells dysfunction: an emerging endocrinopathy linked to coronary disease[J]. J Am Coll Cardiol, 1990, 16: 349-356.
, ΑΌΡ¥“Ϋ“©
[3] Yanagisawa M., Kurihara H., Kimura S. et al. A novel peptide, vasoconstriction, endothelin is produced by vascular endothelium and modulates smooth muscle Ca2+ channels[J]. J Hypertens, 1988, 6(suppl): S188ΓΪS191.
[4] Kaname Saida, Youji Mitsui, Norio Ishida. A novel peptide, vasoactive intestinal contractor of a new (endothelin) peptide family[J]. J Biol Chem, 1989, 264: 14613-14616.
[5] Tomoh Masak, M D, Sadao Kimura, et al. Molecular and cellular mechanism of endothelin regulation. Implication for vascular function[J]. Circulation, 1991, 84: 457-468.
[ ’Ηε»’ΤΎ] 1999-06-17
[–όΜΊ»’ΤΎ] 1999-12-22
ΣΠ, ΑΌΡ¥“Ϋ“©
ΒΞΈΜΘΚΈΪΖΜ“Ϋ―ß‘Κ≤Γάμ…ζάμΫΧ―– “Θ§ …ΫΕΪ ΈΪΖΜ 261042
ΙΊΦϋ¥ ΘΚ“»ΒΚΥΊΘΜΡΎΤΛΥθ―ΣΙήκΡάύΘΜ÷ςΕ·¬ωΘΜΗΏ―ΣΧ«÷Δ
÷–Ιζ≤Γάμ…ζάμ‘”÷Ψ001006
[’Σ “Σ] ΡΩΒΡΘΚ ―–ΨΩΗΏΧ«―Σ÷Δ ±“»ΒΚΥΊΕ‘ΡΎΤΛΥΊ-1(ET-1)Υθ―ΣΙήΉς”ΟΒΡ”ΑœλΓΘΖΫΖ®ΘΚ Η¥÷ΤΗΏΧ«―Σ÷Δ¥σ σΡΘ–ΆΘΜΫΪΗΏΧ«¥σ σΚΆ’ΐ≥Θ¥σ σΒΡάκΧε÷ςΕ·¬ω―ΣΙήΜΖ÷Ο”ΎΈό“»ΒΚΥΊΚΆΗΏ”Ύ…ζάμ≈®Ε»(40 mIU/L)“»ΒΚΥΊΒΡKH“Κ÷–Θ§Ιέ≤λΝΫΉι¥σ σ―ΣΙήΕ‘10-9 mol/L ET-1ΒΡΖ¥”ΠΓΘΫαΙϊΘΚ ΗΏΧ«¥σ σ―ΣΙήΕ‘ET-1ΒΡΖ¥”ΠΟςœ‘»θ”Ύ’ΐ≥Θ¥σ σ(P<0.01)ΘΜΗΏ≈®Ε»“»ΒΚΥΊΩ…Φθ»θET-1Ε‘’ΐ≥Θ¥σ σ―ΣΙήΒΡ ’ΥθΉς”Ο(P<0.01)ΘΜ“»ΒΚΥΊ≤ΜΡήΦθ»θET-1Ε‘ΗΏΧ«¥σ σ―ΣΙήΒΡ ’ΥθΉς”ΟΓΘΫα¬έΘΚ (1)≥ΛΤΎΗΏΧ«―Σ÷Δ Ι―ΣΙήΕ‘ET-1ΒΡΖ¥”ΠΫΒΒΆΘΜ(2)“»ΒΚΥΊΩ…Φθ»θET-1Ε‘’ΐ≥Θ¥σ σ―ΣΙήΒΡ ’ΥθΉς”ΟΘΜ(3)≥ΛΤΎΗΏΧ«―Σ÷Δ Ι“»ΒΚΥΊΕ‘ET-1Υθ―ΣΙήΜν–‘ΒΡ”ΑœλΦθ–ΓΓΘ
, http://www.100md.com
[÷–ΆΦΖ÷άύΚ≈] R587.1ΘΜQ578 [ΈΡœΉ±ξ Ε¬κ] A
[ΈΡ’¬±ύΚ≈] 1000-4718(2000)10-0894-03
Insulin influences the vasoconstriction caused by
endothelin-1 in the hyperglycemic rat
DING Yi WANG Jia-fu LIU Tong-mei DUAN Wen-zuo SONG Xiu-yuan GONG Jian-ling
(Department of Pathophysiolgy, Weifang Medical College, Weifang 261042, China)
, ΑΌΡ¥“Ϋ“©
[Abstract] AIMΘΚ To investigate the effects of insulin on aortic constriction caused by endothelin-1(ET-1) in normal and hyperglycemic rats. METHODSΘΚ Hyperglycemic rat models were prepared. Two aortic rings were immersed in the Krebs-Hensleit fluid with and without insulin (40 mIU/L) and the responses of rings to 10-9mol/L ET-1 were observed. RESULTSΘΚET-1 induced more obvious aortic ring constriction in normal rats than those in hyperglycemic rats (P<0.01). Rings constriction caused by ET-1 were attenuated in normal rats if the rings were immersed in the KH fluid with insulin (P<0.01), but no obvious changes were found in hyperglycemic rats. CONCLUSIONΘΚ (1) the vasoconstriction of aortic rings caused by ET-1 can be reduced by hyperglycemia. (2) Insulin can attenuate the aortic response to ET-1. (3) Insulin can not attenuate the vasoconstriction caused by ET-1 in hyperglycemic rats. These results suggest that insulin may affect vasoconstriction caused by ET-1, which may be involved in the pathogenesis of vascular complication in diabetic or insulin resistance condition.
, http://www.100md.com
[MeSH] Insulin; Endothelins; Aorta; Hyperglycemia
ΡΎΤΛΥΊ(endothelin, ET)÷ς“Σ”…―ΣΙήΡΎΤΛœΗΑϊ≤ζ…ζΘ§―ΣΙήΤΫΜ§ΦΓœΗΑϊ“≤Ω…≤ζ…ζET-1Θ§“ρ¥Υ―ΣΙήΤΫΜ§ΦΓœΗΑϊΦ» «ET-1ΒΡά¥‘¥”÷ «÷ς“ΣΒΡΑ–ΤςΙΌΓΘET-1ΚΆΈΜ”Ύ―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡETA ήΧεΫαΚœΕχΖΔΜ”«Ω¥σΒΡΥθ―ΣΙήΉς”ΟΓΘET-1ΒΡΝμ“Μ ήΧεETB‘ρ÷ς“ΣΈΜ”Ύ―ΣΙήΡΎΤΛœΗΑϊΘ§»œΈΣΩ…Ρή”κΡΎΤΛ φ’≈“ρΉ”ΚΆ«ΑΝ–ΜΖΥΊΒΡ ΆΖ≈”–ΙΊΓΘ
Χ«Ρρ≤Γ≤ΔΖΔ―ΣΙήΦ≤≤Γ «Χ«Ρρ≤Γ≤Γ»ΥΥάΆωΒΡ÷ς“Σ‘≠“ρΓΘΡΩ«Α―–ΨΩ»œΈΣΗΏ“»ΒΚΥΊ―Σ÷ΔΦΑ“»ΒΚΥΊΒ÷ΩΙΩ…Ρή «ΒΦ÷¬―ΣΙή≤ΔΖΔ÷ΔΒΡ÷Ί“Σ“ρΥΊΘ§Εχ≥ΛΤΎΗΏΧ«―Σ÷Δ”÷ΆυΆυΒΦ÷¬ΗΏ“»ΒΚΥΊ―Σ÷ΔΓΘ“ρ¥ΥΘ§ΗΏΧ«―Σ÷ΔΦ» «Χ«Ρρ≤ΓΒΡ≤Γ±δΧΊ’ςΘ§”÷ «ΒΦ÷¬Χ«Ρρ≤Γ―ΣΙή≤ΔΖΔ÷ΔΒΡ÷ς“Σ‘≠“ρΘ§ΒΪΨΏΧεΜζ÷Τ≤Μ«εΓΘ”–―–ΨΩΖΔœ÷Χ«Ρρ≤Γ≤Γ»ΥΧεΡΎET-1ΒΡ≈®Ε»‘ωΦ”Θ§≤Δ”κ–Ρ―ΣΙήΒΡΥπΚΠ≥ΧΕ»Οή«–œύΙΊ[1]ΓΘ“‘…œΉ ΝœΧα Ψ“»ΒΚΥΊΓΔET-1‘ΎΧ«Ρρ≤Γ―ΣΙή≤ΔΖΔ÷ΔΒΡΖΔ≤Γ÷–ΖΔΜ”÷Ί“ΣΉς”ΟΘ§ΒΪΥϋΟ«‘ΎΖΔ≤Γ÷–ΒΡΙΊœΒΡΩ«Α…–≤Μ«ε≥ΰΓΘ±Ψ Β―ι÷Φ‘ΎΧΫΧ÷ΗΏ”Ύ…ζάμ≈®Ε»ΒΡ“»ΒΚΥΊΕ‘ET-1Υθ―ΣΙήΉς”ΟΒΡ”Αœλ“‘ΦΑ≥ΛΤΎΗΏΧ«―Σ÷Δ ±¥Υ”Αœλ”–ΈόΗΡ±δΓΘ
, ΑΌΡ¥“Ϋ“©
≤Ρ Νœ ΚΆ ΖΫ Ζ®
“ΜΓΔ ≤ΡΝœ
ET-1(SigmaΙΪΥΨ)Θ§“»ΒΚΥΊ(–λ÷ί…ζΈοΜ·―ß÷Τ“©≥ß)Θ§Krebs-Hensleit“Κ(KH“Κ)ΒΡΉι≥…»γœ¬(mmol/L)ΘΚNaCl 11.5, CaCl2 1.8, MgSO4 1.2, NaHCO3 25.0, Glu 11.0, NaH2PO4 1.2, KCl 5.8ΓΘ’≈ΝΠΜΜΡήΤς(ΚΫΧλΙΛ“Β≤Ω¥ΪΗ–Τς―–ΨΩΥυ)Θ§ΝΩ≥ΧΈΣ10 gΓΘΕΰΒά…ζάμΦ«¬Φ“«(≥…ΕΦ“«Τς≥ß)Θ§Φ«¬Φ÷ΫΥΌ1 mm/minΓΘ
ΕΰΓΔ Β―ιΕ·ΈοΒΡΉΦ±Η
―Γ»ΓΫΓΩΒ≥…ΡξWistar¥σ σ(…ΫΕΪ“ΫΩΤ¥σ―ß Β―ιΕ·Έο÷––ΡΧαΙ©)12÷ΜΘ§–έ–‘Θ§Χε÷Ί200-250 gΓΘΥφΜζΖ÷ΈΣΝΫΉιΘ§ΟΩΉι6÷ΜΘ§Τδ÷–“ΜΉιΗχ”ηΗΏΧ«“ϊ ≥ΈΣΗΏΧ«ΉιΘΜΝμ“ΜΉιΈΣΕ‘’’ΉιΓΘ12÷ήΚσΘ§≤βΒΟΗΏΧ«Ήι¥σ σΒΡ―ΣΧ«(10.73Γά1.27) mmol/LΚΆ―Σ«ε“»ΒΚΥΊ(24.57Γά5.79) mIU/LΨυΟςœ‘ΗΏ”ΎΕ‘’’Ήι[(7.54Γά0.78) mmol/L, P<0.05]ΚΆ[(15.68Γά1.69) mIU/LΘ§ P<0.05]ΓΘ
, http://www.100md.com
»ΐΓΔ άκΧε―ΣΙήΜΖΒΡ÷Τ±Η
≤…”Ο≈δΕ‘ΒΡΝΫΉι¥σ σΘ§““Ο―¬ιΉμœ¬Θ§ΩΣ–Ί―ΗΥΌ»Γ≥ω–Ί÷ςΕ·¬ωΘ§‘Ύ Δ”–37ΓφΓΔ―θΚœKH“ΚΒΡΤΫΟσ÷–Ή–œΗΖ÷άκ―ΣΙή÷ήΈßΒΡ÷§ΖΨΚΆΫαΒόΉι÷·ΚσΘ§ΫΪΤδΦτ≥… ΐΕΈ2-3 mmΒΡΕ·¬ωΜΖΘ§―Γ»Γ÷–ΦδΈΜ÷ΟΒΡΕ·¬ωΜΖ±Η”ΟΓΘ
ΥΡΓΔ ―ΣΙήΙύΝς
ΫΪΝΫ÷Μ¥σ σΕ·¬ωΜΖΖ÷±π”ΟΝΫΗυL–ΈΗ÷’κ¥Ι÷±–ϋΙ“”ΎΉΑ”–KH“ΚΒΡΆ§“Μ‘ΓΗΉΒΡΆ§“ΜΥ°ΤΫ(37 ΓφΘ§pH 7.35-7.45)Θ§“‘95% O2-5% CO2Έ§≥÷―θΖ÷―Ι‘Ύ10.9 kPa,Μυ¥Γ’≈ΝΠΈΣ2 gΘ§ΤΫΚβ ±ΦδΈΣ90 minΘ§ΤΎΦδ”Ο30 mmol/LΒΡKCl ’Υθ“Μ¥ΈΘ§»ΜΚσ”ΟKH“Κœ¥Ά―÷ΝΜυœΏΘ§¥ΐ”ΟΓΘ
œ»”Ο≤ΜΚ§“»ΒΚΥΊΒΡKH“ΚΤΫΚβΚσΘ§Φ”»κET-1(10-9mol/L)÷ΝΉν¥σΖ¥”ΠΘ§”ΟKH“Κœ¥Ά―÷ΝΜυœΏΘΜ‘Ό“‘Κ§“»ΒΚΥΊ(40 mIU/L)ΒΡKH“Κ÷Ί–¬ΤΫΚβΘ§Φ”»κET-1(10-9 mol/L)÷ΝΉν¥σΖ¥”ΠΓΘ
, http://www.100md.com
ΈεΓΔ Ά≥ΦΤ¥Πάμ
ΉιΡΎ±»Ϋœ≤…”Ο≈δΕ‘±»ΫœΒΡtΦλ―ιΘ§ΉιΦδ±»Ϋœ≤…”ΟΝΫΨυ ΐ±»ΫœΒΡtΦλ―ιΓΘ ΐΨί”Ο
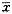 Γάs±μ ΨΓΘ
Γάs±μ ΨΓΘΫα Ιϊ
ΗΏΧ«¥σ σ―ΣΙή”κΕ‘’’¥σ σ―ΣΙή±»ΫœΘ§“»ΒΚΥΊΖθ”ΐ«ΑΚΆ“»ΒΚΥΊΖθ”ΐΚσΕ‘ET-1ΒΡΖ¥”ΠΕΦ”–Οςœ‘ΒΡ≤ν“λ(Tab 1)ΓΘ“»ΒΚΥΊΖθ”ΐ«ΑΘ§ΗΏΧ«¥σ σ―ΣΙήΕ‘ET-1 (10-9 mol/L)ΒΡΉν¥σΖ¥”ΠΟςœ‘»θ”ΎΕ‘’’¥σ σ―ΣΙή(P<0.01)Θ§Εχ‘Ύ“»ΒΚΥΊΖθ”ΐΚσΕ‘ET-1ΒΡΖ¥”ΠΟςœ‘«Ω”ΎΕ‘’’¥σ σ―ΣΙή(P<0.01Θ§Fig 1)ΓΘΕ‘’’¥σ σ―ΣΙή‘Ύ“»ΒΚΥΊΖθ”ΐ«ΑΓΔΚσΕ‘ET-1ΒΡΖ¥”Π”–œ‘÷χ–‘≤ν“λΘ§Ψ≠“»ΒΚΥΊΖθ”ΐΚσ―ΣΙήΕ‘ET-1(10-9 mol/L)“ΐΤπΒΡ ’ΥθΖ¥”ΠΫœ“»ΒΚΥΊΦ”»κ«ΑΟςœ‘Φθ»θ(P<0.01Θ§Fig 2)ΓΘΕχΗΏΧ«¥σ σ―ΣΙή‘Ύ“»ΒΚΥΊΖθ”ΐ«ΑΚσΕ‘ET-1ΒΡΖ¥”ΠΈόΟςœ‘≤ν“λ(P>0.05)ΓΘ
, ΑΌΡ¥“Ϋ“©
±μ1 10-9 mol/L ET-1 Ε‘÷ςΕ·¬ω―ΣΙήΜΖΉν¥σ’≈ΝΠΒΡ”Αœλ
Tab 1 Effects of ET-1 (10-9mol/L) on Maximum Tension
of Aortic Rings (
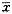 Γάs) Group
Γάs) GroupMaximum Tension(mg)
Before Insulin
After Insulin
Control
108.04Γά7.32
, http://www.100md.com
37.95Γά10.97* *
Experiment
77.95Γά15.66*
94.02Γά20.91*
*P<0.01 vs control;* *P<0.01 vs before insulin.

Fig 1 Effects of constriction of aortic rings caused by ET-1 (10-9 mol/L) in normal and hyperglycemic rats before and after insulin (40 mIU/L) immersion. n=6.
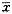 Γάs.* *P<0.01 vs control.
Γάs.* *P<0.01 vs control., ΑΌΡ¥“Ϋ“©
ΆΦ1 ’ΐ≥Θ¥σ σΚΆΗΏΧ«¥σ σ―ΣΙή‘Ύ40 mIU/L“»ΒΚΥΊΖθ”ΐ«ΑΓΔΚσΕ‘10-9 mol/L ET-1Ζ¥”ΠΒΡ±»Ϋœ

Fig 2 Effects of 40 mIU/L insulin on constriction of aortic rings caused by 10-9 mol/L ET-1 in normal and hyperglycemic rats. n=6.
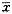 Γάs.* * P<0.01 vs NO insulin.
Γάs.* * P<0.01 vs NO insulin.Χ÷ ¬έ
ΗΏΧ«―Σ÷Δ «Χ«Ρρ≤ΓΒΡ÷ς“Σ≤Γ±δΧΊ’ςΘ§Εχ≥ΛΤΎΗΏΧ«―Σ÷ΔΆυΆυΒΦ÷¬ΗΏ“»ΒΚΥΊ―Σ÷ΔΒΡ≥ωœ÷Θ§≤Δ«“ΖΔœ÷Χ«Ρρ≤ΓΚΆ“»ΒΚΥΊΒ÷ΩΙ(insulin resistance, IR) ±ΗΏΧ«―Σ÷ΔΚœ≤ΔΗΏ“»ΒΚΥΊ―Σ÷ΔΩ…Φ”ΥΌ–Ρ―ΣΙήΦ≤≤ΓΒΡΖΔ…ζΓΘHealyΖΔœ÷ΗΏΥ°ΤΫ“»ΒΚΥΊΩ…¥ΧΦΛ―ΣΙήΡΎΤΛœΗΑϊΚœ≥…ΚΆ ΆΖ≈ET-1[2]Θ§«“Χ«Ρρ≤Γ≤Γ»Υ―ΣΫ§ET-1≈®Ε»‘ωΦ””κ–Ρ―ΣΙήΒΡΥπΚΠ≥ΧΕ»Οή«–œύΙΊΓΘ
, http://www.100md.com
±Ψ Β―ιΖΔœ÷Θ§10-9 mol/L ET-1Φ¥Ρή Ι’ΐ≥Θ¥σ σ―ΣΙήΟςœ‘ ’ΥθΘ§’β”κ“‘ΆυΒΡ±®Βά“Μ÷¬ΓΘET-1«Ω¥σΕχ≥÷ΨΟΒΡΥθ―ΣΙήΉς”Ο÷ς“Σ «Ά®Ιΐ”κ―ΣΙήΤΫΜ§ΦΓœΗΑϊ…œΒΡETA ήΧεΫαΚœΘ§ΦΛΜν―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡCa2+Ά®ΒάΘ§ Ι[Ca2+]i‘ωΦ”Εχ Βœ÷ΒΡΓΘΈ“Ο«ΖΔœ÷‘Ύ“»ΒΚΥΊΖθ”ΐ«ΑΘ§ΗΏΧ«¥σ σ―ΣΙήΕ‘10-9 mol/L ET-1ΒΡΖ¥”ΠΟςœ‘ΒΆ”ΎΕ‘’’ΓΘ“ΜΖΫΟφΩ…Ρή «”…”Ύ≥ΛΤΎΗΏΧ«―Σ÷Δ Ι―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡ±μ–ΆΖΔ…ζΗΡ±δΘ§”… ’Υθ±μ–ΆΉΣ±δΈΣΚœ≥…±μ–ΆΘ§ΕχΒΦ÷¬Τδ ’ΥθΡήΝΠΫΒΒΆΓΘΝμ“ΜΖΫΟφΩ…Ρή «ΗΏΧ«―Σ÷Δ¥ΧΦΛΡΎΤΛœΗΑϊΚœ≥…ΚΆ ΆΖ≈ET-1Θ§―ΣΫ§ET-1ΒΡ≈®Ε»‘ωΦ” ΙETA ήΧεœ¬ΒςΘ§¥”Εχ Ι―ΣΙήΕ‘ET-1ΒΡΟτΗ––‘ΫΒΒΆΘ§Ζ¥”ΠΦθ»θΓΘ»Ζ«–Μζ÷Τ”–¥ΐΫχ“Μ≤ΫΧΫΧ÷ΓΘΨί±®ΒάΘ§ΩΎΖΰ¥σΝΩΤœΧ―Χ«Κσ―ΣΫ§ET-1‘ωΦ”ΓΘΧεΆβ Β―ι“≤÷ΛΟςΗΏΥ°ΤΫΤœΧ―Χ«Ω…¥ΧΦΛ―ΣΙήΡΎΤΛœΗΑϊ ΆΖ≈ET-1[3]ΓΘ
±Ψ Β―ιΫαΙϊœ‘ ΨΘ§ΗΏ”Ύ…ζάμΥ°ΤΫΒΡ“»ΒΚΥΊΩ… Ι’ΐ≥Θ¥σ σ―ΣΙήΕ‘ET-1ΒΡΖ¥”ΠΟςœ‘Φθ»θΓΘ“»ΒΚΥΊΩ…ΡήΆ®Ιΐ(1)Φ”«ΩET-1Ε‘ΡΎΤΛœΗΑϊΒΡ¥ΧΦΛΘ§ Ι φ―ΣΙήΈο÷ ΒΡ ΆΖ≈‘ωΦ”ΘΜ(2)”Αœλ―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡΤœΧ―Χ«…ψ»ΓΚΆάκΉ”ΉΣ‘ΥΕχ Βœ÷ΒΡΓΘ»ΜΕχ“»ΒΚΥΊ≤ΜΡή”ΑœλΗΏΧ«―Σ÷Δ¥σ σ―ΣΙήΕ‘ET-1ΒΡΖ¥”ΠΓΘ’βΩ…Ρή «”…”Ύ≥ΛΤΎΗΏΧ«―Σ÷Δ ΙΜζΧε≤ζ…ζIRΘ§“»ΒΚΥΊ≤ΜΡήΖΔΜ”Τδ’ΐ≥ΘΒΡ…ζάμΙΠΡήΘ§Φ”÷°Θ§≥ΛΤΎΗΏΧ«―Σ÷ΔΩ…ΡήΆ®Ιΐ(1)ΗΏ≈®Ε»ΤœΧ―Χ«ΒΡ÷±Ϋ”ΕΨ–‘Ής”ΟΓΔ(2)Χ«ΜυΜ·÷’≤ζΈοΒΡΜΐάέΓΔ(3)ΤΤΜΒœΗΑϊΡΎ–≈Κ≈¥ΪΒίœΒΆ≥ΦΑ‘λ≥…ΦΌ»±―θΓΔ(4)Φ”ΥΌΉ‘”…ΜυΒΡ≤ζ…ζΒ»ΆΨΨΕ Ι―ΣΙήΡΎΤΛ ήΥπΘ§ΙΠΡή≥ωœ÷“λ≥ΘΘ§ φ―ΣΙήΈο÷ (»γ―ΣΙή φ’≈“ρΉ”ΓΔΗΈΥΊΒ»)ΒΡ ΆΖ≈Φθ…ΌΥυ÷¬ΓΘKanameΒ»»œΈΣΡΎΤΛ «ΉηΒ≤“»ΒΚΥΊΒΡΤΝ’œ[4]Θ§―ΣΫ§÷–ΒΡ“»ΒΚΥΊΡήΖώ’ΐ≥ΘΖΔΜ”Ής”ΟΒΡΨωΕ®“ρΥΊ «“»ΒΚΥΊΒΡΩγΡΛΉΣ‘Υ[5]ΓΘ“―”–―–ΨΩ÷ΛΟςΩ…άϊ”ΟΡΎΤΛΟφΜΐΒΡΦθ…ΌΚΆΙΠΡή“λ≥Θ «ΒΦ÷¬―ΣΙήΉι÷·ΖΔ…ζIRΒΡ÷ς“Σ‘≠“ρΓΘ≥ΛΤΎΗΏΧ«―Σ÷Δ…œ―ΣΙήΡΎΤΛ ήΥπΘ§“»ΒΚΥΊ“ρΕχ≤ΜΡήΖΔΜ”’ΐ≥ΘΉς”ΟΓΘΨΏΧεΜζ÷Τ”–¥ΐΫχ“Μ≤ΫΧΫΧ÷ΓΘ
, ΑΌΡ¥“Ϋ“©
Ήέ…œΥυ ωΘ§≥ΛΤΎΗΏΧ«―Σ÷ΔΩ…ΡήΆ®Ιΐ―ΣΙήΡΎΤΛΥπ…ΥΘ§―ΣΙήΤΫΜ§ΦΓœΗΑϊΒΡΙΐΕ»‘ω÷≥“‘ΦΑ≤ζ…ζIRΘ§¥”Εχ Ι―ΣΙήΕ‘Υθ―ΣΙήΈο÷ ΒΡΖ¥”Π‘ω«ΩΘ§―ΣΙή’≈ΝΠ‘ωΦ”Θ§’β–©ΗΡ±δΕΦ”–÷ζ”ΎΧ«Ρρ≤Γ―ΣΙή≤ΔΖΔ÷ΔΒΡΖΔ…ζΚΆΖΔ’ΙΓΘ
[ΜυΫπœνΡΩ] …ΫΕΪ ΓΫΧΈ·Ή ÷ζΩΈΧβ
Tel: 0536-8290829
[≤Έ ΩΦ ΈΡ œΉ]
[1] Masafumi Takahashi. Involvement of adhesion molecules in human monocyte adhesion to and transmigration through endothelial cells in vitro[J]. Atherosclerosis, 1994, 10: 73-81.
[2] Healy B. Endothelial cells dysfunction: an emerging endocrinopathy linked to coronary disease[J]. J Am Coll Cardiol, 1990, 16: 349-356.
, ΑΌΡ¥“Ϋ“©
[3] Yanagisawa M., Kurihara H., Kimura S. et al. A novel peptide, vasoconstriction, endothelin is produced by vascular endothelium and modulates smooth muscle Ca2+ channels[J]. J Hypertens, 1988, 6(suppl): S188ΓΪS191.
[4] Kaname Saida, Youji Mitsui, Norio Ishida. A novel peptide, vasoactive intestinal contractor of a new (endothelin) peptide family[J]. J Biol Chem, 1989, 264: 14613-14616.
[5] Tomoh Masak, M D, Sadao Kimura, et al. Molecular and cellular mechanism of endothelin regulation. Implication for vascular function[J]. Circulation, 1991, 84: 457-468.
[ ’Ηε»’ΤΎ] 1999-06-17
[–όΜΊ»’ΤΎ] 1999-12-22
ΣΠ, ΑΌΡ¥“Ϋ“©