毛细管电泳法测定盐酸西替利嗪糖浆中西替利嗪的含量
作者:魏玲 周威 俞如英
单位:魏玲 周威(厦门中山医院 厦门 361000);俞如英(中国药品生物制品检定所 北京 100050)
关键词:盐酸西替利嗪;毛细管电泳法;含量测定
中国新药杂志001010
[摘要] 目的:建立毛细管电泳法测定盐酸西替利嗪糖浆剂中 西替利嗪含量的方法。方法:以30mmol/L磷酸二氢钠(pH2.7)缓冲液为运行缓冲液, 运行电压为20kV, 检测波长为230nm。结果:盐酸西替利嗪在60~140μg/ml浓度范围内有良好的线性关系(r=0.9 993),回收率为98.4%,RSD=1.8%(n=6)。结论:毛细管电泳法可用于盐酸西替利嗪糖浆剂中西替利嗪的定量测定。
[中图分类号]R927.2 [文献标识码] B
, 百拇医药
[文章编号]1003-3734(2000)10-0694-03
Determination of cetirizine in cetirizine HCl syrup by
capillary zone electrophoresis
WEI Ling
(National Institute of Pharmaceutical and Biological Products,Beijin g 100050,China)
ZHOU Wei
(Xiamen Zhongshan Hospital,Xiamen 361000,Chi na)
, 百拇医药
YU Ru-yin
(National Institute of Pharmaceutical and Biological Products,Beijin g 100050,China)
[Abstract] Objective:To establish a capillary zone electropho retic me thod for determining cetirizine in cetirizine HCL syrup.Methods:A runn ing buffer consisted of 30 mmol/L NaH2PO4(pH2.7),a voltage of 20 kV and a UV detector at 230 nm were adopted in this methos.Results:A linear range of 60~140 μg/ml,a average recovery of 98.4% were obtained with a RSD=1.8%(n =6).Conclusion:Capillary zone electrophoresis can be used to determi ne the content of cctirizinc in cctirizinc HCL syrup.
, 百拇医药
[Key words] cetirizine hydrochloride;capillary zone electrophoresis ;assay
盐酸西替利嗪是对H1受体有选择性拮抗作用的抗组胺药, 在临床上主要用于治疗季节性 、 常年性、过敏性鼻炎以及荨麻疹[1]。盐酸西替利嗪制剂药典未收载。文献报道[2,3]用分光光度法和高效液相色谱法测定盐酸西替利嗪片剂中的西替利嗪含量 ,也有报道[4]用氯仿提取后用分光光度法测定糖浆剂中的西替利嗪含量,其他有 关西替利嗪的测定均是有关体液分析的报道,作者未见有毛细管电泳法测定盐酸西替利嗪的 文献。由印度Cipla公司进口我国的盐酸西替利嗪糖浆剂采用HPLC测定含量,由于糖浆中含 糖量高,易对色谱柱造成污染,使色谱柱使用寿命降低。本实验采用区带毛细管电泳法(CZE)测定了盐酸西替利嗪糖浆剂中的西替利嗪的含量,方法简单、快速、专属性好,分离效 率高,分析时间短,采用内标法定量,结果准确,制剂中的糖对分离无影响。
, 百拇医药
材料与方法
1 仪器与试药
SpectroPHORESIS 1000型高效毛细管电泳仪配FOCUS高速扫描紫外-可见光检测器( 美 国TSP公司),PC1000工作站(美国TSP公司)。盐酸西替利嗪对照品、盐酸西替利嗪糖浆和 空白糖浆均由印度Cipla公司提供。盐酸氯环利嗪由中国药品生物制品检定所提供。磷酸氢 二钠和磷酸均为分析纯。试验用水为二次蒸馏水。
2 实验方法
2.1 毛细管电泳分离条件 石英毛细管柱:内径50(m,总长度40cm ,有效长度32.5cm(美国Polymicro Technologic 公司),运行缓冲液为30mmol/L 磷酸氢 二钠缓冲液(用磷酸调pH值为2.7),运行电压为20kV,柱温度为20℃,检测波长为230nm, 真空进样5s,每次分析前先将毛细管柱用水清洗2min(20℃)。
, 百拇医药
2.2 线性关系 精密称取盐酸西替利嗪对照品50mg,置50 ml量瓶中,加水溶 解并稀释至刻度,制成1mg/ml的溶液,作为对照品储备溶液。精密称取盐酸氯环利嗪对照品 50mg,置50 ml量瓶中,加水溶解并稀释至刻度,制成1mg/ml的溶液,作为内标储备溶液。 精密吸取对照品储备溶液0.6, 0.8, 1.0, 1.2 和1.4ml,分别置10ml量瓶中,再分别加入内 标储备溶液1.0ml,加水稀释至刻度,摇匀,进样。以盐酸西替利嗪浓度对西替利嗪峰面积 与内标峰面积之比作线性回归,结果在60~140μg/ml浓度范围内有良好的线性关系, 回归方程为:Y=11.19X+0.06, r = 0.9993。其中,Y为盐酸西替利嗪与内标峰面积比 ,X为西替利嗪浓度((g/ml)。
2.3 回收率试验 分别精密吸取线性关系项下对照品储备溶液和内标储备溶 液各1ml,置10ml量瓶中,加入空白糖浆1.0ml,加水稀释至刻度,摇匀,作为供试品溶液 ;另分别精密吸取线性关系项下对照品储备溶液和内标储备溶液各1ml,置10ml量瓶中作为 对照溶液。分别取上述二溶液,测定。重复测定6次,以每份溶液的平均测定值与对照溶液 进行比较,计算回收率为98.4%,RSD=1.8%(n=6)。
, 百拇医药
2.4 精密度试验 取回收率试验项下的供试品溶液,按上述试验条件试验, 重复测定5次, 盐酸西替利嗪和盐酸氯环利嗪峰的迁移时间的RSD分别为0.62%和0.75%,盐酸西替利嗪和盐 酸氯环利嗪的峰面积之比的RSD为1.76%。
2.5 样品测定 精密吸取盐酸西替利嗪糖浆1.0ml,置10ml量瓶中,加入 内标溶液1.0ml,加水稀释至刻度,摇匀,制成样品溶液,测定;另分别精密吸取线 性关系项下对照品储备溶液和内标储备溶液各1ml,置10ml量瓶中作为对照溶液,同法测定, 用内标法计算盐酸西替利嗪糖浆剂中西替利嗪的含量。
结 果
1 典型分离电泳结果
见图1。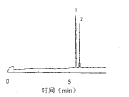
, http://www.100md.com
1 内标;2 西替利嗪
图1 盐酸西替利嗪糖浆剂毛细管电泳图
2 测定结果 3批糖浆剂,结果3批分别为(99.2±0.9)%,(100.3±0.8)%,(99.6±1 .2)%(n=3)。
讨 论
运行缓冲液的pH值和离子强度对分离测定影响较大。降低运行缓冲液 的浓度(或离子强度)能够降低运行电流,从而降低焦耳热,而增加运行缓冲液的浓度(或 离子强度)可以降低溶质有效表面电荷以减少管壁对溶质的吸附作用。
在pH为3条件下,考察了10,20,30和40mmol/L磷酸二氢钠缓冲液对分 离的影响,结果表明,在30 mmol/L条件下,溶质的有效浓度最大,同时电流也较低。
在磷酸二氢钠浓度为30mmol/L的条件下,考察了pH为2.5,3,4,5 和7时,溶质的迁移时间 的变化。随着运行缓冲液的pH值增加,西替利嗪和内标峰的迁移时间略为减小,而辅料中的 一个较大的干扰峰随pH值的增加而很快降低,当pH值>5时,该峰与盐酸西替利嗪峰几乎重叠 。这是由于随着运行缓冲液的pH值增加,盐酸西替利嗪和盐酸氯环利嗪的离子化程度降低, 有效迁移速率降低;而随着pH值的增加,电渗流增大,使分离度降低。 一般认为毛细管电泳的定量精密度比HPLC差,这是由于毛细管电泳的进样时间短(一般 为数秒),因此,难以用外标法准确定量。用内标法则可以使其定量精密度达到与HPLC相似 的水平。本实验采用盐酸氯环利嗪为内标,测定精密度小于2%,能够达到HPLC定量的要求 。
, 百拇医药
实验初期,盐酸西替利嗪浓度配制成0.5mg/ml,而使测 定的回收率低。这是由于样品含糖量较大,稀释后粘度仍然比对照溶液大,而毛细管电泳进 样时,样品溶液的粘度对进样量影响较大,溶液的粘度保持一致才能使进样量一致。后将样 品溶液稀释成0.1mg/ml,得到较满意的结果。
[作者简介] 魏玲(1965-),女,主管药师,主要从事药物分析工 作。联系电话:67017755-319。
[参考文献]
[1] Reynolds JEF ed. Martingdale-The Extra Pharmacopoeia[M].31st ed. London:Pharmaceutical Press,1996.436-437.
[2] Suryanarayana MV,Reddy BP,Krupadanam GLD, et al. HPLC determinatio n of cetirizine dihydrochloride[J].Indian Drugs, 1992, 29(13)∶605-612.
, http://www.100md.com
[3] Walily AFME, Korany MA, Gimdy AE, et al. Spectrophotometric and high performance liquid chromatographic determination of cetirizine dihydrochloride in pharmaceutical tablets[J].J Pharm Biomed Anal, 1998, 17(3)∶435-442 .
[4] Gard A, Badme N, Kaul P, et al. Estimation of cetirizine dihydrochlo ride in syrups[J].Indian Drugs, 1995, 32(8)∶ 409-415.
收稿:2000-02-29
修回:2000-04-17, http://www.100md.com
单位:魏玲 周威(厦门中山医院 厦门 361000);俞如英(中国药品生物制品检定所 北京 100050)
关键词:盐酸西替利嗪;毛细管电泳法;含量测定
中国新药杂志001010
[摘要] 目的:建立毛细管电泳法测定盐酸西替利嗪糖浆剂中 西替利嗪含量的方法。方法:以30mmol/L磷酸二氢钠(pH2.7)缓冲液为运行缓冲液, 运行电压为20kV, 检测波长为230nm。结果:盐酸西替利嗪在60~140μg/ml浓度范围内有良好的线性关系(r=0.9 993),回收率为98.4%,RSD=1.8%(n=6)。结论:毛细管电泳法可用于盐酸西替利嗪糖浆剂中西替利嗪的定量测定。
[中图分类号]R927.2 [文献标识码] B
, 百拇医药
[文章编号]1003-3734(2000)10-0694-03
Determination of cetirizine in cetirizine HCl syrup by
capillary zone electrophoresis
WEI Ling
(National Institute of Pharmaceutical and Biological Products,Beijin g 100050,China)
ZHOU Wei
(Xiamen Zhongshan Hospital,Xiamen 361000,Chi na)
, 百拇医药
YU Ru-yin
(National Institute of Pharmaceutical and Biological Products,Beijin g 100050,China)
[Abstract] Objective:To establish a capillary zone electropho retic me thod for determining cetirizine in cetirizine HCL syrup.Methods:A runn ing buffer consisted of 30 mmol/L NaH2PO4(pH2.7),a voltage of 20 kV and a UV detector at 230 nm were adopted in this methos.Results:A linear range of 60~140 μg/ml,a average recovery of 98.4% were obtained with a RSD=1.8%(n =6).Conclusion:Capillary zone electrophoresis can be used to determi ne the content of cctirizinc in cctirizinc HCL syrup.
, 百拇医药
[Key words] cetirizine hydrochloride;capillary zone electrophoresis ;assay
盐酸西替利嗪是对H1受体有选择性拮抗作用的抗组胺药, 在临床上主要用于治疗季节性 、 常年性、过敏性鼻炎以及荨麻疹[1]。盐酸西替利嗪制剂药典未收载。文献报道[2,3]用分光光度法和高效液相色谱法测定盐酸西替利嗪片剂中的西替利嗪含量 ,也有报道[4]用氯仿提取后用分光光度法测定糖浆剂中的西替利嗪含量,其他有 关西替利嗪的测定均是有关体液分析的报道,作者未见有毛细管电泳法测定盐酸西替利嗪的 文献。由印度Cipla公司进口我国的盐酸西替利嗪糖浆剂采用HPLC测定含量,由于糖浆中含 糖量高,易对色谱柱造成污染,使色谱柱使用寿命降低。本实验采用区带毛细管电泳法(CZE)测定了盐酸西替利嗪糖浆剂中的西替利嗪的含量,方法简单、快速、专属性好,分离效 率高,分析时间短,采用内标法定量,结果准确,制剂中的糖对分离无影响。
, 百拇医药
材料与方法
1 仪器与试药
SpectroPHORESIS 1000型高效毛细管电泳仪配FOCUS高速扫描紫外-可见光检测器( 美 国TSP公司),PC1000工作站(美国TSP公司)。盐酸西替利嗪对照品、盐酸西替利嗪糖浆和 空白糖浆均由印度Cipla公司提供。盐酸氯环利嗪由中国药品生物制品检定所提供。磷酸氢 二钠和磷酸均为分析纯。试验用水为二次蒸馏水。
2 实验方法
2.1 毛细管电泳分离条件 石英毛细管柱:内径50(m,总长度40cm ,有效长度32.5cm(美国Polymicro Technologic 公司),运行缓冲液为30mmol/L 磷酸氢 二钠缓冲液(用磷酸调pH值为2.7),运行电压为20kV,柱温度为20℃,检测波长为230nm, 真空进样5s,每次分析前先将毛细管柱用水清洗2min(20℃)。
, 百拇医药
2.2 线性关系 精密称取盐酸西替利嗪对照品50mg,置50 ml量瓶中,加水溶 解并稀释至刻度,制成1mg/ml的溶液,作为对照品储备溶液。精密称取盐酸氯环利嗪对照品 50mg,置50 ml量瓶中,加水溶解并稀释至刻度,制成1mg/ml的溶液,作为内标储备溶液。 精密吸取对照品储备溶液0.6, 0.8, 1.0, 1.2 和1.4ml,分别置10ml量瓶中,再分别加入内 标储备溶液1.0ml,加水稀释至刻度,摇匀,进样。以盐酸西替利嗪浓度对西替利嗪峰面积 与内标峰面积之比作线性回归,结果在60~140μg/ml浓度范围内有良好的线性关系, 回归方程为:Y=11.19X+0.06, r = 0.9993。其中,Y为盐酸西替利嗪与内标峰面积比 ,X为西替利嗪浓度((g/ml)。
2.3 回收率试验 分别精密吸取线性关系项下对照品储备溶液和内标储备溶 液各1ml,置10ml量瓶中,加入空白糖浆1.0ml,加水稀释至刻度,摇匀,作为供试品溶液 ;另分别精密吸取线性关系项下对照品储备溶液和内标储备溶液各1ml,置10ml量瓶中作为 对照溶液。分别取上述二溶液,测定。重复测定6次,以每份溶液的平均测定值与对照溶液 进行比较,计算回收率为98.4%,RSD=1.8%(n=6)。
, 百拇医药
2.4 精密度试验 取回收率试验项下的供试品溶液,按上述试验条件试验, 重复测定5次, 盐酸西替利嗪和盐酸氯环利嗪峰的迁移时间的RSD分别为0.62%和0.75%,盐酸西替利嗪和盐 酸氯环利嗪的峰面积之比的RSD为1.76%。
2.5 样品测定 精密吸取盐酸西替利嗪糖浆1.0ml,置10ml量瓶中,加入 内标溶液1.0ml,加水稀释至刻度,摇匀,制成样品溶液,测定;另分别精密吸取线 性关系项下对照品储备溶液和内标储备溶液各1ml,置10ml量瓶中作为对照溶液,同法测定, 用内标法计算盐酸西替利嗪糖浆剂中西替利嗪的含量。
结 果
1 典型分离电泳结果
见图1。

, http://www.100md.com
1 内标;2 西替利嗪
图1 盐酸西替利嗪糖浆剂毛细管电泳图
2 测定结果 3批糖浆剂,结果3批分别为(99.2±0.9)%,(100.3±0.8)%,(99.6±1 .2)%(n=3)。
讨 论
运行缓冲液的pH值和离子强度对分离测定影响较大。降低运行缓冲液 的浓度(或离子强度)能够降低运行电流,从而降低焦耳热,而增加运行缓冲液的浓度(或 离子强度)可以降低溶质有效表面电荷以减少管壁对溶质的吸附作用。
在pH为3条件下,考察了10,20,30和40mmol/L磷酸二氢钠缓冲液对分 离的影响,结果表明,在30 mmol/L条件下,溶质的有效浓度最大,同时电流也较低。
在磷酸二氢钠浓度为30mmol/L的条件下,考察了pH为2.5,3,4,5 和7时,溶质的迁移时间 的变化。随着运行缓冲液的pH值增加,西替利嗪和内标峰的迁移时间略为减小,而辅料中的 一个较大的干扰峰随pH值的增加而很快降低,当pH值>5时,该峰与盐酸西替利嗪峰几乎重叠 。这是由于随着运行缓冲液的pH值增加,盐酸西替利嗪和盐酸氯环利嗪的离子化程度降低, 有效迁移速率降低;而随着pH值的增加,电渗流增大,使分离度降低。 一般认为毛细管电泳的定量精密度比HPLC差,这是由于毛细管电泳的进样时间短(一般 为数秒),因此,难以用外标法准确定量。用内标法则可以使其定量精密度达到与HPLC相似 的水平。本实验采用盐酸氯环利嗪为内标,测定精密度小于2%,能够达到HPLC定量的要求 。
, 百拇医药
实验初期,盐酸西替利嗪浓度配制成0.5mg/ml,而使测 定的回收率低。这是由于样品含糖量较大,稀释后粘度仍然比对照溶液大,而毛细管电泳进 样时,样品溶液的粘度对进样量影响较大,溶液的粘度保持一致才能使进样量一致。后将样 品溶液稀释成0.1mg/ml,得到较满意的结果。
[作者简介] 魏玲(1965-),女,主管药师,主要从事药物分析工 作。联系电话:67017755-319。
[参考文献]
[1] Reynolds JEF ed. Martingdale-The Extra Pharmacopoeia[M].31st ed. London:Pharmaceutical Press,1996.436-437.
[2] Suryanarayana MV,Reddy BP,Krupadanam GLD, et al. HPLC determinatio n of cetirizine dihydrochloride[J].Indian Drugs, 1992, 29(13)∶605-612.
, http://www.100md.com
[3] Walily AFME, Korany MA, Gimdy AE, et al. Spectrophotometric and high performance liquid chromatographic determination of cetirizine dihydrochloride in pharmaceutical tablets[J].J Pharm Biomed Anal, 1998, 17(3)∶435-442 .
[4] Gard A, Badme N, Kaul P, et al. Estimation of cetirizine dihydrochlo ride in syrups[J].Indian Drugs, 1995, 32(8)∶ 409-415.
收稿:2000-02-29
修回:2000-04-17, http://www.100md.com