HBV S基因与IL-12基因联合免疫小鼠的免疫应答
作者:王全楚 周永兴 姚志强 冯志华
单位:王全楚(第四军医大学唐都医院传染科,陕西 西安 710038);周永兴(第四军医大学唐都医院传染科,陕西 西安 710038);姚志强(第四军医大学唐都医院传染科,陕西 西安 710038);冯志华(第四军医大学唐都医院传染科,陕西 西安 710038)
关键词:肝炎病毒;乙型;基因免;IL-12
第四军医大学学报000404 摘 要:目的 观察小鼠对IL-12基因表达质粒与HBV S基因疫苗联合免疫的免 疫 应答. 方法 用已构建的HBV S基因疫苗(pCR3.1-S)和表达IL-12 p35和p40 蛋白的真核表达载体pW RG3169分别给BALB/c小鼠多点肌肉注射,2 wk后追加免疫1次,用ELISA法及MTT 法检测小鼠 血清抗-HBs及脾细胞对HBsAg的特异性增殖反应. 结果 免疫接种2 wk后小鼠 血清抗-HBs滴度 及脾细胞对HBsAg的刺激指数均明显高于对照组,pWRG3169+pCR3.1-S组明显高于单纯pCR3. 1-S注射组. 结论 IL-12表达质粒可以增强pCR3.1-S基因疫苗诱导的体液 和细胞免疫应答强度;尤以细胞免疫增高明显.
, 百拇医药
中图号:R512.6 文献标识码:A
文章编号:1000-2790(2000)04-0402-03
Enhanced immune responses in BALB/c mice coimmunized with IL-12 gene expressi on plasmid and hepatitis B virus surface DNA-based vaccine
WANG Quan-Chu, ZHOU Yong-Xing, YAO Zhi-Qiang, FENG Zhi-Hua
(Department of Infectious Diseases, Tangdu Hospital, Fourth Military Medical University, Xi’an 710038, China)
, 百拇医药
Abstract: AIM To study enhanced immune response in mice co immunized with HB V surface DNA-based vaccine and IL-12 gene expression plasmid. METHODS The HBV surface gene was cloned into a eukaryotic expression vector (pC R3.1-S). The Balb/c mice were immunized at multiplesites by intramuscular inje ction with pCR3.1-S and IL-12 gene expression plasmid (pWRG3169). Each mouse w as boosted 2 weeks after the immunization. The anti-HBs antibody was detected b y ELISA and the sti m ulatory index of splenocytes on HBsAg was measured by MTT method. RESULTS[ WTBZ] T he titer of anti-HBs antibody and the stimulatory index of splenocytes from mic e coimmunized with pWRG3169 and PCR3.1-S was significantly higher than that of t he mice injected with pCR3.1-S alone. Antibody titer and SI of immunized mice w e re higher than those of the control group. CONCLUSION This study d emonstrates that coimmunization of IL-12 gene expression plasmid and HBV surfa ce gene can enhance humoral and cellular immune response of immunized mice.
, http://www.100md.com
Keywords:hepatitis B virus; gene immunization; interleuk in-12
0 引言
基因免疫是近几年发展起来的新的生物技术,不仅可诱导体液免疫应答,而且可诱导强 烈而 持久的细胞免疫应答[1]. 细胞因子可通过不同作用环节调节和增强DNA的免疫效应 ,发挥免 疫佐剂作用. IL-12在机体免疫功能中具有重要作用, 尤其 是对Th1/Th2平衡的影响备受关注[2]. 为探求HBV基因免疫的增强策略,我们 对 IL-12基因表达质粒与HBV S基因联合免疫的小鼠细胞和体液免疫应答进行了研究 .
1 材料和方法
1.1 材料 编码IL-12 p35和p40蛋白的真核表达载体pWR G3169由美国 R akhmilevich博士惠赠[3]. 含HBV S基因的质粒pCR3.1-S由姚志强教授在 比利时鲁汶 大学构建:以计算机设计PCR引物,从HBV患者血清(adw型)中获得HBV S基因序列,以 T-A 克隆法插入真核表达载体pCR3.1(Invitrogen公司产品),酶切、电泳,鉴定正向插入片段 ,最后得到重组质粒pCR3.1-S. 质粒的大量制备以两种质粒分别转化感受态大肠杆菌JM1 09(本室保存),筛选阳性 克隆,经LB培养基扩增,按碱裂解法提取质粒,聚乙二醇(PEG)法纯化,通过紫外分光光 度计测定其浓度,按1 g*L-1溶于无菌生理盐水中, -20℃储存备用.
, http://www.100md.com
1.2 方法 选用6~8 wk龄雌性BALB/c小鼠(本校实验动物中心提供 ),随机分为3组,S基因对照组(每次注射pCR3.1-S 100 μg)、增强组(每次注射pCR3. 1-S和pWRG3169各100 μg)、对照组(每次注射空载体pCR3.1 100 μg),每组小鼠5只. 注射前以2.5 g*L-1盐酸布比卡因100 μg预处理小鼠股四头肌,24 h 后将相应质 粒直接多点注射处理后肌肉,间隔2 wk后追加免疫1次. 不同时间间隔剪尾取血. 免疫4 wk后,处死小鼠,取小鼠脾细胞,洗涤后用含100 mL*L-1胎牛血清的RPMI 1 640培养液重悬,制成细胞悬液浓度为1×109*L-1,加入96孔板,每孔 100 μg,平行3孔,前2孔分别加入HBsAg 5 μg/孔和1∶300植物血凝素(PHA),第3孔 只加buffer,作对照. 37℃,50 mL*L-1 CO2 温育72 h,加入四甲基偶氮唑盐(MT T)10 μg,37℃继续孵 育4 h,弃去孔内培养液,每孔加入DMSO 150 μL,振荡10 min,使结晶物充分溶解,在酶 免疫检测仪上测各孔A490 nm,计算刺激指数(SI),SI=实验孔A490 nm /对照孔A490 nm. 抗-HBs抗体检测: 在HBsAg包被好的96孔ELISA软板(华美生 物技术公司)中加入生理 盐水稀释过的小鼠血清(1∶50),37℃孵育1 h,洗涤后加入HRP标记羊抗鼠IgG,洗涤,加 TMB 为底物,于波长450 nm处测ELlSA A490 nm. (ELISA仪系Bio-Rad公司产品), 以检测A490 nm/阴性对照A490 nm>=2.1为阳性.
, http://www.100md.com
2 结果
以XbaI酶切重组质粒pCR3.1-S,获得630 bp 片段,结果符合酶切图谱.
2.1 T细胞抗原特异性增殖反应 增强组除对HBsAg表 现出特异性增殖反应外,IL-12也对PHA有非特异性增殖反应(Tab 1).
表 1 小鼠脾细胞对HBsAg 增殖反应的刺激指数
Tab 1 Stimulatory index of splenocytes on HBsAg (n=5,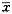 ±s)
±s)
SI
Group
, 百拇医药 HBsAg
PHA
pCR3.1-S+pWRG3169
1.9±0.6ac
1.5±0.2ac
pCR3.1-S
1.4±0.3a
1.2±0.1c
pCR3.1
0.9±0.1
1.0±0.1
, 百拇医药
aP<0.05 vs pCR3.1,cP<0.05 vs pCR3.1-S group.2.2 小鼠血清抗-HBs-IgG 2 wk后实 验组和增 强组均产生了抗-HBs特异性抗体. 免疫4 wk后增强组抗-HBs效价高于实验组( P<0.05,Fig 1).
图 1 重组质粒免疫小鼠血清的抗HBs效价
Fig 1 Serum antiHBs titers of mice immunized with pCR3.1-S, p WRG3169 plus pCR3.1-S or pCR3.1
3 讨论
IL-12是目前认为的作用免疫细胞范围最广、作用最强的细胞素. 它对免疫应答的调节 是通 过促进Th1细胞的形成及分泌细胞因子而刺激T细胞的分化增殖,促进CTL,LAK细胞等的形成 ,从而增强机体对病原体的杀伤及清除作用. 我们的实验结果表明,编码IL-12的表达质粒 可以提高pCR3.1-S诱导的体液和细胞免疫强度,尤以后者为甚. 这与Chow等[4]报 告的结果 一致,但与Kim研究结论相反. 产生这种差异的原因还不清楚,可能与重组表 达载体在体内 转染细胞类型不同及IL-12在体内的表达量和生物活性不同有关. Chow[4]将5种含 细胞因子编 码基因的重组表达载体(pIL-12 pIL-4,pIL-2,pIFN-r,pGM-CSF)分别与含HBsAg编码 基因的 重组表达载体一起肌注小鼠,发现5种细胞因子的重组表达载体均使抗-HBs的IgG抗体产生 增加(pIFN-R除外). Kim等[5]将IL-12基因生编码人类免疫缺陷病毒1抗原的 基因一同免疫 动物,发现特异性抗体应答降低,而T 细胞增殖反应和抗原特异性细胞毒活性明显增强. 这 种特异性的细胞免疫应答不仅对预防乙型肝炎病毒感染具有保护作用,而且对慢性病毒感染 具有治疗和清除作用. MacGregor等[6]率先将基因疫苗用于艾滋病的临床治疗,15 例无症状 AIDS患者均产生特异性体液免疫,部分表现出较强的CTL反应和淋巴细胞增殖活性. 如何充 分利用IL-12的细胞免疫增强作用,将基因免疫过渡到慢性乙型肝炎患者的临床治疗,将是 今后努力的一个方向.
, http://www.100md.com
基金项目:国家自然科学基金资助项目(39770065)
作者简介:王全楚(1966-),男(汉族),湖北省云梦县人. 主治医师,硕士,已发表论文30篇. 现工作单位:河南郑州153医院传染科. Tel.( 029)3577595
参考文献:
[1] Schirmbeck R,Bohm W,Ando K et al. Nucleic acid vaccinati on primes hepatit is B virus surface antigen specific cytotoxic. T Lymphocytes in nonresponder mic e[J]. J Virol, 1995;69(10):5929-5934.
[2] Gately MK, Renzetti LM, Magram J et al. The interleukin-1 2/interleukin-12 receptor system: Role in normal and pathologic immune responses[J]. Annu R ev lmmunol, 1998;16:495-517.
, http://www.100md.com
[3] Rakhmilevich AL, Turner J, Ford MJ et al. Gene gun-mediate d skin transfec tion with interleukin12 gene results in regression of established primary and me tastic murine tumors[J]. Proc Natl Sci USA,1996;93(13):6291-6296.
[4] Chow YH, Chiang BL, Lee YL et al. Development of Th1 and Th 2 populations a nd the nature of immune response to hepatitis B virus DNA vaccine can be modula ted by codelivery of various cytokine genes[J]. J lmmunol, 1998;160(3):132 0-1329.
, 百拇医药
[5] Kim JJ, Ayyavoo V, Bagarazzi ML et al. In vivo engineering of a cellular immune response by coadministration of IL-12 expression vector with a DNA imm unogen[J]. J Immunol,1997;158(2):816-823.
[6] MacGregor RR, Boyer JD, Ugen KE et al. First human trial o f a DNA-based vaccine for treatment of human immunodeficiency virus type 1 infection: Safety and host response[J]. J Infect Dis,1998;178(1):92-100.
收稿日期:1999-08-27; 修回日期:1999-10-19, http://www.100md.com
单位:王全楚(第四军医大学唐都医院传染科,陕西 西安 710038);周永兴(第四军医大学唐都医院传染科,陕西 西安 710038);姚志强(第四军医大学唐都医院传染科,陕西 西安 710038);冯志华(第四军医大学唐都医院传染科,陕西 西安 710038)
关键词:肝炎病毒;乙型;基因免;IL-12
第四军医大学学报000404 摘 要:目的 观察小鼠对IL-12基因表达质粒与HBV S基因疫苗联合免疫的免 疫 应答. 方法 用已构建的HBV S基因疫苗(pCR3.1-S)和表达IL-12 p35和p40 蛋白的真核表达载体pW RG3169分别给BALB/c小鼠多点肌肉注射,2 wk后追加免疫1次,用ELISA法及MTT 法检测小鼠 血清抗-HBs及脾细胞对HBsAg的特异性增殖反应. 结果 免疫接种2 wk后小鼠 血清抗-HBs滴度 及脾细胞对HBsAg的刺激指数均明显高于对照组,pWRG3169+pCR3.1-S组明显高于单纯pCR3. 1-S注射组. 结论 IL-12表达质粒可以增强pCR3.1-S基因疫苗诱导的体液 和细胞免疫应答强度;尤以细胞免疫增高明显.
, 百拇医药
中图号:R512.6 文献标识码:A
文章编号:1000-2790(2000)04-0402-03
Enhanced immune responses in BALB/c mice coimmunized with IL-12 gene expressi on plasmid and hepatitis B virus surface DNA-based vaccine
WANG Quan-Chu, ZHOU Yong-Xing, YAO Zhi-Qiang, FENG Zhi-Hua
(Department of Infectious Diseases, Tangdu Hospital, Fourth Military Medical University, Xi’an 710038, China)
, 百拇医药
Abstract: AIM To study enhanced immune response in mice co immunized with HB V surface DNA-based vaccine and IL-12 gene expression plasmid. METHODS The HBV surface gene was cloned into a eukaryotic expression vector (pC R3.1-S). The Balb/c mice were immunized at multiplesites by intramuscular inje ction with pCR3.1-S and IL-12 gene expression plasmid (pWRG3169). Each mouse w as boosted 2 weeks after the immunization. The anti-HBs antibody was detected b y ELISA and the sti m ulatory index of splenocytes on HBsAg was measured by MTT method. RESULTS[ WTBZ] T he titer of anti-HBs antibody and the stimulatory index of splenocytes from mic e coimmunized with pWRG3169 and PCR3.1-S was significantly higher than that of t he mice injected with pCR3.1-S alone. Antibody titer and SI of immunized mice w e re higher than those of the control group. CONCLUSION This study d emonstrates that coimmunization of IL-12 gene expression plasmid and HBV surfa ce gene can enhance humoral and cellular immune response of immunized mice.
, http://www.100md.com
Keywords:hepatitis B virus; gene immunization; interleuk in-12
0 引言
基因免疫是近几年发展起来的新的生物技术,不仅可诱导体液免疫应答,而且可诱导强 烈而 持久的细胞免疫应答[1]. 细胞因子可通过不同作用环节调节和增强DNA的免疫效应 ,发挥免 疫佐剂作用. IL-12在机体免疫功能中具有重要作用, 尤其 是对Th1/Th2平衡的影响备受关注[2]. 为探求HBV基因免疫的增强策略,我们 对 IL-12基因表达质粒与HBV S基因联合免疫的小鼠细胞和体液免疫应答进行了研究 .
1 材料和方法
1.1 材料 编码IL-12 p35和p40蛋白的真核表达载体pWR G3169由美国 R akhmilevich博士惠赠[3]. 含HBV S基因的质粒pCR3.1-S由姚志强教授在 比利时鲁汶 大学构建:以计算机设计PCR引物,从HBV患者血清(adw型)中获得HBV S基因序列,以 T-A 克隆法插入真核表达载体pCR3.1(Invitrogen公司产品),酶切、电泳,鉴定正向插入片段 ,最后得到重组质粒pCR3.1-S. 质粒的大量制备以两种质粒分别转化感受态大肠杆菌JM1 09(本室保存),筛选阳性 克隆,经LB培养基扩增,按碱裂解法提取质粒,聚乙二醇(PEG)法纯化,通过紫外分光光 度计测定其浓度,按1 g*L-1溶于无菌生理盐水中, -20℃储存备用.
, http://www.100md.com
1.2 方法 选用6~8 wk龄雌性BALB/c小鼠(本校实验动物中心提供 ),随机分为3组,S基因对照组(每次注射pCR3.1-S 100 μg)、增强组(每次注射pCR3. 1-S和pWRG3169各100 μg)、对照组(每次注射空载体pCR3.1 100 μg),每组小鼠5只. 注射前以2.5 g*L-1盐酸布比卡因100 μg预处理小鼠股四头肌,24 h 后将相应质 粒直接多点注射处理后肌肉,间隔2 wk后追加免疫1次. 不同时间间隔剪尾取血. 免疫4 wk后,处死小鼠,取小鼠脾细胞,洗涤后用含100 mL*L-1胎牛血清的RPMI 1 640培养液重悬,制成细胞悬液浓度为1×109*L-1,加入96孔板,每孔 100 μg,平行3孔,前2孔分别加入HBsAg 5 μg/孔和1∶300植物血凝素(PHA),第3孔 只加buffer,作对照. 37℃,50 mL*L-1 CO2 温育72 h,加入四甲基偶氮唑盐(MT T)10 μg,37℃继续孵 育4 h,弃去孔内培养液,每孔加入DMSO 150 μL,振荡10 min,使结晶物充分溶解,在酶 免疫检测仪上测各孔A490 nm,计算刺激指数(SI),SI=实验孔A490 nm /对照孔A490 nm. 抗-HBs抗体检测: 在HBsAg包被好的96孔ELISA软板(华美生 物技术公司)中加入生理 盐水稀释过的小鼠血清(1∶50),37℃孵育1 h,洗涤后加入HRP标记羊抗鼠IgG,洗涤,加 TMB 为底物,于波长450 nm处测ELlSA A490 nm. (ELISA仪系Bio-Rad公司产品), 以检测A490 nm/阴性对照A490 nm>=2.1为阳性.
, http://www.100md.com
2 结果
以XbaI酶切重组质粒pCR3.1-S,获得630 bp 片段,结果符合酶切图谱.
2.1 T细胞抗原特异性增殖反应 增强组除对HBsAg表 现出特异性增殖反应外,IL-12也对PHA有非特异性增殖反应(Tab 1).
表 1 小鼠脾细胞对HBsAg 增殖反应的刺激指数
Tab 1 Stimulatory index of splenocytes on HBsAg (n=5,
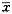 ±s)
±s)SI
Group
, 百拇医药 HBsAg
PHA
pCR3.1-S+pWRG3169
1.9±0.6ac
1.5±0.2ac
pCR3.1-S
1.4±0.3a
1.2±0.1c
pCR3.1
0.9±0.1
1.0±0.1
, 百拇医药
aP<0.05 vs pCR3.1,cP<0.05 vs pCR3.1-S group.2.2 小鼠血清抗-HBs-IgG 2 wk后实 验组和增 强组均产生了抗-HBs特异性抗体. 免疫4 wk后增强组抗-HBs效价高于实验组( P<0.05,Fig 1).

图 1 重组质粒免疫小鼠血清的抗HBs效价
Fig 1 Serum antiHBs titers of mice immunized with pCR3.1-S, p WRG3169 plus pCR3.1-S or pCR3.1
3 讨论
IL-12是目前认为的作用免疫细胞范围最广、作用最强的细胞素. 它对免疫应答的调节 是通 过促进Th1细胞的形成及分泌细胞因子而刺激T细胞的分化增殖,促进CTL,LAK细胞等的形成 ,从而增强机体对病原体的杀伤及清除作用. 我们的实验结果表明,编码IL-12的表达质粒 可以提高pCR3.1-S诱导的体液和细胞免疫强度,尤以后者为甚. 这与Chow等[4]报 告的结果 一致,但与Kim研究结论相反. 产生这种差异的原因还不清楚,可能与重组表 达载体在体内 转染细胞类型不同及IL-12在体内的表达量和生物活性不同有关. Chow[4]将5种含 细胞因子编 码基因的重组表达载体(pIL-12 pIL-4,pIL-2,pIFN-r,pGM-CSF)分别与含HBsAg编码 基因的 重组表达载体一起肌注小鼠,发现5种细胞因子的重组表达载体均使抗-HBs的IgG抗体产生 增加(pIFN-R除外). Kim等[5]将IL-12基因生编码人类免疫缺陷病毒1抗原的 基因一同免疫 动物,发现特异性抗体应答降低,而T 细胞增殖反应和抗原特异性细胞毒活性明显增强. 这 种特异性的细胞免疫应答不仅对预防乙型肝炎病毒感染具有保护作用,而且对慢性病毒感染 具有治疗和清除作用. MacGregor等[6]率先将基因疫苗用于艾滋病的临床治疗,15 例无症状 AIDS患者均产生特异性体液免疫,部分表现出较强的CTL反应和淋巴细胞增殖活性. 如何充 分利用IL-12的细胞免疫增强作用,将基因免疫过渡到慢性乙型肝炎患者的临床治疗,将是 今后努力的一个方向.
, http://www.100md.com
基金项目:国家自然科学基金资助项目(39770065)
作者简介:王全楚(1966-),男(汉族),湖北省云梦县人. 主治医师,硕士,已发表论文30篇. 现工作单位:河南郑州153医院传染科. Tel.( 029)3577595
参考文献:
[1] Schirmbeck R,Bohm W,Ando K et al. Nucleic acid vaccinati on primes hepatit is B virus surface antigen specific cytotoxic. T Lymphocytes in nonresponder mic e[J]. J Virol, 1995;69(10):5929-5934.
[2] Gately MK, Renzetti LM, Magram J et al. The interleukin-1 2/interleukin-12 receptor system: Role in normal and pathologic immune responses[J]. Annu R ev lmmunol, 1998;16:495-517.
, http://www.100md.com
[3] Rakhmilevich AL, Turner J, Ford MJ et al. Gene gun-mediate d skin transfec tion with interleukin12 gene results in regression of established primary and me tastic murine tumors[J]. Proc Natl Sci USA,1996;93(13):6291-6296.
[4] Chow YH, Chiang BL, Lee YL et al. Development of Th1 and Th 2 populations a nd the nature of immune response to hepatitis B virus DNA vaccine can be modula ted by codelivery of various cytokine genes[J]. J lmmunol, 1998;160(3):132 0-1329.
, 百拇医药
[5] Kim JJ, Ayyavoo V, Bagarazzi ML et al. In vivo engineering of a cellular immune response by coadministration of IL-12 expression vector with a DNA imm unogen[J]. J Immunol,1997;158(2):816-823.
[6] MacGregor RR, Boyer JD, Ugen KE et al. First human trial o f a DNA-based vaccine for treatment of human immunodeficiency virus type 1 infection: Safety and host response[J]. J Infect Dis,1998;178(1):92-100.
收稿日期:1999-08-27; 修回日期:1999-10-19, http://www.100md.com