ά����Գ���άϸ�����õ�����۲�
���ߣ���ά�� ���� ������ ����� �Ź��� ���� ���ǻ� ��Խ�
��λ��100041 �й�ҽѧ��ѧԺ�й�Э��ҽ�ƴ�ѧ�������ҽԺ(��ά�������ȣ������壬������ǻۣ���Խ�)��������(�Ź���)���й�ҽѧ��ѧԺҩ���о���(�����)
�ؼ��ʣ�ά�������άϸ����3HTdR������
�л�ҽѧ������־980407 ��ժҪ�� Ŀ�� ̽��ά���������۵����û������������ٴ��Ŀ����ԡ����� ���ó���άϸ��������������������3HTdR(������ऺ���)�������άϸ��DNA�У��о�ά�����������������άϸ��������ֳ��DNA�ϳɼ����ṹ��Ӱ�졣��� ά����Գ���άϸ��������ֳ��DNA�ϳ��в�ͬ�̶ȵ��������ã��ʼ���ЧӦ��ϵ��ɨ��羵����羵�۲���ʾ��ά����Գ���άϸ���ϳɽ�ԭ���������á����� ά���������۵����û������������Ƴ���άϸ��������ֳ�����ֳ���άϸ��DNA�ϳɼ�Ӱ�����άϸ����ԭ�ϳ��йء�
, http://www.100md.com
The effect of retinoic acid on fibroblast in vitro culture Song Weiming, Sun Guangci, Guan Zhengyu,et at. Plastic Surgery Hospital, China Academy of Medical Sciences and Peking Union Medical College. Beijing 100041
��Abstract�� Objective To investigate the possible mechanism of retinoic acid used for the treatment of scar, and clarifying its possibilities in the application of treatment of scar. Methods The effect of retinoic acid on growth proliferation, DNA synthesis and ultrastructure of fibroblasts was studied by means of the techniques of the fibroblast in vitro culture and the 3HTdR incorporation into DNA of fibroblasts. Results The results demonstrated that retinoic acid inhibits the growth proliferation and DNA synthesis of fibroblasts in vitro culture and a dose-dependent relationship between growth proliferation, DNA synethesis of fibroblasts and retinoic acid concentration was observed. Electron microscopic observateion (SEM and TEM) showed that fibrous substances on the cell surface and outside the cell had decreased. All the results indicated that retinoic acid inhibits collagen synthesis of fibroblasts. Conclusion The mechanism of retinoic acid used for the treatment of scar have a bearing on the inhibitation of growth proliferation, interruption of DNA synthesis and interference of collagen synthesis of the fibroblasts.
, ��Ĵҽҩ
��Key words�� Retinoic acid Fibroblast 3H-TdR Scar
�������ϵ��о��������������ۺ��۸������ɳ���άϸ�����µĽ�ԭ�����ϳɺͳ�������[1]����ˣ������������о������ó���άϸ������������ͨ������������������о�����άϸ����������ֳ����ԭ�ϳɵ�ϸ�������Ӱ�����أ���ϸ��ˮƽ�ϲ������γ����������ĵ� �ػ���[2��3]��ά����(Retinoic Acid,RA)��ά����A�����ҩ����й㷺��ҩ������[4��5��6]���������������յ�һ�����ٴ�Ч��[7��8]��Ϊ̽��RA�����۵����û����������о���RA��������������άϸ����Ӱ�졣
���Ϻͷ���
һ��ҩƷ���Լ���RA���й�ҽѧ��ѧԺҩ���о����ṩ��MEM Eagle ������ϵ����GIBC��˾��Ʒ���ȵ����ἰTritonX100Ϊ�¹�Merck��˾����������ţѪ��Ϊ����Ʒ��3HTdR Ϊ�й�ԭ���ܿ�ѧ�о�Ժ��Ʒ��PPO��PoPoPΪ�Ϻ��Լ�һ����Ʒ����ἰEpon812Ϊ����SERVA��˾������
, http://www.100md.com
��������άϸ���������������г���Ƥ������������Ưϴ�����飬���ں�20 %����ţѪ���MEM Eagle ����Һ�У���37 �� ����5 %CO2���������������������ܵ������0.2 %�ȵ���ø���������������ڿ��е��ǵ�5��25��[9]��
��������άϸ��������ֳ��ȡ��7��15���Ķ���������ϸ����ÿ������ƿ����8��104��������24Сʱ������ԭ����Һ��ʵ������벻ͬŨ�ȵ�RA(10-5-10-8mol/L)���ֱ���1��2��3��4��6��ʱ������ϸ��������ȡ����ʱ����ͬδ��ҩ��ϸ����Ϊ���գ�ÿ��ʵ���ҩ��Ũ����3���ظ���Ʒ��ÿ��ʵ���ظ�3�Σ�ȡ������
�ġ�3HTdR���룺ȡ��7��9���Ķ���������ϸ��������ϸ��ҺŨ��Ϊ6��104/ml��������24��ϸ�������壬ÿ��ϸ����Һ1.5 ml����37 �棬��5 %CO2������������������24Сʱ������ԭ����Һ�������黻����ҩ�������Һ����ҩ�黻����ʵ���������Ũ�ȵĺ�ҩ����Һ��ÿ��1.5 ml���ں�����Ũ��Ϊ37 KBg/ml(I��Ci/ml)��3HTdR��ÿһҩ��Ũ�ȼ�������5��ƽ�пס���������24Сʱ��������������δ�����3HTdR����������DHank��sҺϴ��3�Σ�ÿ����0.1N��NaOH 1ml�������·���30���ӣ�ȡ0.5 ml������˸Һ(PPO 2.8g,PoPoP 0.05 g,���ױ�334 ml��Triton X100 116 ml)��Beckman Һ����LS8000���з�����Լ�����
, ��Ĵҽҩ
�塢ϸ�����ṹ��ȡ��7��11���Ķ���������ϸ����ɨ��羵����2��105/ƿ�����ڴ��ǵ�����ƿ�ڣ���羵����2��105/ƿ�����ڲ����ǵ�����ƿ�ڣ�����24Сʱ��ѡϸ������������Һ����ʵ�顣ɨ��羵����羵ʵ�����Ϊ�������ҩ�顣��ҩ��ֱ�Ӻ�����Ũ��Ϊ30 ��g/ml��RA������ҩ��Ϊ���գ���������3���ɨ��羵����羵������
1.ɨ��羵�걾�Ʊ����Dz�Ƭ�ı걾����DHank��sҺ��ϴ ������2.5 %���ȩ��1 %���̶��������0.1 M���Ỻ��Һ��˫��ˮ��ϴ�����ϵ�е���Ũ�ȵľƾ���ˮ��CO2�ٽ�������ӽ���ƽ�Ȼ��������S520��ɨ��羵�¹۲졣
2.��羵�걾�Ʊ���������ƿ�ڵ�ϸ������Ƥ���ӽ�ϸ��������£��ռ������Ĺ��У��������ռ�ϸ������2.5 % ���ȩ�̶� ��0.1 M���Ỻ��Һ��ϴ������1 %���̶���˫��ˮ��ϴ �������ϵ�е���Ũ�ȵı�ͪ��ˮ��Epon812����LKB������Ƭ����Ƭ�������ƺ��۴���Ǧ˫Ⱦ��Ȼ��������H600����羵�¹۲졣
, ��Ĵҽҩ
�� ��
һ��RA�Գ���άϸ����������������
1.RA��ͬ����������(ͼ1)������RAŨ�ȶ�Ϊ10-6��10-8mol/L,�۲�����6��Գ���άϸ����������Ӱ�졣���������RA�Գ���άϸ���������������ã���ҩ��Ũ�ȵ����߶���ǿ���ʼ���ЧӦ��ϵ��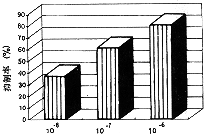
ͼ1 RA��ͬ����Ũ�ȶԳ���άϸ����Ӱ��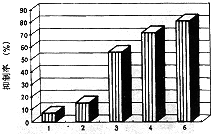
ͼ2 RA��ͬ����ʱ��Գ���άϸ����Ӱ��
2.RA��ͬʱ�������(ͼ2)����RAŨ�ȶ�Ϊ10-6mol/L,�ֱ�۲�1��2��3��4��6��5����ͬʱ�����άϸ����������Ӱ�졣�����ʾ��RA�Գ���άϸ���������������ã���ҩ������ʱ����ӳ�����ǿ����ʱ��ЧӦ��ϵ��
, ��Ĵҽҩ
����RA�Գ���άϸ��DNA�ϳɵ�Ӱ��
��DNA��л��ǰ������3HTdR�������άϸ��DNA�У��۲�ϸ����DNA�ϳ�ˮƽ�������������ʵ������ʾ������RAŨ�����ӣ�3HTdR�����½���3HTdR�����������������ʼ���ЧӦ��ϵ��������RA�����£�����άϸ��DNA�ϳɼ��٣�����������״̬��
����RA�Գ���άϸ�����ṹ��Ӱ��
1.ɨ��羵�۲�(ͼ3)����ɨ��羵�¸�ҩ�����άϸ��������ά״���ʺ���״ͻ�����Լ��٣���������Ϊ��ͺ��
�����飬ɨ��羵��3 000
, ��Ĵҽҩ
ά�����飬��羵��1 200
ͼ3 ����άϸ��ɨ��羵�۲�
���������άϸ������ɼ�������ά״���ʲ���֯����״��ά���������άϸ��������ά״���ʼ��ټ���
2.��羵�۲�(ͼ4)������羵�¸�ҩ�����άϸ�������Ĵ������������Լ��٣������������������ţ�ǻ��������ϡ�٣��е��������ݻ��������������ϵĺ˵������в�ͬ�̶ȵ��ѿ����ͽ���������������ͻ���ݻ�����Ĥ�ڲ����С�����Լ��٣���Ĥ������ʷ����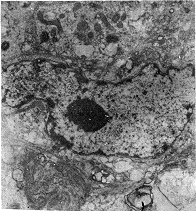
�����飬ɨ��羵��3 000
ά�����飬��羵��1 200
, ��Ĵҽҩ
ͼ4 ����άϸ����羵�۲�
���������άϸ�������ھ��зḻ�Ĵ����������������壻ά���������άϸ�����ڴ����������������ţ��������ݻ����������ѿ����ͽ�ۣ����������ͣ����ݻ���
�� ��
�۵��γ��Ǵ������ϵĽ�����˿��������������ӣ��;ֲ�ϸ������ѧ���ԣ���Ҫȡ���ڣ������õ���Ƥϸ��������Ǩ�ƺ��ǣ��ڳ���άϸ�������ϳɽ�ԭ�ij����ͽ���������άϸ���ɷ�Ϊ�ϳ��ͺ������͡��������о���Ϊ���۵��������������ڳ���άϸ�������Ľ��[10]����ˣ����ڴ������Ϲ�����ʹ��ij��ҩ����ܴ�ʹ��Ƥϸ����ֳ�ֻ��������ʵ����Ƴ�(��)��άϸ���Ĺ�����ֳ�ͻ��ԣ���Ӧ�ﵽ�ٽ��˿����ϲ���ֹ�����������������á�
����άϸ���Ǻϳɽ�ԭ����Ҫϸ��������άϸ���ϳ�����ڽ�ԭ��������ǿ�����άϸ���Ĵ�����ֳ�������ܵ��½�ԭ����������[11]���������룬����άϸ���Ĵ�����ֳ��Ȼ�ᵼ�½�ԭ�Ĺ��������������ϳ���άϸ����������ֳ��������ֹ�۵ķ����뷢չ��
, ��Ĵҽҩ
������ϸ��ѧ�����ﻯѧ�о�����[12]����ԭ�������ڳ���άϸ���Ĵ����������ںϳɣ�������������������������˵����干ͬ�γɵ�һ�����ϻ��ܵ�λ����ϸ����������ϳɵ���Ҫ���ء�����֤ʵ[13]������άϸ�������������ϵĺ˵������ǽ�ԭ����ǰ��ϳɵij���������֤�����ֺϳ����ò����ڵ����˵������ϣ������ڶ�ۺ˵������Ͻ��С����ԣ��˵�������������Ĥ�ϵĸ��š������Լ��������Ľṹ�仯���Խ�ԭ���ĺϳɹ��ܾ�����Ҫ���塣
���о������������ҩ�����άϸ���������Լ��٣�ϸ����������������RA��ʱ�䡢������ЧӦ��ϵ��3HTdR�������������ơ��羵�۲���ʾ����ҩ��ϸ����̬�����Ա仯������Ϊ�����������ϵĶ�ۺ˵������ѿ����ͽ�ۣ����������ųɴ� С���ȵ����ݣ�������������ϡ�ٻ����������ϸ�������ϸ��������ά״��������٣�����ͻ������١�˵��RA���Ե�Ӱ�����άϸ���������ͺ˵����壬ͨ���Ե����ʺϳɹ��̵����ã����ƽ�ԭ�����ɣ�����۲쵽RA���������Ӱ��Ҳ�����ԡ���������ϸ������������л�����ģ��ϳɷ�Ӧ��Ҫ��������ˣ�ͨ����һ;��Ҳ��Ӱ�쵽����άϸ���ϳɽ�ԭ���Ĺ��ܡ��ݴ��Ʋ⣬RA�����۵����û������������Ƴ���άϸ��������ֳ�����ֳ���άϸ����DNA�ϳɼ�Ӱ�콺ԭ�ĺϳ��йء�
, ��Ĵҽҩ
Ȼ�����۵��γɼ��临�ӣ�RA�����ڵ�ʵ������ѧ�����У��Ƿ�Ҳ��������ʵ����ֳ���������ԣ������һ���о�������RA�����۵����û��������Ƕ���[14]��Ҫ��ȫ���������д�����̽�֡�
���� RA�Գ���άϸ��3HTdR�����Ӱ�� Ũ��
(mol/L)
cpm
( )
)
������(%)
(������-ʵ����)/������X100%
Pֵ
, ��Ĵҽҩ
������
2274��270
10-7
563��157
75.2
<0.01
10-6
449��196
80.3
<0.01
10-5
418��76
, ��Ĵҽҩ
81.6
<0.01
10-4
341��39
85.0
<0.01
���о����ɱ����й�ҽѧ��ѧԺ����ҽѧ�о���ϸ�����������ף����������Ѻ�ҽԺ�羵�ҹ�Ψ��ʢ��졢��ʯ������������ش���л��
������������������������
�����
1 Diegelmann R F, Cohen I D, McCoy B J. Growth kinetics and collagen synthesis of normal skin, normal scar and keloid fibrolasts in vitro. J Cell Physiol, 1979,98:341346.
, ��Ĵҽҩ
2 Mooy L S, Tan EML, Holness R, et al. Effects of phenytoin on collagen metabolism and growth of skin fibroblast in culture. Clin Res, 1983, 31:22A.
3 Datubo-Brown D D, Blight A. Inhibition of human fibroblast growth in vitro by a snake oil. Br J Plast Surg, 1990,43:183186.
4 Orfanos C E, Ehlert R, Gollnick H. The retinoids: A review of their clinical pharmacology and therapeutic use. Drugs, 1987,34:459503.
, http://www.100md.com
5 Martin S, Tallman M D, Peter H, et al. Retinoids in cancer treatment. J Clin Pharmacol, 1992,32:868873.
6 De Luca L M, Darwiche N, Jones C S, et al.Retinoids in differen tiation and neoplasia. Sci Am Sci Med, 1995,2:2837.
7 Panabiere-Castaings M H. Retinoic acid in the treatment of keloids. J Dermatol Surg Oncol, 1988,14:12751276.
8 Daly T J, Golitz L E, Weston M L. A double-blind placebo controlled efficacy study tretinoin cream 0.05 % in the treatment of keloids and hypertrophic scars. Clin Res, 1986,34:159A.
, http://www.100md.com
9 Heckman C A, Vroman L, Pitlick A. The nature of substrate attached materials in human fibroblast cultures: Localization of cell and fetal calf serum components. Tissue and cell 1977,9:317334.
10 Gabbiani G,Hirschel B J,Ryan G B,et al.Granulation tissue as a contractile organ:A study of structure and function.J Exp Med,1972,135:719728.
11 Cohen I K, McCoy B J.The biloogy and control of surface overhealing. World J Surg, 1980, 4:289295.
, ��Ĵҽҩ
12 ��������.����ҽѧ���ṹ�������������.��������ѧ�����磬1984.346354.
13 Hay E D. Extracellular matrix. J Cell Biol,1981,91:205223.
14 Sung L H, Tsuchihashi M. Tenshin S, et al. Effect of retinoic acid on contraction of collagen gel induced by fibroblasts. Biochem Biophys Res Commun, 1994,205:455459.
(�ո壺1997-12-17 �أ�1998-07-17), ��Ĵҽҩ
��λ��100041 �й�ҽѧ��ѧԺ�й�Э��ҽ�ƴ�ѧ�������ҽԺ(��ά�������ȣ������壬������ǻۣ���Խ�)��������(�Ź���)���й�ҽѧ��ѧԺҩ���о���(�����)
�ؼ��ʣ�ά�������άϸ����3HTdR������
�л�ҽѧ������־980407 ��ժҪ�� Ŀ�� ̽��ά���������۵����û������������ٴ��Ŀ����ԡ����� ���ó���άϸ��������������������3HTdR(������ऺ���)�������άϸ��DNA�У��о�ά�����������������άϸ��������ֳ��DNA�ϳɼ����ṹ��Ӱ�졣��� ά����Գ���άϸ��������ֳ��DNA�ϳ��в�ͬ�̶ȵ��������ã��ʼ���ЧӦ��ϵ��ɨ��羵����羵�۲���ʾ��ά����Գ���άϸ���ϳɽ�ԭ���������á����� ά���������۵����û������������Ƴ���άϸ��������ֳ�����ֳ���άϸ��DNA�ϳɼ�Ӱ�����άϸ����ԭ�ϳ��йء�
, http://www.100md.com
The effect of retinoic acid on fibroblast in vitro culture Song Weiming, Sun Guangci, Guan Zhengyu,et at. Plastic Surgery Hospital, China Academy of Medical Sciences and Peking Union Medical College. Beijing 100041
��Abstract�� Objective To investigate the possible mechanism of retinoic acid used for the treatment of scar, and clarifying its possibilities in the application of treatment of scar. Methods The effect of retinoic acid on growth proliferation, DNA synthesis and ultrastructure of fibroblasts was studied by means of the techniques of the fibroblast in vitro culture and the 3HTdR incorporation into DNA of fibroblasts. Results The results demonstrated that retinoic acid inhibits the growth proliferation and DNA synthesis of fibroblasts in vitro culture and a dose-dependent relationship between growth proliferation, DNA synethesis of fibroblasts and retinoic acid concentration was observed. Electron microscopic observateion (SEM and TEM) showed that fibrous substances on the cell surface and outside the cell had decreased. All the results indicated that retinoic acid inhibits collagen synthesis of fibroblasts. Conclusion The mechanism of retinoic acid used for the treatment of scar have a bearing on the inhibitation of growth proliferation, interruption of DNA synthesis and interference of collagen synthesis of the fibroblasts.
, ��Ĵҽҩ
��Key words�� Retinoic acid Fibroblast 3H-TdR Scar
�������ϵ��о��������������ۺ��۸������ɳ���άϸ�����µĽ�ԭ�����ϳɺͳ�������[1]����ˣ������������о������ó���άϸ������������ͨ������������������о�����άϸ����������ֳ����ԭ�ϳɵ�ϸ�������Ӱ�����أ���ϸ��ˮƽ�ϲ������γ����������ĵ� �ػ���[2��3]��ά����(Retinoic Acid,RA)��ά����A�����ҩ����й㷺��ҩ������[4��5��6]���������������յ�һ�����ٴ�Ч��[7��8]��Ϊ̽��RA�����۵����û����������о���RA��������������άϸ����Ӱ�졣
���Ϻͷ���
һ��ҩƷ���Լ���RA���й�ҽѧ��ѧԺҩ���о����ṩ��MEM Eagle ������ϵ����GIBC��˾��Ʒ���ȵ����ἰTritonX100Ϊ�¹�Merck��˾����������ţѪ��Ϊ����Ʒ��3HTdR Ϊ�й�ԭ���ܿ�ѧ�о�Ժ��Ʒ��PPO��PoPoPΪ�Ϻ��Լ�һ����Ʒ����ἰEpon812Ϊ����SERVA��˾������
, http://www.100md.com
��������άϸ���������������г���Ƥ������������Ưϴ�����飬���ں�20 %����ţѪ���MEM Eagle ����Һ�У���37 �� ����5 %CO2���������������������ܵ������0.2 %�ȵ���ø���������������ڿ��е��ǵ�5��25��[9]��
��������άϸ��������ֳ��ȡ��7��15���Ķ���������ϸ����ÿ������ƿ����8��104��������24Сʱ������ԭ����Һ��ʵ������벻ͬŨ�ȵ�RA(10-5-10-8mol/L)���ֱ���1��2��3��4��6��ʱ������ϸ��������ȡ����ʱ����ͬδ��ҩ��ϸ����Ϊ���գ�ÿ��ʵ���ҩ��Ũ����3���ظ���Ʒ��ÿ��ʵ���ظ�3�Σ�ȡ������
�ġ�3HTdR���룺ȡ��7��9���Ķ���������ϸ��������ϸ��ҺŨ��Ϊ6��104/ml��������24��ϸ�������壬ÿ��ϸ����Һ1.5 ml����37 �棬��5 %CO2������������������24Сʱ������ԭ����Һ�������黻����ҩ�������Һ����ҩ�黻����ʵ���������Ũ�ȵĺ�ҩ����Һ��ÿ��1.5 ml���ں�����Ũ��Ϊ37 KBg/ml(I��Ci/ml)��3HTdR��ÿһҩ��Ũ�ȼ�������5��ƽ�пס���������24Сʱ��������������δ�����3HTdR����������DHank��sҺϴ��3�Σ�ÿ����0.1N��NaOH 1ml�������·���30���ӣ�ȡ0.5 ml������˸Һ(PPO 2.8g,PoPoP 0.05 g,���ױ�334 ml��Triton X100 116 ml)��Beckman Һ����LS8000���з�����Լ�����
, ��Ĵҽҩ
�塢ϸ�����ṹ��ȡ��7��11���Ķ���������ϸ����ɨ��羵����2��105/ƿ�����ڴ��ǵ�����ƿ�ڣ���羵����2��105/ƿ�����ڲ����ǵ�����ƿ�ڣ�����24Сʱ��ѡϸ������������Һ����ʵ�顣ɨ��羵����羵ʵ�����Ϊ�������ҩ�顣��ҩ��ֱ�Ӻ�����Ũ��Ϊ30 ��g/ml��RA������ҩ��Ϊ���գ���������3���ɨ��羵����羵������
1.ɨ��羵�걾�Ʊ����Dz�Ƭ�ı걾����DHank��sҺ��ϴ ������2.5 %���ȩ��1 %���̶��������0.1 M���Ỻ��Һ��˫��ˮ��ϴ�����ϵ�е���Ũ�ȵľƾ���ˮ��CO2�ٽ�������ӽ���ƽ�Ȼ��������S520��ɨ��羵�¹۲졣
2.��羵�걾�Ʊ���������ƿ�ڵ�ϸ������Ƥ���ӽ�ϸ��������£��ռ������Ĺ��У��������ռ�ϸ������2.5 % ���ȩ�̶� ��0.1 M���Ỻ��Һ��ϴ������1 %���̶���˫��ˮ��ϴ �������ϵ�е���Ũ�ȵı�ͪ��ˮ��Epon812����LKB������Ƭ����Ƭ�������ƺ��۴���Ǧ˫Ⱦ��Ȼ��������H600����羵�¹۲졣
, ��Ĵҽҩ
�� ��
һ��RA�Գ���άϸ����������������
1.RA��ͬ����������(ͼ1)������RAŨ�ȶ�Ϊ10-6��10-8mol/L,�۲�����6��Գ���άϸ����������Ӱ�졣���������RA�Գ���άϸ���������������ã���ҩ��Ũ�ȵ����߶���ǿ���ʼ���ЧӦ��ϵ��

ͼ1 RA��ͬ����Ũ�ȶԳ���άϸ����Ӱ��

ͼ2 RA��ͬ����ʱ��Գ���άϸ����Ӱ��
2.RA��ͬʱ�������(ͼ2)����RAŨ�ȶ�Ϊ10-6mol/L,�ֱ�۲�1��2��3��4��6��5����ͬʱ�����άϸ����������Ӱ�졣�����ʾ��RA�Գ���άϸ���������������ã���ҩ������ʱ����ӳ�����ǿ����ʱ��ЧӦ��ϵ��
, ��Ĵҽҩ
����RA�Գ���άϸ��DNA�ϳɵ�Ӱ��
��DNA��л��ǰ������3HTdR�������άϸ��DNA�У��۲�ϸ����DNA�ϳ�ˮƽ�������������ʵ������ʾ������RAŨ�����ӣ�3HTdR�����½���3HTdR�����������������ʼ���ЧӦ��ϵ��������RA�����£�����άϸ��DNA�ϳɼ��٣�����������״̬��
����RA�Գ���άϸ�����ṹ��Ӱ��
1.ɨ��羵�۲�(ͼ3)����ɨ��羵�¸�ҩ�����άϸ��������ά״���ʺ���״ͻ�����Լ��٣���������Ϊ��ͺ��

�����飬ɨ��羵��3 000

, ��Ĵҽҩ
ά�����飬��羵��1 200
ͼ3 ����άϸ��ɨ��羵�۲�
���������άϸ������ɼ�������ά״���ʲ���֯����״��ά���������άϸ��������ά״���ʼ��ټ���
2.��羵�۲�(ͼ4)������羵�¸�ҩ�����άϸ�������Ĵ������������Լ��٣������������������ţ�ǻ��������ϡ�٣��е��������ݻ��������������ϵĺ˵������в�ͬ�̶ȵ��ѿ����ͽ���������������ͻ���ݻ�����Ĥ�ڲ����С�����Լ��٣���Ĥ������ʷ����

�����飬ɨ��羵��3 000

ά�����飬��羵��1 200
, ��Ĵҽҩ
ͼ4 ����άϸ����羵�۲�
���������άϸ�������ھ��зḻ�Ĵ����������������壻ά���������άϸ�����ڴ����������������ţ��������ݻ����������ѿ����ͽ�ۣ����������ͣ����ݻ���
�� ��
�۵��γ��Ǵ������ϵĽ�����˿��������������ӣ��;ֲ�ϸ������ѧ���ԣ���Ҫȡ���ڣ������õ���Ƥϸ��������Ǩ�ƺ��ǣ��ڳ���άϸ�������ϳɽ�ԭ�ij����ͽ���������άϸ���ɷ�Ϊ�ϳ��ͺ������͡��������о���Ϊ���۵��������������ڳ���άϸ�������Ľ��[10]����ˣ����ڴ������Ϲ�����ʹ��ij��ҩ����ܴ�ʹ��Ƥϸ����ֳ�ֻ��������ʵ����Ƴ�(��)��άϸ���Ĺ�����ֳ�ͻ��ԣ���Ӧ�ﵽ�ٽ��˿����ϲ���ֹ�����������������á�
����άϸ���Ǻϳɽ�ԭ����Ҫϸ��������άϸ���ϳ�����ڽ�ԭ��������ǿ�����άϸ���Ĵ�����ֳ�������ܵ��½�ԭ����������[11]���������룬����άϸ���Ĵ�����ֳ��Ȼ�ᵼ�½�ԭ�Ĺ��������������ϳ���άϸ����������ֳ��������ֹ�۵ķ����뷢չ��
, ��Ĵҽҩ
������ϸ��ѧ�����ﻯѧ�о�����[12]����ԭ�������ڳ���άϸ���Ĵ����������ںϳɣ�������������������������˵����干ͬ�γɵ�һ�����ϻ��ܵ�λ����ϸ����������ϳɵ���Ҫ���ء�����֤ʵ[13]������άϸ�������������ϵĺ˵������ǽ�ԭ����ǰ��ϳɵij���������֤�����ֺϳ����ò����ڵ����˵������ϣ������ڶ�ۺ˵������Ͻ��С����ԣ��˵�������������Ĥ�ϵĸ��š������Լ��������Ľṹ�仯���Խ�ԭ���ĺϳɹ��ܾ�����Ҫ���塣
���о������������ҩ�����άϸ���������Լ��٣�ϸ����������������RA��ʱ�䡢������ЧӦ��ϵ��3HTdR�������������ơ��羵�۲���ʾ����ҩ��ϸ����̬�����Ա仯������Ϊ�����������ϵĶ�ۺ˵������ѿ����ͽ�ۣ����������ųɴ� С���ȵ����ݣ�������������ϡ�ٻ����������ϸ�������ϸ��������ά״��������٣�����ͻ������١�˵��RA���Ե�Ӱ�����άϸ���������ͺ˵����壬ͨ���Ե����ʺϳɹ��̵����ã����ƽ�ԭ�����ɣ�����۲쵽RA���������Ӱ��Ҳ�����ԡ���������ϸ������������л�����ģ��ϳɷ�Ӧ��Ҫ��������ˣ�ͨ����һ;��Ҳ��Ӱ�쵽����άϸ���ϳɽ�ԭ���Ĺ��ܡ��ݴ��Ʋ⣬RA�����۵����û������������Ƴ���άϸ��������ֳ�����ֳ���άϸ����DNA�ϳɼ�Ӱ�콺ԭ�ĺϳ��йء�
, ��Ĵҽҩ
Ȼ�����۵��γɼ��临�ӣ�RA�����ڵ�ʵ������ѧ�����У��Ƿ�Ҳ��������ʵ����ֳ���������ԣ������һ���о�������RA�����۵����û��������Ƕ���[14]��Ҫ��ȫ���������д�����̽�֡�
���� RA�Գ���άϸ��3HTdR�����Ӱ�� Ũ��
(mol/L)
cpm
(
 )
)������(%)
(������-ʵ����)/������X100%
Pֵ
, ��Ĵҽҩ
������
2274��270
10-7
563��157
75.2
<0.01
10-6
449��196
80.3
<0.01
10-5
418��76
, ��Ĵҽҩ
81.6
<0.01
10-4
341��39
85.0
<0.01
���о����ɱ����й�ҽѧ��ѧԺ����ҽѧ�о���ϸ�����������ף����������Ѻ�ҽԺ�羵�ҹ�Ψ��ʢ��졢��ʯ������������ش���л��
������������������������
�����
1 Diegelmann R F, Cohen I D, McCoy B J. Growth kinetics and collagen synthesis of normal skin, normal scar and keloid fibrolasts in vitro. J Cell Physiol, 1979,98:341346.
, ��Ĵҽҩ
2 Mooy L S, Tan EML, Holness R, et al. Effects of phenytoin on collagen metabolism and growth of skin fibroblast in culture. Clin Res, 1983, 31:22A.
3 Datubo-Brown D D, Blight A. Inhibition of human fibroblast growth in vitro by a snake oil. Br J Plast Surg, 1990,43:183186.
4 Orfanos C E, Ehlert R, Gollnick H. The retinoids: A review of their clinical pharmacology and therapeutic use. Drugs, 1987,34:459503.
, http://www.100md.com
5 Martin S, Tallman M D, Peter H, et al. Retinoids in cancer treatment. J Clin Pharmacol, 1992,32:868873.
6 De Luca L M, Darwiche N, Jones C S, et al.Retinoids in differen tiation and neoplasia. Sci Am Sci Med, 1995,2:2837.
7 Panabiere-Castaings M H. Retinoic acid in the treatment of keloids. J Dermatol Surg Oncol, 1988,14:12751276.
8 Daly T J, Golitz L E, Weston M L. A double-blind placebo controlled efficacy study tretinoin cream 0.05 % in the treatment of keloids and hypertrophic scars. Clin Res, 1986,34:159A.
, http://www.100md.com
9 Heckman C A, Vroman L, Pitlick A. The nature of substrate attached materials in human fibroblast cultures: Localization of cell and fetal calf serum components. Tissue and cell 1977,9:317334.
10 Gabbiani G,Hirschel B J,Ryan G B,et al.Granulation tissue as a contractile organ:A study of structure and function.J Exp Med,1972,135:719728.
11 Cohen I K, McCoy B J.The biloogy and control of surface overhealing. World J Surg, 1980, 4:289295.
, ��Ĵҽҩ
12 ��������.����ҽѧ���ṹ�������������.��������ѧ�����磬1984.346354.
13 Hay E D. Extracellular matrix. J Cell Biol,1981,91:205223.
14 Sung L H, Tsuchihashi M. Tenshin S, et al. Effect of retinoic acid on contraction of collagen gel induced by fibroblasts. Biochem Biophys Res Commun, 1994,205:455459.
(�ո壺1997-12-17 �أ�1998-07-17), ��Ĵҽҩ