11例银屑病患者口腔损害的病理表现
作者:
单位:高恒(430022武汉,同济医科大学附属协和医院口腔科);李辉(湖北医科大学口腔医学院);武汉市一医院皮肤科(胡长发)
关键词:口腔粘膜;银屑病;组织病理;免疫病理
临床口腔医学杂志990215 高恒 李辉 胡长发
胡长发
提 要 探讨口腔粘膜是否可发生银屑病。于450例有皮损的银屑病患者中发现有口腔病损者11例,且口腔病损与皮损间有消长一致的关系。作者对这些口腔病损进行了组织病理学和免疫病理学研究。结果显示:口腔病损上皮不全角化,棘层增厚(棘皮症),角源细胞分裂活性增加,结缔组织乳头延长,钉突亦相应增长,毛细血管扩张,上皮内炎性细胞浸润,上皮浅层有时可见到Munro’s微脓肿。角层、棘细胞间及基底细胞间和基底膜处有免疫复合物沉积。上述结果与银屑病皮损相似。提示口腔粘膜可发生银屑病。
, 百拇医药
Pathology of 11 patients wiht psoriasis on the oral lesions Gao Heng et al.Department of Stomatology, Affiliated Union Hospital, Tong Ji Medical University, Wuhan 430022
Abstract To identify that psoriasis can occurs on oral mucosa. The oral cavity of 450 patients with psoriatic cutaneous lesions have been examined. 11 patients of these have oral lesions, the occurrence and relief of oral lesions varied and associated with that of cutaneous lesions. Usi ng routine histopathological and immunohistopathological methods investigated th ese oral lesions,found epithelial parakeratotic hyperkeratosis、epithelial thick ening(acanthosis)、increase of mitotic activity in keratincytes、elongation of p apillae with relevant elongation of the rete ridges、dilatation of capillaries、 Munro’s microabscesses at upper epithelia and deposition of immunocomplex in the stratum comeum、intercellular space of spinous and basal cells and in basal me mbrane zone.The results resembled that of cutaneous lesions.Suggest that pso riasis could appears on oral mucosa.
, 百拇医药
Key words Oral mucosa Psoriasis Histopath ology lmmunohistopathology
材料与方法
1. 抗体:荧光抗体是武汉市一医院皮肤病研究室提供的异硫氰酸荧光素标记的兔抗人lgG、lgA、C3,F/P=2,浓度为1mg/ml。
2. 取材:局麻下在口腔病损处切取约1.0×1.0cm组织块,再将每一组织块分成约等大二部分,一部分立即放于液氮罐中,备免疫病理切片之用,另一部分则置于10%福尔马林液中固定,作常规组织切片之用。
3. 常规组织切片制作与HE染色:10%福尔马林液中固定24小时的组织块被顺序脱水、二甲苯透明、石腊包埋,切取4.0μm厚制切片。苏木精-伊红染色,中性树胶封固。
, 百拇医药
4. 直接免疫荧光切片制作及观察:①取出冷冻新鲜组织块,OCT包埋,冷冻切片机连续切片,厚4.0μm,用丙酮在室温下固定10分钟,存放于普通4℃冰箱。磷酸缓冲液(PBS),pH7.2,0.15M,冲洗切片5分钟。分别滴抗人lgG、lgA和C3于同一组织块的不同切片上。置湿盒孵育30分钟。PBS冲洗5分钟,电扇干燥,用缓冲甘油封固,加盖玻片。②自发荧光对照:病损组织切片不加标记抗体,直接封片观察。③阴性对照:正常人口腔粘膜冰冻切片分别用前述几种标记抗体染色,作阴性对照,观察试剂效果。④用Leitz显微镜落射光观察。
结果
1. 上皮组织的改变:上皮可见不全角化,不全角化层见染色较深的固缩核。上皮钉突向下延伸,有的呈典型的上细下粗的棒状,末端肥大,该处棘细胞层增加,少则7~8层多则十几层,基底细胞及紧邻基底细胞的棘细胞的胞质呈明显的嗜碱性,有丝分裂数增加(图1、2)。
, 百拇医药
图1 ▲示上皮浅层不全角化,↑示钉突呈棒状,棘层明显增加。 (HE12.5×6.3)
图2 上皮内见炎性细胞,↑处炎性细胞与基底细胞接触密切,▲示基底细胞及其上的棘细胞胞质呈嗜碱性,有丝分裂数增加。 (HE12.5×100)
2. 固有层的改变:固有层乳头伸长、增宽,有的部位伸长的乳头十分接近上皮表面,其上仅覆2~3层上皮细胞,毛细血管扩张(图3)。在牛肉色变病损中毛细血管扩张、迂曲明显。
图3 ↑示毛细血管扩张,▲示中性白细胞正穿入基底层。 (HE12.5×100)
3. 炎性细胞浸润与Munros微脓肿:上皮及固有层内散在有炎性细胞,表现为多形核和单核细胞,乳头顶端可见变得细长的中性白细胞正穿入基底层(图3)。不全角化处可见散在中性白细胞。作者在一例左颊粘膜糜烂病损处的不全角化层内见到数个胞膜消失,胞质呈均质状,核固缩的中性多核白细胞聚集在一起,形成上皮内的微脓肿(图4)。
, http://www.100md.com
图4 ↑处上皮内多个中性白细胞聚集,形成微脓肿。 (HE12.5×100)
在牛肉色变病损中,作者还观察了粘膜下层小涎腺组织的腺泡,显示腺泡内无淋巴细胞浸润,腺泡完整,仅于腺泡间结缔组织中见少许散在的炎性细胞(图5)。
图5 腺泡结构清晰,无炎性细胞浸润。 (HE12.5×40)
4. 免疫病理学表现:直接免疫荧光观察发现,所有的病损均有角层免疫复合物的沉积,基底膜处亦可见到抗体沉积,基底细胞间,紧邻基底细胞上方的棘细胞间及乳头上部偶尔可见到免疫复和物的沉积(表1)。
表1 三种免疫复和物在口腔粘膜病损中沉积的情况 No
角层
, 百拇医药
基底细胞及棘细胞间
基底膜
乳头上部
1
lgG.lgA
lgG
lgG
-
2
lgG.C3
-
-
-
, 百拇医药
3
lgG
-
lgG
-
4
lgG
-
lgG.C3
-
5
lgG.C3
lgG
, 百拇医药
lgG
-
6
lgG.lgA
lgG
lgG.C3
lgG
7
lgG
-
lgG.lgA
lgA
8
, http://www.100md.com
lgG.C3
-
C3
-
9
lgG
lgA
lgA
lgA
10
lgG
-
-
, http://www.100md.com
-
11
lgG
-
-
-
免疫复合物的沉积在角层表现为板层状或斑片状(图6)。基底膜处为线状沉积,基底细胞间及棘细胞间则环绕细胞,表现为网状,乳头上部的沉积为团块状(图7)。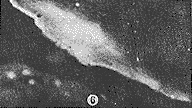
图6 上皮角层lgG沉积。 (HE12.5×40)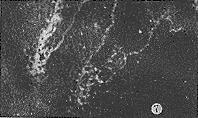
图7 lgA在基底膜带、乳头上部、基底细胞及棘细胞间的沉积。 (HE12.5×40)
, 百拇医药
病损组织无明显自发荧光,阴性对照切片无荧光发出。
讨论
G Trigonides等报道的口腔银屑病病损其病理学表现有:上皮的不全角化,乳头伸长、增宽,棘细胞层增加,固有层毛细血管扩张,上皮内或上皮下炎性细胞浸润,不全角化层的Munro's微脓肿[2]。同GTrigondes等报道的一样,其他有关口腔银屑病报道中组织病理学的描述与皮损类似[3,4]。作者的组织病理学结果与G Trigonides等的一致。
作者仅在一例糜烂型口腔病损中见到Munro's微脓肿,这可能与口腔活动频繁,粘膜表面与周围组织不断摩擦,而致Munro's微脓肿消失有关。即使皮损中也非所有患者均可见到此种微脓肿[6]。
牛肉色变病损镜下显示其固有层毛细血管扩张、迂曲明显,局部充瘀血显著,这种病理学改变与临床上见到粘膜表面呈牛肉色外观有密切关系。粘膜下层小诞腺的腺泡完整,无淋巴细胞浸润,说明患者没有舍格林氏综合症,其口干症状可能与全身的低热有关。另外,口腔银屑病的组织病理象还要注意与口腔白斑和扁平苔癣相鉴别[7]。
, 百拇医药
VC Weiss等[8]提到银屑病皮损的角层有lgG、C3沉积。有时在基底膜处、棘细胞间亦可见到免疫复合物的沉积,但与天疱疮的棘细胞间免疫荧光染色的形态有明显区别,前者在表皮较下层呈点状,在较上层呈不连续的粗细不均的虚线状,分布在乳头上变薄的棘层中,染色较弱;后者是纤细连续均匀的线状,分布于疱壁和大疱周围棘细胞间,染色较强,此外前者未见到固定补体,后者见固定补体[9,10]。SL Fischman等[11]对一例口腔银屑病病损做免疫病理学观察,发现角层中有lgG、lgA和C4的免疫复合物沉积,作者的结果与银屑病皮损和SLFischman的观察结果相似。
目前,许多学者认为免疫学异常在银屑病的发病中起重要作用[12]。正常人血清中含有能与角层起反应的抗体,但它们只在血清中而不与正常皮肤角层起反应,起屏障作用的部位可能在真皮—表皮交界处[8]。SlgA免疫复合物激活的补体和白细胞共同破坏这种屏障,使角层抗原暴露,发生抗原抗体反应,进而激活补体,趋化多形核白细胞(PMNs)[13],表皮内的PMNs是以间歇的形式从乳头毛细血管涌入基底层到达上皮内的,即形成“喷出乳头”[1]。趋化因子、循环免疫复合物和激活的补体能改变PMNs的形态和功能,细胞变得细长,胞核居于一端,这种发生变化的细胞可产生一种蛋白酶使角源细胞(KC)的分裂活性增强[1]。作者观察到上皮内变形分叶状核的炎性细胞即可认为是PMNs,乳头顶端可见较多变形炎性细胞正穿入基底层,可能即为“喷出乳头”现象。镜下见到的形态为圆形的炎性细胞可能主要是淋巴细胞。有人在实验中观察到银屑病皮损中的淋巴细胞是T淋巴细胞,而且主要为T辅助细胞,未见到B淋巴细胞,T淋巴细胞通过多种免疫学途径能导致进一步的炎症和其他病理过程[14]。
, 百拇医药
基底膜、乳头的免疫复合物沉积可能与循环免疫复合物有关。作者认为来自血清的免疫反应物可在此作用,激活补体,使角层抗原暴露。基底细胞极其上方的棘细胞间见到的免疫荧光染色,因观察到的这种免疫病理表现的例数较少,又未做动态研究,因而对基底细胞与棘细胞间免疫复合物的内在关系不能得到一个明确结论。这些免疫复合物可能与口腔粘膜损害的发生密切相关。
11例银屑病口腔病损的组织病理学和免疫病理学研究结果显示口腔粘膜是可以发生银屑病的。
参考文献
[1]Greaves MW. Neutrophil polymorphonuclears,mediators and the pathogenesis of psoriasis.Br J Dermatol. 1983,109:115~118
[2]Trigonides G,Markopoulos AK,Konstantinidis AB. Dermal psoriasis in volving the oral cavity. J Oral Med, 1986,41:98~101
, 百拇医药
[3]Pyle GW, Vitt M,Nieusma G.Oral psoriasis:Report of Case.J Oral Max illofac Surg, 1994,52:185~187
[4]Robinson CM, Di Biase AT, Liegh IM, et al. Oral psoriasis. Br J De rmatol, 1996,134:347~349
[5]Thomas J. Fissured tongue in generalized pustular psoriasis. Arch Dermatol, 1993,129:1346
[6]刘承煌(主编).银屑病的临床和研究.第一版.上海:上海科学技术文献出版社,1994:164~169
[7]Pisanty S, Ship ll. Oral psoriasis. Oral Surg, 1970,30:351~355
, http://www.100md.com
[8]Weiss VC, Broek HVD, Barrett S, et al. lmmunopathology of ps oriasi s: A comparison with other parakeratotic lesions. J lnvest Dermatol, 1982,78:256 ~260
[9]胡长发,孙曾拯,袁劲松等.银屑病免疫病理学研究方法的改进.中华病理学杂志,1984,13:149~151
[10]胡长发,孙曾拯,王苇蓁等.银屑病皮损中棘层细胞间体内结合自身抗体.临床皮肤科杂志,1989,18:120~122
[11]Fischman SL. Barnett ML. Nisengard RJ. Histopathologic, ultra structural, and immunologic findings in an oral psoriatic lesion. Oral Surg,1977 ,44:253~260
, http://www.100md.com
[12]Kaneko F,Gushiken H,Kawagishi l,et al. Analysis of immunologi cal responses in psoriatic lesions:(1) immunopathological studies on psoriatic l esions. J lnvest Dermatol,1980,75:436~439
[13]Ramirez-Bosca A,Martinez-Ojeda L,Valcuende-Cavero F, et al .A study of local immunity in psoriasis. Br J Dermatol, 1988,119:587~595
[14]顾绍裘.单克隆抗体对银屑病初发损害内浸润细胞的免疫组织化学表现型的初步鉴定.中国免疫学杂志,1985,1:11~12
(收稿:1999—02—13), 百拇医药
单位:高恒(430022武汉,同济医科大学附属协和医院口腔科);李辉(湖北医科大学口腔医学院);武汉市一医院皮肤科(胡长发)
关键词:口腔粘膜;银屑病;组织病理;免疫病理
临床口腔医学杂志990215 高恒 李辉
 胡长发
胡长发提 要 探讨口腔粘膜是否可发生银屑病。于450例有皮损的银屑病患者中发现有口腔病损者11例,且口腔病损与皮损间有消长一致的关系。作者对这些口腔病损进行了组织病理学和免疫病理学研究。结果显示:口腔病损上皮不全角化,棘层增厚(棘皮症),角源细胞分裂活性增加,结缔组织乳头延长,钉突亦相应增长,毛细血管扩张,上皮内炎性细胞浸润,上皮浅层有时可见到Munro’s微脓肿。角层、棘细胞间及基底细胞间和基底膜处有免疫复合物沉积。上述结果与银屑病皮损相似。提示口腔粘膜可发生银屑病。
, 百拇医药
Pathology of 11 patients wiht psoriasis on the oral lesions Gao Heng et al.Department of Stomatology, Affiliated Union Hospital, Tong Ji Medical University, Wuhan 430022
Abstract To identify that psoriasis can occurs on oral mucosa. The oral cavity of 450 patients with psoriatic cutaneous lesions have been examined. 11 patients of these have oral lesions, the occurrence and relief of oral lesions varied and associated with that of cutaneous lesions. Usi ng routine histopathological and immunohistopathological methods investigated th ese oral lesions,found epithelial parakeratotic hyperkeratosis、epithelial thick ening(acanthosis)、increase of mitotic activity in keratincytes、elongation of p apillae with relevant elongation of the rete ridges、dilatation of capillaries、 Munro’s microabscesses at upper epithelia and deposition of immunocomplex in the stratum comeum、intercellular space of spinous and basal cells and in basal me mbrane zone.The results resembled that of cutaneous lesions.Suggest that pso riasis could appears on oral mucosa.
, 百拇医药
Key words Oral mucosa Psoriasis Histopath ology lmmunohistopathology
材料与方法
1. 抗体:荧光抗体是武汉市一医院皮肤病研究室提供的异硫氰酸荧光素标记的兔抗人lgG、lgA、C3,F/P=2,浓度为1mg/ml。
2. 取材:局麻下在口腔病损处切取约1.0×1.0cm组织块,再将每一组织块分成约等大二部分,一部分立即放于液氮罐中,备免疫病理切片之用,另一部分则置于10%福尔马林液中固定,作常规组织切片之用。
3. 常规组织切片制作与HE染色:10%福尔马林液中固定24小时的组织块被顺序脱水、二甲苯透明、石腊包埋,切取4.0μm厚制切片。苏木精-伊红染色,中性树胶封固。
, 百拇医药
4. 直接免疫荧光切片制作及观察:①取出冷冻新鲜组织块,OCT包埋,冷冻切片机连续切片,厚4.0μm,用丙酮在室温下固定10分钟,存放于普通4℃冰箱。磷酸缓冲液(PBS),pH7.2,0.15M,冲洗切片5分钟。分别滴抗人lgG、lgA和C3于同一组织块的不同切片上。置湿盒孵育30分钟。PBS冲洗5分钟,电扇干燥,用缓冲甘油封固,加盖玻片。②自发荧光对照:病损组织切片不加标记抗体,直接封片观察。③阴性对照:正常人口腔粘膜冰冻切片分别用前述几种标记抗体染色,作阴性对照,观察试剂效果。④用Leitz显微镜落射光观察。
结果
1. 上皮组织的改变:上皮可见不全角化,不全角化层见染色较深的固缩核。上皮钉突向下延伸,有的呈典型的上细下粗的棒状,末端肥大,该处棘细胞层增加,少则7~8层多则十几层,基底细胞及紧邻基底细胞的棘细胞的胞质呈明显的嗜碱性,有丝分裂数增加(图1、2)。

, 百拇医药
图1 ▲示上皮浅层不全角化,↑示钉突呈棒状,棘层明显增加。 (HE12.5×6.3)

图2 上皮内见炎性细胞,↑处炎性细胞与基底细胞接触密切,▲示基底细胞及其上的棘细胞胞质呈嗜碱性,有丝分裂数增加。 (HE12.5×100)
2. 固有层的改变:固有层乳头伸长、增宽,有的部位伸长的乳头十分接近上皮表面,其上仅覆2~3层上皮细胞,毛细血管扩张(图3)。在牛肉色变病损中毛细血管扩张、迂曲明显。

图3 ↑示毛细血管扩张,▲示中性白细胞正穿入基底层。 (HE12.5×100)
3. 炎性细胞浸润与Munros微脓肿:上皮及固有层内散在有炎性细胞,表现为多形核和单核细胞,乳头顶端可见变得细长的中性白细胞正穿入基底层(图3)。不全角化处可见散在中性白细胞。作者在一例左颊粘膜糜烂病损处的不全角化层内见到数个胞膜消失,胞质呈均质状,核固缩的中性多核白细胞聚集在一起,形成上皮内的微脓肿(图4)。

, http://www.100md.com
图4 ↑处上皮内多个中性白细胞聚集,形成微脓肿。 (HE12.5×100)
在牛肉色变病损中,作者还观察了粘膜下层小涎腺组织的腺泡,显示腺泡内无淋巴细胞浸润,腺泡完整,仅于腺泡间结缔组织中见少许散在的炎性细胞(图5)。

图5 腺泡结构清晰,无炎性细胞浸润。 (HE12.5×40)
4. 免疫病理学表现:直接免疫荧光观察发现,所有的病损均有角层免疫复合物的沉积,基底膜处亦可见到抗体沉积,基底细胞间,紧邻基底细胞上方的棘细胞间及乳头上部偶尔可见到免疫复和物的沉积(表1)。
表1 三种免疫复和物在口腔粘膜病损中沉积的情况 No
角层
, 百拇医药
基底细胞及棘细胞间
基底膜
乳头上部
1
lgG.lgA
lgG
lgG
-
2
lgG.C3
-
-
-
, 百拇医药
3
lgG
-
lgG
-
4
lgG
-
lgG.C3
-
5
lgG.C3
lgG
, 百拇医药
lgG
-
6
lgG.lgA
lgG
lgG.C3
lgG
7
lgG
-
lgG.lgA
lgA
8
, http://www.100md.com
lgG.C3
-
C3
-
9
lgG
lgA
lgA
lgA
10
lgG
-
-
, http://www.100md.com
-
11
lgG
-
-
-
免疫复合物的沉积在角层表现为板层状或斑片状(图6)。基底膜处为线状沉积,基底细胞间及棘细胞间则环绕细胞,表现为网状,乳头上部的沉积为团块状(图7)。

图6 上皮角层lgG沉积。 (HE12.5×40)

图7 lgA在基底膜带、乳头上部、基底细胞及棘细胞间的沉积。 (HE12.5×40)
, 百拇医药
病损组织无明显自发荧光,阴性对照切片无荧光发出。
讨论
G Trigonides等报道的口腔银屑病病损其病理学表现有:上皮的不全角化,乳头伸长、增宽,棘细胞层增加,固有层毛细血管扩张,上皮内或上皮下炎性细胞浸润,不全角化层的Munro's微脓肿[2]。同GTrigondes等报道的一样,其他有关口腔银屑病报道中组织病理学的描述与皮损类似[3,4]。作者的组织病理学结果与G Trigonides等的一致。
作者仅在一例糜烂型口腔病损中见到Munro's微脓肿,这可能与口腔活动频繁,粘膜表面与周围组织不断摩擦,而致Munro's微脓肿消失有关。即使皮损中也非所有患者均可见到此种微脓肿[6]。
牛肉色变病损镜下显示其固有层毛细血管扩张、迂曲明显,局部充瘀血显著,这种病理学改变与临床上见到粘膜表面呈牛肉色外观有密切关系。粘膜下层小诞腺的腺泡完整,无淋巴细胞浸润,说明患者没有舍格林氏综合症,其口干症状可能与全身的低热有关。另外,口腔银屑病的组织病理象还要注意与口腔白斑和扁平苔癣相鉴别[7]。
, 百拇医药
VC Weiss等[8]提到银屑病皮损的角层有lgG、C3沉积。有时在基底膜处、棘细胞间亦可见到免疫复合物的沉积,但与天疱疮的棘细胞间免疫荧光染色的形态有明显区别,前者在表皮较下层呈点状,在较上层呈不连续的粗细不均的虚线状,分布在乳头上变薄的棘层中,染色较弱;后者是纤细连续均匀的线状,分布于疱壁和大疱周围棘细胞间,染色较强,此外前者未见到固定补体,后者见固定补体[9,10]。SL Fischman等[11]对一例口腔银屑病病损做免疫病理学观察,发现角层中有lgG、lgA和C4的免疫复合物沉积,作者的结果与银屑病皮损和SLFischman的观察结果相似。
目前,许多学者认为免疫学异常在银屑病的发病中起重要作用[12]。正常人血清中含有能与角层起反应的抗体,但它们只在血清中而不与正常皮肤角层起反应,起屏障作用的部位可能在真皮—表皮交界处[8]。SlgA免疫复合物激活的补体和白细胞共同破坏这种屏障,使角层抗原暴露,发生抗原抗体反应,进而激活补体,趋化多形核白细胞(PMNs)[13],表皮内的PMNs是以间歇的形式从乳头毛细血管涌入基底层到达上皮内的,即形成“喷出乳头”[1]。趋化因子、循环免疫复合物和激活的补体能改变PMNs的形态和功能,细胞变得细长,胞核居于一端,这种发生变化的细胞可产生一种蛋白酶使角源细胞(KC)的分裂活性增强[1]。作者观察到上皮内变形分叶状核的炎性细胞即可认为是PMNs,乳头顶端可见较多变形炎性细胞正穿入基底层,可能即为“喷出乳头”现象。镜下见到的形态为圆形的炎性细胞可能主要是淋巴细胞。有人在实验中观察到银屑病皮损中的淋巴细胞是T淋巴细胞,而且主要为T辅助细胞,未见到B淋巴细胞,T淋巴细胞通过多种免疫学途径能导致进一步的炎症和其他病理过程[14]。
, 百拇医药
基底膜、乳头的免疫复合物沉积可能与循环免疫复合物有关。作者认为来自血清的免疫反应物可在此作用,激活补体,使角层抗原暴露。基底细胞极其上方的棘细胞间见到的免疫荧光染色,因观察到的这种免疫病理表现的例数较少,又未做动态研究,因而对基底细胞与棘细胞间免疫复合物的内在关系不能得到一个明确结论。这些免疫复合物可能与口腔粘膜损害的发生密切相关。
11例银屑病口腔病损的组织病理学和免疫病理学研究结果显示口腔粘膜是可以发生银屑病的。
参考文献
[1]Greaves MW. Neutrophil polymorphonuclears,mediators and the pathogenesis of psoriasis.Br J Dermatol. 1983,109:115~118
[2]Trigonides G,Markopoulos AK,Konstantinidis AB. Dermal psoriasis in volving the oral cavity. J Oral Med, 1986,41:98~101
, 百拇医药
[3]Pyle GW, Vitt M,Nieusma G.Oral psoriasis:Report of Case.J Oral Max illofac Surg, 1994,52:185~187
[4]Robinson CM, Di Biase AT, Liegh IM, et al. Oral psoriasis. Br J De rmatol, 1996,134:347~349
[5]Thomas J. Fissured tongue in generalized pustular psoriasis. Arch Dermatol, 1993,129:1346
[6]刘承煌(主编).银屑病的临床和研究.第一版.上海:上海科学技术文献出版社,1994:164~169
[7]Pisanty S, Ship ll. Oral psoriasis. Oral Surg, 1970,30:351~355
, http://www.100md.com
[8]Weiss VC, Broek HVD, Barrett S, et al. lmmunopathology of ps oriasi s: A comparison with other parakeratotic lesions. J lnvest Dermatol, 1982,78:256 ~260
[9]胡长发,孙曾拯,袁劲松等.银屑病免疫病理学研究方法的改进.中华病理学杂志,1984,13:149~151
[10]胡长发,孙曾拯,王苇蓁等.银屑病皮损中棘层细胞间体内结合自身抗体.临床皮肤科杂志,1989,18:120~122
[11]Fischman SL. Barnett ML. Nisengard RJ. Histopathologic, ultra structural, and immunologic findings in an oral psoriatic lesion. Oral Surg,1977 ,44:253~260
, http://www.100md.com
[12]Kaneko F,Gushiken H,Kawagishi l,et al. Analysis of immunologi cal responses in psoriatic lesions:(1) immunopathological studies on psoriatic l esions. J lnvest Dermatol,1980,75:436~439
[13]Ramirez-Bosca A,Martinez-Ojeda L,Valcuende-Cavero F, et al .A study of local immunity in psoriasis. Br J Dermatol, 1988,119:587~595
[14]顾绍裘.单克隆抗体对银屑病初发损害内浸润细胞的免疫组织化学表现型的初步鉴定.中国免疫学杂志,1985,1:11~12
(收稿:1999—02—13), 百拇医药