曲格列酮――新一代口服降糖药
作者:王丽云 胡仁明 罗邦尧
单位:王丽云(上海第二医科大学 附属瑞金医院 内分泌科,上海 200025 现在:宜兴市人民医院内科,江苏 宜兴 214200);胡仁明 罗邦尧(上海第二医科大学 附属瑞金医院 内分泌科,上海 200025)
关键词:曲格列酮;非胰岛素依赖型糖尿病;血葡萄糖;药物疗法
中国新药与临床杂志000431 [摘要] 本文综述治疗Ⅱ型糖尿病的新药曲格列酮的药理作用、药物动力学以及在糖尿病治疗上的应用。
[中图分类号]R977.15
[文献标识码]A
[文章编号]1007-7669(2000)04-0315-03
, http://www.100md.com
曲格列酮(troglitazone)是新一代口服降糖药,系噻唑烷二酮的衍生物。它主要通过降低胰岛素抵抗,增加肝脏、骨骼肌、脂肪等外周组织对葡萄糖的利用,抑制肝糖原的生成起降血糖的作用,对胰岛β细胞功能无直接作用。美国食品与药品管理局(FDA)宣布,曲格列酮作为一种治疗糖尿病的新药,对所有的Ⅱ型糖尿病病人有效。化学结构式如图1。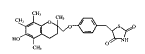
图1 曲格列酮的化学结构式
药理作用
1 曲格列酮的作用机制 曲格列酮直接与过氧化物酶增生激活受体(peroxisome proliferator-activated receptor γ, PPARγ)结合,并激活该核受体,后者与维A酸受体X结合,形成异二聚体,与特定的反应元件结合,通过某些辅活化因子(coactivator)和辅抑制因子(corepressor)介导,激活或抑制某些基因的转录以增强胰岛素的效应。PPARγ在脂肪形成的级联反应中起关键作用,并与Ⅱ型糖尿病的发病有关。
, 百拇医药
研究发现,曲格列酮增加人骨骼肌细胞PPARγ的mRNA的表达[1];使外周组织对葡萄糖和(或)2-脱氧葡萄糖的摄取增强;促进胰岛素与浆膜结合;增加外周组织细胞上葡萄糖转运蛋白-1(Glut 1)和葡萄糖转运蛋白-4(Glut 4)的表达[2];抑制果糖-1,6-二磷酸酶及其活性,使肝糖原的合成降低。曲格列酮在体外与骨骼肌细胞培养发现其糖原的合成活动增加。抑制长链脂肪酸氧化。葡萄糖诱导后胰岛素受体敏感性的下降是通过蛋白激酶C介导的,曲格列酮能逆转高糖对胰岛素受体激酶的抑制。
2 对胰岛素敏感性和胰岛素水平的影响 曲格列酮改善外周组织对胰岛素的敏感性,降低血浆胰岛素水平。研究显示,每日服用曲格列酮100 mg以上即可使血浆胰岛素水平下降。美国一项292例Ⅱ型糖尿病的研究发现,单用曲格列酮200~800 mg.d-1治疗6~12 wk后,血浆胰岛素水平下降5 %~34 %,C肽水平下降22 %。而相当剂量的格列本脲片使胰岛素水平增加22 %[3]。葡萄糖钳夹试验显示治疗后病人的葡萄糖利用增加,较大剂量的曲格列酮使葡萄糖的利用增加约45 %。曲格列酮降低胰岛素原水平。14例Ⅱ型糖尿病病人用曲格列酮200~800 mg.d-1使空腹胰岛素原、免疫活性胰岛素分别下降42 %和26 %,平均空腹胰岛素原/免疫活性胰岛素比值从38 %下降至33 %[4]。
, http://www.100md.com
3 对肝糖原生成的影响 曲格列酮治疗后肝糖原生成下降。肝糖原的生成和空腹血糖水平显著相关。一项93例Ⅱ型糖尿病病人的研究证实,大于600 mg.d-1的剂量使用6 mo后肝脏糖原生成显著降低[5]。
4 对脂肪代谢的作用 曲格列酮治疗使高密度脂蛋白(HDL)水平升高,三酰甘油水平降低,游离脂肪酸水平下降,提高脂蛋白的抗氧化能力。单予曲格列酮600~800 mg.d-1,3~6 mo后,HDL水平提高8 %~12 %。在1项114例Ⅱ型糖尿病研究中发现,治疗后HDL上升16 %,三酰甘油下降32 %[6]。在体外实验中,浓度为0.5~25 mg.L-1的曲格列酮明显抑制HDL及LDL氧化,且这种作用呈剂量依赖性。20名正常人每日服用800 mg后,LDL抗氧化能力提高24 %。在欧洲及美国的研究中,大剂量应用使游离脂肪酸水平明显下降。
, 百拇医药
5 对心血管的作用 曲格列酮在体外抑制血管平滑肌细胞增殖、游走,促进阻力血管舒张。平滑肌的增殖和游走与血管的再狭窄有关。这种抑制作用在5~40 μmol.L-1浓度范围内是呈剂量依赖性的,而不是药物的毒性作用引起[7]。
18例Ⅱ型糖尿病病人用曲格列酮200~600 mg.d-1,6 mo后,血浆纤溶酶原激活物抑制物-Ⅰ(plasminogen activator inhibitor-1;PAI-1)从68.8 μg.L-1降至40.4 μg.L-1;8例中有7例恢复正常。Ⅱ型糖尿病病人应用曲格列酮800 mg.d-1, 48 wk后,心脏指数增加13.2 %,心搏指数增加9.2 %,这些指标的改变可能与舒张压的下降有关。曲格列酮使收缩压、舒张压及平均动脉压下降。血压的下降与胰岛素水平的降低有关。17例伴轻度高血压的Ⅱ型糖尿病病人经曲格列酮400 mg.d-1治疗8 wk后,血压从(21.9/12.1) kPa降至(20.7/10.9) kPa,而格列本脲组血压上升1.1 %[8]。
, http://www.100md.com
药物动力学
曲格列酮口服后迅速吸收,2~3 h达血浆峰浓度,血浆峰浓度及浓度-时间曲线下面积与剂量呈相关性。2~5 d达药物稳态浓度,T(1)/(2)约为9 h。曲格列酮在体内主要与蛋白结合(>99 %),这种结合是可逆的。在动物实验中,该药物主要分布在肝脏,小部分分布在脂肪,在脑组织中含量极低。曲格列酮的主要代谢产物是硫酸盐结合物、葡萄糖醛酸结合物和醌,其中硫酸盐结合物在血浆中的浓度最大。曲格列酮主要由胆道排泌,在粪便中排出,尿中仅有少量的药物及代谢产物。
临床应用
1 单独用于治疗Ⅱ型糖尿病 多项研究在原用降糖药停用3 wk以上或在饮食控制的基础上,加用曲格列酮或安慰剂,比较2组疗效,疗程一般为3~6 mo。证实曲格列酮对糖代谢有肯定疗效。治疗后空腹血糖下降20 %以上,其下降幅度与剂量呈相关性。糖化血红蛋白(HbAlc)及胰岛素水平显著下降,200 mg.d-1组平均下降15 %,600 mg.d-1组下降42 %[9]。与磺酰脲类相比,曲格列酮降糖作用缓慢、温和,并能明显降低胰岛素水平,而磺酰脲类使胰岛素水平升高。1项541例Ⅱ型糖尿病的研究显示,曲格列酮200~600 mg.d-1与格列本脲12 mg.d-1相比,2组治疗后空腹血糖水平和HbAlc无明显差异,但最低剂量的曲格列酮降低HbAlc的作用低于格列本脲,单用曲格列酮使胰岛素水平下降,而格列本脲使胰岛素水平上升。
, http://www.100md.com
2 与磺酰脲类合用治疗Ⅱ型糖尿病 多起报道认为,对采用磺酰脲类治疗后,疗效不满意的Ⅱ型糖尿病病人,加用曲格列酮,可使糖代谢改善,与安慰剂组有明显差别。一项137例的研究显示,在原用磺酰脲类治疗无效的基础上加用曲格列酮后,空腹血糖从10.6 mmol.L-1下降至8.3 mmol.L-1,HbAlc从9.1 %降至7.7 %,并在以后的维持治疗期间血糖和HbAlc分别维持在8.4~9.1 mmol.L-1和7.7 %~8.2 %。血浆胰岛素水平也显著降低。从治疗后胰岛素、空腹血糖、HbAlc水平来看,格列本脲和曲格列酮联合治疗比单用格列本脲要有效得多。
3 与双胍类合用治疗Ⅱ型糖尿病 目前只有少数报道。原单用二甲双胍(metformin)治疗组在加用曲格列酮后,与单用二甲双胍治疗相比,空腹血糖下降32 %,HbAlc下降13 %,提示2药合用具有相加作用[10]。
, 百拇医药
4 与胰岛素合用 在原有胰岛素治疗的基础上加用曲格列酮,比加大胰岛素剂量更为有效。在血糖控制在正常范围的情况下,加用曲格列酮可减少胰岛素的用量。17例用胰岛素治疗的Ⅱ型糖尿病病人,加用曲格列酮400 mg.d-1治疗12 wk后,空腹及餐后1 h血糖分别下降23 %和20 %,HbAlc下降8 %。
5 副作用 许多临床试验证明,曲格列酮无严重副作用。其副作用在停药后即可消失。曲格列酮治疗的常见副作用有胃肠道症状,如恶心、呕吐、腹胀、腹泻、上腹部疼痛等。可有浮肿、呼吸道感染、可逆性黄疸(肝活检显示为特应性的药物反应)。实验室检查的异常有红细胞计数、血红蛋白、血细胞比容降低,乳酸脱氢酶升高[11]。单用曲格列酮未见有低血糖反应,与磺酰脲类或胰岛素联用低血糖的发生率约为3 %~5 %。
作为一类新的口服降糖药曲格列酮具有广阔的应用前景。目前,已被用于与胰岛素抵抗有关的其他疾病治疗,如多囊卵巢综合征、妊娠糖尿病等。
, 百拇医药
[参考文献]
[1] Park KS, Abram-Carter L, Mudaliar S, et al. Troglitazon effects on gene expression in human skeletal muscle involve regulation of PRARγ [J]. Diabetes, 1997, 46 Suppl 1:22A-23A.
[2] Park K, Abrams L, Nikoulina S, et al. Effects on glucose transport and glycogen synthase activity in human skeletal muscle cultures from obses non-diabetes and NIDDM subjects [J]. Diabetes, 1996, 45 Suppl 2:93A-94A.
, 百拇医药
[3] Kumar S, Boulton AJM, Beck-Nielsen H, et al. Troglitazon, an insulin action enhancer improves metabolic control in NIDDM patients [J]. Diabetologia, 1996, 39:701-709.
[4] Prigeon RL, Porte D. Effect of troglitazon on proinsulin and insulin levels in persons with NIDDM [J]. Diabetes, 1996, 45 Suppl 2: 323A-325A.
[5] Troglitazon study group. The effects of troglitazon in NIDDM [J]. Diabetes, 1997, 46 Suppl 1: 149A-151A.
, 百拇医药
[6] Ghazzi MN, Perez JE, Antonucci TK, et al. Cardiac and glycemic benefits of troglitazon treatment in NIDDM [J]. Diabetes, 1997, 46:433-439.
[7] Morikang E, Benson SC, Kurtz TW, et al. Effects of thiazolidinediones on growth and differentiation of human aorta and coronary myocytes [J]. Am J Hypertens, 1997, 10:440-446.
[8] Driscoll J, Ghazzi M, Perez J, et al. A 96-week follow-up on cardiac safety in patients with type Ⅱ diabetes treated with troglitazon [J]. Diabetes, 1997, 46 Suppl 1:149A-151A.
, http://www.100md.com
[9] Valiguett T, Huang S, Whitcomb R. Effects of troglitazon monotherapy in patients with NIDDM: a 6-month multicenter study [J]. Diabetes, 1997,46: Suppl 1:43A-45A.
[10] Inzucchi SE, Maggs DG, Spollett GR, et al. Efficacy and metabolic effects of troglitazon and metformin in NIDDM [J]. Diabetes, 1997, 46 Suppl 1: 34A-36A.
[11] Iwamoto Y, Kosaka K, Kuzuya T, et al. Effect of combination therapy of troglitazon and sulphonylureas in patients with type 2 diabetes who were poorly controlled by sulphonylurea therapy alone [J]. Diabetes Med, 1996, 13:365-370.
[收稿日期]1998-08-06 [接受日期]1999-01-18, 百拇医药
单位:王丽云(上海第二医科大学 附属瑞金医院 内分泌科,上海 200025 现在:宜兴市人民医院内科,江苏 宜兴 214200);胡仁明 罗邦尧(上海第二医科大学 附属瑞金医院 内分泌科,上海 200025)
关键词:曲格列酮;非胰岛素依赖型糖尿病;血葡萄糖;药物疗法
中国新药与临床杂志000431 [摘要] 本文综述治疗Ⅱ型糖尿病的新药曲格列酮的药理作用、药物动力学以及在糖尿病治疗上的应用。
[中图分类号]R977.15
[文献标识码]A
[文章编号]1007-7669(2000)04-0315-03
, http://www.100md.com
曲格列酮(troglitazone)是新一代口服降糖药,系噻唑烷二酮的衍生物。它主要通过降低胰岛素抵抗,增加肝脏、骨骼肌、脂肪等外周组织对葡萄糖的利用,抑制肝糖原的生成起降血糖的作用,对胰岛β细胞功能无直接作用。美国食品与药品管理局(FDA)宣布,曲格列酮作为一种治疗糖尿病的新药,对所有的Ⅱ型糖尿病病人有效。化学结构式如图1。
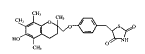
图1 曲格列酮的化学结构式
药理作用
1 曲格列酮的作用机制 曲格列酮直接与过氧化物酶增生激活受体(peroxisome proliferator-activated receptor γ, PPARγ)结合,并激活该核受体,后者与维A酸受体X结合,形成异二聚体,与特定的反应元件结合,通过某些辅活化因子(coactivator)和辅抑制因子(corepressor)介导,激活或抑制某些基因的转录以增强胰岛素的效应。PPARγ在脂肪形成的级联反应中起关键作用,并与Ⅱ型糖尿病的发病有关。
, 百拇医药
研究发现,曲格列酮增加人骨骼肌细胞PPARγ的mRNA的表达[1];使外周组织对葡萄糖和(或)2-脱氧葡萄糖的摄取增强;促进胰岛素与浆膜结合;增加外周组织细胞上葡萄糖转运蛋白-1(Glut 1)和葡萄糖转运蛋白-4(Glut 4)的表达[2];抑制果糖-1,6-二磷酸酶及其活性,使肝糖原的合成降低。曲格列酮在体外与骨骼肌细胞培养发现其糖原的合成活动增加。抑制长链脂肪酸氧化。葡萄糖诱导后胰岛素受体敏感性的下降是通过蛋白激酶C介导的,曲格列酮能逆转高糖对胰岛素受体激酶的抑制。
2 对胰岛素敏感性和胰岛素水平的影响 曲格列酮改善外周组织对胰岛素的敏感性,降低血浆胰岛素水平。研究显示,每日服用曲格列酮100 mg以上即可使血浆胰岛素水平下降。美国一项292例Ⅱ型糖尿病的研究发现,单用曲格列酮200~800 mg.d-1治疗6~12 wk后,血浆胰岛素水平下降5 %~34 %,C肽水平下降22 %。而相当剂量的格列本脲片使胰岛素水平增加22 %[3]。葡萄糖钳夹试验显示治疗后病人的葡萄糖利用增加,较大剂量的曲格列酮使葡萄糖的利用增加约45 %。曲格列酮降低胰岛素原水平。14例Ⅱ型糖尿病病人用曲格列酮200~800 mg.d-1使空腹胰岛素原、免疫活性胰岛素分别下降42 %和26 %,平均空腹胰岛素原/免疫活性胰岛素比值从38 %下降至33 %[4]。
, http://www.100md.com
3 对肝糖原生成的影响 曲格列酮治疗后肝糖原生成下降。肝糖原的生成和空腹血糖水平显著相关。一项93例Ⅱ型糖尿病病人的研究证实,大于600 mg.d-1的剂量使用6 mo后肝脏糖原生成显著降低[5]。
4 对脂肪代谢的作用 曲格列酮治疗使高密度脂蛋白(HDL)水平升高,三酰甘油水平降低,游离脂肪酸水平下降,提高脂蛋白的抗氧化能力。单予曲格列酮600~800 mg.d-1,3~6 mo后,HDL水平提高8 %~12 %。在1项114例Ⅱ型糖尿病研究中发现,治疗后HDL上升16 %,三酰甘油下降32 %[6]。在体外实验中,浓度为0.5~25 mg.L-1的曲格列酮明显抑制HDL及LDL氧化,且这种作用呈剂量依赖性。20名正常人每日服用800 mg后,LDL抗氧化能力提高24 %。在欧洲及美国的研究中,大剂量应用使游离脂肪酸水平明显下降。
, 百拇医药
5 对心血管的作用 曲格列酮在体外抑制血管平滑肌细胞增殖、游走,促进阻力血管舒张。平滑肌的增殖和游走与血管的再狭窄有关。这种抑制作用在5~40 μmol.L-1浓度范围内是呈剂量依赖性的,而不是药物的毒性作用引起[7]。
18例Ⅱ型糖尿病病人用曲格列酮200~600 mg.d-1,6 mo后,血浆纤溶酶原激活物抑制物-Ⅰ(plasminogen activator inhibitor-1;PAI-1)从68.8 μg.L-1降至40.4 μg.L-1;8例中有7例恢复正常。Ⅱ型糖尿病病人应用曲格列酮800 mg.d-1, 48 wk后,心脏指数增加13.2 %,心搏指数增加9.2 %,这些指标的改变可能与舒张压的下降有关。曲格列酮使收缩压、舒张压及平均动脉压下降。血压的下降与胰岛素水平的降低有关。17例伴轻度高血压的Ⅱ型糖尿病病人经曲格列酮400 mg.d-1治疗8 wk后,血压从(21.9/12.1) kPa降至(20.7/10.9) kPa,而格列本脲组血压上升1.1 %[8]。
, http://www.100md.com
药物动力学
曲格列酮口服后迅速吸收,2~3 h达血浆峰浓度,血浆峰浓度及浓度-时间曲线下面积与剂量呈相关性。2~5 d达药物稳态浓度,T(1)/(2)约为9 h。曲格列酮在体内主要与蛋白结合(>99 %),这种结合是可逆的。在动物实验中,该药物主要分布在肝脏,小部分分布在脂肪,在脑组织中含量极低。曲格列酮的主要代谢产物是硫酸盐结合物、葡萄糖醛酸结合物和醌,其中硫酸盐结合物在血浆中的浓度最大。曲格列酮主要由胆道排泌,在粪便中排出,尿中仅有少量的药物及代谢产物。
临床应用
1 单独用于治疗Ⅱ型糖尿病 多项研究在原用降糖药停用3 wk以上或在饮食控制的基础上,加用曲格列酮或安慰剂,比较2组疗效,疗程一般为3~6 mo。证实曲格列酮对糖代谢有肯定疗效。治疗后空腹血糖下降20 %以上,其下降幅度与剂量呈相关性。糖化血红蛋白(HbAlc)及胰岛素水平显著下降,200 mg.d-1组平均下降15 %,600 mg.d-1组下降42 %[9]。与磺酰脲类相比,曲格列酮降糖作用缓慢、温和,并能明显降低胰岛素水平,而磺酰脲类使胰岛素水平升高。1项541例Ⅱ型糖尿病的研究显示,曲格列酮200~600 mg.d-1与格列本脲12 mg.d-1相比,2组治疗后空腹血糖水平和HbAlc无明显差异,但最低剂量的曲格列酮降低HbAlc的作用低于格列本脲,单用曲格列酮使胰岛素水平下降,而格列本脲使胰岛素水平上升。
, http://www.100md.com
2 与磺酰脲类合用治疗Ⅱ型糖尿病 多起报道认为,对采用磺酰脲类治疗后,疗效不满意的Ⅱ型糖尿病病人,加用曲格列酮,可使糖代谢改善,与安慰剂组有明显差别。一项137例的研究显示,在原用磺酰脲类治疗无效的基础上加用曲格列酮后,空腹血糖从10.6 mmol.L-1下降至8.3 mmol.L-1,HbAlc从9.1 %降至7.7 %,并在以后的维持治疗期间血糖和HbAlc分别维持在8.4~9.1 mmol.L-1和7.7 %~8.2 %。血浆胰岛素水平也显著降低。从治疗后胰岛素、空腹血糖、HbAlc水平来看,格列本脲和曲格列酮联合治疗比单用格列本脲要有效得多。
3 与双胍类合用治疗Ⅱ型糖尿病 目前只有少数报道。原单用二甲双胍(metformin)治疗组在加用曲格列酮后,与单用二甲双胍治疗相比,空腹血糖下降32 %,HbAlc下降13 %,提示2药合用具有相加作用[10]。
, 百拇医药
4 与胰岛素合用 在原有胰岛素治疗的基础上加用曲格列酮,比加大胰岛素剂量更为有效。在血糖控制在正常范围的情况下,加用曲格列酮可减少胰岛素的用量。17例用胰岛素治疗的Ⅱ型糖尿病病人,加用曲格列酮400 mg.d-1治疗12 wk后,空腹及餐后1 h血糖分别下降23 %和20 %,HbAlc下降8 %。
5 副作用 许多临床试验证明,曲格列酮无严重副作用。其副作用在停药后即可消失。曲格列酮治疗的常见副作用有胃肠道症状,如恶心、呕吐、腹胀、腹泻、上腹部疼痛等。可有浮肿、呼吸道感染、可逆性黄疸(肝活检显示为特应性的药物反应)。实验室检查的异常有红细胞计数、血红蛋白、血细胞比容降低,乳酸脱氢酶升高[11]。单用曲格列酮未见有低血糖反应,与磺酰脲类或胰岛素联用低血糖的发生率约为3 %~5 %。
作为一类新的口服降糖药曲格列酮具有广阔的应用前景。目前,已被用于与胰岛素抵抗有关的其他疾病治疗,如多囊卵巢综合征、妊娠糖尿病等。
, 百拇医药
[参考文献]
[1] Park KS, Abram-Carter L, Mudaliar S, et al. Troglitazon effects on gene expression in human skeletal muscle involve regulation of PRARγ [J]. Diabetes, 1997, 46 Suppl 1:22A-23A.
[2] Park K, Abrams L, Nikoulina S, et al. Effects on glucose transport and glycogen synthase activity in human skeletal muscle cultures from obses non-diabetes and NIDDM subjects [J]. Diabetes, 1996, 45 Suppl 2:93A-94A.
, 百拇医药
[3] Kumar S, Boulton AJM, Beck-Nielsen H, et al. Troglitazon, an insulin action enhancer improves metabolic control in NIDDM patients [J]. Diabetologia, 1996, 39:701-709.
[4] Prigeon RL, Porte D. Effect of troglitazon on proinsulin and insulin levels in persons with NIDDM [J]. Diabetes, 1996, 45 Suppl 2: 323A-325A.
[5] Troglitazon study group. The effects of troglitazon in NIDDM [J]. Diabetes, 1997, 46 Suppl 1: 149A-151A.
, 百拇医药
[6] Ghazzi MN, Perez JE, Antonucci TK, et al. Cardiac and glycemic benefits of troglitazon treatment in NIDDM [J]. Diabetes, 1997, 46:433-439.
[7] Morikang E, Benson SC, Kurtz TW, et al. Effects of thiazolidinediones on growth and differentiation of human aorta and coronary myocytes [J]. Am J Hypertens, 1997, 10:440-446.
[8] Driscoll J, Ghazzi M, Perez J, et al. A 96-week follow-up on cardiac safety in patients with type Ⅱ diabetes treated with troglitazon [J]. Diabetes, 1997, 46 Suppl 1:149A-151A.
, http://www.100md.com
[9] Valiguett T, Huang S, Whitcomb R. Effects of troglitazon monotherapy in patients with NIDDM: a 6-month multicenter study [J]. Diabetes, 1997,46: Suppl 1:43A-45A.
[10] Inzucchi SE, Maggs DG, Spollett GR, et al. Efficacy and metabolic effects of troglitazon and metformin in NIDDM [J]. Diabetes, 1997, 46 Suppl 1: 34A-36A.
[11] Iwamoto Y, Kosaka K, Kuzuya T, et al. Effect of combination therapy of troglitazon and sulphonylureas in patients with type 2 diabetes who were poorly controlled by sulphonylurea therapy alone [J]. Diabetes Med, 1996, 13:365-370.
[收稿日期]1998-08-06 [接受日期]1999-01-18, 百拇医药