人B7-1、IFN-γ双顺反子逆转录病毒载体的构建和表达
作者:曹善津 钱和年 冯捷 付天云 叶雪 姚煜
单位:北京大学人民医院妇科肿瘤中心,北京 100044
关键词:B7-1;逆转录病毒科;干扰素γ;重组;代谢
北京医科大学学报000604 [摘 要]目的:制备免疫基因修饰的卵巢癌肿瘤疫苗。方法:利用口蹄疫病毒的内在性核糖体插入位点(internal ribosome entry sites,IRES),通过基因克隆技术构建人B7-1、IFN-γ双顺反子逆转录病毒载体PLXSN/B7-1 IFN-γ。结果:将PLXSN/B7-1 IFN-γ转染逆转录病毒包装细胞,包装成病毒,经滴度测定后,转导卵巢上皮癌细胞系3AO,筛选稳定表达克隆,RT-PCR和免疫流式细胞测定均可证实B7-1、IFN-γ在同一转导细胞的共表达。结论:口蹄疫病毒的IRES可提供B7-1、IFN-γ的共表达。
, 百拇医药 [中图分类号]R979.1 [文献标识码]A
[文章编号]1000-1530(2000)06-0492-04
The construction and its co-expression of bicistronic retroviral vector encoding human B7-1 and IFN-γ
CAO Shan-Jin,QIAN He-Nian,FENG Jie,FU Tian-Yun,YE Xue,YAO Yu
(Gynecologic Oncology Center,Peking University People's Hospital,Beijing 100044)
ABSTRACT Objective:For the preparation of immuno-gene modified ovarian carcinoma vaccine.Methods:Employing foot-and-mouth disease virus internal ribosome entry site(IRES),the bicistronic retroviral vector encoding human B7-1 and IFN-γ (PLXSN/B7-1 IFN-γ) was constructed by gene cloning techniques.Results:After the package and determination of the retrovirus titer,3AO,an ovarian epithelial carcinoma cell line,was transducted by the virus.The co-expression of B7-1 and IFN-γ in a single transducted cell can be detected by RT-PCR and immuno-flow cytometry.Conclusion:The IRES of foot-and -mouth disease virus can provide the co-expression of B7-1 and IFN-γ.
, 百拇医药
KEY WORDS B7-1;Retroviridae;Interferon-γ gamma,recombinant/metab;
肿瘤的免疫基因治疗在肿瘤生物治疗中占有重要地位。已经证实多种细胞因子单独转染肿瘤细胞即可增强其免疫原性或诱导其免疫功能[1]。多个细胞因子联合是研究热点之一。依据T细胞活化的双信号学说[2],增强肿瘤细胞的MHC Ⅰ类分子的表达,并且提供共刺激分子或许是肿瘤免疫基因治疗的优化组合。IFN-γ可增加MHC Ⅰ类分子的表达,并且可增加内在抗原的处理能力[3~4],而B7-1的转染可提供共刺激分子,因此,同时利用B7-1和IFN-γ修饰肿瘤细胞制备肿瘤疫苗,或许可为肿瘤的免疫基因治疗提供新的途径。为便于应用,我们利用口蹄疫病毒的内在性核糖体插入位点(internal ribosome entry sites,IRES)成功地构建了B7-1、IFN-γ双顺反子逆转录病毒载体,转导肿瘤细胞得到了两者的共表达。
, http://www.100md.com
1 材料与方法
1.1 主要试剂
限制性内切酶、T4 DNA 连接酶等购自Promega GIBCO-BRL 公司,DOTAP脂质体转染试剂购自Boehringer mannheim 公司。
1.2 质粒载体和细胞株
人B7-1 (CD80) cDNA (PCDNA3 B7-1)由北京大学泌尿研究所邢念增博士提供,人IFN-γ cDNA(GCEN IFN-γ)由上海第二医科大学人类基因治疗中心陈诗书教授惠赠,含口蹄疫病毒内在性核糖体插入位点的质粒(PLNF2X)由美国华盛顿大学技术转让部提供。PUC18、逆转录病毒载体-PLXSN由本室保存。逆转录病毒包装细胞PT67购自CLONTECH 公司 (Clontech RetroPackTM PT67),小鼠成纤维细胞NIH3T3,取自美国模式物培养所,人上皮性卵巢癌细胞系3AO取自中科院上海细胞库,由本室冻存,传代培养。
, http://www.100md.com
2 结果
2.1 逆转录病毒载体B7-1的构建(图1)
人B7-1 cDNA基因编码序列为第318~第1181,其两侧为EcoR Ⅰ,位于pCDNA3之中,以EcoR Ⅰ酶切,回收1.0 kb的片段,将其插入逆转录病毒载体PLXSN的多克隆位点EcoR Ⅰ,粘端连接反应,转化TOP10,小量提取质粒,筛选正向重组克隆(PLXSN/B7-1) 。正、反向重组子经EcoR Ⅰ酶切均可释放出900bp 左右的B7-1条带,而经Sac Ⅰ酶切,正向重组子可切出3 214bp、2 004bp和1 646bp的3个片段,反向重组子则切出3 124bp、2 304bp和1 304bp的3个片段,借以鉴别。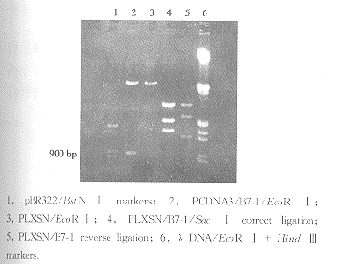
图1 PLXSN/B7-1的构建和酶切鉴定
, http://www.100md.com
Figure 1 The construction and mapping of restriction
endonulease digestion of PLXSN/B7-1
2.2 IFN-γ构建入IRES 的下游
2.2.1 IFN-γ的克隆 首先利用PCR克隆技术扩增IFN-γ,在IFN-γ引物上游加上Hpa Ⅰ 位点,在其下游加上BamH Ⅰ、Xho Ⅰ位点,以便于以后的克隆。IFN-γ的引物由SyberSyn公司合成。
正义链
5′-CGCTGAGTTAACATGAAATATACAAGTTATA-TCTTGGC-3′
反义链
, 百拇医药
5′-GTACGTCTCGAGGATCCTTACTGGGATGCTC-TTCGACC-3′
IFN-γ的PCR条件:dNTP选择0.2 μmol.L-1,上下游引物均为1 μmol.L-1,Mg2+ 3.0 mmol.L-1,94 ℃ 1 min→60 ℃ 45 s→72 ℃ 45 s,28个循环,15 g.L-1琼脂糖凝胶电泳回收500 bp的片段,以Klenow酶补平,克隆入PUC18 HincⅡ,平端连接反应,经蓝白斑筛选,酶切鉴定重组克隆,PUC18/IFN-γ,并采用双脱氧末端终止法进行测序(由SynerSyn公司完成),测序结果与文献[5]、GeneBank(J00219)发表序列完全一致。
2.2.2 IFN-γ构建入IRES的下游 PUC18/IFN-γ经Hpa Ⅰ、Xho Ⅰ双酶切,回收500bp的片段,将其克隆入PLNF2X载体IRES下游的多克隆位点Hpa Ⅰ和Xho Ⅰ,一平一粘定向连接,经转化TOP10,筛选、酶切鉴定重组克隆,PLNF2X/IFN-γ。PLNF2X/IFN-γ经Hind Ⅲ酶切可释放出IFN-γ,经Sma Ⅰ酶切重组克隆可切出3 094bp、1 995bp和1 429bp 3条带,空载体则切出3 094bp、1 995bp和1 029bp的3条带,重组克隆的第3条带大于空载体,借以鉴别(图2)。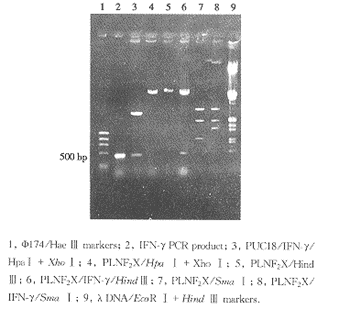
, 百拇医药
图2 PLNF2X/IFN-γ的构建和酶切鉴定
Figure 2 The construction and mapping of restriction
endonulease digestion map of PLNF2X/IFN-γ
2.3 将IRESIFN-γ克隆入PLXSN/B7-1
PLNF2X/IFN-γ经Sma Ⅰ、BamH Ⅰ酶切,回收含有IRESIFN-γ约900bp的片段,克隆入逆转录病毒载体PLXSN/B7-1的多克隆位点Hpa Ⅰ、BamH Ⅰ,一平一粘定向克隆,经转化TOP10,筛选重组克隆,PLXSN/B7-1 IFN-γ,酶切鉴定。其构建策略(图3)。
2.4 逆转录病毒的包装及滴度测定[6]
, 百拇医药
将编码B7-1和IFN-γ的双顺反子重组逆转录病毒载体PLXSN/B7-1 IFN-γ和空载体PLXSN,采用脂质体方法,转染逆转录病毒包装细胞PT67,操作按说明书进行。经G418筛选,大约2周后出现抗性克隆,约3周时克隆变大,采用滤纸消化法转移单克隆,扩大培养,至产病毒细胞株80%融合时,换液收集24 h的病毒液。病毒滴度的测定采用生物学方法,各筛选出一株高滴度的产病毒细胞株。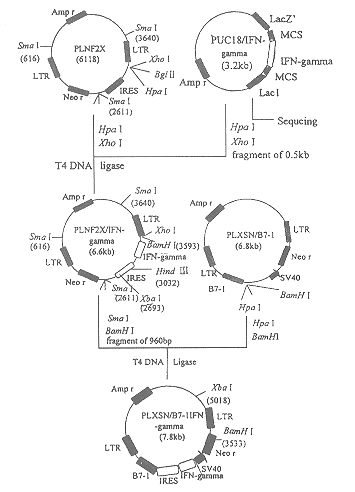
图3 PLXSN/B7-1IFN-γ的构建示意图
Figure 3 Diagram of the construction of bicistronic retroviral
vector of B7-1 and IFN-γ
2.5 卵巢癌细胞系的转导
, 百拇医药
3AO传代24 h后,使细胞达到30%~40%汇合(confluent),将收集的24 h病毒上清,加Polybrene( Sigma )至8 mg.L-1,0.45 μm针头式滤器过滤,加入上述细胞中,感染24 h后,换为完全RPMI1640,再过24 h,1∶5传代入G418筛选培养基中,G418的质量浓度为600 mg.L-1,每4~5天换液1次,至3周左右出现克隆,至克隆增大后,仍采用滤纸法消化转移克隆,每种转移4~6个克隆,此时G418质量浓度降为300 mg.L-1维持,满瓶后,再传代时撤掉G418,扩大培养。
2.6 B7-1、IFN-γ在转导细胞系共表达
2.6.1 RT-PCR 采用GIBCO公司的TRIZOL试剂提取细胞的总RNA,利用IFN-γ的下游引物进行特异引物的反转录,然后进行B7-1、IFN-γ的聚合链酶反应。B7-1的引物由SynerSyn公司合成。
, http://www.100md.com
正义链5′-ATGGGCCACACACGGAGG-3′
反义链5′-TTATACTGGGCGTACACT-3′
IFN-γ的引物见上。其扩增产物分别为867bp和500bp。逆转录反应在25 μl的反应体系中,含总RNA 2 μg,IFN-γ的下游引物25 pmol,200 μmol.L-1-MLV,按Promega公司M-MLV说明书进行。B7-1的PCR扩增条件为:95 ℃ 1 min,47 ℃ 1 min,70 ℃ 1 min,35个循环,IFN-γ的PCR扩增条件同上,35个循环。同时设原始3AO细胞作为对照,则无B7、IFN-γ的扩增。
2.6.2 免疫流式细胞测定 转导的卵巢癌细胞3AO/B7-1IFN-γ,培养至90%汇合时,加3 mmol.L-1的莫能星(moensin)6 h,以阻断IFN-γ的释放,之后以2.5 g.L-1胰蛋白酶和0.2 g.L-1EDTA消化成单细胞悬液,立即标记。B7-1、IFNγ的抗体均购自库尔特公司,B7-1系PE直标抗体,而IFN-γ系FITC直标抗体,标记方法按照库尔特公司产品说明书和文献[7]报道进行。
, http://www.100md.com
2.7 B7-1、IFN-γ共表达的RT-PCR
利用IFN-γ的下游引物进行特异引物的反转录,可分别扩增出867bp和500bp的B7-1、IFN-γ条带,说明B7-1和IFN-γ的共表达,并且其表达来自于同一条mRNA(图4)。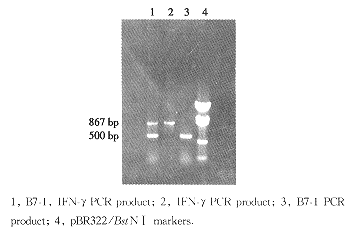
图4 B7-1、IFN-γ共表达的RT-PCR
Figure 4 The co-expression of B7-1,IFN-γ detected by RT-PCR
2.8 B7-1、IFN-γ共表达的免疫流式测定(图5)
利用免疫双标记可检测到在同一细胞B7-1、IFN-γ的共表达,其共表达百分率为32.2%,而未转导或转导PLXSN空载体的3AO细胞则无B7-1、IFN-γ的表达(0.22%)。
, http://www.100md.com
3 讨论
用免疫基因修饰肿瘤细胞以增强其免疫原性是肿瘤免疫基因治疗的策略之一。通过基因转染技术,使肿瘤细胞表达某些细胞因子,通过自分泌提高肿瘤细胞自身MHC分子的表达,或通过旁分泌作用于抗原呈递细胞或T细胞可诱导肿瘤免疫反应。IL-2、IL-4、IFN-γ、GM-CSF单独转染肿瘤细胞均诱导了T细胞免疫;另外一个重要的策略则是使肿瘤细胞具备抗原呈递细胞的某些功能,如转染共刺激分子B7-1,也诱导了肿瘤排斥[1]。然而,在某些肿瘤,即使转染某些细胞因子或B7-1并不足以引起肿瘤排斥,这可归咎于肿瘤细胞MHC分子、肿瘤抗原的表达下调或缺乏,缺乏粘附分子、分泌免疫抑制因子,从而降低了肿瘤细胞的免疫原性,而且肿瘤细胞还缺乏共刺激分子的表达,而B7介导的肿瘤排斥与肿瘤细胞的免疫原性密切相关[8~9]。Hurwttz[10]的研究表明,利用B7-1和IFN-γ共同修饰黑色素瘤可诱导很强的肿瘤免疫,明显优于单独转染一种因子的肿瘤疫苗。卵巢癌细胞缺乏共刺激分子的表达,MHCⅠ、Ⅱ类分子的表达缺失或降低(另文发表),因而同样适用于B7-1、IFN-γ双细胞因子的免疫基因治疗。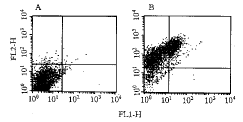
, 百拇医药
图5 B7-1、IFN-γ共表达的免疫流式细胞测定
Figure 5 Immuno-flow cytometry detection of the co-expression
of B7-1 and IFN-γ
如何构建双细胞因子的共表达载体,目前有双转染、双启动子载体、双顺反子载体3种方法[10~12]。此3种方法之中,利用IRES构建双/多顺反子表达载体具有操作简便,基因的表达效率相同等优点,因而在基因治疗中具有重要的作用。利用IRES构建双/多顺反子表达载体是基于真核细胞蛋白质翻译的链内启动模式机制而设计的[13]。本文利于口蹄疫病毒的IRES首次成功地构建了B7-1、IFN-γ共表达载体,转导卵巢癌细胞系3AO,利用RT-PCR和免疫流式细胞测定证实了两者在同一细胞的共表达,利用IFN-γ的下游引物进行特异引物的反转录,可同时扩增出B7-1和IFN-γ,表明两者的翻译来自于同一条mRNA。
, 百拇医药
本研究首先利用FMDS IRES成功地构建了B7-1和IFN-γ共表达逆转录病毒载体,为制备B7-1和IFN-γ修饰的肿瘤疫苗奠定了基础,其进一步的应用研究正在进行之中。本研究同时也为构建其它多细胞因子或双亚基细胞因子(如IL-12)表达载体的研究提供了借鉴。
参考文献
1,Berd D.Cancer vaccine:Reborn or just recycled[J]? Seminars Oncol,1998,25:605-601
2,June CH,Bluestron JA,Nadler LM,et al.The B7 and CD28 receptor families[J].Immunol Today,1994,15:321
3,Driscoll J,Brown MG,Finley D,et al.MHC-linked LMP gene products specifically after peptidaseactivities of proteasome[J].Nature,1993,365:262-264
, 百拇医药
4,Gaczynska M,Rock KL,Goldberg AL.Gamma-interferonand expression of MHC genes regulate peptidehydrolysis by proteasomes[J].Nature,1993,365:264-267
5,Devos R,Cheroutre H,Taya Y,et al.Molecularcloning of human immune interferon cDNA and itsexpression eukaryotic cells[J].Nucleic Acid Res,1982,10:2487-2501
6,蒋 泊,张亚历,周殿元主编.分子生物学常用实验方法[M].北京:人民军医出版社,1996.160-161
7,Jung T,Schauer U,Heusser C,et al.Detection of intracellular cytokines by flow cytometry[J].Jimmuno Meth,1993,159:197-207
, 百拇医药
8,Allison JP,Hurwitz AA and Leach DR.Manipulation of costimulatory signals to enhance antitumor T cell responses[J].Curr Opin Immunol,1995,7:682-686
9,Chen L,McGowan P,Ashe S.et al.Tumor immunogenesity determines the effect of B7 co-stimulation on T cells-mediated tumor immunity[J].J Exp Med,1994,179:523-532
10,Hurwttz AA,Townsend SE,Yu TF,et al.Enhancement of the anti-tumor immune response using a combination of intyerferon- and B7 expression in an experimental mammary carcinoma[J].Int J Cancer,1998,77:107-113
, 百拇医药
11,Ramesh N,Kim ST,Wei MQ,et al.High-titer bicistronic retroviral vectors employing foot-and-mouth disease virus internal ribosome entry site[J].Nucleic Acid Res,1996,24:2697-2700
12,Rosenthal FM,Cronin K,Bannerji R,et al.Augmintation of antitumor immunity by tumor cells transduced with a retroviral vector carrying the interleukin-2 and interferon-cDNAs[J].Blood,1994,83:1289-1298
13,沈 琲,方福德主编.真核基因表达调控[M].北京:高等教育出版社,1996.51-53
收稿日期:1999-03-03, http://www.100md.com
单位:北京大学人民医院妇科肿瘤中心,北京 100044
关键词:B7-1;逆转录病毒科;干扰素γ;重组;代谢
北京医科大学学报000604 [摘 要]目的:制备免疫基因修饰的卵巢癌肿瘤疫苗。方法:利用口蹄疫病毒的内在性核糖体插入位点(internal ribosome entry sites,IRES),通过基因克隆技术构建人B7-1、IFN-γ双顺反子逆转录病毒载体PLXSN/B7-1 IFN-γ。结果:将PLXSN/B7-1 IFN-γ转染逆转录病毒包装细胞,包装成病毒,经滴度测定后,转导卵巢上皮癌细胞系3AO,筛选稳定表达克隆,RT-PCR和免疫流式细胞测定均可证实B7-1、IFN-γ在同一转导细胞的共表达。结论:口蹄疫病毒的IRES可提供B7-1、IFN-γ的共表达。
, 百拇医药 [中图分类号]R979.1 [文献标识码]A
[文章编号]1000-1530(2000)06-0492-04
The construction and its co-expression of bicistronic retroviral vector encoding human B7-1 and IFN-γ
CAO Shan-Jin,QIAN He-Nian,FENG Jie,FU Tian-Yun,YE Xue,YAO Yu
(Gynecologic Oncology Center,Peking University People's Hospital,Beijing 100044)
ABSTRACT Objective:For the preparation of immuno-gene modified ovarian carcinoma vaccine.Methods:Employing foot-and-mouth disease virus internal ribosome entry site(IRES),the bicistronic retroviral vector encoding human B7-1 and IFN-γ (PLXSN/B7-1 IFN-γ) was constructed by gene cloning techniques.Results:After the package and determination of the retrovirus titer,3AO,an ovarian epithelial carcinoma cell line,was transducted by the virus.The co-expression of B7-1 and IFN-γ in a single transducted cell can be detected by RT-PCR and immuno-flow cytometry.Conclusion:The IRES of foot-and -mouth disease virus can provide the co-expression of B7-1 and IFN-γ.
, 百拇医药
KEY WORDS B7-1;Retroviridae;Interferon-γ gamma,recombinant/metab;
肿瘤的免疫基因治疗在肿瘤生物治疗中占有重要地位。已经证实多种细胞因子单独转染肿瘤细胞即可增强其免疫原性或诱导其免疫功能[1]。多个细胞因子联合是研究热点之一。依据T细胞活化的双信号学说[2],增强肿瘤细胞的MHC Ⅰ类分子的表达,并且提供共刺激分子或许是肿瘤免疫基因治疗的优化组合。IFN-γ可增加MHC Ⅰ类分子的表达,并且可增加内在抗原的处理能力[3~4],而B7-1的转染可提供共刺激分子,因此,同时利用B7-1和IFN-γ修饰肿瘤细胞制备肿瘤疫苗,或许可为肿瘤的免疫基因治疗提供新的途径。为便于应用,我们利用口蹄疫病毒的内在性核糖体插入位点(internal ribosome entry sites,IRES)成功地构建了B7-1、IFN-γ双顺反子逆转录病毒载体,转导肿瘤细胞得到了两者的共表达。
, http://www.100md.com
1 材料与方法
1.1 主要试剂
限制性内切酶、T4 DNA 连接酶等购自Promega GIBCO-BRL 公司,DOTAP脂质体转染试剂购自Boehringer mannheim 公司。
1.2 质粒载体和细胞株
人B7-1 (CD80) cDNA (PCDNA3 B7-1)由北京大学泌尿研究所邢念增博士提供,人IFN-γ cDNA(GCEN IFN-γ)由上海第二医科大学人类基因治疗中心陈诗书教授惠赠,含口蹄疫病毒内在性核糖体插入位点的质粒(PLNF2X)由美国华盛顿大学技术转让部提供。PUC18、逆转录病毒载体-PLXSN由本室保存。逆转录病毒包装细胞PT67购自CLONTECH 公司 (Clontech RetroPackTM PT67),小鼠成纤维细胞NIH3T3,取自美国模式物培养所,人上皮性卵巢癌细胞系3AO取自中科院上海细胞库,由本室冻存,传代培养。
, http://www.100md.com
2 结果
2.1 逆转录病毒载体B7-1的构建(图1)
人B7-1 cDNA基因编码序列为第318~第1181,其两侧为EcoR Ⅰ,位于pCDNA3之中,以EcoR Ⅰ酶切,回收1.0 kb的片段,将其插入逆转录病毒载体PLXSN的多克隆位点EcoR Ⅰ,粘端连接反应,转化TOP10,小量提取质粒,筛选正向重组克隆(PLXSN/B7-1) 。正、反向重组子经EcoR Ⅰ酶切均可释放出900bp 左右的B7-1条带,而经Sac Ⅰ酶切,正向重组子可切出3 214bp、2 004bp和1 646bp的3个片段,反向重组子则切出3 124bp、2 304bp和1 304bp的3个片段,借以鉴别。

图1 PLXSN/B7-1的构建和酶切鉴定
, http://www.100md.com
Figure 1 The construction and mapping of restriction
endonulease digestion of PLXSN/B7-1
2.2 IFN-γ构建入IRES 的下游
2.2.1 IFN-γ的克隆 首先利用PCR克隆技术扩增IFN-γ,在IFN-γ引物上游加上Hpa Ⅰ 位点,在其下游加上BamH Ⅰ、Xho Ⅰ位点,以便于以后的克隆。IFN-γ的引物由SyberSyn公司合成。
正义链
5′-CGCTGAGTTAACATGAAATATACAAGTTATA-TCTTGGC-3′
反义链
, 百拇医药
5′-GTACGTCTCGAGGATCCTTACTGGGATGCTC-TTCGACC-3′
IFN-γ的PCR条件:dNTP选择0.2 μmol.L-1,上下游引物均为1 μmol.L-1,Mg2+ 3.0 mmol.L-1,94 ℃ 1 min→60 ℃ 45 s→72 ℃ 45 s,28个循环,15 g.L-1琼脂糖凝胶电泳回收500 bp的片段,以Klenow酶补平,克隆入PUC18 HincⅡ,平端连接反应,经蓝白斑筛选,酶切鉴定重组克隆,PUC18/IFN-γ,并采用双脱氧末端终止法进行测序(由SynerSyn公司完成),测序结果与文献[5]、GeneBank(J00219)发表序列完全一致。
2.2.2 IFN-γ构建入IRES的下游 PUC18/IFN-γ经Hpa Ⅰ、Xho Ⅰ双酶切,回收500bp的片段,将其克隆入PLNF2X载体IRES下游的多克隆位点Hpa Ⅰ和Xho Ⅰ,一平一粘定向连接,经转化TOP10,筛选、酶切鉴定重组克隆,PLNF2X/IFN-γ。PLNF2X/IFN-γ经Hind Ⅲ酶切可释放出IFN-γ,经Sma Ⅰ酶切重组克隆可切出3 094bp、1 995bp和1 429bp 3条带,空载体则切出3 094bp、1 995bp和1 029bp的3条带,重组克隆的第3条带大于空载体,借以鉴别(图2)。

, 百拇医药
图2 PLNF2X/IFN-γ的构建和酶切鉴定
Figure 2 The construction and mapping of restriction
endonulease digestion map of PLNF2X/IFN-γ
2.3 将IRESIFN-γ克隆入PLXSN/B7-1
PLNF2X/IFN-γ经Sma Ⅰ、BamH Ⅰ酶切,回收含有IRESIFN-γ约900bp的片段,克隆入逆转录病毒载体PLXSN/B7-1的多克隆位点Hpa Ⅰ、BamH Ⅰ,一平一粘定向克隆,经转化TOP10,筛选重组克隆,PLXSN/B7-1 IFN-γ,酶切鉴定。其构建策略(图3)。
2.4 逆转录病毒的包装及滴度测定[6]
, 百拇医药
将编码B7-1和IFN-γ的双顺反子重组逆转录病毒载体PLXSN/B7-1 IFN-γ和空载体PLXSN,采用脂质体方法,转染逆转录病毒包装细胞PT67,操作按说明书进行。经G418筛选,大约2周后出现抗性克隆,约3周时克隆变大,采用滤纸消化法转移单克隆,扩大培养,至产病毒细胞株80%融合时,换液收集24 h的病毒液。病毒滴度的测定采用生物学方法,各筛选出一株高滴度的产病毒细胞株。

图3 PLXSN/B7-1IFN-γ的构建示意图
Figure 3 Diagram of the construction of bicistronic retroviral
vector of B7-1 and IFN-γ
2.5 卵巢癌细胞系的转导
, 百拇医药
3AO传代24 h后,使细胞达到30%~40%汇合(confluent),将收集的24 h病毒上清,加Polybrene( Sigma )至8 mg.L-1,0.45 μm针头式滤器过滤,加入上述细胞中,感染24 h后,换为完全RPMI1640,再过24 h,1∶5传代入G418筛选培养基中,G418的质量浓度为600 mg.L-1,每4~5天换液1次,至3周左右出现克隆,至克隆增大后,仍采用滤纸法消化转移克隆,每种转移4~6个克隆,此时G418质量浓度降为300 mg.L-1维持,满瓶后,再传代时撤掉G418,扩大培养。
2.6 B7-1、IFN-γ在转导细胞系共表达
2.6.1 RT-PCR 采用GIBCO公司的TRIZOL试剂提取细胞的总RNA,利用IFN-γ的下游引物进行特异引物的反转录,然后进行B7-1、IFN-γ的聚合链酶反应。B7-1的引物由SynerSyn公司合成。
, http://www.100md.com
正义链5′-ATGGGCCACACACGGAGG-3′
反义链5′-TTATACTGGGCGTACACT-3′
IFN-γ的引物见上。其扩增产物分别为867bp和500bp。逆转录反应在25 μl的反应体系中,含总RNA 2 μg,IFN-γ的下游引物25 pmol,200 μmol.L-1-MLV,按Promega公司M-MLV说明书进行。B7-1的PCR扩增条件为:95 ℃ 1 min,47 ℃ 1 min,70 ℃ 1 min,35个循环,IFN-γ的PCR扩增条件同上,35个循环。同时设原始3AO细胞作为对照,则无B7、IFN-γ的扩增。
2.6.2 免疫流式细胞测定 转导的卵巢癌细胞3AO/B7-1IFN-γ,培养至90%汇合时,加3 mmol.L-1的莫能星(moensin)6 h,以阻断IFN-γ的释放,之后以2.5 g.L-1胰蛋白酶和0.2 g.L-1EDTA消化成单细胞悬液,立即标记。B7-1、IFNγ的抗体均购自库尔特公司,B7-1系PE直标抗体,而IFN-γ系FITC直标抗体,标记方法按照库尔特公司产品说明书和文献[7]报道进行。
, http://www.100md.com
2.7 B7-1、IFN-γ共表达的RT-PCR
利用IFN-γ的下游引物进行特异引物的反转录,可分别扩增出867bp和500bp的B7-1、IFN-γ条带,说明B7-1和IFN-γ的共表达,并且其表达来自于同一条mRNA(图4)。

图4 B7-1、IFN-γ共表达的RT-PCR
Figure 4 The co-expression of B7-1,IFN-γ detected by RT-PCR
2.8 B7-1、IFN-γ共表达的免疫流式测定(图5)
利用免疫双标记可检测到在同一细胞B7-1、IFN-γ的共表达,其共表达百分率为32.2%,而未转导或转导PLXSN空载体的3AO细胞则无B7-1、IFN-γ的表达(0.22%)。
, http://www.100md.com
3 讨论
用免疫基因修饰肿瘤细胞以增强其免疫原性是肿瘤免疫基因治疗的策略之一。通过基因转染技术,使肿瘤细胞表达某些细胞因子,通过自分泌提高肿瘤细胞自身MHC分子的表达,或通过旁分泌作用于抗原呈递细胞或T细胞可诱导肿瘤免疫反应。IL-2、IL-4、IFN-γ、GM-CSF单独转染肿瘤细胞均诱导了T细胞免疫;另外一个重要的策略则是使肿瘤细胞具备抗原呈递细胞的某些功能,如转染共刺激分子B7-1,也诱导了肿瘤排斥[1]。然而,在某些肿瘤,即使转染某些细胞因子或B7-1并不足以引起肿瘤排斥,这可归咎于肿瘤细胞MHC分子、肿瘤抗原的表达下调或缺乏,缺乏粘附分子、分泌免疫抑制因子,从而降低了肿瘤细胞的免疫原性,而且肿瘤细胞还缺乏共刺激分子的表达,而B7介导的肿瘤排斥与肿瘤细胞的免疫原性密切相关[8~9]。Hurwttz[10]的研究表明,利用B7-1和IFN-γ共同修饰黑色素瘤可诱导很强的肿瘤免疫,明显优于单独转染一种因子的肿瘤疫苗。卵巢癌细胞缺乏共刺激分子的表达,MHCⅠ、Ⅱ类分子的表达缺失或降低(另文发表),因而同样适用于B7-1、IFN-γ双细胞因子的免疫基因治疗。

, 百拇医药
图5 B7-1、IFN-γ共表达的免疫流式细胞测定
Figure 5 Immuno-flow cytometry detection of the co-expression
of B7-1 and IFN-γ
如何构建双细胞因子的共表达载体,目前有双转染、双启动子载体、双顺反子载体3种方法[10~12]。此3种方法之中,利用IRES构建双/多顺反子表达载体具有操作简便,基因的表达效率相同等优点,因而在基因治疗中具有重要的作用。利用IRES构建双/多顺反子表达载体是基于真核细胞蛋白质翻译的链内启动模式机制而设计的[13]。本文利于口蹄疫病毒的IRES首次成功地构建了B7-1、IFN-γ共表达载体,转导卵巢癌细胞系3AO,利用RT-PCR和免疫流式细胞测定证实了两者在同一细胞的共表达,利用IFN-γ的下游引物进行特异引物的反转录,可同时扩增出B7-1和IFN-γ,表明两者的翻译来自于同一条mRNA。
, 百拇医药
本研究首先利用FMDS IRES成功地构建了B7-1和IFN-γ共表达逆转录病毒载体,为制备B7-1和IFN-γ修饰的肿瘤疫苗奠定了基础,其进一步的应用研究正在进行之中。本研究同时也为构建其它多细胞因子或双亚基细胞因子(如IL-12)表达载体的研究提供了借鉴。
参考文献
1,Berd D.Cancer vaccine:Reborn or just recycled[J]? Seminars Oncol,1998,25:605-601
2,June CH,Bluestron JA,Nadler LM,et al.The B7 and CD28 receptor families[J].Immunol Today,1994,15:321
3,Driscoll J,Brown MG,Finley D,et al.MHC-linked LMP gene products specifically after peptidaseactivities of proteasome[J].Nature,1993,365:262-264
, 百拇医药
4,Gaczynska M,Rock KL,Goldberg AL.Gamma-interferonand expression of MHC genes regulate peptidehydrolysis by proteasomes[J].Nature,1993,365:264-267
5,Devos R,Cheroutre H,Taya Y,et al.Molecularcloning of human immune interferon cDNA and itsexpression eukaryotic cells[J].Nucleic Acid Res,1982,10:2487-2501
6,蒋 泊,张亚历,周殿元主编.分子生物学常用实验方法[M].北京:人民军医出版社,1996.160-161
7,Jung T,Schauer U,Heusser C,et al.Detection of intracellular cytokines by flow cytometry[J].Jimmuno Meth,1993,159:197-207
, 百拇医药
8,Allison JP,Hurwitz AA and Leach DR.Manipulation of costimulatory signals to enhance antitumor T cell responses[J].Curr Opin Immunol,1995,7:682-686
9,Chen L,McGowan P,Ashe S.et al.Tumor immunogenesity determines the effect of B7 co-stimulation on T cells-mediated tumor immunity[J].J Exp Med,1994,179:523-532
10,Hurwttz AA,Townsend SE,Yu TF,et al.Enhancement of the anti-tumor immune response using a combination of intyerferon- and B7 expression in an experimental mammary carcinoma[J].Int J Cancer,1998,77:107-113
, 百拇医药
11,Ramesh N,Kim ST,Wei MQ,et al.High-titer bicistronic retroviral vectors employing foot-and-mouth disease virus internal ribosome entry site[J].Nucleic Acid Res,1996,24:2697-2700
12,Rosenthal FM,Cronin K,Bannerji R,et al.Augmintation of antitumor immunity by tumor cells transduced with a retroviral vector carrying the interleukin-2 and interferon-cDNAs[J].Blood,1994,83:1289-1298
13,沈 琲,方福德主编.真核基因表达调控[M].北京:高等教育出版社,1996.51-53
收稿日期:1999-03-03, http://www.100md.com