NIDDM大鼠骨骼肌组织GLUT4mRNA表达及其与胰岛素分泌关系的实验研究
作者:钱东生 何敏 罗琳 朱毅芳 鄂群
单位:钱东生 何敏 罗琳 朱毅芳(南通医学院药理学教研室);鄂群(病理学教研室,南通226001)
关键词:非胰岛素依赖型糖尿病葡萄糖转运体4胰岛素
中国临床药理学与治疗学000410
目的观察非胰岛素依赖型糖尿病(NIDDM)大鼠骨骼肌葡萄糖转运体4(glucose transporter 4,GLUT4)mRNA表达及其与胰岛素分泌的关系。方法制备NIDDM大鼠模型,用Northernblot方法测定骨骼肌组织中GLUT4mRNA表达量;放射免疫法测定血清胰岛素含量;免疫组化法观察胰岛胰岛素阳性β细胞。结果NIDDM大鼠骨骼肌GLUT4mRNA表达显著低下,仅为对照组的45%(P<0.01);其空腹基础胰岛素水平正常,但葡萄糖耐量试验胰岛素水平较对照组明显降低,2h胰岛素分泌有延迟现象;免疫组化实验NIDDM大鼠胰岛体积减少一半以上,胰岛素阳性β细胞数量明显减少。结论NIDDM大鼠骨骼肌GLUT4mRNA表达量低下,该反应与体内胰岛素分泌水平呈现一定的正相关性。
, http://www.100md.com
中图分类号R567.1
Experiment study of the GLUT4 mRNA expression
in the skeletal muscle and the relationship between GLUT4 mRNA expression and insulin secretion in NIDDM rats
QIAN Dong_Sheng HE Min LUO Lin ZHU Yi_Fang
(Department of Pharmacology)
E Qun
(Department of Pathology, Nantong Medical College, Nantong 226001)
, 百拇医药
Aim To observe the glucose transporter 4 (GLUT4) mRNA expression in the skeletal muscle and the relationship between GLUT4 mRNA expression and insulin secretion in non_insulin_dependent diabetes mellitus (NIDDM) rats.Methods The rat models of NIDDM were made. The GLUT4 mRNA expression in skeletal muscle was observed with Northern blot method. The serum insulin was determined by radioimmunoassay. The change of insulin positive β cell in islet was observed by immunohistochemistry.Results The GLUT4 mRNA expression in skeletal muscle in NIDDM rats was decreased to 45% of that in normal rats (P<0.01).The fast serum insulin level was normal, but in oral glucose test, the secretion of insulin was reduced markedly and a phenomenon of delayed secretion was observed. Immunohistochemistry experiment displayed that the volume of islet in NIDDM rats was smaller than half of that in normal rats and the number of insulin positive β cells reduced markedly.Conclusion The present study showes that in NIDDM rats the GLUT4 mRNA expression in skeletal muscle is lower and this response is considered to have some positive correlation with insulin secretion.
, http://www.100md.com
Key words non_insulin_dependent diabetes mellitus(NIDDM); glucose transporter 4(GLUT4); insulin
非胰岛素依赖型糖尿病(NIDDM)大鼠模型的建立对于研究药物对该病的防治作用具有重要意义。本实验室给予新生大鼠一次性腹腔注射链脲佐菌素(streptozotocin,STZ),9wk后成功地制备了NIDDM大鼠模型[1]。骨骼肌是最主要的利用葡萄糖的外周组织,葡萄糖转运体4(glucosetransporter4,GLUT4)在该组织中具有高表达[2],其介导葡萄糖的跨膜转运,为骨骼肌利用葡萄糖的主要限速步骤[3],当GLUT4发生改变时,可导致葡萄糖跨膜转运异常。本实验研究NIDDM大鼠骨骼肌组织中GLUT4mRNA的表达及其与胰岛素分泌的关系,对GLUT4在NIDDM发病机理中的作用进行初步探索。
, 百拇医药
1 材料与方法
1.1材料
1.1.1动物SD大鼠,雌雄兼用,南通医学院实验动物中心提供。合格证:苏动(质)98025,苏动(环)98062。
1.1.2试剂链脲佐菌素(STZ),Sigma公司;限制性核酸内切酶,华美生物工程公司;随机引物标记试剂盒,Promega公司;Hybond_N+尼龙膜,Amersham公司;Trizol,Gibco公司;[α32P]_dCTP,北京亚辉公司。含葡萄糖转运体4(GLUT4)cDNA(2086bp)质粒,南通医学院分子生物学研究室郑震林博士惠赠;含3_磷酸甘油醛脱氢酶(GAPDH)cDNA(1008bp)质粒,南通医学院生物化学教研室刘飞博士惠赠;125I_胰岛素放免测定试剂盒,北京北方生物技术研究所;抗胰岛素抗体,购自Zymed公司;Biotin标记二抗和ABC试剂盒,购自武汉博士德公司;其余试剂均为国产分析纯。
, 百拇医药
1.2方法
1.2.1NIDDM大鼠模型的制备[1,4]取1d龄SD大鼠,一次性腹腔注射链脲佐菌素(STZ)(溶于0.1mol.L-1柠檬酸缓冲液,pH4.5)95mg.kg-1,对照组腹腔注射等量柠檬酸缓冲液。大鼠断奶后,正常饲料喂养。9wk后测定糖耐量、血清胰岛素等,造模成功者用于实验研究。
1.2.2基础胰岛素、口服葡萄糖后胰岛素水平测定取模型组和正常对照组大鼠各8只,禁食12h,尾静脉取血400μl,15min后灌注20%葡萄糖溶液(2g.kg-1),于口服葡萄糖后0、15、30、60、120min取血各400μl,所采血样4℃5000rpm离心10min,取血浆100μl,用FMJ_182型γ_放射免疫计数器(上海原子能研究所),按胰岛素放免分析试剂盒说明书测定血胰岛素水平。
, http://www.100md.com
1.2.3标本收集正常和NIDDM大鼠,用20%乌拉坦麻醉,迅速取大腿肌肉组织,置于液氮中,进行总RNA提取。另取大鼠胰腺组织固定,进行免疫组化实验。
1.2.4RNA提取及Northernblot用Trizol试剂提取肌肉组织总RNA,紫外分光光度计测定RNA浓度。总RNA经甲醛变性胶电泳后,毛细管法转移至尼龙膜,80℃固定2h。含GLUT4cDNA质粒经扩增、提取、酶切、电泳、回收,得到GLUT4cDNA,随机引物标记[α32P]_dCTP。尼龙膜于65℃磷酸盐缓冲液中预杂交、杂交,洗膜后-70℃放射自显影。所有样膜经洗脱探针后用GAPDHcDNA探针再杂交,作内参照以校正RNA上样量,最后图像分析杂交信号进行光密度(A值)扫描。
1.2.5免疫组化实验胰腺组织石蜡包埋后切片厚4~5μm。切片经二甲苯脱蜡、系列酒精水化,0.01mol.L-1pH7.4PBS缓冲液洗涤3次,滴加蒸馏水新鲜配置的3%H2O2,室温5~10min,以消除内源性过氧化物酶;PBS洗3次后,用正常血清封闭,室温10min;吸去正常血清,滴加1∶50小鼠抗胰岛素抗体,4℃过夜,PBS洗3次;滴加生物素化山羊抗小鼠IgG(1∶200),37℃30min;PBS洗3次后加ABC试剂,37℃30min;PBS洗3次后,加DAB显色液,室温显色,镜下控制反应时间,蒸馏水洗涤,苏木精复染,分色,系列酒精脱水,二甲苯透明,中性树胶封片。
, http://www.100md.com
1.3统计学处理数据采用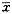 ±s表示,采用组间t检验。
±s表示,采用组间t检验。
2 结果
2.1Northernblot检测骨骼肌组织GLUT4mRNA表达对照组GLUT4mRNA有高表达,NIDDM组大鼠GLUT4mRNA表达明显低下,表达量只有对照组的45%,见图1,表1。
图1NIDDM大鼠骨骼肌GLUT4mRNA表达Northernblot分析
A:对照组;B:NIDDM组 表1NIDDM大鼠骨骼肌GLUT4mRNA表达变化(
表1NIDDM大鼠骨骼肌GLUT4mRNA表达变化(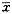 ±s,n=6)
±s,n=6)
, http://www.100md.com
2.2NIDDM大鼠基础胰岛素及糖耐量试验胰岛素分泌水平NIDDM大鼠空腹基础胰岛素水平与对照组比较无明显差别。NIDDM大鼠口服葡萄糖后,胰岛素水平较对照组明显降低,15、30、60min血清胰岛素量与对照组比较差异非常显著,但120min胰岛素有延时分泌现象,见表2。
表1 NIDDM 大鼠骨骼肌GLUT4mRNA表达变化(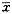 ±s) 组别
±s) 组别
GLUT4mRNA 表达量
对照组
0.935±0.044
NIDDM组
0.425±0.095**
, http://www.100md.com
数据示GLUT4mRNA密度值与GAPDHmRNA密度值的比值。与对照组比较**P<0.01表2 NIDDM大鼠基础血清胰岛素及糖耐量试验血清胰岛素水平(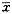 ±sn=8) 组别
±sn=8) 组别
基础胰岛素/μU.ml-1
糖耐量试验胰岛素μU.ml-1
15min
30min
60min
120min
对照组
13.7±3.8
, http://www.100md.com
31.7±12.3
26.1±9.0
21.0±6.5
16.3±5.8
NIDDM组
12.3±4.9
14.4±7.2**
15.4±6.1*
12.4±7.2
17.2±8.4
2.3免疫组化实验对照组大鼠胰岛形态正常,NIDDM大鼠胰岛数量与对照组比较无明显差异,但体积减少一半以上。对照组大鼠胰岛胰岛素阳性β细胞棕黄色颗粒多,颜色深,而NIDDM大鼠胰岛胰岛素阳性β细胞棕黄色颗粒较少,颜色较浅,表明β细胞数量明显减少,见图2。
, 百拇医药
图2免疫组化实验结果
左图:对照大鼠胰岛(×500);右图:NIDDM大鼠胰岛(×500)
3 讨论
葡萄糖从细胞外向细胞内的转运是通过葡萄糖转运蛋白(glucosetransporters,GLUTs)实现的。GLUTs具有12种亚型,目前已明确其中6种亚型,这些转运蛋白的表达具有组织和细胞特异性,呈现独特的动力学和调节葡萄糖转运的特征。在外周组织中,最主要的利用葡萄糖的组织是骨骼肌,GLUT4在该组织中具有高表达,它促进进食后葡萄糖在该组织中转运,在维持全身葡萄糖体内平衡方面发挥重要作用[2]。
GLUT4为胰岛素敏感型葡萄糖转运体,研究表明,胰岛素可促进GLUT4mRNA的表达以及随后的GLUT4转运蛋白合成增加。对于胰岛素依赖型糖尿病大鼠(IDDM),胰岛功能完全丧失,血浆胰岛素水平低下,因此,GLUT4mRNA表达量及GLUT4转运蛋白合成减少,导致葡萄糖从外周向细胞内转运减少,血糖升高,引发糖尿病,用胰岛素治疗后,GLUT4mRNA及GLUT4水平又可增加[5~7]。非胰岛素依赖型糖尿病(NIDDM)的主要病变是胰岛素抵抗,胰岛病理改变大都较轻,血浆胰岛素水平有双向变化,即有时增高或分泌延时,高血糖及低血糖可以交替出现[8]。GLUT4mRNA在NIDDM大鼠体内表达的研究国内未见报道。我们成功地制备了NIDDM大鼠模型,与文献报道结果一致[4,9]。在此基础上,研究了骨骼肌组织中GLUT4mRNA表达量的变化,结果表明NIDDM大鼠GLUT4mRNA表达量明显低于对照组大鼠。
, 百拇医药
对GLUT4mRNA表达与胰岛素分泌关系的研究发现,在NIDDM大鼠,胰岛素基础分泌量正常,口服葡萄糖耐量试验胰岛素分泌在1h内明显低于对照组,2h有延时分泌现象。免疫组化研究发现NIDDM大鼠胰岛体积明显缩小,胰岛β细胞数量明显减少,表明胰岛受到一定程度的损伤,但没有完全破坏。以上实验结果表明,NIDDM大鼠体内胰岛功能尚存,但对葡萄糖刺激的反应性低下,尽管有延时分泌,但总体胰岛素水平较对照组低,导致GLUT4mRNA表达量及随后的GLUT4合成减少,骨骼肌等外周组织转运葡萄糖能力下降,从而诱发NIDDM。
许多研究表明,GLUT4质和量的异常是胰岛素受体后抵抗的主要原因之一。本研究结果对于认识NIDDM的发病机制具有一定的意义。本研究亦有助于从分子基因水平探索药物防治糖尿病的作用及机理。
钱东生,男,38岁,硕士,副教授。
参 考 文 献
, http://www.100md.com
1,钱生,朱毅芳,何敏,等.非胰岛素依赖型糖尿病大鼠模型制备的实验研究.南通医学院学报,2000;20(1):18
2,Mueckler M. Facilitative glucose transporters.Eur J Biochem,1994;219(3):713
3,Fink RI, Wallace P, Brechtel G, et al. Evidence that glucose transport is rate limiting for in vivo glucose uptake.Metabolism, 1992;41(8):897
4,Itzchak A, Ré my B, Monique P,et al. Normalization of insulin secretion by a selective α 2_adrenoceptor antagonist restores GLUT_4 glucose transporter ex_ pression in adipose tissue of type Ⅱ diabetic rats. Endocrinology, 1996; 137:2022 5,Sivitz WI, Bailey HL, Donohoue P.Rat adipose ob mRNA level in states of altered circulating glucose and insulin. Biochem Biophys Res Commum, 1996; 220(3):520
, 百拇医药
6,Wang H, Chen J, Chai J. A study of mRNA expres_ sion of glucose transporter gene in rats with diabetes mellitus. Chin Med J, 1995;108(12):892
7,Hoenack C,Roesen P.Inhibition of angiotension type 1 receptor prevents decline of glucose transporter (GLUT4) in diabetic rat heart. Diabetes,1996;45 suppl 1:S82
8,霍玉书.治疗糖尿病(消渴症)中药药效学研究的设计方法.中药新药与临床药理,1995;6(4):26
9,Portha B, Blondel O, Serradas P,et al. The rat model of non_insulin dependent diabetes induced by neonatal streptozotocin. Diabete Metab, 1989;15(2): 61
2000-06-27收稿,2000-08-16修回, 百拇医药
单位:钱东生 何敏 罗琳 朱毅芳(南通医学院药理学教研室);鄂群(病理学教研室,南通226001)
关键词:非胰岛素依赖型糖尿病葡萄糖转运体4胰岛素
中国临床药理学与治疗学000410
目的观察非胰岛素依赖型糖尿病(NIDDM)大鼠骨骼肌葡萄糖转运体4(glucose transporter 4,GLUT4)mRNA表达及其与胰岛素分泌的关系。方法制备NIDDM大鼠模型,用Northernblot方法测定骨骼肌组织中GLUT4mRNA表达量;放射免疫法测定血清胰岛素含量;免疫组化法观察胰岛胰岛素阳性β细胞。结果NIDDM大鼠骨骼肌GLUT4mRNA表达显著低下,仅为对照组的45%(P<0.01);其空腹基础胰岛素水平正常,但葡萄糖耐量试验胰岛素水平较对照组明显降低,2h胰岛素分泌有延迟现象;免疫组化实验NIDDM大鼠胰岛体积减少一半以上,胰岛素阳性β细胞数量明显减少。结论NIDDM大鼠骨骼肌GLUT4mRNA表达量低下,该反应与体内胰岛素分泌水平呈现一定的正相关性。
, http://www.100md.com
中图分类号R567.1
Experiment study of the GLUT4 mRNA expression
in the skeletal muscle and the relationship between GLUT4 mRNA expression and insulin secretion in NIDDM rats
QIAN Dong_Sheng HE Min LUO Lin ZHU Yi_Fang
(Department of Pharmacology)
E Qun
(Department of Pathology, Nantong Medical College, Nantong 226001)
, 百拇医药
Aim To observe the glucose transporter 4 (GLUT4) mRNA expression in the skeletal muscle and the relationship between GLUT4 mRNA expression and insulin secretion in non_insulin_dependent diabetes mellitus (NIDDM) rats.Methods The rat models of NIDDM were made. The GLUT4 mRNA expression in skeletal muscle was observed with Northern blot method. The serum insulin was determined by radioimmunoassay. The change of insulin positive β cell in islet was observed by immunohistochemistry.Results The GLUT4 mRNA expression in skeletal muscle in NIDDM rats was decreased to 45% of that in normal rats (P<0.01).The fast serum insulin level was normal, but in oral glucose test, the secretion of insulin was reduced markedly and a phenomenon of delayed secretion was observed. Immunohistochemistry experiment displayed that the volume of islet in NIDDM rats was smaller than half of that in normal rats and the number of insulin positive β cells reduced markedly.Conclusion The present study showes that in NIDDM rats the GLUT4 mRNA expression in skeletal muscle is lower and this response is considered to have some positive correlation with insulin secretion.
, http://www.100md.com
Key words non_insulin_dependent diabetes mellitus(NIDDM); glucose transporter 4(GLUT4); insulin
非胰岛素依赖型糖尿病(NIDDM)大鼠模型的建立对于研究药物对该病的防治作用具有重要意义。本实验室给予新生大鼠一次性腹腔注射链脲佐菌素(streptozotocin,STZ),9wk后成功地制备了NIDDM大鼠模型[1]。骨骼肌是最主要的利用葡萄糖的外周组织,葡萄糖转运体4(glucosetransporter4,GLUT4)在该组织中具有高表达[2],其介导葡萄糖的跨膜转运,为骨骼肌利用葡萄糖的主要限速步骤[3],当GLUT4发生改变时,可导致葡萄糖跨膜转运异常。本实验研究NIDDM大鼠骨骼肌组织中GLUT4mRNA的表达及其与胰岛素分泌的关系,对GLUT4在NIDDM发病机理中的作用进行初步探索。
, 百拇医药
1 材料与方法
1.1材料
1.1.1动物SD大鼠,雌雄兼用,南通医学院实验动物中心提供。合格证:苏动(质)98025,苏动(环)98062。
1.1.2试剂链脲佐菌素(STZ),Sigma公司;限制性核酸内切酶,华美生物工程公司;随机引物标记试剂盒,Promega公司;Hybond_N+尼龙膜,Amersham公司;Trizol,Gibco公司;[α32P]_dCTP,北京亚辉公司。含葡萄糖转运体4(GLUT4)cDNA(2086bp)质粒,南通医学院分子生物学研究室郑震林博士惠赠;含3_磷酸甘油醛脱氢酶(GAPDH)cDNA(1008bp)质粒,南通医学院生物化学教研室刘飞博士惠赠;125I_胰岛素放免测定试剂盒,北京北方生物技术研究所;抗胰岛素抗体,购自Zymed公司;Biotin标记二抗和ABC试剂盒,购自武汉博士德公司;其余试剂均为国产分析纯。
, 百拇医药
1.2方法
1.2.1NIDDM大鼠模型的制备[1,4]取1d龄SD大鼠,一次性腹腔注射链脲佐菌素(STZ)(溶于0.1mol.L-1柠檬酸缓冲液,pH4.5)95mg.kg-1,对照组腹腔注射等量柠檬酸缓冲液。大鼠断奶后,正常饲料喂养。9wk后测定糖耐量、血清胰岛素等,造模成功者用于实验研究。
1.2.2基础胰岛素、口服葡萄糖后胰岛素水平测定取模型组和正常对照组大鼠各8只,禁食12h,尾静脉取血400μl,15min后灌注20%葡萄糖溶液(2g.kg-1),于口服葡萄糖后0、15、30、60、120min取血各400μl,所采血样4℃5000rpm离心10min,取血浆100μl,用FMJ_182型γ_放射免疫计数器(上海原子能研究所),按胰岛素放免分析试剂盒说明书测定血胰岛素水平。
, http://www.100md.com
1.2.3标本收集正常和NIDDM大鼠,用20%乌拉坦麻醉,迅速取大腿肌肉组织,置于液氮中,进行总RNA提取。另取大鼠胰腺组织固定,进行免疫组化实验。
1.2.4RNA提取及Northernblot用Trizol试剂提取肌肉组织总RNA,紫外分光光度计测定RNA浓度。总RNA经甲醛变性胶电泳后,毛细管法转移至尼龙膜,80℃固定2h。含GLUT4cDNA质粒经扩增、提取、酶切、电泳、回收,得到GLUT4cDNA,随机引物标记[α32P]_dCTP。尼龙膜于65℃磷酸盐缓冲液中预杂交、杂交,洗膜后-70℃放射自显影。所有样膜经洗脱探针后用GAPDHcDNA探针再杂交,作内参照以校正RNA上样量,最后图像分析杂交信号进行光密度(A值)扫描。
1.2.5免疫组化实验胰腺组织石蜡包埋后切片厚4~5μm。切片经二甲苯脱蜡、系列酒精水化,0.01mol.L-1pH7.4PBS缓冲液洗涤3次,滴加蒸馏水新鲜配置的3%H2O2,室温5~10min,以消除内源性过氧化物酶;PBS洗3次后,用正常血清封闭,室温10min;吸去正常血清,滴加1∶50小鼠抗胰岛素抗体,4℃过夜,PBS洗3次;滴加生物素化山羊抗小鼠IgG(1∶200),37℃30min;PBS洗3次后加ABC试剂,37℃30min;PBS洗3次后,加DAB显色液,室温显色,镜下控制反应时间,蒸馏水洗涤,苏木精复染,分色,系列酒精脱水,二甲苯透明,中性树胶封片。
, http://www.100md.com
1.3统计学处理数据采用
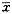 ±s表示,采用组间t检验。
±s表示,采用组间t检验。2 结果
2.1Northernblot检测骨骼肌组织GLUT4mRNA表达对照组GLUT4mRNA有高表达,NIDDM组大鼠GLUT4mRNA表达明显低下,表达量只有对照组的45%,见图1,表1。

图1NIDDM大鼠骨骼肌GLUT4mRNA表达Northernblot分析
A:对照组;B:NIDDM组
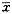 ±s,n=6)
±s,n=6), http://www.100md.com
2.2NIDDM大鼠基础胰岛素及糖耐量试验胰岛素分泌水平NIDDM大鼠空腹基础胰岛素水平与对照组比较无明显差别。NIDDM大鼠口服葡萄糖后,胰岛素水平较对照组明显降低,15、30、60min血清胰岛素量与对照组比较差异非常显著,但120min胰岛素有延时分泌现象,见表2。
表1 NIDDM 大鼠骨骼肌GLUT4mRNA表达变化(
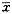 ±s) 组别
±s) 组别GLUT4mRNA 表达量
对照组
0.935±0.044
NIDDM组
0.425±0.095**
, http://www.100md.com
数据示GLUT4mRNA密度值与GAPDHmRNA密度值的比值。与对照组比较**P<0.01表2 NIDDM大鼠基础血清胰岛素及糖耐量试验血清胰岛素水平(
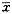 ±sn=8) 组别
±sn=8) 组别基础胰岛素/μU.ml-1
糖耐量试验胰岛素μU.ml-1
15min
30min
60min
120min
对照组
13.7±3.8
, http://www.100md.com
31.7±12.3
26.1±9.0
21.0±6.5
16.3±5.8
NIDDM组
12.3±4.9
14.4±7.2**
15.4±6.1*
12.4±7.2
17.2±8.4
2.3免疫组化实验对照组大鼠胰岛形态正常,NIDDM大鼠胰岛数量与对照组比较无明显差异,但体积减少一半以上。对照组大鼠胰岛胰岛素阳性β细胞棕黄色颗粒多,颜色深,而NIDDM大鼠胰岛胰岛素阳性β细胞棕黄色颗粒较少,颜色较浅,表明β细胞数量明显减少,见图2。

, 百拇医药
图2免疫组化实验结果
左图:对照大鼠胰岛(×500);右图:NIDDM大鼠胰岛(×500)
3 讨论
葡萄糖从细胞外向细胞内的转运是通过葡萄糖转运蛋白(glucosetransporters,GLUTs)实现的。GLUTs具有12种亚型,目前已明确其中6种亚型,这些转运蛋白的表达具有组织和细胞特异性,呈现独特的动力学和调节葡萄糖转运的特征。在外周组织中,最主要的利用葡萄糖的组织是骨骼肌,GLUT4在该组织中具有高表达,它促进进食后葡萄糖在该组织中转运,在维持全身葡萄糖体内平衡方面发挥重要作用[2]。
GLUT4为胰岛素敏感型葡萄糖转运体,研究表明,胰岛素可促进GLUT4mRNA的表达以及随后的GLUT4转运蛋白合成增加。对于胰岛素依赖型糖尿病大鼠(IDDM),胰岛功能完全丧失,血浆胰岛素水平低下,因此,GLUT4mRNA表达量及GLUT4转运蛋白合成减少,导致葡萄糖从外周向细胞内转运减少,血糖升高,引发糖尿病,用胰岛素治疗后,GLUT4mRNA及GLUT4水平又可增加[5~7]。非胰岛素依赖型糖尿病(NIDDM)的主要病变是胰岛素抵抗,胰岛病理改变大都较轻,血浆胰岛素水平有双向变化,即有时增高或分泌延时,高血糖及低血糖可以交替出现[8]。GLUT4mRNA在NIDDM大鼠体内表达的研究国内未见报道。我们成功地制备了NIDDM大鼠模型,与文献报道结果一致[4,9]。在此基础上,研究了骨骼肌组织中GLUT4mRNA表达量的变化,结果表明NIDDM大鼠GLUT4mRNA表达量明显低于对照组大鼠。
, 百拇医药
对GLUT4mRNA表达与胰岛素分泌关系的研究发现,在NIDDM大鼠,胰岛素基础分泌量正常,口服葡萄糖耐量试验胰岛素分泌在1h内明显低于对照组,2h有延时分泌现象。免疫组化研究发现NIDDM大鼠胰岛体积明显缩小,胰岛β细胞数量明显减少,表明胰岛受到一定程度的损伤,但没有完全破坏。以上实验结果表明,NIDDM大鼠体内胰岛功能尚存,但对葡萄糖刺激的反应性低下,尽管有延时分泌,但总体胰岛素水平较对照组低,导致GLUT4mRNA表达量及随后的GLUT4合成减少,骨骼肌等外周组织转运葡萄糖能力下降,从而诱发NIDDM。
许多研究表明,GLUT4质和量的异常是胰岛素受体后抵抗的主要原因之一。本研究结果对于认识NIDDM的发病机制具有一定的意义。本研究亦有助于从分子基因水平探索药物防治糖尿病的作用及机理。
钱东生,男,38岁,硕士,副教授。
参 考 文 献
, http://www.100md.com
1,钱生,朱毅芳,何敏,等.非胰岛素依赖型糖尿病大鼠模型制备的实验研究.南通医学院学报,2000;20(1):18
2,Mueckler M. Facilitative glucose transporters.Eur J Biochem,1994;219(3):713
3,Fink RI, Wallace P, Brechtel G, et al. Evidence that glucose transport is rate limiting for in vivo glucose uptake.Metabolism, 1992;41(8):897
4,Itzchak A, Ré my B, Monique P,et al. Normalization of insulin secretion by a selective α 2_adrenoceptor antagonist restores GLUT_4 glucose transporter ex_ pression in adipose tissue of type Ⅱ diabetic rats. Endocrinology, 1996; 137:2022 5,Sivitz WI, Bailey HL, Donohoue P.Rat adipose ob mRNA level in states of altered circulating glucose and insulin. Biochem Biophys Res Commum, 1996; 220(3):520
, 百拇医药
6,Wang H, Chen J, Chai J. A study of mRNA expres_ sion of glucose transporter gene in rats with diabetes mellitus. Chin Med J, 1995;108(12):892
7,Hoenack C,Roesen P.Inhibition of angiotension type 1 receptor prevents decline of glucose transporter (GLUT4) in diabetic rat heart. Diabetes,1996;45 suppl 1:S82
8,霍玉书.治疗糖尿病(消渴症)中药药效学研究的设计方法.中药新药与临床药理,1995;6(4):26
9,Portha B, Blondel O, Serradas P,et al. The rat model of non_insulin dependent diabetes induced by neonatal streptozotocin. Diabete Metab, 1989;15(2): 61
2000-06-27收稿,2000-08-16修回, 百拇医药