布洛芬混悬液在正常人体内的相对生物利用度和药代动力学
作者:李 智 谌立伟 郭兆贵
单位:湖南医科大学临床药理国家培训中心(长沙 410078)
关键词:布洛芬;药代动力学;色谱法,高压液相
湖南医学/990402 摘 要 【目的】比较研究布洛芬混悬液和市售布洛芬片的生物利用度和药代动力学。【方法】选择8名健康男性志愿者,随机分为两组,进行单次混悬液或片剂交叉给药600 mg后,利用HPLC法测定血浆中布洛芬浓度。【结果】两组血浆的布洛芬浓度分别在(0.92±0.33)和(1.68±0.51) h达到峰值(13.88±1.92)和(11.07±2.51) μg/ml。血药浓度曲线下面积(AUC)分别达(47.77±3.46)和(45.23±5.21) μg/(min.ml),混悬液的相对生物利用度(F)为(105.6±11.3)%。【结论】布洛芬混悬液和市售布洛芬片两种制剂具有生物等效性。
, 百拇医药
Pharmacokinetics and Relative Bioavailability of a Suspension Formulation of Ibuprofen in Normal Volunteers
LI Zhi,CHEN Liwei,GUO Zhaogui
National Training Center of Clinical Pharmacology, Hunan Medical University, Changsha,410078
Abstract 【Objective】The pharmacokinetics and relative bioavailability of a suspension formulation of ibuprofen and commercial ibuprofen tablets were compared after a single oral dose of ibuprofen in normal volunteers.【Methods】Eight healthy male volunteers were selected and divided randomly into 2 groups.Following a single oral dose (600 mg)of suspension or tablets administered alternatively,a HPLC assay was developed to measure plasma concentrations of ibuprofen.【Results】 After a single oral dose (600 mg) the peak levels of ibuprofen in plasma averaged 13.88±1.92 and 11.07±2.51 μg/ml at 0.92±0.33 and 1.68±0.51 h and the area under curve (AUC) were 47.77±3.46 and 45.23±5.21 μg/(min.ml) for suspension and commercial tablet formulations respectively. The relative bioavailability of suspension formulation was 105.6±11.3%.【Conclusions】The results of two one sided tests showed that these two formulations were bioequivalent.
, 百拇医药
Key words ibuprofen; pharmacokinetics; chromatography,high pressure liquid
布洛芬(ibuprofen)是常用的一种非类固醇类抗炎药,又称为异丁基苯丙酸,属苯丙酸类衍生物。具有解热、镇痛、抗风湿等药理作用,临床上用于治疗类风湿性关节炎、骨骼肌疾病、急性痛风等疾病,亦用作退热和镇痛,可治疗由感冒引起的头痛、发热、咳嗽、鼻塞等症状。为生产出较理想的用于小儿解热的布洛芬制剂,珠海金沙(湖南)制药有限公司研制了给药方便和味道好的小儿型布洛芬混悬剂。本文采用高效液相色谱法测定8名健康志愿者口服单剂量布洛芬混悬液和片剂后,求得经时过程的血药浓度,并计算出有关的药代动力学参数和相对生物利用度,对其生物等效性作出评价。
1 材料与方法
1.1 仪器与试剂 Waters高压液相色谱仪;490型多波长检测器;Baseline 810数据采样和分析系统;布洛芬混悬剂由金沙公司生产,含布洛芬20 mg/ml;普通市售片由湖南制药厂生产(简称市售片), 每片含布洛芬100 mg,甲醇(HPLC级); 磷酸二氢钾(AR);盐酸(AR);乙腈(HPLC级)
, 百拇医药
1.2 血浆中布洛芬浓度测定
1.2.1 色谱条件[1,2] Sprisorb C18 250×4.6 mm(粒度5 μm)不锈钢柱;流动相为甲醇∶0.02 mol/L 磷酸二氢钾缓冲液(pH= 3.8)(70∶30 v/v);流速为1.0 ml/min;紫外检测波长为230 nm;灵敏度为0.04 AUFS;柱温为(50± 0.2)℃;进样量20 μl。
1.2.2 血浆样品的处理与测定[1~4] 取血浆样品0.2 ml,置1.5 ml塑料具塞离心管中,加内标(消炎痛,用乙腈配制成浓度7.0 μg/ml)0.2 ml置超声器水浴中超声处理约0.5 min,Eppendorf(5 415c)离心机上离心20 min,速度为14 000 r/min。取上清液20 μl进样检测血浆中布洛芬浓度。最低检测浓度为0.15 μg/ml,本法平均回收率为100.4 %,变异系数RSD为3.4 %。
, 百拇医药
1.3 健康志愿者试验
1.3.1 志愿者 8名健康男性志愿者,平均年龄(28.5±6)岁,平均体重(54.6±8)kg。受试者肝功能正常,无胃和十二指肠溃疡, 在试验前和试验期间均未服用其它药物并禁烟酒。
1.3.2 单剂量试验 8名健康男性志愿者,随机分成两组,每组4人。每组受试者禁食12~16 h后,分别口服布洛芬片剂0.6 g或同剂量混悬液(20 mg/ml, 30 ml), 温开水100 ml 送服。服药后食用统一的餐食(早、中、晚餐)。于服药后0.5,1,2,3,4,5,6,8,12 h采血。肝素抗凝,分离血浆后-20 ℃保存至测定。两周后进行交叉实验[5]。
1.4 统计分析 本实验所得布洛芬血药浓度数据用中国药理学会数学药理专业委员会编制的3P87药代动力学程序模拟药时曲线,计算药代动力学参数。采用配对 t检验法[5,6],求二制剂相对生物利用度,用交叉设计方法,以布洛芬片剂为标准,对其混悬液进行评价。
, 百拇医药
2 结果
8名受试者交叉服用单剂量的布洛芬混悬液和片剂后,血药浓度在1~2 h达高峰,2 h后血药浓度下降较快,12 h有的受试血药浓度已降至检测低限。平均血药浓度-时间数据列于表1,附图为单剂量口服混悬液和片剂后的平均药时曲线图。血浆药物浓度时间数据用计算机药代动力学软件3P87进行分析,求得药代动力学参数见表2。
表1 布洛芬不同剂型后不同时间的平均血药浓度(μg/ml) 时间(h)
混悬液
片剂
0.5
10.19±1.08
3.69±3.02
, 百拇医药
1
13.47±2.59
7.09±3.34
2
11.61±3.40
14.73±2.81
3
7.36±2.63
7.95±1.69
4
5.06±1.72
5.97±1.55
, http://www.100md.com
5
3.01±0.76
3.84±1.72
6
2.33±0.50
3.07±1.11
8
1.37±0.41
1.62±0.90
12
0.48±0.44
0.44±0.29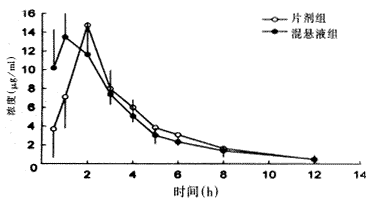
, 百拇医药
附图 单剂量口服600 mg布洛芬混悬液和片剂后的平均血药浓度
表2 单剂量口服不同剂型布洛芬后的药代动力学参数( ±s) 组别
±s) 组别
T a (h)
a (h)
T e (h)
e (h)
Cmax(μg/ml)
Tpk(h)
, http://www.100md.com
AUC0~oc
[μg/(min.ml)]
混悬液
0.76±0.19
2.13±0.32
13.88±1.92
0.92±0.33
47.77±3.46
片 剂
1.12±0.23
2.38±0.22
, http://www.100md.com
11.07±2.51
1.68±0.51
45.23±5.21
从表2可以看出混悬液的Tpk明显提前于片剂(P<0.01);混悬液的Cmax高于片剂(P<0.05)而消除半衰期基本接近(P>0.05)。混悬液和片剂的血药浓度曲线下面积AUC基本相同,以片剂为标准算得混悬液的相对生物利用度为(105.6±11.3)%。
3 讨论
用HPLC方法测定布洛芬的血浓度国内外报道很多[1~4,7,8],本法参照文献,用乙腈沉淀蛋白,无须提取、吹干等繁杂操作,取上清液直接进样,方法简便。作者在实验中发现,布洛芬的最大吸收波长在225 nm处,用225 nm作检测波长灵敏度高,但血中大多数干扰物质在此波长有吸收,基线噪音大。最后选择了干扰峰少、灵敏度又足够大的230 nm作为检测波长。
, http://www.100md.com
单剂量试验的结果表明,布洛芬混悬液的达峰时间明显提前于片剂(P<0.01),高峰浓度也高于片剂(P<0.05),但两者的AUC和T e基本一致,这说明两者的吸收动力学有明显差异而吸收程度和消除动力学性质基本一致。两种制剂的布洛芬主要药代动力学参数经配对t检验,除Tpk值P<0.01和Cmax值P<0.05外,其他参数均为P>0.05,差异无显著性。结果说明了珠海金沙(湖南)制药有限公司生产的小儿型布洛芬混悬液和普通市售片剂为等效制剂。
e基本一致,这说明两者的吸收动力学有明显差异而吸收程度和消除动力学性质基本一致。两种制剂的布洛芬主要药代动力学参数经配对t检验,除Tpk值P<0.01和Cmax值P<0.05外,其他参数均为P>0.05,差异无显著性。结果说明了珠海金沙(湖南)制药有限公司生产的小儿型布洛芬混悬液和普通市售片剂为等效制剂。
参考文献
1 余 琛,洪有采,张 慧,等. 反相HPLC法测定血清布洛芬含量.药物分析杂志,1994,14
(4):34~37
2 王 宇,柴 虹,朱钦德,等. 高效液相色谱法测定血浆中布洛芬浓度(I).华西药学杂志,1989,4(1):29~31
, 百拇医药
3 赵志春,陆克干,胡激扬,等.人血浆中布洛芬的高效液相色谱法测定及其药代动力学研究.
药物分析杂志,1989,9(1):1~4
4 唐 星,何仲贵,蔡玉珉. 布洛芬在人血浆中的药物浓度测定方法及其在健康人体内的药代动
力学研究.沈阳药学院学报,1992,9(1):1~3
5 曾衍霖.对《新药生物等效度》申报材料写作的规范建议.中国临床药理学杂志,1995,11:58
~60
6 黄圣凯,韩可勤.生物等效性评价的统计学方法.中国临床药理学杂志,1993,9:43~45
7 Wagner JG,Albert KS,Szpunar GJ,et al.Pharmacokinetics of ibuprofen in man
IV:absorption and disposition.J Pharmacokin Biopharm,1984,12(4):381~399
8 Litowitz H,Olanoff L,Hoppel CL.Determination of ibuprofen in human plasma by
High-performance liquid chromatography.J Chromatogr,1984,311(2):443~448
19981221 收稿, 百拇医药
单位:湖南医科大学临床药理国家培训中心(长沙 410078)
关键词:布洛芬;药代动力学;色谱法,高压液相
湖南医学/990402 摘 要 【目的】比较研究布洛芬混悬液和市售布洛芬片的生物利用度和药代动力学。【方法】选择8名健康男性志愿者,随机分为两组,进行单次混悬液或片剂交叉给药600 mg后,利用HPLC法测定血浆中布洛芬浓度。【结果】两组血浆的布洛芬浓度分别在(0.92±0.33)和(1.68±0.51) h达到峰值(13.88±1.92)和(11.07±2.51) μg/ml。血药浓度曲线下面积(AUC)分别达(47.77±3.46)和(45.23±5.21) μg/(min.ml),混悬液的相对生物利用度(F)为(105.6±11.3)%。【结论】布洛芬混悬液和市售布洛芬片两种制剂具有生物等效性。
, 百拇医药
Pharmacokinetics and Relative Bioavailability of a Suspension Formulation of Ibuprofen in Normal Volunteers
LI Zhi,CHEN Liwei,GUO Zhaogui
National Training Center of Clinical Pharmacology, Hunan Medical University, Changsha,410078
Abstract 【Objective】The pharmacokinetics and relative bioavailability of a suspension formulation of ibuprofen and commercial ibuprofen tablets were compared after a single oral dose of ibuprofen in normal volunteers.【Methods】Eight healthy male volunteers were selected and divided randomly into 2 groups.Following a single oral dose (600 mg)of suspension or tablets administered alternatively,a HPLC assay was developed to measure plasma concentrations of ibuprofen.【Results】 After a single oral dose (600 mg) the peak levels of ibuprofen in plasma averaged 13.88±1.92 and 11.07±2.51 μg/ml at 0.92±0.33 and 1.68±0.51 h and the area under curve (AUC) were 47.77±3.46 and 45.23±5.21 μg/(min.ml) for suspension and commercial tablet formulations respectively. The relative bioavailability of suspension formulation was 105.6±11.3%.【Conclusions】The results of two one sided tests showed that these two formulations were bioequivalent.
, 百拇医药
Key words ibuprofen; pharmacokinetics; chromatography,high pressure liquid
布洛芬(ibuprofen)是常用的一种非类固醇类抗炎药,又称为异丁基苯丙酸,属苯丙酸类衍生物。具有解热、镇痛、抗风湿等药理作用,临床上用于治疗类风湿性关节炎、骨骼肌疾病、急性痛风等疾病,亦用作退热和镇痛,可治疗由感冒引起的头痛、发热、咳嗽、鼻塞等症状。为生产出较理想的用于小儿解热的布洛芬制剂,珠海金沙(湖南)制药有限公司研制了给药方便和味道好的小儿型布洛芬混悬剂。本文采用高效液相色谱法测定8名健康志愿者口服单剂量布洛芬混悬液和片剂后,求得经时过程的血药浓度,并计算出有关的药代动力学参数和相对生物利用度,对其生物等效性作出评价。
1 材料与方法
1.1 仪器与试剂 Waters高压液相色谱仪;490型多波长检测器;Baseline 810数据采样和分析系统;布洛芬混悬剂由金沙公司生产,含布洛芬20 mg/ml;普通市售片由湖南制药厂生产(简称市售片), 每片含布洛芬100 mg,甲醇(HPLC级); 磷酸二氢钾(AR);盐酸(AR);乙腈(HPLC级)
, 百拇医药
1.2 血浆中布洛芬浓度测定
1.2.1 色谱条件[1,2] Sprisorb C18 250×4.6 mm(粒度5 μm)不锈钢柱;流动相为甲醇∶0.02 mol/L 磷酸二氢钾缓冲液(pH= 3.8)(70∶30 v/v);流速为1.0 ml/min;紫外检测波长为230 nm;灵敏度为0.04 AUFS;柱温为(50± 0.2)℃;进样量20 μl。
1.2.2 血浆样品的处理与测定[1~4] 取血浆样品0.2 ml,置1.5 ml塑料具塞离心管中,加内标(消炎痛,用乙腈配制成浓度7.0 μg/ml)0.2 ml置超声器水浴中超声处理约0.5 min,Eppendorf(5 415c)离心机上离心20 min,速度为14 000 r/min。取上清液20 μl进样检测血浆中布洛芬浓度。最低检测浓度为0.15 μg/ml,本法平均回收率为100.4 %,变异系数RSD为3.4 %。
, 百拇医药
1.3 健康志愿者试验
1.3.1 志愿者 8名健康男性志愿者,平均年龄(28.5±6)岁,平均体重(54.6±8)kg。受试者肝功能正常,无胃和十二指肠溃疡, 在试验前和试验期间均未服用其它药物并禁烟酒。
1.3.2 单剂量试验 8名健康男性志愿者,随机分成两组,每组4人。每组受试者禁食12~16 h后,分别口服布洛芬片剂0.6 g或同剂量混悬液(20 mg/ml, 30 ml), 温开水100 ml 送服。服药后食用统一的餐食(早、中、晚餐)。于服药后0.5,1,2,3,4,5,6,8,12 h采血。肝素抗凝,分离血浆后-20 ℃保存至测定。两周后进行交叉实验[5]。
1.4 统计分析 本实验所得布洛芬血药浓度数据用中国药理学会数学药理专业委员会编制的3P87药代动力学程序模拟药时曲线,计算药代动力学参数。采用配对 t检验法[5,6],求二制剂相对生物利用度,用交叉设计方法,以布洛芬片剂为标准,对其混悬液进行评价。
, 百拇医药
2 结果
8名受试者交叉服用单剂量的布洛芬混悬液和片剂后,血药浓度在1~2 h达高峰,2 h后血药浓度下降较快,12 h有的受试血药浓度已降至检测低限。平均血药浓度-时间数据列于表1,附图为单剂量口服混悬液和片剂后的平均药时曲线图。血浆药物浓度时间数据用计算机药代动力学软件3P87进行分析,求得药代动力学参数见表2。
表1 布洛芬不同剂型后不同时间的平均血药浓度(μg/ml) 时间(h)
混悬液
片剂
0.5
10.19±1.08
3.69±3.02
, 百拇医药
1
13.47±2.59
7.09±3.34
2
11.61±3.40
14.73±2.81
3
7.36±2.63
7.95±1.69
4
5.06±1.72
5.97±1.55
, http://www.100md.com
5
3.01±0.76
3.84±1.72
6
2.33±0.50
3.07±1.11
8
1.37±0.41
1.62±0.90
12
0.48±0.44
0.44±0.29

, 百拇医药
附图 单剂量口服600 mg布洛芬混悬液和片剂后的平均血药浓度
表2 单剂量口服不同剂型布洛芬后的药代动力学参数(
 ±s) 组别
±s) 组别T
 a (h)
a (h)T
 e (h)
e (h)Cmax(μg/ml)
Tpk(h)
, http://www.100md.com
AUC0~oc
[μg/(min.ml)]
混悬液
0.76±0.19
2.13±0.32
13.88±1.92
0.92±0.33
47.77±3.46
片 剂
1.12±0.23
2.38±0.22
, http://www.100md.com
11.07±2.51
1.68±0.51
45.23±5.21
从表2可以看出混悬液的Tpk明显提前于片剂(P<0.01);混悬液的Cmax高于片剂(P<0.05)而消除半衰期基本接近(P>0.05)。混悬液和片剂的血药浓度曲线下面积AUC基本相同,以片剂为标准算得混悬液的相对生物利用度为(105.6±11.3)%。
3 讨论
用HPLC方法测定布洛芬的血浓度国内外报道很多[1~4,7,8],本法参照文献,用乙腈沉淀蛋白,无须提取、吹干等繁杂操作,取上清液直接进样,方法简便。作者在实验中发现,布洛芬的最大吸收波长在225 nm处,用225 nm作检测波长灵敏度高,但血中大多数干扰物质在此波长有吸收,基线噪音大。最后选择了干扰峰少、灵敏度又足够大的230 nm作为检测波长。
, http://www.100md.com
单剂量试验的结果表明,布洛芬混悬液的达峰时间明显提前于片剂(P<0.01),高峰浓度也高于片剂(P<0.05),但两者的AUC和T
 e基本一致,这说明两者的吸收动力学有明显差异而吸收程度和消除动力学性质基本一致。两种制剂的布洛芬主要药代动力学参数经配对t检验,除Tpk值P<0.01和Cmax值P<0.05外,其他参数均为P>0.05,差异无显著性。结果说明了珠海金沙(湖南)制药有限公司生产的小儿型布洛芬混悬液和普通市售片剂为等效制剂。
e基本一致,这说明两者的吸收动力学有明显差异而吸收程度和消除动力学性质基本一致。两种制剂的布洛芬主要药代动力学参数经配对t检验,除Tpk值P<0.01和Cmax值P<0.05外,其他参数均为P>0.05,差异无显著性。结果说明了珠海金沙(湖南)制药有限公司生产的小儿型布洛芬混悬液和普通市售片剂为等效制剂。参考文献
1 余 琛,洪有采,张 慧,等. 反相HPLC法测定血清布洛芬含量.药物分析杂志,1994,14
(4):34~37
2 王 宇,柴 虹,朱钦德,等. 高效液相色谱法测定血浆中布洛芬浓度(I).华西药学杂志,1989,4(1):29~31
, 百拇医药
3 赵志春,陆克干,胡激扬,等.人血浆中布洛芬的高效液相色谱法测定及其药代动力学研究.
药物分析杂志,1989,9(1):1~4
4 唐 星,何仲贵,蔡玉珉. 布洛芬在人血浆中的药物浓度测定方法及其在健康人体内的药代动
力学研究.沈阳药学院学报,1992,9(1):1~3
5 曾衍霖.对《新药生物等效度》申报材料写作的规范建议.中国临床药理学杂志,1995,11:58
~60
6 黄圣凯,韩可勤.生物等效性评价的统计学方法.中国临床药理学杂志,1993,9:43~45
7 Wagner JG,Albert KS,Szpunar GJ,et al.Pharmacokinetics of ibuprofen in man
IV:absorption and disposition.J Pharmacokin Biopharm,1984,12(4):381~399
8 Litowitz H,Olanoff L,Hoppel CL.Determination of ibuprofen in human plasma by
High-performance liquid chromatography.J Chromatogr,1984,311(2):443~448
19981221 收稿, 百拇医药