成年SD大鼠的NGF药代动力学研究
作者:王小川
单位:同济医科大学实验动物学部 武汉430030
关键词:NGF;药代动力学;ELISA
数理医药学杂志990231
摘要 采取静脉注射和皮下注射两种给药方式,对清洁级成成年SD大鼠分别于给药后不同时间采取尾静脉血,通过双抗体夹心型ELISA方法检测了血清NGF的含量,并求出了得主要药代动力学参数。
NGF是神经系统重要的生物活性分子之一,具有保护神经细胞存活、促进其生长、分化的作用[1]。近年来,有关NGF药代动力学的研究在国外已有报道[2],认为静脉给予NGF后分布相和消除相半衰期分别为5~6min和2~3h,皮下给药的消除半衰期明显延长,两种给药方式的清除率没有显著性差异。国内关于NGF的药代动力学尚未见报道,本文对14只清洁级SD大鼠作为受试对象,6只以静脉注射给药,8只以皮下注射给药,剂量均为35μg/kg大鼠体重进行了药代动力学研究。
, 百拇医药
1 材料与方法
1.1 受试对象
清洁级SD雄性大鼠,体重250~300g,试验前观察一个星期。受试动物由同济医科大学实验动物学部提供。
Table 1 Experimental Subjects for
Pharmacokinetics Study of NGF Group
Number
Strain
Sex
Body Weight
A: iv
, 百拇医药
6
SD
male
269±13g
B: sc
8
SD
male
275±14g
1.2 药品
NGF:批号940806,武汉生物制品研究所;ANTI-NGF:批号034H8841,产品号N-5142,Sigma公司,美国。
1.3 给药方案及血样的收集
, 百拇医药
A组采用尾静脉注射给药,B组于大鼠两肩胛皮下注射,两组剂量均为35μg/kg体重。NGF用PBS稀释成35μg/ml,则大鼠给药剂量为1ml/kg鼠重。
A组在给药前及给药后5min、 20min、 40min、 1h、 2h、 4h、 6h、 8h采取血样;B组采血时间为给药前和给药后5min、 20min、 40min、 1h、 2h、 4h、 6h、 8h、 10h、 12h、 24h、 28h。每次自尾静脉采血500μl,静置30min后,以3000rpm离心20min,取血清200μl分装于2个EP管内(各100μl),于低温冰箱-20℃保存,待测。
1.4 大鼠血清测定
以辣根过氧化物酶HRP为标记试剂标记神经生长因子抗体Anti-NGF采用双抗体夹心型酶联免疫方法NGF进行检测,其检出限为25.6pg/ml,线性范围40~2560pg/ml。该方法操作方便且快速准确。本文静脉注射组6只大鼠血清用PBS以1∶10稀释,皮下注射组8只大鼠血清12h前用PBS以1∶1稀释,采用双抗体夹心型酶联免疫方法测定每批样品,均同时制作标准曲线。
, 百拇医药
1.5 数据处理
本实验测得NGF血药浓度数据用中国药理学会数学药理专业委员会编制的药代动力学程序模拟药时曲线,并计算药代动力学参数。
2 结果
2.1 血药浓度
A组药时曲线经拟合后符合一房室模型(见图1);B组的平均血药浓度测定结果及药-时曲线见图2,其药-时曲线符合二房室模型(表2)。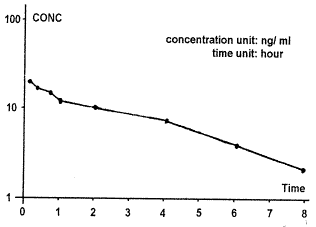
Fig 1 Mean Serum Concentration-time curve
after a dose of 35μg/kg NGF iv (n=6)
, http://www.100md.com
Fig 2 Mean Serum Concentration-time curve
after a dose of 35μg/kg NGF sc (n=8)
2.2 药代动力学参数
2.2.1 皮下给药组A为7.81±7.69ng/ml, Ka为0.89±0.16h-1, V为5.99±0.35l/kg, t1/2α为2.47±1.78h, t1/2β为5.02±1.35h, Tmax为2.33±0.25h,Cmax为3.98±0.24ng/ml, CL为0.96±0.08l*kg-1*h-1。
2.2.2 静脉注射给药组Co为17.83±2.95ng/ml, Ke为0.29±0.04h-1, V为2.01±0.31l/kg, t1/2为2.40±0.36h, CL为0.59±0.14l*kg-1*h-1。
, http://www.100md.com
2.3 生物利用度F
皮下给予NGF 35μg/kg体重测得血药浓度-时间曲线下面积AUC为36.07±2.12ng*h*ml-1;静脉注射NGF 35μg/kg体重测得血药浓度-时间曲线下面积AUC为61.93±14.10ng*h*ml-1。根据F=AUC(血管处给药)/AUC(静注给药),计算皮下给药的绝对生物利用度为58.24±3.42%。
2.4 两种给药方式药代动力学参数比较(见表2)
Table 2 Comparision of Pharmacokinetic Parametes of NGF by iv and sc Parameters
unit
Route of Administration
, 百拇医药
F
t
P
iv
sc
t1/2α
min
2.47±1.78
t1/2β
h
2.40±0.36
5.02±1.35
, 百拇医药 14*
5.24
<0.05
CL
l*kg-1*h-1
0.59±0.14
0.96±0.08
3.06
6.38
<0.05
V
l/kg
, 百拇医药
2.01±0.31
5.99±0.35
1.26
22.01
<0.01
Cmax
ng/ml
3.98±0.24
Tmax
h
2.33±0.25
AUC
, http://www.100md.com
Ng*h*ml-1
61.93±14.10
36.07±2.12
44*
4.45
<0.05
F(%)
100
58.24±3.42
注:* 方差不齐,作t′-test
3 讨论
对清洁级SD大鼠以35μg/kg的剂量采用皮下注射NGF,尾静脉采血,通过双抗体夹心型ELISA方法测得NGF血清含量,经3P87程序拟合,求得药代动力学参数。结果表明,皮下注射给药后吸收较快,平均2.33h就达到血药峰值,说明NGF皮下注射在体内释放、吸收良好,平均血药峰值为3.98±0.24ng/ml,曲线下面积为36.07±2.12ng*h*ml-1,与文献报道的结果一致[2]。
, http://www.100md.com
静脉注射的血药浓度数据经计算机拟合,符合一房室模型,与文献报道不同[2]。文献中报道t1/2α为5min,即分布迅速完成,它的采血方式是心脏穿刺取血,本实验是通过尾静脉取血,因此NGF静脉注射后,在分布相的血液没有采集到,所以,药时曲线只相当于文献中的消除相。曲线下面积也较文献报道的要小。
由于NGF在酸性(pH低于5)、碱性(pH高于8)或单纯稀释时会解离[3],本实验没有采取经口给药途径,同时由于受试对象采用的是小动物,采血量及采血方式对动物损伤较大,因此没有采用自身对照的实验设计方法,所以生物利用度的计算是通过皮下给药及静脉注射给药后测得的药时曲线下面积平均值比较而得,同时静脉注射后的曲线下面积较文献报道要小,生物利用度较文献[2]报道大。这可能与NGF的制备工艺和采用的原料有关。
血液中NGF很快地就消除是由于NGF结合到血清蛋白酶抑制剂α2巨球蛋白[4],然后又快速地结合到肝细胞上,从血液循环中消除掉[5],可见NGF的消除受肝功能影响较大,主要是通过肝脏代谢。从尿中测不出NGF,与文献[2]一致。
, 百拇医药
参考文献
1 Levi-Montacili R. the nerve growth factor thirty-five years later. Science, 1987, 237: 1154.
2 Maria, AT et al. Pharmacokinetics of never growth factor following different routes of adminstration to adult rats, 1994,127: 178~183.
3 刘湘梅.神经生长的生物学与病理学.科学出版社,1985,82~83.
4 Koo PH et al. Interaction of never growth factor with murine α2-macroglobulin. J Neurosci Res, 1989,22: 247~261.
5 Feldman SR et al. Binding of α2-macrogiobulin to hepatocytes: Mechanism of in vivo clearance. Biochem Biophys Res Commun, 1985,128: 795~802.
收稿日期:1998-10-15, 百拇医药
单位:同济医科大学实验动物学部 武汉430030
关键词:NGF;药代动力学;ELISA
数理医药学杂志990231
摘要 采取静脉注射和皮下注射两种给药方式,对清洁级成成年SD大鼠分别于给药后不同时间采取尾静脉血,通过双抗体夹心型ELISA方法检测了血清NGF的含量,并求出了得主要药代动力学参数。
NGF是神经系统重要的生物活性分子之一,具有保护神经细胞存活、促进其生长、分化的作用[1]。近年来,有关NGF药代动力学的研究在国外已有报道[2],认为静脉给予NGF后分布相和消除相半衰期分别为5~6min和2~3h,皮下给药的消除半衰期明显延长,两种给药方式的清除率没有显著性差异。国内关于NGF的药代动力学尚未见报道,本文对14只清洁级SD大鼠作为受试对象,6只以静脉注射给药,8只以皮下注射给药,剂量均为35μg/kg大鼠体重进行了药代动力学研究。
, 百拇医药
1 材料与方法
1.1 受试对象
清洁级SD雄性大鼠,体重250~300g,试验前观察一个星期。受试动物由同济医科大学实验动物学部提供。
Table 1 Experimental Subjects for
Pharmacokinetics Study of NGF Group
Number
Strain
Sex
Body Weight
A: iv
, 百拇医药
6
SD
male
269±13g
B: sc
8
SD
male
275±14g
1.2 药品
NGF:批号940806,武汉生物制品研究所;ANTI-NGF:批号034H8841,产品号N-5142,Sigma公司,美国。
1.3 给药方案及血样的收集
, 百拇医药
A组采用尾静脉注射给药,B组于大鼠两肩胛皮下注射,两组剂量均为35μg/kg体重。NGF用PBS稀释成35μg/ml,则大鼠给药剂量为1ml/kg鼠重。
A组在给药前及给药后5min、 20min、 40min、 1h、 2h、 4h、 6h、 8h采取血样;B组采血时间为给药前和给药后5min、 20min、 40min、 1h、 2h、 4h、 6h、 8h、 10h、 12h、 24h、 28h。每次自尾静脉采血500μl,静置30min后,以3000rpm离心20min,取血清200μl分装于2个EP管内(各100μl),于低温冰箱-20℃保存,待测。
1.4 大鼠血清测定
以辣根过氧化物酶HRP为标记试剂标记神经生长因子抗体Anti-NGF采用双抗体夹心型酶联免疫方法NGF进行检测,其检出限为25.6pg/ml,线性范围40~2560pg/ml。该方法操作方便且快速准确。本文静脉注射组6只大鼠血清用PBS以1∶10稀释,皮下注射组8只大鼠血清12h前用PBS以1∶1稀释,采用双抗体夹心型酶联免疫方法测定每批样品,均同时制作标准曲线。
, 百拇医药
1.5 数据处理
本实验测得NGF血药浓度数据用中国药理学会数学药理专业委员会编制的药代动力学程序模拟药时曲线,并计算药代动力学参数。
2 结果
2.1 血药浓度
A组药时曲线经拟合后符合一房室模型(见图1);B组的平均血药浓度测定结果及药-时曲线见图2,其药-时曲线符合二房室模型(表2)。

Fig 1 Mean Serum Concentration-time curve
after a dose of 35μg/kg NGF iv (n=6)

, http://www.100md.com
Fig 2 Mean Serum Concentration-time curve
after a dose of 35μg/kg NGF sc (n=8)
2.2 药代动力学参数
2.2.1 皮下给药组A为7.81±7.69ng/ml, Ka为0.89±0.16h-1, V为5.99±0.35l/kg, t1/2α为2.47±1.78h, t1/2β为5.02±1.35h, Tmax为2.33±0.25h,Cmax为3.98±0.24ng/ml, CL为0.96±0.08l*kg-1*h-1。
2.2.2 静脉注射给药组Co为17.83±2.95ng/ml, Ke为0.29±0.04h-1, V为2.01±0.31l/kg, t1/2为2.40±0.36h, CL为0.59±0.14l*kg-1*h-1。
, http://www.100md.com
2.3 生物利用度F
皮下给予NGF 35μg/kg体重测得血药浓度-时间曲线下面积AUC为36.07±2.12ng*h*ml-1;静脉注射NGF 35μg/kg体重测得血药浓度-时间曲线下面积AUC为61.93±14.10ng*h*ml-1。根据F=AUC(血管处给药)/AUC(静注给药),计算皮下给药的绝对生物利用度为58.24±3.42%。
2.4 两种给药方式药代动力学参数比较(见表2)
Table 2 Comparision of Pharmacokinetic Parametes of NGF by iv and sc Parameters
unit
Route of Administration
, 百拇医药
F
t
P
iv
sc
t1/2α
min
2.47±1.78
t1/2β
h
2.40±0.36
5.02±1.35
, 百拇医药 14*
5.24
<0.05
CL
l*kg-1*h-1
0.59±0.14
0.96±0.08
3.06
6.38
<0.05
V
l/kg
, 百拇医药
2.01±0.31
5.99±0.35
1.26
22.01
<0.01
Cmax
ng/ml
3.98±0.24
Tmax
h
2.33±0.25
AUC
, http://www.100md.com
Ng*h*ml-1
61.93±14.10
36.07±2.12
44*
4.45
<0.05
F(%)
100
58.24±3.42
注:* 方差不齐,作t′-test
3 讨论
对清洁级SD大鼠以35μg/kg的剂量采用皮下注射NGF,尾静脉采血,通过双抗体夹心型ELISA方法测得NGF血清含量,经3P87程序拟合,求得药代动力学参数。结果表明,皮下注射给药后吸收较快,平均2.33h就达到血药峰值,说明NGF皮下注射在体内释放、吸收良好,平均血药峰值为3.98±0.24ng/ml,曲线下面积为36.07±2.12ng*h*ml-1,与文献报道的结果一致[2]。
, http://www.100md.com
静脉注射的血药浓度数据经计算机拟合,符合一房室模型,与文献报道不同[2]。文献中报道t1/2α为5min,即分布迅速完成,它的采血方式是心脏穿刺取血,本实验是通过尾静脉取血,因此NGF静脉注射后,在分布相的血液没有采集到,所以,药时曲线只相当于文献中的消除相。曲线下面积也较文献报道的要小。
由于NGF在酸性(pH低于5)、碱性(pH高于8)或单纯稀释时会解离[3],本实验没有采取经口给药途径,同时由于受试对象采用的是小动物,采血量及采血方式对动物损伤较大,因此没有采用自身对照的实验设计方法,所以生物利用度的计算是通过皮下给药及静脉注射给药后测得的药时曲线下面积平均值比较而得,同时静脉注射后的曲线下面积较文献报道要小,生物利用度较文献[2]报道大。这可能与NGF的制备工艺和采用的原料有关。
血液中NGF很快地就消除是由于NGF结合到血清蛋白酶抑制剂α2巨球蛋白[4],然后又快速地结合到肝细胞上,从血液循环中消除掉[5],可见NGF的消除受肝功能影响较大,主要是通过肝脏代谢。从尿中测不出NGF,与文献[2]一致。
, 百拇医药
参考文献
1 Levi-Montacili R. the nerve growth factor thirty-five years later. Science, 1987, 237: 1154.
2 Maria, AT et al. Pharmacokinetics of never growth factor following different routes of adminstration to adult rats, 1994,127: 178~183.
3 刘湘梅.神经生长的生物学与病理学.科学出版社,1985,82~83.
4 Koo PH et al. Interaction of never growth factor with murine α2-macroglobulin. J Neurosci Res, 1989,22: 247~261.
5 Feldman SR et al. Binding of α2-macrogiobulin to hepatocytes: Mechanism of in vivo clearance. Biochem Biophys Res Commun, 1985,128: 795~802.
收稿日期:1998-10-15, 百拇医药