阿柔比星A聚乳酸毫微粒冻干针剂小鼠体内分布研究
作者:何林 蒋学华
单位:何林 蒋学华(华西医科大学药学院,成都 610041)
关键词:阿柔比星A;聚乳酸;毫微粒;体内分布
中国抗生素杂志000317 摘 要 对阿柔比星A冻干针剂与阿柔比星A(ACRB-A)聚乳酸毫微粒冻干针剂给予小鼠尾静脉注射后体内分布进行比较。采用HPLC法分别测定小鼠给药后血液及主要脏器中ACRB-A浓度。结果,阿柔比星A聚乳酸毫微粒在小鼠肝脏中的浓度高于对照品浓度。提示阿柔比星A制成毫微粒后可显著提高肝脏靶向性。
Study on the distribution of aclarubicin A poly lactide nanoparticle lyophilization in mice
He Lin
, http://www.100md.com
(Department of Pharmaceutical,The People′s Hospital of Sichuan Province,Chengdu 610072)
Jiang Xuehua
(School of Pharmacy,West China University of Medical Sciences,Chengdu 610041)
ABSTRACT Objective: Comparing the distribution of aclarubicin A lyophilization and aclarubicin A poly lactide nanoparticle (ACRB-A-PLA-NP) lyophilization in mice.Method: HPLC is selected to determine the concentration of aclarubicin A in plasma and in main organisms.Results: The concentratin of ACRB-A-PLA-NP in liver is higher than that of the reference.Conclusion: ACRB-A can be significantly concentrated in liver after prepared in nanoparticle.
, 百拇医药
KEY WORDS Aclarubicin A;Poly lactide;Nanoparticle;In vivo distribution
阿柔比星A(aclarubicin A,ACRB)是第二代蒽环类抗癌抗生素,临床用于胃癌、肺癌、乳腺癌、急性白血病、卵巢癌及恶性淋巴瘤等多种癌的治疗。主要缺点是骨髓抑制、心脏毒性、胃肠不适等毒副作用[1]。为了提高ACRB-A的抗癌效果及药物稳定性,降低毒副作用,曾以聚乳酸(poly lactide,PLA)为载体材料,制备了阿柔比星A聚乳酸毫微粒(ACRB-A-PLA-NP)[2]。本文在文献的基础上[3]采用了HPLC法测定了ACRB-A-PLA-NP在动物体内各组织中的分布。
1 材料与仪器
1.1 材料
, http://www.100md.com ACRB-A对照品(四川抗菌素工业研究所提供);ACRB-A聚乳酸毫微粒冻干针剂(自制,批号970113);注射用盐酸ACRB-A冻干剂(江苏扬州制药厂,批号950305);其余试剂皆为分析纯。
1.2 仪器
LC-6A高效液色谱仪(日本岛津);SPD-6AV紫外可见检测器(日本岛津);CR-4A数据处理机(日本岛津);TGL-16高速离心机(上海医疗器械六厂)。
1.3 动物
一级昆明种小鼠(华西医科大学实验动物中心),体重18~22g。
2 方法与结果
2.1 血浆及各组织中ACRB-A的HPLC测定法
2.1.1色谱条件 分析柱:Alltech C18 micro(250mm×4.6mm i.d,5μm);预柱:YWG-ODS(1cm×4.6mm i.d);流动相:0.2mol/L乙酸铵(pH2.5±0.1)∶甲醇=1∶3; 柱温:35℃; 流速:1ml/min; 检测波长:432nm。
, 百拇医药
2.1.2 样品预处理与测定 取小鼠心、肝、脾、肺、肾样品,分别精密称重,加入1倍量用生理盐水(脾加入2倍)制成50%匀浆液。精密量取0.25ml匀浆液(或血浆),同样方法称定其重量,加入0.1ml内标液(内含双嘧达莫的乙酸乙酯溶液),振摇后,加入0.1ml氨水,100mg NaCl及0.8ml乙酸乙酯,旋涡混合5min,离心12000r/min 10min,取上清液0.6ml,于40℃减压挥干,残渣用100μl流动相溶解,旋涡混合1min,离心5000r/min 5min,取上清液20μl进样,按上述色谱条件进行分析,结果见图1。
2.1.3 标准曲线方程的测定 分别取空白血浆及心、肝、脾、肺、肾匀浆样品,精密加入不同量ACRB-A储备液,配制成不浓度的标准溶液,从“加入0.1ml内标液”起,按样品预处理与测定方法进行处理与测定,记录样品峰与内标峰的峰面积As、Ai,峰面积之比R=As/Ai对浓度进行线性回归,得到血浆及各组织样品的回归方程分别为:
, 百拇医药
血:0.25~10.0μg/ml,R=0.000245+1.561C,r=0.9996
肾:0.25~10.0μg/g,R=-0.02+0.77C,r=0.9991
肝:1.0~40.0μg/g,R=-0.0439+0.0993C,r=0.9992
肺:0.5~20.0μg/g,R=-0.0006+0.163C,r=0.9991
图1
a:血浆空白及样品HPLC图;b:肾空白及样品HPLC图;c:肝空白及样品HPLC图;
d:肺空白及样品HPLC图;e:心空白及样品HPLC图;f:脾空白及样品HPLC图
, http://www.100md.com
心:0.5~20.0μg/g,R=-0.0105+0.108C,r=0.9990
脾:0.5~20.0μg/g,R=-0.0566+0.560C,r=0.9993
2.1.4 萃取回收率的测定 精密量取ACRB-A储备液不同量,配制高、中、低三种不同浓度的ACRB-A液,取20μl进样,记录峰面积A1。另取血浆或匀浆液0.25ml,加入ACRB-A储备液不同量,配制同样高、中、低三种不同浓度的ACRB-A液,按样品预处理与测定方法进行操作,记录样品峰的面积A2。以A2/A1之比计算萃取回收率,结果见表1。
由表1可见,除肾以外,ACRB-A在小鼠各组织中的萃取回率都在80%以上,且较稳定,说明对样品的预处理方法是可行的。
2.1.5 方法回收率的测定 分别量取空白血浆或组织匀浆液0.25ml,加入不同量ACRB-A储备液,配制成高、中、低三种不同浓度的ACRB-A溶液,从“加入0.1ml内标液”起, 按样品预处理与测定方法进行操作,记录样品峰与内标峰的面积As、Ai,以R=As/Ai代入标准曲线方程计算测定,以测定浓度与配制浓度之比计算回收率,结果见表2。
, http://www.100md.com
表1 ACRB-A在不同组织中的萃取回收率(%,n=3) 样品
[μg/ml(μg/g)]
0.5
5.0
20.0
Mean±SD
血
88.2±1.9
92.6±1.1
89.5±2.7
90.1±2.3
肾
, http://www.100md.com
72.4±2.1
78.5±2.6
76.9±3.0
75.9±3.2
肝
85.2±1.6
80.4±3.5
88.6±2.5
84.7±4.1
心
80.4±1.0
84.2±2.2
, http://www.100md.com
86.5±1.4
83.7±3.1
肺
78.1±1.9
82.5±2.0
80.7±2.4
80.4±2.2
脾
84.8±3.1
87.2±2.7
83.0±1.0
85.0±2.1
, http://www.100md.com
由表2可见,三种浓度在不同脏器中的平均回收率在96.6%~103.5%范围内,方法准确度较高。
2.1.6 方法重现性考察 配制高、中、低三种不同浓度样品液,各样品平行操作5份,按样品预处理与测定方法进行操作,得到三种浓度不同脏器供试品测定结果的日内相对标准差≤4.8%,日间相对标准差≤7.0%,方法重现性较好。 表2 方法回收率测定结果 样品
加入
(μg/ml,μg/g)
测定
(μg/ml,μg/g)
回收
(%)
Mean±SD
, 百拇医药
(%)
样品
加入
(μg/ml,μg/g)
测定
(μg/ml,μg/g)
回收
(%)
Mean±SD
(%)
血
0.5
0.54±0.01
, 百拇医药
108.2±2.5
肺
0.8
0.84±0.01
104.4±0.8
2.0
2.03±0.05
101.3±2.5
102.1±4.6
0.5
5.07±0.14
101.4±2.9
, http://www.100md.com
101.6±2.9
8.0
7.80±0.07
97.5±0.8
15.0
14.86±0.29
97.8±1.9
肾
0.5
0.48±0.01
96.4±1.9
心
, 百拇医药
0.8
0.86±0.01
107.7±1.4
2.0
1.92±0.03
95.9±1.3
96.6±1.5
5.0
5.16±0.05
103.4±1.0
103.5±4.4
8.0
, 百拇医药
7.80±0.10
97.6±1.2
15.0
14.70±0.33
98.0±2.2
肝
2.0
1.88±0.03
94.2±1.7
脾
0.8
0.82±0.01
, 百拇医药
102.9±1.2
20.0
20.33±0.24
101.7±1.2
97.8±3.5
5.0
5.08±0.17
101.6±3.4
100.7±3.0
40.0
39.09±0.45
97.7±1.1
, http://www.100md.com
15.0
14.67±0.17
97.8±1.1
2.2 尾静脉给予小鼠ACRB-A冻干剂和ACRB-A-PLA-NP冻干剂后的体内分布研究
选取体重为20±2g的健康小白鼠70只,随机分成14组,每组5只,按10mg/kg剂量分别尾静脉注射分散后的ACRB-A冻干剂和ACRB-A-PLA-NP冻干剂,给药后分别于5、15min和0.5、1、2、4、8、12、24、72、96、144h取一组,眼眶取血后,断颈处死,取心、肝、脾、肺、肾各器官,滤纸吸干其水分和血迹,称定重量(血液按小鼠体重的8%计),按样品预处理与测定方法进行操作,记录As和Ai;将R=As/Ai代入各标准曲线方程,求得血液及各器官在不同时间的浓度,血液及各脏器的药时曲线见图2。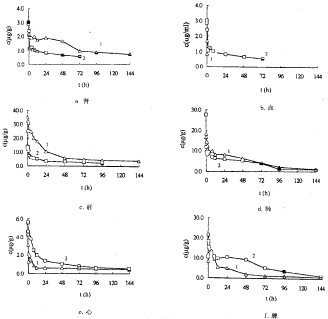
, 百拇医药
图2 血液及各脏器的药时曲线
1:ACRB-A-PLA-NP;2:ACRB-A
3 讨论
3.1 由图可见,药物制成毫微粒后,提高了药物在肝、肾、肺中的浓度,降低了药物在血、心、脾中的浓度。按药物在这六种主要器官的百分比计算,毫微粒组在肝脏中的百分比浓度为77.91%~89.33%,平均为84.49%;对照组为39.83%~66.31%,平均为51.20%,平均提高了33.29%,说明将ACRB-A制成ACRB-PLA-NP后,提高了对肝脏的亲和性,达到了肝靶向的要求。
3.2 ACRB-A-PLA-NP静注给药后,血液中药物浓度降低很快,0.25h后即不能检出,而同样给药剂量条件下,对照组直到96h后才不能检出。这可能是由于ACRB-A-PLA-NP释药缓慢,药物浓集于肝脏后即缓慢释放,肝脏作为药物的储库,因而使血中药物浓度一直处于较低水平而不能检出。同时说明靶向给药系统与普通给药系统在血液中的作用过程显著不同,靶向给药系统在血液中的吸收、分布、消除不同于普通给药系统,在进行靶向给药系统的药物动力学研究时,已不能将普通给药制剂血液动力学的研究方法简单地应用于靶向给药系统,而应寻求靶向给药系统新的研究方法。
, 百拇医药
国家自然科学基金资助项目(合同号39570842)及国家医药技术创新博士项目(合同号95-B-09)
何林,男,生于1967年,博士,主管药师.
参考文献
1,现代临床治疗药物大全编委会编.现代临床治疗药物大全.北京:中国医药科技出版社,1995:628
2,何林,蒋学华,李屯.阿克拉霉素A聚乳酸毫微粒制备工艺研究.中国药学杂志,1998;33(5):289
3,蒋学华,廖工铁,尹华熙.阿柔比星A毫微粒冻干针剂含量测定方法.中国抗生素杂志,1994;19(6):433
收稿:1999-06-15, 百拇医药
单位:何林 蒋学华(华西医科大学药学院,成都 610041)
关键词:阿柔比星A;聚乳酸;毫微粒;体内分布
中国抗生素杂志000317 摘 要 对阿柔比星A冻干针剂与阿柔比星A(ACRB-A)聚乳酸毫微粒冻干针剂给予小鼠尾静脉注射后体内分布进行比较。采用HPLC法分别测定小鼠给药后血液及主要脏器中ACRB-A浓度。结果,阿柔比星A聚乳酸毫微粒在小鼠肝脏中的浓度高于对照品浓度。提示阿柔比星A制成毫微粒后可显著提高肝脏靶向性。
Study on the distribution of aclarubicin A poly lactide nanoparticle lyophilization in mice
He Lin
, http://www.100md.com
(Department of Pharmaceutical,The People′s Hospital of Sichuan Province,Chengdu 610072)
Jiang Xuehua
(School of Pharmacy,West China University of Medical Sciences,Chengdu 610041)
ABSTRACT Objective: Comparing the distribution of aclarubicin A lyophilization and aclarubicin A poly lactide nanoparticle (ACRB-A-PLA-NP) lyophilization in mice.Method: HPLC is selected to determine the concentration of aclarubicin A in plasma and in main organisms.Results: The concentratin of ACRB-A-PLA-NP in liver is higher than that of the reference.Conclusion: ACRB-A can be significantly concentrated in liver after prepared in nanoparticle.
, 百拇医药
KEY WORDS Aclarubicin A;Poly lactide;Nanoparticle;In vivo distribution
阿柔比星A(aclarubicin A,ACRB)是第二代蒽环类抗癌抗生素,临床用于胃癌、肺癌、乳腺癌、急性白血病、卵巢癌及恶性淋巴瘤等多种癌的治疗。主要缺点是骨髓抑制、心脏毒性、胃肠不适等毒副作用[1]。为了提高ACRB-A的抗癌效果及药物稳定性,降低毒副作用,曾以聚乳酸(poly lactide,PLA)为载体材料,制备了阿柔比星A聚乳酸毫微粒(ACRB-A-PLA-NP)[2]。本文在文献的基础上[3]采用了HPLC法测定了ACRB-A-PLA-NP在动物体内各组织中的分布。
1 材料与仪器
1.1 材料
, http://www.100md.com ACRB-A对照品(四川抗菌素工业研究所提供);ACRB-A聚乳酸毫微粒冻干针剂(自制,批号970113);注射用盐酸ACRB-A冻干剂(江苏扬州制药厂,批号950305);其余试剂皆为分析纯。
1.2 仪器
LC-6A高效液色谱仪(日本岛津);SPD-6AV紫外可见检测器(日本岛津);CR-4A数据处理机(日本岛津);TGL-16高速离心机(上海医疗器械六厂)。
1.3 动物
一级昆明种小鼠(华西医科大学实验动物中心),体重18~22g。
2 方法与结果
2.1 血浆及各组织中ACRB-A的HPLC测定法
2.1.1色谱条件 分析柱:Alltech C18 micro(250mm×4.6mm i.d,5μm);预柱:YWG-ODS(1cm×4.6mm i.d);流动相:0.2mol/L乙酸铵(pH2.5±0.1)∶甲醇=1∶3; 柱温:35℃; 流速:1ml/min; 检测波长:432nm。
, 百拇医药
2.1.2 样品预处理与测定 取小鼠心、肝、脾、肺、肾样品,分别精密称重,加入1倍量用生理盐水(脾加入2倍)制成50%匀浆液。精密量取0.25ml匀浆液(或血浆),同样方法称定其重量,加入0.1ml内标液(内含双嘧达莫的乙酸乙酯溶液),振摇后,加入0.1ml氨水,100mg NaCl及0.8ml乙酸乙酯,旋涡混合5min,离心12000r/min 10min,取上清液0.6ml,于40℃减压挥干,残渣用100μl流动相溶解,旋涡混合1min,离心5000r/min 5min,取上清液20μl进样,按上述色谱条件进行分析,结果见图1。
2.1.3 标准曲线方程的测定 分别取空白血浆及心、肝、脾、肺、肾匀浆样品,精密加入不同量ACRB-A储备液,配制成不浓度的标准溶液,从“加入0.1ml内标液”起,按样品预处理与测定方法进行处理与测定,记录样品峰与内标峰的峰面积As、Ai,峰面积之比R=As/Ai对浓度进行线性回归,得到血浆及各组织样品的回归方程分别为:
, 百拇医药
血:0.25~10.0μg/ml,R=0.000245+1.561C,r=0.9996
肾:0.25~10.0μg/g,R=-0.02+0.77C,r=0.9991
肝:1.0~40.0μg/g,R=-0.0439+0.0993C,r=0.9992
肺:0.5~20.0μg/g,R=-0.0006+0.163C,r=0.9991

图1
a:血浆空白及样品HPLC图;b:肾空白及样品HPLC图;c:肝空白及样品HPLC图;
d:肺空白及样品HPLC图;e:心空白及样品HPLC图;f:脾空白及样品HPLC图
, http://www.100md.com
心:0.5~20.0μg/g,R=-0.0105+0.108C,r=0.9990
脾:0.5~20.0μg/g,R=-0.0566+0.560C,r=0.9993
2.1.4 萃取回收率的测定 精密量取ACRB-A储备液不同量,配制高、中、低三种不同浓度的ACRB-A液,取20μl进样,记录峰面积A1。另取血浆或匀浆液0.25ml,加入ACRB-A储备液不同量,配制同样高、中、低三种不同浓度的ACRB-A液,按样品预处理与测定方法进行操作,记录样品峰的面积A2。以A2/A1之比计算萃取回收率,结果见表1。
由表1可见,除肾以外,ACRB-A在小鼠各组织中的萃取回率都在80%以上,且较稳定,说明对样品的预处理方法是可行的。
2.1.5 方法回收率的测定 分别量取空白血浆或组织匀浆液0.25ml,加入不同量ACRB-A储备液,配制成高、中、低三种不同浓度的ACRB-A溶液,从“加入0.1ml内标液”起, 按样品预处理与测定方法进行操作,记录样品峰与内标峰的面积As、Ai,以R=As/Ai代入标准曲线方程计算测定,以测定浓度与配制浓度之比计算回收率,结果见表2。
, http://www.100md.com
表1 ACRB-A在不同组织中的萃取回收率(%,n=3) 样品
[μg/ml(μg/g)]
0.5
5.0
20.0
Mean±SD
血
88.2±1.9
92.6±1.1
89.5±2.7
90.1±2.3
肾
, http://www.100md.com
72.4±2.1
78.5±2.6
76.9±3.0
75.9±3.2
肝
85.2±1.6
80.4±3.5
88.6±2.5
84.7±4.1
心
80.4±1.0
84.2±2.2
, http://www.100md.com
86.5±1.4
83.7±3.1
肺
78.1±1.9
82.5±2.0
80.7±2.4
80.4±2.2
脾
84.8±3.1
87.2±2.7
83.0±1.0
85.0±2.1
, http://www.100md.com
由表2可见,三种浓度在不同脏器中的平均回收率在96.6%~103.5%范围内,方法准确度较高。
2.1.6 方法重现性考察 配制高、中、低三种不同浓度样品液,各样品平行操作5份,按样品预处理与测定方法进行操作,得到三种浓度不同脏器供试品测定结果的日内相对标准差≤4.8%,日间相对标准差≤7.0%,方法重现性较好。 表2 方法回收率测定结果 样品
加入
(μg/ml,μg/g)
测定
(μg/ml,μg/g)
回收
(%)
Mean±SD
, 百拇医药
(%)
样品
加入
(μg/ml,μg/g)
测定
(μg/ml,μg/g)
回收
(%)
Mean±SD
(%)
血
0.5
0.54±0.01
, 百拇医药
108.2±2.5
肺
0.8
0.84±0.01
104.4±0.8
2.0
2.03±0.05
101.3±2.5
102.1±4.6
0.5
5.07±0.14
101.4±2.9
, http://www.100md.com
101.6±2.9
8.0
7.80±0.07
97.5±0.8
15.0
14.86±0.29
97.8±1.9
肾
0.5
0.48±0.01
96.4±1.9
心
, 百拇医药
0.8
0.86±0.01
107.7±1.4
2.0
1.92±0.03
95.9±1.3
96.6±1.5
5.0
5.16±0.05
103.4±1.0
103.5±4.4
8.0
, 百拇医药
7.80±0.10
97.6±1.2
15.0
14.70±0.33
98.0±2.2
肝
2.0
1.88±0.03
94.2±1.7
脾
0.8
0.82±0.01
, 百拇医药
102.9±1.2
20.0
20.33±0.24
101.7±1.2
97.8±3.5
5.0
5.08±0.17
101.6±3.4
100.7±3.0
40.0
39.09±0.45
97.7±1.1
, http://www.100md.com
15.0
14.67±0.17
97.8±1.1
2.2 尾静脉给予小鼠ACRB-A冻干剂和ACRB-A-PLA-NP冻干剂后的体内分布研究
选取体重为20±2g的健康小白鼠70只,随机分成14组,每组5只,按10mg/kg剂量分别尾静脉注射分散后的ACRB-A冻干剂和ACRB-A-PLA-NP冻干剂,给药后分别于5、15min和0.5、1、2、4、8、12、24、72、96、144h取一组,眼眶取血后,断颈处死,取心、肝、脾、肺、肾各器官,滤纸吸干其水分和血迹,称定重量(血液按小鼠体重的8%计),按样品预处理与测定方法进行操作,记录As和Ai;将R=As/Ai代入各标准曲线方程,求得血液及各器官在不同时间的浓度,血液及各脏器的药时曲线见图2。

, 百拇医药
图2 血液及各脏器的药时曲线
1:ACRB-A-PLA-NP;2:ACRB-A
3 讨论
3.1 由图可见,药物制成毫微粒后,提高了药物在肝、肾、肺中的浓度,降低了药物在血、心、脾中的浓度。按药物在这六种主要器官的百分比计算,毫微粒组在肝脏中的百分比浓度为77.91%~89.33%,平均为84.49%;对照组为39.83%~66.31%,平均为51.20%,平均提高了33.29%,说明将ACRB-A制成ACRB-PLA-NP后,提高了对肝脏的亲和性,达到了肝靶向的要求。
3.2 ACRB-A-PLA-NP静注给药后,血液中药物浓度降低很快,0.25h后即不能检出,而同样给药剂量条件下,对照组直到96h后才不能检出。这可能是由于ACRB-A-PLA-NP释药缓慢,药物浓集于肝脏后即缓慢释放,肝脏作为药物的储库,因而使血中药物浓度一直处于较低水平而不能检出。同时说明靶向给药系统与普通给药系统在血液中的作用过程显著不同,靶向给药系统在血液中的吸收、分布、消除不同于普通给药系统,在进行靶向给药系统的药物动力学研究时,已不能将普通给药制剂血液动力学的研究方法简单地应用于靶向给药系统,而应寻求靶向给药系统新的研究方法。
, 百拇医药
国家自然科学基金资助项目(合同号39570842)及国家医药技术创新博士项目(合同号95-B-09)
何林,男,生于1967年,博士,主管药师.
参考文献
1,现代临床治疗药物大全编委会编.现代临床治疗药物大全.北京:中国医药科技出版社,1995:628
2,何林,蒋学华,李屯.阿克拉霉素A聚乳酸毫微粒制备工艺研究.中国药学杂志,1998;33(5):289
3,蒋学华,廖工铁,尹华熙.阿柔比星A毫微粒冻干针剂含量测定方法.中国抗生素杂志,1994;19(6):433
收稿:1999-06-15, 百拇医药