从噬菌体抗体库筛选获得中和性人源抗甲型肝炎病毒Fab抗体
作者:曹经瑗 梁米芳 郭可謇 孟庆玲 尚丹 李德新 詹美云
单位:曹经瑗 郭可謇 孟庆玲 尚丹 詹美云(中国预防医学科学院病毒学研究所肝炎研究室 北京 100052);梁米芳 李德新(出血热研究室)
关键词:肝炎病毒;甲型;免疫球蛋白类Fab;噬菌体抗体库
中华实验和临床病毒学杂志000403 【摘要】 目的 研制人源抗甲型肝炎病毒基因工程抗体,为预防甲型肝炎病毒感染提供有效的方法。方法 采用噬菌体表面展示技术,从一名甲型肝炎恢复期病人的抗凝血中分离淋巴细胞,提取总RNA逆转录后,用一组人IgG Fab特异性引物扩增。结果 克隆和表达了8株人源抗甲型肝炎病毒抗体Fab段基因,经ELISA检测为特异性人抗甲型肝炎病毒Fab段抗体。结论 该8株人源抗甲型肝炎病毒Fab抗体都能与具有中和活性的鼠抗甲型肝炎病毒单克隆抗体产生竞争抑制反应,选其中的2株做体外中和实验,证明都有中和甲型肝炎病毒的活性。
, 百拇医药
Human Fab antibodies derived from phage display library neutralize hepatitis A virus in vitro
CAO Jingyuan, LIANG Mifang,GUO Kejian
(Institute of Virology,Chinese Academy of Preventive Medicine,Beijing 100052,China)
【Abstract】 Objective Development of recombinant human monoclonal antibody to hepatitis A virus as a emergent measure for prevention of hepatitis A virus infection. Methods Human neutralizing monoclonal antibody Fab fragments to HAV have been developed by using phage display technique. The heavy and light chains of human IgG Fab genes were amplified from a HAV patient in convalescent stage. The combinatorial phage antibody library was established by inserting both heavy and light chains of Fab genes into phagemid vector pComb3 and followed by help phage infection after 4 rounds of panning with purified HAV as coated antigen. Results The human Fab fragments to HAV were selected and expressed in bacteria. Conclusion The specific binding of Fab antibodies to HAV were demonstrated by their reaction with HAV antigen in ELISA. These results provide the basis for further development of a neutralizing recombinant human whole IgG molecule and hold promise for future use in the prophylaxis of HAV infection.
, 百拇医药
【Key words】 Hepatitis A virus; Immunoglobulins, Fab; Phage display library
甲型肝炎病毒属小RNA病毒科甲型肝炎病毒属,是经肠道传播的疾病。甲型肝炎病毒虽不易导致慢性感染,但危害人民的身体健康,并且能够造成一定的经济损失。虽然有甲型肝炎疫苗可以应用,但并没有纳入计划免疫。高效价人源免疫球蛋白作为一种被动免疫手段,在一旦有发病或流行征兆时使用不失为一种有效的应急措施。但人源制品来源困难且可能有病原微生物的污染,动物抗体因异种蛋白不宜应用〔1,2〕。随着分子生物学和分子免疫学研究的发展,体外表达基因工程单克隆抗体已经成为可能。近年发展起来的噬菌体表面展示技术中比
较有代表性的表达系统是美国Scripps研究所的pComb3系统〔3,4〕。目前研究成功的有:抗呼吸道合胞病毒(RSV)抗体〔5〕,抗乙型肝炎病毒表面抗原(HBsAg)抗体〔6〕,抗汉坦病毒抗体〔3〕及抗丙型肝炎(HCV)抗体〔7〕等。本文报道用噬菌体抗体库技术克隆出具有中和活性的抗甲型肝炎病毒的人源单克隆抗体及其特异性鉴定。
, http://www.100md.com
1 材料和方法
1.1 材料来源 实验所用质粒为pComb3〔4〕,辅助噬菌体为VSCM13,均为美国Scripps研究所馈赠。大肠埃希菌菌株为XL1Blue。甲型肝炎病毒毒株为JN13,由本室分离保存传至13代。用于甲型肝炎病毒增殖的细胞株为FRHk4细胞。
1.2 人源IgG Fab段基因的逆转录-PCR法扩增 用淋巴细胞分离液(上海试剂二厂)从一甲型肝炎病人恢复期10 ml抗凝血中(用等体积Hank′s液稀释后)分离淋巴细胞,具体方法参见文献〔8〕,用Trizol试剂提取总细胞RNA,溶于45 μl DEPC处理的水中,用cDNA合成试剂盒(美国Gibco BRL公司)通过Oligo-dT引物经逆转录合成cDNA,用一组特异性人IgG Fab κ链、λ链及γ链引物(参见文献〔3〕),对人源轻链和重链Fd基因进行PCR扩增。
1.3 噬菌体抗体基因库的建立 基本参见文献〔3〕。先将轻链用Xba Ⅰ/Sac Ⅰ酶切,与相应酶切后的载体质粒pComb3连接,用电穿孔转化大肠埃希菌XL 1Blue细胞,扩增转化后的细菌,提取质粒得到轻链载体DNA,将此载体用Xho Ⅰ/Spe Ⅰ酶切,与用Xho Ⅰ/Spe Ⅰ酶切的重链Fd片段连接,电转入XL 1Blue细胞,按文献〔3〕所述建立噬菌体抗体库。
, 百拇医药
1.4 用于抗体富集筛选的甲型肝炎病毒抗原的制备 甲型肝炎病毒在Frhk4细胞上培养24 d后收获,基本按文献〔9〕方法通过蔗糖垫层超速离心纯化甲型肝炎病毒抗原,纯化后的甲型肝炎病毒抗原可直接用于包被ELISA板。
1.5 噬菌体抗体库的特异性富集筛选 基本按文献〔4〕进行。将上述纯化的甲型肝炎病毒抗原1∶50(ELISA A值大于1.5)稀释后每孔60 μl包被6孔ELISA板,经封闭后,加入上述噬菌体抗体库60 μl/孔,经吸附-洗涤-洗脱后,按文献〔3〕中程序经培养及辅助噬菌体感染后进行下一轮筛选。如此反复筛选4~5次。
1.6 重组抗体的制备及阳性克隆的ELISA检测 基本按文献〔3,4〕进行。用纯化甲型肝炎病毒抗原包被ELISA板,加入上述抗体,用辣根过氧化物酶标记的羊抗人Fab抗体(Sigma公司产品)检测。阴性对照为载体pComb3转化菌或抗汉坦病毒Fab抗体转化菌按同样方法制备的细菌裂解液。
, 百拇医药
1.7 重组抗体的竞争抑制实验 用纯化的鼠抗甲型肝炎病毒单克隆抗体(本室制备)包被ELISA板孔,加入部分纯化的甲型肝炎病毒抗原,然后同时加入用上述方法筛选出的Fab阳性克隆及用辣根过氧化物酶标记的鼠抗甲型肝炎病毒单克隆抗体,仍用上述的阴性对照。以抑制率≥50%为阳性结果。
1.8 重组抗体的体外中和实验 基本按文献〔10〕进行。将FRhk4细胞在小试管中培养成单层,将来自不同克隆表达的Fab可溶性裂解液上清及阴性对照以0.22 μm微孔滤膜无菌过滤后,1∶2稀释,然后分别各取500 μl,与500 μl适当稀释的经等量氯仿处理后的甲型肝炎病毒混合(本实验用了30个TCID50的病毒量),37℃孵育1.5 h,每个稀释度做4管,每管接种混合物0.2 ml,37℃吸附1.5 h,然后每管加入0.8 ml含2%牛血清的Eargle′s培养液,33℃培养24 d,收获细胞,每管加入0.2 ml含2%牛血清的0.01 mol/L PBS,冻化3次后,ELISA检测甲型肝炎病毒抗原。本实验同时设阴性菌裂解液,甲型肝炎病毒抗体阳性人血清,病毒滴度及细胞对照。抗原检测为阴性(P/N值小于2.1)即病毒被中和。
, http://www.100md.com
2 结果
2.1 Fd段和轻链基因的扩增 从一甲型肝炎恢复期病人(发病后3个月)采抗凝血10 ml,用竞争抑制ELISA检测其甲型肝炎病毒总抗体,滴度为1∶5 120。图1显示纯化后的轻重链PCR产物经0.8%的琼脂糖凝胶电泳检测,在700 bp左右见到扩增带。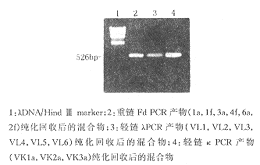
图1 PCR扩增和纯化人源IgG Fab轻重链基因
Fig.1 PCR amplification and purification of human IgG light
and heavy chains of Fab genes
1:λDNA/Hind Ⅲ marker.2:Mixture of purified products of Fd chain (1a,1f,3a,4f,6a,2f).3:Mixture of purified PCR prducts of λ chain (VL1,VL2,VL3,VL4,VL5,VL6).4:Mixture of purified PCR products of κ chain(Vk1a,Vk2a,Vk3a)
, http://www.100md.com
2.2 人源噬菌体抗体库的构建和抗甲型肝炎病毒抗体特异性富集筛选 轻链电转后,取少量细菌铺盘,测定库容为106,随机挑取10个克隆,用Xba Ⅰ+Sac Ⅰ酶切,有7个克隆能切出700 bp左右条带,说明轻链库重组率为70%。重链经电转后,测定库容为106,挑取10个菌落,用Xho Ⅰ+Xba Ⅰ酶切鉴定,5个有轻重链共同插入,说明重链Fd段重组率为50%。经4轮富集筛选后挑选出8株人源Fab抗体,图2为有轻重链基因插入的阳性克隆用Xba Ⅰ和Xho Ⅰ酶切后的结果。带噬菌体基因Ⅲ和人抗体Fab段轻重链基因插入的克隆应切出约2.2 kb的条带以及3.0 kb的载体带。图3显示随筛选轮数的增加,带有双链基因插入的克隆也逐渐增加,到最后一轮约有90%克隆显示有重链和轻链基因的插入。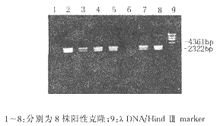
图2 经过4轮富集筛选后8株阳性克隆的
, 百拇医药 内切酶鉴定(Xho Ⅰ+Xba Ⅰ)
Fig.2 Restriction enzyme identification of 8 positive Fab gene
clones selected from phage antibody library after four
rounds of panning
1-8:Fab gene positive clones.9:λ DNA/Hind Ⅲ marker
2.3 重组克隆的ELISA鉴定 表1表明,所有8株具有双链基因插入的克隆均能与甲型肝炎病毒抗原反应,而阴性对照不能与甲型肝炎病毒抗原反应。8株重组抗体在1∶1 000稀释时均能与HRP标记的鼠抗甲型肝炎病毒单克隆抗体产生竞争抑制反应,抑制率在90%以上,而上述阴性对照不能与鼠抗甲型肝炎病毒单克隆抗体产生竞争抑制反应,说明所筛选出来的噬菌体抗体为甲型肝炎病毒特异性抗体。见表2。
, 百拇医药
图3 有轻重链基因双链插入的克隆随筛选轮数增加而增加
Fig.3 Enrichment of positive Fab clones
2.4 重组人源抗甲型肝炎病毒抗体Fab段的体外中和活性 对上述2株阳性克隆表达后的细菌裂解液上清进行了体外中和实验(HAFab9及HAFab16),结果表明,这2株克隆和阳性对照血清均能中和甲型肝炎病毒,而阴性对照则不能中和,见表3。
3 讨论
我们用噬菌体表面展示技术,得到了有中和活性的抗甲型肝炎病毒人源基因工程单克隆抗体Fab段基因及表达产物,这为以后构建人源中和性抗甲型肝炎病毒全IgG分子的表达及应用打下了良好的基础。
表1用纯化的甲型肝炎抗原直接包被ELISA板,检测噬菌体抗体与甲型肝炎抗原的结合反应
, 百拇医药
Tab.1 Specific binding of expressed human Fab antibodies with purified HAV antigen detected by ELISA 分项Type
克隆
Clones
阴性对照
Negative control
8
9
11
12
16
, http://www.100md.com 17
18
20
A值(492 nm)
A value
0.99
1.11
1.07
1.17
1.15
0.95
1.09
0.97
, 百拇医药
0.06
P/N值
P/N value
16.5
18.5
17.8
19.5
19.1
15.8
18.1
16.2
-
表2噬菌体抗体的ELISA竞争抑制实验
, 百拇医药
Tab.2 Competitive inhibition ELISA of expressed human Fab antibodies with mouse McAb for attachment to HAV antigen
克隆1∶1 000稀释Clones 1∶1 000 diluted
阴性对照
Negative control
8
9
11
12
16
17
, 百拇医药
18
20
A值(492 nm)
A value
0.09
0.09
0.08
0.05
0.04
0.07
0.10
0.07
1.00
, http://www.100md.com
抑制率(%)
Inhibition ratio(%)
91
91
92
95
96
93
90
93
0
表3 重组Fab抗体对甲型肝炎病毒的中和活性
Tab.3 Neutralizing activity of 2 human recombinant
, 百拇医药
Fab antibodies against HAV 样本
Sample
阳性管数/管数
Positive no./Tube
重组抗体Fab 9(1∶2稀释)
Human kecomlinout Fab 9(1∶2 diluted)
0/4
重组抗体Fab 16(1∶2稀释)
Human kecomlinout Fab 16(1∶2 diluted)
0/4
, 百拇医药
阳性血清对照(1∶100稀释)
Positive control(human serum,1∶100 diluted)
0/4
阴性菌裂解上清对照(1∶2稀释)
Negative control(E.coli lysate,1∶2 diluted)
4/4
病毒对照
Virus control
4/4
正常细胞对照
, http://www.100md.com
Normal cell control
0/4
甲型肝炎病毒属小RNA病毒科肝病毒属,没有包膜,只有一个血清型,抗原变异小,抗原结构相对稳定,结构蛋白主要由VP1,VP2,VP3组成,VP4较小,很少在病毒表面检测到。主要中和抗原结合位点在VP1和VP3的位置并且是构型依赖性,它的中和抗原决定簇是由密切相关的排列紧密的一组抗原位点组成〔11〕。我们得到的重组Fab克隆能中和甲型肝炎病毒,从目前结果看两倍稀释的粗制Fab抗体能完全中和30个TCID50的病毒量,但是否能中和更多的病毒则需将Fab抗体纯化浓缩后,进一步加大病毒量和抗体量做中和实验。虽然此次中和实验只用了两株重组Fab抗体,但我们得到的这几株重组人抗甲型肝炎病毒抗体Fab段均能与鼠抗甲型肝炎病毒单克隆抗体产生竞争抑制反应,而后者又能与人抗甲型肝炎病毒恢复期血清产生竞争抑制反应,且鼠抗体及人恢复期血清都有中和甲型肝炎病毒的活性,故推测我们得到的其他重组Fab抗体也应有中和活性。
, 百拇医药
从实验中8株Fab单抗与鼠单抗的竞争抑制实验表明,我们得到的这几株克隆很可能是抗同一位点的克隆。故应筛选更多的具有中和活性且抗不同位点的克隆。用常规Western blot难以检测到我们得到的重组Fab抗体到底是抗甲型肝炎病毒哪种结构蛋白的,但从我们初步的与抗VP1鼠单抗的竞争抑制实验表明,我们的单抗很可能是抗VP1的,这些还需进一步实验证实。
本课题受国家自然科学基金资助(39700123)
参 考 文 献
1,阮力,汪垣,强伯勤.新型疫苗研究的现状与展望.1992年杭州战略研讨会文集.北京:学苑出版社,1992,83-96.
2,Emmanuel BW,Richard BH,Gregory AP,et al.Concurrent administration of inactivated hepatitias A vaccine with immunglobulin in healthy adults.Vaccine,1999,17:1468-1473.
, http://www.100md.com
3,梁米芳,李德新,杭长寿,等.人源中和性抗汉滩病毒单克隆抗体Fab段基因的获得和表达.病毒学报,1997,13:297-308.
4,Carlos F,Barbas Ⅲ.Assembly of combinatorial antibody libraries on phage surfaces:The gene Ⅲ site. Proc Natl Acad Sci USA,1991,88:7978-7982.
5,James EC,Jr.,Page SG,et al.Isolation of a second recombinant human respiratory syncytial virus monoclonal antibody fragment (Fab RSVF2-5) that exhibits therapeutic efficacy in Vivo.J Infect Dis,1998,177:1073-1076.
, http://www.100md.com
6,陈竞华,王琰,刘群英,等.人源性噬菌体抗体库的构建及HBsAg人单抗的筛选.中华微生物学和免疫学杂志,1995,15:158-162.
7,Shiu W,Jacqueline MB,Jackson P,et al.Human recombinant antibodies specific for hepatitis C virus core and envelope E2 peptides from an immune phage display library.Virology,1996,219:531-535.
8,董志伟,王琰,主编.抗体工程.北京:北京医科大学中国协和医科大学联合出版社,1997.
9,Hughes JV,Stanton LW,Tomassini JE,et al. Neutralizing monoclonal antibodies to hepatitis A virus:partial localization of a neutralizing antigenic site. J Virol,1984,52:465-473.
, 百拇医药
10,郭可謇,任银海,王全颖,等.甲肝-痘苗重组病毒VMS11HAV25免疫儿童两年的效果观察.高技术通讯,1993,3:16-18.
11,Stanley ML,Ping LH. Antigenic Structure of Hepatitis A Virus. Edited by Bert LS,Ellie. Molecular aspects of Picornavirus infection and detection. American Society for Microbiology,Washington:DC 20006,1989,193-206.
(收稿日期:2000-04-28)
, http://www.100md.com
单位:曹经瑗 郭可謇 孟庆玲 尚丹 詹美云(中国预防医学科学院病毒学研究所肝炎研究室 北京 100052);梁米芳 李德新(出血热研究室)
关键词:肝炎病毒;甲型;免疫球蛋白类Fab;噬菌体抗体库
中华实验和临床病毒学杂志000403 【摘要】 目的 研制人源抗甲型肝炎病毒基因工程抗体,为预防甲型肝炎病毒感染提供有效的方法。方法 采用噬菌体表面展示技术,从一名甲型肝炎恢复期病人的抗凝血中分离淋巴细胞,提取总RNA逆转录后,用一组人IgG Fab特异性引物扩增。结果 克隆和表达了8株人源抗甲型肝炎病毒抗体Fab段基因,经ELISA检测为特异性人抗甲型肝炎病毒Fab段抗体。结论 该8株人源抗甲型肝炎病毒Fab抗体都能与具有中和活性的鼠抗甲型肝炎病毒单克隆抗体产生竞争抑制反应,选其中的2株做体外中和实验,证明都有中和甲型肝炎病毒的活性。
, 百拇医药
Human Fab antibodies derived from phage display library neutralize hepatitis A virus in vitro
CAO Jingyuan, LIANG Mifang,GUO Kejian
(Institute of Virology,Chinese Academy of Preventive Medicine,Beijing 100052,China)
【Abstract】 Objective Development of recombinant human monoclonal antibody to hepatitis A virus as a emergent measure for prevention of hepatitis A virus infection. Methods Human neutralizing monoclonal antibody Fab fragments to HAV have been developed by using phage display technique. The heavy and light chains of human IgG Fab genes were amplified from a HAV patient in convalescent stage. The combinatorial phage antibody library was established by inserting both heavy and light chains of Fab genes into phagemid vector pComb3 and followed by help phage infection after 4 rounds of panning with purified HAV as coated antigen. Results The human Fab fragments to HAV were selected and expressed in bacteria. Conclusion The specific binding of Fab antibodies to HAV were demonstrated by their reaction with HAV antigen in ELISA. These results provide the basis for further development of a neutralizing recombinant human whole IgG molecule and hold promise for future use in the prophylaxis of HAV infection.
, 百拇医药
【Key words】 Hepatitis A virus; Immunoglobulins, Fab; Phage display library
甲型肝炎病毒属小RNA病毒科甲型肝炎病毒属,是经肠道传播的疾病。甲型肝炎病毒虽不易导致慢性感染,但危害人民的身体健康,并且能够造成一定的经济损失。虽然有甲型肝炎疫苗可以应用,但并没有纳入计划免疫。高效价人源免疫球蛋白作为一种被动免疫手段,在一旦有发病或流行征兆时使用不失为一种有效的应急措施。但人源制品来源困难且可能有病原微生物的污染,动物抗体因异种蛋白不宜应用〔1,2〕。随着分子生物学和分子免疫学研究的发展,体外表达基因工程单克隆抗体已经成为可能。近年发展起来的噬菌体表面展示技术中比
较有代表性的表达系统是美国Scripps研究所的pComb3系统〔3,4〕。目前研究成功的有:抗呼吸道合胞病毒(RSV)抗体〔5〕,抗乙型肝炎病毒表面抗原(HBsAg)抗体〔6〕,抗汉坦病毒抗体〔3〕及抗丙型肝炎(HCV)抗体〔7〕等。本文报道用噬菌体抗体库技术克隆出具有中和活性的抗甲型肝炎病毒的人源单克隆抗体及其特异性鉴定。
, http://www.100md.com
1 材料和方法
1.1 材料来源 实验所用质粒为pComb3〔4〕,辅助噬菌体为VSCM13,均为美国Scripps研究所馈赠。大肠埃希菌菌株为XL1Blue。甲型肝炎病毒毒株为JN13,由本室分离保存传至13代。用于甲型肝炎病毒增殖的细胞株为FRHk4细胞。
1.2 人源IgG Fab段基因的逆转录-PCR法扩增 用淋巴细胞分离液(上海试剂二厂)从一甲型肝炎病人恢复期10 ml抗凝血中(用等体积Hank′s液稀释后)分离淋巴细胞,具体方法参见文献〔8〕,用Trizol试剂提取总细胞RNA,溶于45 μl DEPC处理的水中,用cDNA合成试剂盒(美国Gibco BRL公司)通过Oligo-dT引物经逆转录合成cDNA,用一组特异性人IgG Fab κ链、λ链及γ链引物(参见文献〔3〕),对人源轻链和重链Fd基因进行PCR扩增。
1.3 噬菌体抗体基因库的建立 基本参见文献〔3〕。先将轻链用Xba Ⅰ/Sac Ⅰ酶切,与相应酶切后的载体质粒pComb3连接,用电穿孔转化大肠埃希菌XL 1Blue细胞,扩增转化后的细菌,提取质粒得到轻链载体DNA,将此载体用Xho Ⅰ/Spe Ⅰ酶切,与用Xho Ⅰ/Spe Ⅰ酶切的重链Fd片段连接,电转入XL 1Blue细胞,按文献〔3〕所述建立噬菌体抗体库。
, 百拇医药
1.4 用于抗体富集筛选的甲型肝炎病毒抗原的制备 甲型肝炎病毒在Frhk4细胞上培养24 d后收获,基本按文献〔9〕方法通过蔗糖垫层超速离心纯化甲型肝炎病毒抗原,纯化后的甲型肝炎病毒抗原可直接用于包被ELISA板。
1.5 噬菌体抗体库的特异性富集筛选 基本按文献〔4〕进行。将上述纯化的甲型肝炎病毒抗原1∶50(ELISA A值大于1.5)稀释后每孔60 μl包被6孔ELISA板,经封闭后,加入上述噬菌体抗体库60 μl/孔,经吸附-洗涤-洗脱后,按文献〔3〕中程序经培养及辅助噬菌体感染后进行下一轮筛选。如此反复筛选4~5次。
1.6 重组抗体的制备及阳性克隆的ELISA检测 基本按文献〔3,4〕进行。用纯化甲型肝炎病毒抗原包被ELISA板,加入上述抗体,用辣根过氧化物酶标记的羊抗人Fab抗体(Sigma公司产品)检测。阴性对照为载体pComb3转化菌或抗汉坦病毒Fab抗体转化菌按同样方法制备的细菌裂解液。
, 百拇医药
1.7 重组抗体的竞争抑制实验 用纯化的鼠抗甲型肝炎病毒单克隆抗体(本室制备)包被ELISA板孔,加入部分纯化的甲型肝炎病毒抗原,然后同时加入用上述方法筛选出的Fab阳性克隆及用辣根过氧化物酶标记的鼠抗甲型肝炎病毒单克隆抗体,仍用上述的阴性对照。以抑制率≥50%为阳性结果。
1.8 重组抗体的体外中和实验 基本按文献〔10〕进行。将FRhk4细胞在小试管中培养成单层,将来自不同克隆表达的Fab可溶性裂解液上清及阴性对照以0.22 μm微孔滤膜无菌过滤后,1∶2稀释,然后分别各取500 μl,与500 μl适当稀释的经等量氯仿处理后的甲型肝炎病毒混合(本实验用了30个TCID50的病毒量),37℃孵育1.5 h,每个稀释度做4管,每管接种混合物0.2 ml,37℃吸附1.5 h,然后每管加入0.8 ml含2%牛血清的Eargle′s培养液,33℃培养24 d,收获细胞,每管加入0.2 ml含2%牛血清的0.01 mol/L PBS,冻化3次后,ELISA检测甲型肝炎病毒抗原。本实验同时设阴性菌裂解液,甲型肝炎病毒抗体阳性人血清,病毒滴度及细胞对照。抗原检测为阴性(P/N值小于2.1)即病毒被中和。
, http://www.100md.com
2 结果
2.1 Fd段和轻链基因的扩增 从一甲型肝炎恢复期病人(发病后3个月)采抗凝血10 ml,用竞争抑制ELISA检测其甲型肝炎病毒总抗体,滴度为1∶5 120。图1显示纯化后的轻重链PCR产物经0.8%的琼脂糖凝胶电泳检测,在700 bp左右见到扩增带。

图1 PCR扩增和纯化人源IgG Fab轻重链基因
Fig.1 PCR amplification and purification of human IgG light
and heavy chains of Fab genes
1:λDNA/Hind Ⅲ marker.2:Mixture of purified products of Fd chain (1a,1f,3a,4f,6a,2f).3:Mixture of purified PCR prducts of λ chain (VL1,VL2,VL3,VL4,VL5,VL6).4:Mixture of purified PCR products of κ chain(Vk1a,Vk2a,Vk3a)
, http://www.100md.com
2.2 人源噬菌体抗体库的构建和抗甲型肝炎病毒抗体特异性富集筛选 轻链电转后,取少量细菌铺盘,测定库容为106,随机挑取10个克隆,用Xba Ⅰ+Sac Ⅰ酶切,有7个克隆能切出700 bp左右条带,说明轻链库重组率为70%。重链经电转后,测定库容为106,挑取10个菌落,用Xho Ⅰ+Xba Ⅰ酶切鉴定,5个有轻重链共同插入,说明重链Fd段重组率为50%。经4轮富集筛选后挑选出8株人源Fab抗体,图2为有轻重链基因插入的阳性克隆用Xba Ⅰ和Xho Ⅰ酶切后的结果。带噬菌体基因Ⅲ和人抗体Fab段轻重链基因插入的克隆应切出约2.2 kb的条带以及3.0 kb的载体带。图3显示随筛选轮数的增加,带有双链基因插入的克隆也逐渐增加,到最后一轮约有90%克隆显示有重链和轻链基因的插入。

图2 经过4轮富集筛选后8株阳性克隆的
, 百拇医药 内切酶鉴定(Xho Ⅰ+Xba Ⅰ)
Fig.2 Restriction enzyme identification of 8 positive Fab gene
clones selected from phage antibody library after four
rounds of panning
1-8:Fab gene positive clones.9:λ DNA/Hind Ⅲ marker
2.3 重组克隆的ELISA鉴定 表1表明,所有8株具有双链基因插入的克隆均能与甲型肝炎病毒抗原反应,而阴性对照不能与甲型肝炎病毒抗原反应。8株重组抗体在1∶1 000稀释时均能与HRP标记的鼠抗甲型肝炎病毒单克隆抗体产生竞争抑制反应,抑制率在90%以上,而上述阴性对照不能与鼠抗甲型肝炎病毒单克隆抗体产生竞争抑制反应,说明所筛选出来的噬菌体抗体为甲型肝炎病毒特异性抗体。见表2。

, 百拇医药
图3 有轻重链基因双链插入的克隆随筛选轮数增加而增加
Fig.3 Enrichment of positive Fab clones
2.4 重组人源抗甲型肝炎病毒抗体Fab段的体外中和活性 对上述2株阳性克隆表达后的细菌裂解液上清进行了体外中和实验(HAFab9及HAFab16),结果表明,这2株克隆和阳性对照血清均能中和甲型肝炎病毒,而阴性对照则不能中和,见表3。
3 讨论
我们用噬菌体表面展示技术,得到了有中和活性的抗甲型肝炎病毒人源基因工程单克隆抗体Fab段基因及表达产物,这为以后构建人源中和性抗甲型肝炎病毒全IgG分子的表达及应用打下了良好的基础。
表1用纯化的甲型肝炎抗原直接包被ELISA板,检测噬菌体抗体与甲型肝炎抗原的结合反应
, 百拇医药
Tab.1 Specific binding of expressed human Fab antibodies with purified HAV antigen detected by ELISA 分项Type
克隆
Clones
阴性对照
Negative control
8
9
11
12
16
, http://www.100md.com 17
18
20
A值(492 nm)
A value
0.99
1.11
1.07
1.17
1.15
0.95
1.09
0.97
, 百拇医药
0.06
P/N值
P/N value
16.5
18.5
17.8
19.5
19.1
15.8
18.1
16.2
-
表2噬菌体抗体的ELISA竞争抑制实验
, 百拇医药
Tab.2 Competitive inhibition ELISA of expressed human Fab antibodies with mouse McAb for attachment to HAV antigen
克隆1∶1 000稀释Clones 1∶1 000 diluted
阴性对照
Negative control
8
9
11
12
16
17
, 百拇医药
18
20
A值(492 nm)
A value
0.09
0.09
0.08
0.05
0.04
0.07
0.10
0.07
1.00
, http://www.100md.com
抑制率(%)
Inhibition ratio(%)
91
91
92
95
96
93
90
93
0
表3 重组Fab抗体对甲型肝炎病毒的中和活性
Tab.3 Neutralizing activity of 2 human recombinant
, 百拇医药
Fab antibodies against HAV 样本
Sample
阳性管数/管数
Positive no./Tube
重组抗体Fab 9(1∶2稀释)
Human kecomlinout Fab 9(1∶2 diluted)
0/4
重组抗体Fab 16(1∶2稀释)
Human kecomlinout Fab 16(1∶2 diluted)
0/4
, 百拇医药
阳性血清对照(1∶100稀释)
Positive control(human serum,1∶100 diluted)
0/4
阴性菌裂解上清对照(1∶2稀释)
Negative control(E.coli lysate,1∶2 diluted)
4/4
病毒对照
Virus control
4/4
正常细胞对照
, http://www.100md.com
Normal cell control
0/4
甲型肝炎病毒属小RNA病毒科肝病毒属,没有包膜,只有一个血清型,抗原变异小,抗原结构相对稳定,结构蛋白主要由VP1,VP2,VP3组成,VP4较小,很少在病毒表面检测到。主要中和抗原结合位点在VP1和VP3的位置并且是构型依赖性,它的中和抗原决定簇是由密切相关的排列紧密的一组抗原位点组成〔11〕。我们得到的重组Fab克隆能中和甲型肝炎病毒,从目前结果看两倍稀释的粗制Fab抗体能完全中和30个TCID50的病毒量,但是否能中和更多的病毒则需将Fab抗体纯化浓缩后,进一步加大病毒量和抗体量做中和实验。虽然此次中和实验只用了两株重组Fab抗体,但我们得到的这几株重组人抗甲型肝炎病毒抗体Fab段均能与鼠抗甲型肝炎病毒单克隆抗体产生竞争抑制反应,而后者又能与人抗甲型肝炎病毒恢复期血清产生竞争抑制反应,且鼠抗体及人恢复期血清都有中和甲型肝炎病毒的活性,故推测我们得到的其他重组Fab抗体也应有中和活性。
, 百拇医药
从实验中8株Fab单抗与鼠单抗的竞争抑制实验表明,我们得到的这几株克隆很可能是抗同一位点的克隆。故应筛选更多的具有中和活性且抗不同位点的克隆。用常规Western blot难以检测到我们得到的重组Fab抗体到底是抗甲型肝炎病毒哪种结构蛋白的,但从我们初步的与抗VP1鼠单抗的竞争抑制实验表明,我们的单抗很可能是抗VP1的,这些还需进一步实验证实。
本课题受国家自然科学基金资助(39700123)
参 考 文 献
1,阮力,汪垣,强伯勤.新型疫苗研究的现状与展望.1992年杭州战略研讨会文集.北京:学苑出版社,1992,83-96.
2,Emmanuel BW,Richard BH,Gregory AP,et al.Concurrent administration of inactivated hepatitias A vaccine with immunglobulin in healthy adults.Vaccine,1999,17:1468-1473.
, http://www.100md.com
3,梁米芳,李德新,杭长寿,等.人源中和性抗汉滩病毒单克隆抗体Fab段基因的获得和表达.病毒学报,1997,13:297-308.
4,Carlos F,Barbas Ⅲ.Assembly of combinatorial antibody libraries on phage surfaces:The gene Ⅲ site. Proc Natl Acad Sci USA,1991,88:7978-7982.
5,James EC,Jr.,Page SG,et al.Isolation of a second recombinant human respiratory syncytial virus monoclonal antibody fragment (Fab RSVF2-5) that exhibits therapeutic efficacy in Vivo.J Infect Dis,1998,177:1073-1076.
, http://www.100md.com
6,陈竞华,王琰,刘群英,等.人源性噬菌体抗体库的构建及HBsAg人单抗的筛选.中华微生物学和免疫学杂志,1995,15:158-162.
7,Shiu W,Jacqueline MB,Jackson P,et al.Human recombinant antibodies specific for hepatitis C virus core and envelope E2 peptides from an immune phage display library.Virology,1996,219:531-535.
8,董志伟,王琰,主编.抗体工程.北京:北京医科大学中国协和医科大学联合出版社,1997.
9,Hughes JV,Stanton LW,Tomassini JE,et al. Neutralizing monoclonal antibodies to hepatitis A virus:partial localization of a neutralizing antigenic site. J Virol,1984,52:465-473.
, 百拇医药
10,郭可謇,任银海,王全颖,等.甲肝-痘苗重组病毒VMS11HAV25免疫儿童两年的效果观察.高技术通讯,1993,3:16-18.
11,Stanley ML,Ping LH. Antigenic Structure of Hepatitis A Virus. Edited by Bert LS,Ellie. Molecular aspects of Picornavirus infection and detection. American Society for Microbiology,Washington:DC 20006,1989,193-206.
(收稿日期:2000-04-28)
, http://www.100md.com