细胞外Mn2+对内向整流钾通道(IRK1)的阻断作用
作者:谢安 臧益民 朱妙章
单位:第四军医大学基础部生理学教研室,西安 710032
关键词:Mn2+;内向整流钾通道;电压钳;爪蟾卵母细胞
中国应用生理学杂志000412
摘要 目的和方法:采用双微电极电压钳(TEV)法研究细胞外Mn2+ 对非洲爪蟾卵母细胞表达的内向整流钾通道(IRK1)的阻断作用。结果:细 胞外Mn2+浓度分别为0、1.25、2.5、5、10和20 mmol/L,K+浓度为90 mmol/L,可 见Mn2+对IRK1的瞬间电流(施加电压后2 ms)具有Mn2+浓度依赖性和电压依赖性 阻断作用;细胞外加Mn2+后反转电位没有变化,因而IRK1对之不通透。细胞外Mn 2+浓度较低时,抑制作用的效力比Mn2+浓度较高时强;细胞外K+浓度为90 mmol/ L和Ba2+浓度为30 μmol/L时,Mn2+可竞争性与Ba2+争夺结合位点,随 着Mn2+浓度增加,电流失活过程逐渐减缓,电场距离分数由0.45逐渐变小至0.28,Ba 2+在通道中的结合位点也逐渐离开通道,说明多离子通道IRKl中具有多离于阻断形式 ,同时也表明Mn2+与Ba2+。都是IRKl的一种快速开通道阻断剂。结论 :细胞外Mn2+对IRK1的抑制作用通过了表面电荷机制和快速开通道阻断。
, http://www.100md.com
中图分类号: Q424文献标识码:A
文章编号: 1000-6843(2000)04-0331-04
THE BLOCKING EFFECTS OF EXTRACELLULAR Mn2+ ON THE
INWARD RECTIFIER POTASSIUM CHANNEL (IRKl)
XIE An ZANG Yi-min ZHU Miao-zhang
(Department of Physiology, Basic Science Institute, the Fourth Milita ry Medical University, Xi'an 710032)
, 百拇医药
ABSTRACT Aim and Methods: Two-microelectrode voltage clamp (TEV) method was used to study the blocking effects of extracellular Mn2+ on the inward rectifier pota ssium channel (IRK1) expressed in the Xenopus oocytes. Results: Mn2+ can concentration-, time- and vol-tage dependently block IRK1 instan taneous currents (2 ms after voltage applied ). Mn2+ has almost no effect on the gating property of IRK1. IRK1 can not permeate Mn2+ because reverse potential did not changed. External Mn2+ can inhibit IRK1 macroscopic c urrents more powerfully when external Mn2+ concentration is lower and exte rnal Mn2+ can increases standard chord conductance of IRK1, Conclu sion: External Mn2+ works through surface potential mechanism. Ba 2+ is considered as one fast open channel blocker of IRK1 and three expone ntial fitting results indicates that external Mn2+ can compete with Ba 2+ in the same binding site in IRK1 when external Ba2+ concentration is 30 μmol/L. These mean two different mechanisms about external Mn2+ blocki ng exist.
, 百拇医药
KEY WORDS: manganese; inward rectifier potassium channel; voltage clamp; xenopus oocytes
探讨Mn2+对内向整流钾通道(IRK1)的阻断作用不仅在二价阳离子对IRK1阻断的分子机 制的研究中有重要意义,而且对于了解IRK1结构和功能有很大帮助。以往的研究由于技术水 平有限,对通道瞬间电流的分析不够准确(施加电压后10 ms)[1],采用的数据分析 方法也不够准确[2]。已知Mn2+对IRK1的阻断作用主要表现在Mn2+可 以加快IRK1内向电流的失活过程,尤其在失活的开始部分。本文使用高质量电流曲线对Mn 2+的阻断作用做了较精确的评价,以期得出更准确的分析结论。
1 材料与方法
, 百拇医药
1.1 IRK1的表达
本文使用的IRKI的cDNA由L.Y.Jan博士(加里弗尼亚大学)馈赠。mRNA的线性化由XhoI 酶完成,转录过程使用mCAPTM mRNA capping)试剂盒(Stratagene Inc,La,Jolla ,CA),由T3多聚酶转录。mRNA的检测用凝胶电泳;其浓度测量用光谱仪,并于-80℃贮存。 使用第Ⅴ和Ⅵ期的非州爪蟾卵母细胞;在无钙的Barth液中使用胶原酶Ⅰ(SIGMA)处理1.5 h ,温度20℃,用纳升注射器(Drummond Scientific)将mRNA(1.85 ng/nl,30 ng)注入细胞 ;在正常带有抗菌素的Barth液中孵育24 h后使用。
1.2 电流记录方法
全细胞电流记录使用双微电极电压钳(TEV)法,放大器为CA-1(Dagan Corp).用两个有3M KCI的微电极刺入细胞中,一个(尖端电阻0.2~0.3 MΩ)做为电流电极,另一个(尖端电 阻约0.5 MΩ)做为电压电极,两个电极尖端的形态特别重要,并且镀上Sylgard。感受电压 的电极置于细胞1 mm左右的距离。为了测量串联电阻,一个微电极置于细胞上前方约5 μm 处,串联电阻一般小于0.2 KΩ,在需要的时候使用串联电阻补偿。使用一接地的金属板置 于微电板之间以减少电容耦合干扰。另一个电流电极用于进行电容补偿,旋转三个时间常数 和三个相位延迟可以很好地进行电容补偿。漏电流在分析数据时再除去。
, 百拇医药
第一批实验对照浴液中含有(mmol/L):KCl 90,HEPES 5,MgCl2 3和Niflumic酸0. 2(用于阻断内源性Cl-电流),pH7.4。再将0、1.25、2.5、5、10和20 mmol/L的MnCl2加 入对照浴液中。进行两个二价阳离子同时阻断的研究时,第二批实验对照液为(mmol/L):KC l 90,HEPES5,BaCl2 0.03,EGTA 0.1和Niflumic酸0.2,pH7.4。使用氯化盐将游离的M n2+浓度加至1.25、2.5、5、10和20 mmol/L,pH调为7.4。游离的Mn2+和Ba 2+浓度的计算见文献[3]。
换浴液时连续灌流速率约2.5~3.0 ml/min。接触电位用盐桥进行修正。电压波形由486计 算机与Digi Data 1 200(Axon lnstruments)产生。电流滤波频率为2 kHz,采样频率为10 k Hz,数据的获取由pCLAMP6(Axon lnstruments)完成。
, 百拇医药
实验温度为23~25℃。
1.3 数据处理
数据分析采用pCLAMP6,Excel 97与Origin完成。阳离子剂量依赖性阻断数据用下式拟合:
I/I0=(I-U){1+[X]/Kd)}+U (1)
其中I/I0为阻断剂浓度为[X]时电流残留分数,Kd为平衡解离常数,U是在饱和的[ X]时电流不可阻断的分数。
对Mn2+阻断动力学分析是先采用三个指数函数的拟合
I=A1e-(t-k)/τ1-A2e-(t-k)/τ2+A3e-(t-k)/τ3 (2)
, http://www.100md.com
其中τ为时间常数,最长的τ为阻断的时间常数,A为指数函数的权,K为进行拟合的起始时 间。然后进行下式拟合
1/τ=1/τ(0)e-δzFV/RT (3)
其中δ为电场距离分数,z为阻断剂的离子价,F,R和T为三个常用的热力学常数。
数据用均数±标准差(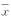 ±s)表示,每组数据例数为3-4例。
±s)表示,每组数据例数为3-4例。
2 结果
2.1 Mn2+对IRK1的阻断作用
Mn2+可加快IRK1的失活过程。这时反转电位没有变化,因而IRK1对Mn2+不 通透(图1A,B)。Mn2+对IRK1瞬间内向电流有Mn2+浓度依赖性阻断作用(图1C) ,细胞外Mn2+浓度越大,IRK1电流越小;细胞外Mn2+浓度较低时,抑制作用的 效力比Mn2+浓度较高时强(图1C);这种阻断也同时具有电压依赖性,超极化越大,Kd 越小、,阻断越明显(图1D)。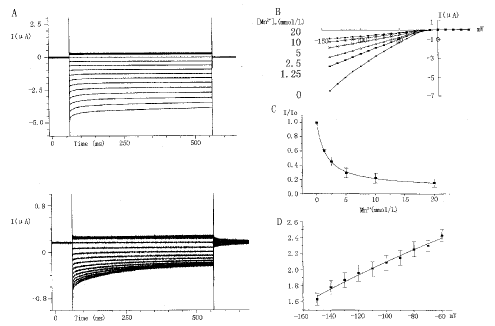
, http://www.100md.com
Fig.1 Concentration dependent blocking effects of extrace
llular Mn2+ on the inward rectifier potassium
channel (IRK1) expressed in the Xenopus oocytes
A. Above: Macroscopic currents without extracellular Mn2+.
Down: IRK1 currents with 20 mmol/L Mn2+. Voltage duration is 500 ms ,amplitude is from +40 mV to-150 mV step -10 mV. Holding potential is-30 mV.
, 百拇医药
B. Instantaneous I-V curve ( 2 ms after voltage applied ) . Data are from A.
C. Concentration dependent blocking effects of extracellular Mn2+ on IRK1 .
D. Voltage dependent blocking effects of extracellular Mn2+ on IRK1
2.2 Ba2+和Mn2+有相同的作用位点
加上不同浓度的Mn2+后,随着细胞外Mn2+浓度增大,Ba2+的作用 逐渐被Mn2+所代替,IRK1电流曲线的失活过程逐渐平缓,时间常数逐渐变大,由公式 (3)得电场距离分数由0.45逐渐变小至0.28(图2)。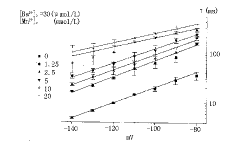
, http://www.100md.com
Fig.2 Mn2+ has the same binding site of Ba2+
External Mn2+ concentration are 0,1.25,2.5,5,10 and
20 mmol/L when external Ba2+,concentration is 30 μmol/L.
The time constants of exponen tial fitting for
blocking are from formula (2),The curves are from formula (3)
3 讨论
, 百拇医药
内向整流钾通道(inward rectifier potassium channel 1,IRK1)广泛存在于骨骼肌细 胞、心肌细胞、神经细胞、胶质细胞、血细胞和内皮细胞等,可维持细胞的静息电位和控制 细胞的兴奋性。
以往所取得的通道电流在电压加上几个ms后才能避开电容电流的影响,进而进行瞬间电 流的分析;而且以往对通道电流进行的拟合也采用的是单指数函数的拟合,对Mn2+对 瞬间内向电流的抑制作用不能很好地拟合[1,2]。通过减小电流电极尖端阻抗,用 Sylgard涂电极尖端等多方改进,我们得到了施加电压下2 ms的高质量电流曲线,并用三个 指数函数对电流曲线进行了完美的的拟合,分析的准确性大大提高。
通过分析证实了Mn2+对IRK1的阻断不仅是Mn2+浓度和电压依赖性的。IRK1 对Mn2+不通透。实验结果表明Mn2+对IRK1的阻断作用可通过两种不同的机制。 一种机制是通过表面电荷机制进行IRKl阻断的,因为细胞外Mn2+浓度较低时,抑制作 用的效力比Mn2+浓度较高时强[4,5];另一种机制是细胞外Mn2+ 是IRK1的一种快速开通道阻断剂,IRK1 呈多离子阻断[6,7]。这一结论被Mn 2+可以与Ba2+在IRK1中相竞争同一结合位点所证实,增加Mn2+浓度可使Ba 2+在通道内的结合位点逐渐被取代,IRK1失活过程越来越慢,电流的表现形式越来越象 Mn2+或Mg2+的作用[2]。因为Ba2+一直被认为是IRK1的快速开 通道阻断剂,可以与Ba2+在IRK1中相竞争同一结合位点的阳离子也是IRK1的一种快速 开通道阻断剂。
, 百拇医药
感谢日本国立生理学研究所的冈田泰伸教授提供资助并提供实验场所,感谢老木成念教 授对本文工作的悉心指导,感谢三轮晃子小姐,Ravshan Z.S.和名古屋大学的鱼助信之副 教授在分子生物学技术上的帮助。感谢加里弗尼亚大学的L.Y.Jan.教授提供的IRK1克隆 。
基金项目:国家自然科学基金资助课题(39840022)
作者简介:谢安(1965-),男,四川人,副教授,博士,从事电生理学研究
4 参考文献
[1] Kubo Y, Timothy J,Jan Y N, et al. Primary structure and functio n al expression of a mouse inward rectifier potassium channel [J]. Nature,19 93,362(11):127-131.
, 百拇医药
[2] Ravshan Z S, Tominaga T, Miwa A, et al. A conserved arginine residue i n the preregion of an inward rectifier K channel (IRKl) as an external barrier f or cationic blockers[J]. J Gen Physiol,1997,110:665-667.
[3] Oiki S, Yamamoto T, Okada Y. Apparent stability constants and purity of Ca -chelating agents evaluated using Ca-selective electrodes by the double-log o ptimization method[J]. Cell Calcium,1994,15:209-216.
[4] Block B M, Stacey W C. Jones S W. Surface charge & lanthanum block of calc ium current in bullfrog sympathetic neurons[J]. Biophysi J, 1997,74:2278- 2284.
, 百拇医药
[5] Mackinnon R. Latorre R, Miller C. Role of surface electrostatics in the op eration of a high conductance Ca2+ activated K+ channel [J]. Biochem istry, 1989,28:8092-8099.
[6] Hill B. Ionic channels of excitable membranes [M]. Si-nauer, Sunder land, M A ed2,1992,350-361.
[7] Doyle D A, Cabra J M, Richard A, et al. The structure of the potassium channel: molecular Basis of K+ conduction and selectivity [J]. Science ,1998,280(3):69-74.
收稿日期:1999-04-08
修回日期:2000-07-04, 百拇医药
单位:第四军医大学基础部生理学教研室,西安 710032
关键词:Mn2+;内向整流钾通道;电压钳;爪蟾卵母细胞
中国应用生理学杂志000412
摘要 目的和方法:采用双微电极电压钳(TEV)法研究细胞外Mn2+ 对非洲爪蟾卵母细胞表达的内向整流钾通道(IRK1)的阻断作用。结果:细 胞外Mn2+浓度分别为0、1.25、2.5、5、10和20 mmol/L,K+浓度为90 mmol/L,可 见Mn2+对IRK1的瞬间电流(施加电压后2 ms)具有Mn2+浓度依赖性和电压依赖性 阻断作用;细胞外加Mn2+后反转电位没有变化,因而IRK1对之不通透。细胞外Mn 2+浓度较低时,抑制作用的效力比Mn2+浓度较高时强;细胞外K+浓度为90 mmol/ L和Ba2+浓度为30 μmol/L时,Mn2+可竞争性与Ba2+争夺结合位点,随 着Mn2+浓度增加,电流失活过程逐渐减缓,电场距离分数由0.45逐渐变小至0.28,Ba 2+在通道中的结合位点也逐渐离开通道,说明多离子通道IRKl中具有多离于阻断形式 ,同时也表明Mn2+与Ba2+。都是IRKl的一种快速开通道阻断剂。结论 :细胞外Mn2+对IRK1的抑制作用通过了表面电荷机制和快速开通道阻断。
, http://www.100md.com
中图分类号: Q424文献标识码:A
文章编号: 1000-6843(2000)04-0331-04
THE BLOCKING EFFECTS OF EXTRACELLULAR Mn2+ ON THE
INWARD RECTIFIER POTASSIUM CHANNEL (IRKl)
XIE An ZANG Yi-min ZHU Miao-zhang
(Department of Physiology, Basic Science Institute, the Fourth Milita ry Medical University, Xi'an 710032)
, 百拇医药
ABSTRACT Aim and Methods: Two-microelectrode voltage clamp (TEV) method was used to study the blocking effects of extracellular Mn2+ on the inward rectifier pota ssium channel (IRK1) expressed in the Xenopus oocytes. Results: Mn2+ can concentration-, time- and vol-tage dependently block IRK1 instan taneous currents (2 ms after voltage applied ). Mn2+ has almost no effect on the gating property of IRK1. IRK1 can not permeate Mn2+ because reverse potential did not changed. External Mn2+ can inhibit IRK1 macroscopic c urrents more powerfully when external Mn2+ concentration is lower and exte rnal Mn2+ can increases standard chord conductance of IRK1, Conclu sion: External Mn2+ works through surface potential mechanism. Ba 2+ is considered as one fast open channel blocker of IRK1 and three expone ntial fitting results indicates that external Mn2+ can compete with Ba 2+ in the same binding site in IRK1 when external Ba2+ concentration is 30 μmol/L. These mean two different mechanisms about external Mn2+ blocki ng exist.
, 百拇医药
KEY WORDS: manganese; inward rectifier potassium channel; voltage clamp; xenopus oocytes
探讨Mn2+对内向整流钾通道(IRK1)的阻断作用不仅在二价阳离子对IRK1阻断的分子机 制的研究中有重要意义,而且对于了解IRK1结构和功能有很大帮助。以往的研究由于技术水 平有限,对通道瞬间电流的分析不够准确(施加电压后10 ms)[1],采用的数据分析 方法也不够准确[2]。已知Mn2+对IRK1的阻断作用主要表现在Mn2+可 以加快IRK1内向电流的失活过程,尤其在失活的开始部分。本文使用高质量电流曲线对Mn 2+的阻断作用做了较精确的评价,以期得出更准确的分析结论。
1 材料与方法
, 百拇医药
1.1 IRK1的表达
本文使用的IRKI的cDNA由L.Y.Jan博士(加里弗尼亚大学)馈赠。mRNA的线性化由XhoI 酶完成,转录过程使用mCAPTM mRNA capping)试剂盒(Stratagene Inc,La,Jolla ,CA),由T3多聚酶转录。mRNA的检测用凝胶电泳;其浓度测量用光谱仪,并于-80℃贮存。 使用第Ⅴ和Ⅵ期的非州爪蟾卵母细胞;在无钙的Barth液中使用胶原酶Ⅰ(SIGMA)处理1.5 h ,温度20℃,用纳升注射器(Drummond Scientific)将mRNA(1.85 ng/nl,30 ng)注入细胞 ;在正常带有抗菌素的Barth液中孵育24 h后使用。
1.2 电流记录方法
全细胞电流记录使用双微电极电压钳(TEV)法,放大器为CA-1(Dagan Corp).用两个有3M KCI的微电极刺入细胞中,一个(尖端电阻0.2~0.3 MΩ)做为电流电极,另一个(尖端电 阻约0.5 MΩ)做为电压电极,两个电极尖端的形态特别重要,并且镀上Sylgard。感受电压 的电极置于细胞1 mm左右的距离。为了测量串联电阻,一个微电极置于细胞上前方约5 μm 处,串联电阻一般小于0.2 KΩ,在需要的时候使用串联电阻补偿。使用一接地的金属板置 于微电板之间以减少电容耦合干扰。另一个电流电极用于进行电容补偿,旋转三个时间常数 和三个相位延迟可以很好地进行电容补偿。漏电流在分析数据时再除去。
, 百拇医药
第一批实验对照浴液中含有(mmol/L):KCl 90,HEPES 5,MgCl2 3和Niflumic酸0. 2(用于阻断内源性Cl-电流),pH7.4。再将0、1.25、2.5、5、10和20 mmol/L的MnCl2加 入对照浴液中。进行两个二价阳离子同时阻断的研究时,第二批实验对照液为(mmol/L):KC l 90,HEPES5,BaCl2 0.03,EGTA 0.1和Niflumic酸0.2,pH7.4。使用氯化盐将游离的M n2+浓度加至1.25、2.5、5、10和20 mmol/L,pH调为7.4。游离的Mn2+和Ba 2+浓度的计算见文献[3]。
换浴液时连续灌流速率约2.5~3.0 ml/min。接触电位用盐桥进行修正。电压波形由486计 算机与Digi Data 1 200(Axon lnstruments)产生。电流滤波频率为2 kHz,采样频率为10 k Hz,数据的获取由pCLAMP6(Axon lnstruments)完成。
, 百拇医药
实验温度为23~25℃。
1.3 数据处理
数据分析采用pCLAMP6,Excel 97与Origin完成。阳离子剂量依赖性阻断数据用下式拟合:
I/I0=(I-U){1+[X]/Kd)}+U (1)
其中I/I0为阻断剂浓度为[X]时电流残留分数,Kd为平衡解离常数,U是在饱和的[ X]时电流不可阻断的分数。
对Mn2+阻断动力学分析是先采用三个指数函数的拟合
I=A1e-(t-k)/τ1-A2e-(t-k)/τ2+A3e-(t-k)/τ3 (2)
, http://www.100md.com
其中τ为时间常数,最长的τ为阻断的时间常数,A为指数函数的权,K为进行拟合的起始时 间。然后进行下式拟合
1/τ=1/τ(0)e-δzFV/RT (3)
其中δ为电场距离分数,z为阻断剂的离子价,F,R和T为三个常用的热力学常数。
数据用均数±标准差(
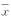 ±s)表示,每组数据例数为3-4例。
±s)表示,每组数据例数为3-4例。2 结果
2.1 Mn2+对IRK1的阻断作用
Mn2+可加快IRK1的失活过程。这时反转电位没有变化,因而IRK1对Mn2+不 通透(图1A,B)。Mn2+对IRK1瞬间内向电流有Mn2+浓度依赖性阻断作用(图1C) ,细胞外Mn2+浓度越大,IRK1电流越小;细胞外Mn2+浓度较低时,抑制作用的 效力比Mn2+浓度较高时强(图1C);这种阻断也同时具有电压依赖性,超极化越大,Kd 越小、,阻断越明显(图1D)。

, http://www.100md.com
Fig.1 Concentration dependent blocking effects of extrace
llular Mn2+ on the inward rectifier potassium
channel (IRK1) expressed in the Xenopus oocytes
A. Above: Macroscopic currents without extracellular Mn2+.
Down: IRK1 currents with 20 mmol/L Mn2+. Voltage duration is 500 ms ,amplitude is from +40 mV to-150 mV step -10 mV. Holding potential is-30 mV.
, 百拇医药
B. Instantaneous I-V curve ( 2 ms after voltage applied ) . Data are from A.
C. Concentration dependent blocking effects of extracellular Mn2+ on IRK1 .
D. Voltage dependent blocking effects of extracellular Mn2+ on IRK1
2.2 Ba2+和Mn2+有相同的作用位点
加上不同浓度的Mn2+后,随着细胞外Mn2+浓度增大,Ba2+的作用 逐渐被Mn2+所代替,IRK1电流曲线的失活过程逐渐平缓,时间常数逐渐变大,由公式 (3)得电场距离分数由0.45逐渐变小至0.28(图2)。

, http://www.100md.com
Fig.2 Mn2+ has the same binding site of Ba2+
External Mn2+ concentration are 0,1.25,2.5,5,10 and
20 mmol/L when external Ba2+,concentration is 30 μmol/L.
The time constants of exponen tial fitting for
blocking are from formula (2),The curves are from formula (3)
3 讨论
, 百拇医药
内向整流钾通道(inward rectifier potassium channel 1,IRK1)广泛存在于骨骼肌细 胞、心肌细胞、神经细胞、胶质细胞、血细胞和内皮细胞等,可维持细胞的静息电位和控制 细胞的兴奋性。
以往所取得的通道电流在电压加上几个ms后才能避开电容电流的影响,进而进行瞬间电 流的分析;而且以往对通道电流进行的拟合也采用的是单指数函数的拟合,对Mn2+对 瞬间内向电流的抑制作用不能很好地拟合[1,2]。通过减小电流电极尖端阻抗,用 Sylgard涂电极尖端等多方改进,我们得到了施加电压下2 ms的高质量电流曲线,并用三个 指数函数对电流曲线进行了完美的的拟合,分析的准确性大大提高。
通过分析证实了Mn2+对IRK1的阻断不仅是Mn2+浓度和电压依赖性的。IRK1 对Mn2+不通透。实验结果表明Mn2+对IRK1的阻断作用可通过两种不同的机制。 一种机制是通过表面电荷机制进行IRKl阻断的,因为细胞外Mn2+浓度较低时,抑制作 用的效力比Mn2+浓度较高时强[4,5];另一种机制是细胞外Mn2+ 是IRK1的一种快速开通道阻断剂,IRK1 呈多离子阻断[6,7]。这一结论被Mn 2+可以与Ba2+在IRK1中相竞争同一结合位点所证实,增加Mn2+浓度可使Ba 2+在通道内的结合位点逐渐被取代,IRK1失活过程越来越慢,电流的表现形式越来越象 Mn2+或Mg2+的作用[2]。因为Ba2+一直被认为是IRK1的快速开 通道阻断剂,可以与Ba2+在IRK1中相竞争同一结合位点的阳离子也是IRK1的一种快速 开通道阻断剂。
, 百拇医药
感谢日本国立生理学研究所的冈田泰伸教授提供资助并提供实验场所,感谢老木成念教 授对本文工作的悉心指导,感谢三轮晃子小姐,Ravshan Z.S.和名古屋大学的鱼助信之副 教授在分子生物学技术上的帮助。感谢加里弗尼亚大学的L.Y.Jan.教授提供的IRK1克隆 。
基金项目:国家自然科学基金资助课题(39840022)
作者简介:谢安(1965-),男,四川人,副教授,博士,从事电生理学研究
4 参考文献
[1] Kubo Y, Timothy J,Jan Y N, et al. Primary structure and functio n al expression of a mouse inward rectifier potassium channel [J]. Nature,19 93,362(11):127-131.
, 百拇医药
[2] Ravshan Z S, Tominaga T, Miwa A, et al. A conserved arginine residue i n the preregion of an inward rectifier K channel (IRKl) as an external barrier f or cationic blockers[J]. J Gen Physiol,1997,110:665-667.
[3] Oiki S, Yamamoto T, Okada Y. Apparent stability constants and purity of Ca -chelating agents evaluated using Ca-selective electrodes by the double-log o ptimization method[J]. Cell Calcium,1994,15:209-216.
[4] Block B M, Stacey W C. Jones S W. Surface charge & lanthanum block of calc ium current in bullfrog sympathetic neurons[J]. Biophysi J, 1997,74:2278- 2284.
, 百拇医药
[5] Mackinnon R. Latorre R, Miller C. Role of surface electrostatics in the op eration of a high conductance Ca2+ activated K+ channel [J]. Biochem istry, 1989,28:8092-8099.
[6] Hill B. Ionic channels of excitable membranes [M]. Si-nauer, Sunder land, M A ed2,1992,350-361.
[7] Doyle D A, Cabra J M, Richard A, et al. The structure of the potassium channel: molecular Basis of K+ conduction and selectivity [J]. Science ,1998,280(3):69-74.
收稿日期:1999-04-08
修回日期:2000-07-04, 百拇医药