腺病毒载体介导的CD自杀基因体外抑瘤效果观察
作者:高军 龙建秋 谷爱梅 李茂 崔龙 戴观荣 潘卫 曹广文
单位:高军 龙建秋 谷爱梅 李茂(海军医学研究所,上海 200433);崔龙 戴观荣 潘卫 曹广文(第二军医大学)
关键词:CD基因;腺病毒;肿瘤
海军医学杂志000309 [摘要] 目的:构建含CD基因的腺病毒载体pAd-CD, 进行肿瘤的 自杀基因治疗。方法:分别 构建了含CD基因和LacZ基因的重组病毒质粒载体,同质粒pJM17共转染293细胞同源重组后包 装为感染性腺病毒颗粒,经滴度测定后,体外分别感染小鼠前胃癌肿瘤细胞MFC。结果:感 染Ad-LacZ的细胞可被X-gal染成蓝色,感染Ad-CD的细胞予前药5-FC可见肿瘤细胞杀伤效果 明显。结论:腺病毒载体可有效地转CD和LacZ基因进入肿瘤细胞,C D基因作为自杀基因进行 体外肿瘤治疗效果明显,本实验构建的新载体及结果为下一步应用于体内肿瘤基因治疗研究 提供了基础。
, http://www.100md.com
[中图分类号] R392.11;R73-362 [ 文献标识码] A
[文章编号] 1009-0754(2000)03-0218-04
In Vitro Tumor-killing Effect of Suicide CD
Gene Induced by Adenovirus Vector
GAO Jun, CUI Long, LONG Jian-qiu,et al
(Naval Medical Research Institute, Shanghai 200433, China)
Abstract: Objective:Construction of an adenovirus—pAd-CD containing bacterial cytosine deaminase was used for tumor suicide gene therapy. Meth od:We constru cted a recombinant adenoviral vector carrying CD or LacZ. The infectious adenovi ruse expressing CD were produced by 293 packaging cells transfected by the r ecom binant plasmid and plasmid pJM17. After titer of the adenovirus, they were us ed to infect mouse tumor cells—MFC in vitro. Result:Cel ls infected by Ad-L acZ were dyed blue by X-gal. Cells infected by Ad-CD were obviously killed after administration of 5-FC. Conclusion:Adenoviral vector can efficiently transfect LacZ and CD gene to tumor cells. CD as a suicide gene is able to kill tumor cel l in vitro. The new adenoviral vector constructed in our lab and the researc h re sults provide sound basis for future application of tumor gene therapy in vivo.
, 百拇医药
Key words: cytosine deaminase gene ; adenovirus vector ;tumor
在人类基因治疗研究中,作为基因转移载体的病毒主要有:逆转录病毒(RV)、腺病毒( Ad)、腺相关病毒(AVV)、HIV病毒及HSV病毒载体。腺病毒载体易于包装和扩增,病毒稳 定,感染宿主范围广,可以感染分裂期细胞和静止期细胞,而且病毒滴度可达1013粒 子/ml,感染效率高,每个细胞可感染数十拷贝病毒基因组,极大地提高了单个细胞目的基因表达 。由于腺病毒载体的这些特点,在肿瘤基因治疗研究中,具有广泛的应用前景。本实验构建 了含CD基因和LacZ基因的重组病毒载体,将此载体经293细胞内重组包装为感染性腺病毒, 体外感染小鼠前胃癌肿瘤细胞MFC,并给予前药5-FC,观察抑瘤效果,为自杀基因应用于结 肠癌的基因治疗研究奠定基础。
1 材料和方法
, 百拇医药 1.1 材料 含CD基因的质粒pCD2,含腺病毒载体E1区缺失的小片段质 粒pΔE1sp1A, 含腺 病毒载体大片段载体质粒pJM17,含LacZ基因的质粒pSV-β-Galactosidase,均在前期文献 上已报道[1],Lipofect AMINETM、DMEM、胎牛血清均购于Gibco公司,X-gal 购于华美公司,凝胶纯化试剂盒购于华顺公司,293细胞和MFC细胞由长海医院普外科提供, 其余材料及试剂为本室贮备。
1.2 含CD基因的腺病毒载体构建 具体过程参见前期报道[1] 。主要步骤如下:①将pCI质 粒的1.3 kb真核细胞基因转录框架插入pΔE1sp1A质粒中, 即为质粒pCI′;②从质粒p CD2中 取出CD基因放入质粒pCI′转录框架的polylinker位点中,即为pAd-CD;③从质粒pSV-β-Ga lactosidase取出LacZ基因放入质粒pCI′转录框架的polylinker位点中,即为pAd-LacZ。
, 百拇医药
1.3 重组腺病毒液的制备[2]
1.3.1 细胞培养 293细胞和MFC细胞均以DMEM培养基(10%小牛血清,0.2 mmol/ L谷氨酰胺,0.1 mol/L丙酮酸)于37℃,含5%CO2的孵箱中培养。
1.3.2 重组腺病毒Ad-CD,Ad-lacZ的包装 293细胞于转染前24 h以(1~5)×105接种于 60 mm培 养皿中,第二天细胞60%~70%融合时开始转染,操作过程如下:在2个1.5 ml的Eppendorf 管 中,分别加入无血清的DMEM培养液90 μl,其中一管内加入10 μl lipofect AMINETM,另 一 管内加入质粒pAd-CD(或质粒pAd-lacZ)和质粒pJM17各2μg,而后将两管液体混匀为转染液 ,室温下放置45 min;将6孔板内细胞培养液吸弃,设置pAD-CD,pAD-lacZ和单纯培养 基对照 组,用2 ml无血清DMEM清洗细胞一遍后,分别对应加入上述的转染液,每孔内补足无血清DM EM培养液至1 ml,5 h后换含10%小牛血清的DMEM培养基继续培养,约10~14 d后出现细胞 病理 效应(cytopathic effect,CPE),即原来贴壁细胞变圆,脱落。4 000 r/min 离心收集病 理细胞,加入1 ml含10%甘油的PBS2+,37℃/-20℃反复冻融病理细胞3次,即为细 胞裂解粗提液,-70℃保存备用。
, http://www.100md.com
1.3.3 重组腺病毒的扩增 将293细胞培养后达80%~90%融合,以1~10 pfu/细胞的感染比 率加 入适当稀释的上述所获粗提液,病毒吸附60min后,加入含10%小牛血清的DMEM培养基,每天 观察2次,当细胞完全出现CPE效应(即绝大多数细胞变圆,但没有完全脱落),将细胞刮落后 同培养基一起离心(800g×15 min)去除上清,将细胞沉淀重悬于适量含10%甘油的PBS 2+缓冲液中,反复冻融3次,分装后,于-70 ℃保存。
1.3.4 病毒滴度测定 快速CPE法测定:在测定前一天,在24孔板中接种1×105细胞/孔 ,第 二天细胞达70%融合后,加入系列稀释的待检病毒悬液400 μl,(用DMEM稀释至10-3 、10-4 、10-5、10-6、10-7、10-8、10-9)每个浓度设复孔,并 设对照,37 ℃感染60 min后,倾去 400 μl上清,加入1 ml DMEM完全培养基继续培养,48 h后观察CPE反应,以达100%CPE现象 孔的病毒稀释倍数计算病毒滴度,公式如下: 颗粒数/ml=(2×105细胞/孔×稀释倍数× 10 pfu/细胞)÷0.4 ml
, http://www.100md.com
1.4 体外转基因效果观察及抑瘤实验 小鼠前胃癌细胞系MFC 以DMEM( 含10%小牛血清、0.2 mmol/L谷氨酰胺、0.1 mol/L丙酮酸钠),37 ℃及5%CO2培养,当培养细胞融后达70%时 ,加入 适量的腺病毒Ad-LacZ进行感染,1 h后换DMEM培养液进行培养,24 h后换成10%甲醛+PBS液 对 细胞固定30 min,PBS洗2次后,加入适量X-gal染色液,于37 ℃染色5~6 h即可看到细胞变 蓝, 倒置显微镜观察及摄影。同时在96孔板中接种1.0×104/孔的MFC细胞,37 ℃及5%CO2培 养12 h 后,分别按20 pfu/细胞的感染比率加入重组腺病毒Ad-CD和Ad-LacZ,感染6 h后弃上清,细 胞 分别称为MFC-CD和MFC-LacZ,加入不同浓度的5-FC进行细胞杀伤实验,梯度浓度为:0.5、0 .75、0.125、0.0075、0.038、0.019、0.001、0.0005、0.00025(mol/L)共孵育48 h,观察细胞变化,并以MTT法检测细胞存活率。
, 百拇医药
2 结 果
2.1 载体构建 在构建携带外源基因的腺病毒载体E1区缺失的小片段时 ,为了使外源基因 能有效表达,在构建过程中首先将真核表达载体质粒pCI中的转录框架构建入腺病毒载 体小片段中,而后再将CD基因和LacZ基因分别装配到框架的多克隆位点中,这样,既能使目 的基因得到有效表达,且使LacZ基因在后期体内外转基因实验中作为对照更具有可比性。pA d-CD和pAd-LacZ 重组腺病毒载体小片段最后经大量扩增后,经多酶切鉴定结果同理论推算 值一致,证明构建成功,构建的重组质粒基因结构图分别如图1所示。
2.2 包装及扩增后的滴度测定 包装后含CD基因的腺病毒Ad-CD滴度为5 ×108颗粒/ml,含Lac Z基因的腺病毒Ad-LacZ滴度为5×108颗粒/ml,扩增后滴度分别为5×1011和5×10 10颗粒/ml。
, http://www.100md.com
2.3 体外转基因效果观察及抑瘤实验 MFC-LacZ细胞的X-gal染色结果 见图2; 对MFC-CD细 胞,予以前药5-FC进行抑瘤实验,其肿瘤生长受抑效果见图3,从图3可以看出,体外转CD基 因的MFC细胞在5-FC作用下生长明显受抑制(P<0.01,n=9),而对照细 胞的生长未出现明显的变化。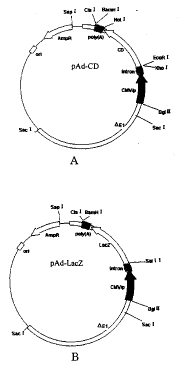
图1 质粒pAd-CD(A)和pAd-LacZ(B)结构示意图
图2 MFC-LacZ细胞的X-gal染色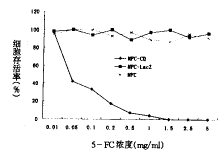
图3 转CD基因MFC胃癌细胞体外生长受抑曲线
, http://www.100md.com
MFC-CD:转CD基因且以5-FC治疗组细胞
MFC-LacZ:转LacZ 基因且以5-FC治疗组细胞
3 讨 论
本实验采用的腺病毒载体为两部分组成,一部分为质粒pJM17,包含有腺病毒5型的环状 基因组全序列和4.3 kb的氨苄青霉素抗性和四环素抗性基因,总长度为40.3 kb,超过了105 % 的腺病毒的包装上限[3],另一部分为质粒p△E1sp1A包含ITR(1~103 bp),核 心包装信号( 194~358 bp),蛋白IX的编码序列及其启动子序列,而去除了3 184 bp(342~352 bp)的 序列。 将这两部分共转染293细胞(提供腺病毒基因组左端11%的基因表达产物),可包装出能携带 外源基因4.7~4.9 kb的复制缺陷的重组腺病毒[4],前期实验构建的带有CD和Lac Z基因的腺 病毒小片段,外源序列为2.8 kb和4.8 kb,均未超出包装上限。经过同源重组包装出 的腺病毒,仍是△E1缺失型,所以必需在293细胞中才能完成增殖过程。
, 百拇医药
本实验中,以pJM17和带有目的基因的pΔE1sp1A同转入293细胞进行同源重组,获得重组腺 病毒,经过多次实验才成功,而且病毒滴度与同类研究相比较低,影响进一步应用研究及以 此方法进行其它目的基因的转基因治疗研究,最近He TC报道[5]一种新的在细菌 内进行同源重 组的腺病毒载体系统,获得重组载体质粒后再转染293细胞,包装出感染性病毒颗粒,提 高了病毒滴度,节省了实验时间,本实验室现以此方法同源重组了CD基因、人白介素12和B7 -1的cDNA的腺病毒载体质粒,包装后病毒产出率较高。参照本次实验结果,应用新的腺 病毒载体系统,将可能在下一步体内实验中得到较好抑瘤效果。
部分受国家自然基金资助,项目号 39600172
[参考文献]
[1] 高 军,朱 伟,崔 龙,等.含CD基因的腺病毒载体的构建[J].海军医 学杂志,1999,20(2):132.
, 百拇医药
[2] Graham FL,Prevec L. Methods for construction of adenovirus vector s[J]. Molecular Biotechnology,1995,3:207.
[3] McGrory J,Bautista D,Graham FL. A simple technique for the rescu e of early region I mutations into infectious human adenovirus type 5[J]. Virolo gy,1988,163:614.
[4] Bett AJ, Haddara W , Prevec L, et al. An effi cient and flexible sys tem for construction of adenovirus vectors with insertions or deletions on early regions 1 and 3[J]. Proc Natl Acad Sci USA ,1994,91:8802.
[5] He TC, Zhou S, Costa LTC, et al. A simplified system for gen erating recombinant adenoviruses[J]. Pro Natl Acad Sci USA, 1998,95:2509 .
(收稿:2000-04-10), 百拇医药
单位:高军 龙建秋 谷爱梅 李茂(海军医学研究所,上海 200433);崔龙 戴观荣 潘卫 曹广文(第二军医大学)
关键词:CD基因;腺病毒;肿瘤
海军医学杂志000309 [摘要] 目的:构建含CD基因的腺病毒载体pAd-CD, 进行肿瘤的 自杀基因治疗。方法:分别 构建了含CD基因和LacZ基因的重组病毒质粒载体,同质粒pJM17共转染293细胞同源重组后包 装为感染性腺病毒颗粒,经滴度测定后,体外分别感染小鼠前胃癌肿瘤细胞MFC。结果:感 染Ad-LacZ的细胞可被X-gal染成蓝色,感染Ad-CD的细胞予前药5-FC可见肿瘤细胞杀伤效果 明显。结论:腺病毒载体可有效地转CD和LacZ基因进入肿瘤细胞,C D基因作为自杀基因进行 体外肿瘤治疗效果明显,本实验构建的新载体及结果为下一步应用于体内肿瘤基因治疗研究 提供了基础。
, http://www.100md.com
[中图分类号] R392.11;R73-362 [ 文献标识码] A
[文章编号] 1009-0754(2000)03-0218-04
In Vitro Tumor-killing Effect of Suicide CD
Gene Induced by Adenovirus Vector
GAO Jun, CUI Long, LONG Jian-qiu,et al
(Naval Medical Research Institute, Shanghai 200433, China)
Abstract: Objective:Construction of an adenovirus—pAd-CD containing bacterial cytosine deaminase was used for tumor suicide gene therapy. Meth od:We constru cted a recombinant adenoviral vector carrying CD or LacZ. The infectious adenovi ruse expressing CD were produced by 293 packaging cells transfected by the r ecom binant plasmid and plasmid pJM17. After titer of the adenovirus, they were us ed to infect mouse tumor cells—MFC in vitro. Result:Cel ls infected by Ad-L acZ were dyed blue by X-gal. Cells infected by Ad-CD were obviously killed after administration of 5-FC. Conclusion:Adenoviral vector can efficiently transfect LacZ and CD gene to tumor cells. CD as a suicide gene is able to kill tumor cel l in vitro. The new adenoviral vector constructed in our lab and the researc h re sults provide sound basis for future application of tumor gene therapy in vivo.
, 百拇医药
Key words: cytosine deaminase gene ; adenovirus vector ;tumor
在人类基因治疗研究中,作为基因转移载体的病毒主要有:逆转录病毒(RV)、腺病毒( Ad)、腺相关病毒(AVV)、HIV病毒及HSV病毒载体。腺病毒载体易于包装和扩增,病毒稳 定,感染宿主范围广,可以感染分裂期细胞和静止期细胞,而且病毒滴度可达1013粒 子/ml,感染效率高,每个细胞可感染数十拷贝病毒基因组,极大地提高了单个细胞目的基因表达 。由于腺病毒载体的这些特点,在肿瘤基因治疗研究中,具有广泛的应用前景。本实验构建 了含CD基因和LacZ基因的重组病毒载体,将此载体经293细胞内重组包装为感染性腺病毒, 体外感染小鼠前胃癌肿瘤细胞MFC,并给予前药5-FC,观察抑瘤效果,为自杀基因应用于结 肠癌的基因治疗研究奠定基础。
1 材料和方法
, 百拇医药 1.1 材料 含CD基因的质粒pCD2,含腺病毒载体E1区缺失的小片段质 粒pΔE1sp1A, 含腺 病毒载体大片段载体质粒pJM17,含LacZ基因的质粒pSV-β-Galactosidase,均在前期文献 上已报道[1],Lipofect AMINETM、DMEM、胎牛血清均购于Gibco公司,X-gal 购于华美公司,凝胶纯化试剂盒购于华顺公司,293细胞和MFC细胞由长海医院普外科提供, 其余材料及试剂为本室贮备。
1.2 含CD基因的腺病毒载体构建 具体过程参见前期报道[1] 。主要步骤如下:①将pCI质 粒的1.3 kb真核细胞基因转录框架插入pΔE1sp1A质粒中, 即为质粒pCI′;②从质粒p CD2中 取出CD基因放入质粒pCI′转录框架的polylinker位点中,即为pAd-CD;③从质粒pSV-β-Ga lactosidase取出LacZ基因放入质粒pCI′转录框架的polylinker位点中,即为pAd-LacZ。
, 百拇医药
1.3 重组腺病毒液的制备[2]
1.3.1 细胞培养 293细胞和MFC细胞均以DMEM培养基(10%小牛血清,0.2 mmol/ L谷氨酰胺,0.1 mol/L丙酮酸)于37℃,含5%CO2的孵箱中培养。
1.3.2 重组腺病毒Ad-CD,Ad-lacZ的包装 293细胞于转染前24 h以(1~5)×105接种于 60 mm培 养皿中,第二天细胞60%~70%融合时开始转染,操作过程如下:在2个1.5 ml的Eppendorf 管 中,分别加入无血清的DMEM培养液90 μl,其中一管内加入10 μl lipofect AMINETM,另 一 管内加入质粒pAd-CD(或质粒pAd-lacZ)和质粒pJM17各2μg,而后将两管液体混匀为转染液 ,室温下放置45 min;将6孔板内细胞培养液吸弃,设置pAD-CD,pAD-lacZ和单纯培养 基对照 组,用2 ml无血清DMEM清洗细胞一遍后,分别对应加入上述的转染液,每孔内补足无血清DM EM培养液至1 ml,5 h后换含10%小牛血清的DMEM培养基继续培养,约10~14 d后出现细胞 病理 效应(cytopathic effect,CPE),即原来贴壁细胞变圆,脱落。4 000 r/min 离心收集病 理细胞,加入1 ml含10%甘油的PBS2+,37℃/-20℃反复冻融病理细胞3次,即为细 胞裂解粗提液,-70℃保存备用。
, http://www.100md.com
1.3.3 重组腺病毒的扩增 将293细胞培养后达80%~90%融合,以1~10 pfu/细胞的感染比 率加 入适当稀释的上述所获粗提液,病毒吸附60min后,加入含10%小牛血清的DMEM培养基,每天 观察2次,当细胞完全出现CPE效应(即绝大多数细胞变圆,但没有完全脱落),将细胞刮落后 同培养基一起离心(800g×15 min)去除上清,将细胞沉淀重悬于适量含10%甘油的PBS 2+缓冲液中,反复冻融3次,分装后,于-70 ℃保存。
1.3.4 病毒滴度测定 快速CPE法测定:在测定前一天,在24孔板中接种1×105细胞/孔 ,第 二天细胞达70%融合后,加入系列稀释的待检病毒悬液400 μl,(用DMEM稀释至10-3 、10-4 、10-5、10-6、10-7、10-8、10-9)每个浓度设复孔,并 设对照,37 ℃感染60 min后,倾去 400 μl上清,加入1 ml DMEM完全培养基继续培养,48 h后观察CPE反应,以达100%CPE现象 孔的病毒稀释倍数计算病毒滴度,公式如下: 颗粒数/ml=(2×105细胞/孔×稀释倍数× 10 pfu/细胞)÷0.4 ml
, http://www.100md.com
1.4 体外转基因效果观察及抑瘤实验 小鼠前胃癌细胞系MFC 以DMEM( 含10%小牛血清、0.2 mmol/L谷氨酰胺、0.1 mol/L丙酮酸钠),37 ℃及5%CO2培养,当培养细胞融后达70%时 ,加入 适量的腺病毒Ad-LacZ进行感染,1 h后换DMEM培养液进行培养,24 h后换成10%甲醛+PBS液 对 细胞固定30 min,PBS洗2次后,加入适量X-gal染色液,于37 ℃染色5~6 h即可看到细胞变 蓝, 倒置显微镜观察及摄影。同时在96孔板中接种1.0×104/孔的MFC细胞,37 ℃及5%CO2培 养12 h 后,分别按20 pfu/细胞的感染比率加入重组腺病毒Ad-CD和Ad-LacZ,感染6 h后弃上清,细 胞 分别称为MFC-CD和MFC-LacZ,加入不同浓度的5-FC进行细胞杀伤实验,梯度浓度为:0.5、0 .75、0.125、0.0075、0.038、0.019、0.001、0.0005、0.00025(mol/L)共孵育48 h,观察细胞变化,并以MTT法检测细胞存活率。
, 百拇医药
2 结 果
2.1 载体构建 在构建携带外源基因的腺病毒载体E1区缺失的小片段时 ,为了使外源基因 能有效表达,在构建过程中首先将真核表达载体质粒pCI中的转录框架构建入腺病毒载 体小片段中,而后再将CD基因和LacZ基因分别装配到框架的多克隆位点中,这样,既能使目 的基因得到有效表达,且使LacZ基因在后期体内外转基因实验中作为对照更具有可比性。pA d-CD和pAd-LacZ 重组腺病毒载体小片段最后经大量扩增后,经多酶切鉴定结果同理论推算 值一致,证明构建成功,构建的重组质粒基因结构图分别如图1所示。
2.2 包装及扩增后的滴度测定 包装后含CD基因的腺病毒Ad-CD滴度为5 ×108颗粒/ml,含Lac Z基因的腺病毒Ad-LacZ滴度为5×108颗粒/ml,扩增后滴度分别为5×1011和5×10 10颗粒/ml。
, http://www.100md.com
2.3 体外转基因效果观察及抑瘤实验 MFC-LacZ细胞的X-gal染色结果 见图2; 对MFC-CD细 胞,予以前药5-FC进行抑瘤实验,其肿瘤生长受抑效果见图3,从图3可以看出,体外转CD基 因的MFC细胞在5-FC作用下生长明显受抑制(P<0.01,n=9),而对照细 胞的生长未出现明显的变化。

图1 质粒pAd-CD(A)和pAd-LacZ(B)结构示意图

图2 MFC-LacZ细胞的X-gal染色

图3 转CD基因MFC胃癌细胞体外生长受抑曲线
, http://www.100md.com
MFC-CD:转CD基因且以5-FC治疗组细胞
MFC-LacZ:转LacZ 基因且以5-FC治疗组细胞
3 讨 论
本实验采用的腺病毒载体为两部分组成,一部分为质粒pJM17,包含有腺病毒5型的环状 基因组全序列和4.3 kb的氨苄青霉素抗性和四环素抗性基因,总长度为40.3 kb,超过了105 % 的腺病毒的包装上限[3],另一部分为质粒p△E1sp1A包含ITR(1~103 bp),核 心包装信号( 194~358 bp),蛋白IX的编码序列及其启动子序列,而去除了3 184 bp(342~352 bp)的 序列。 将这两部分共转染293细胞(提供腺病毒基因组左端11%的基因表达产物),可包装出能携带 外源基因4.7~4.9 kb的复制缺陷的重组腺病毒[4],前期实验构建的带有CD和Lac Z基因的腺 病毒小片段,外源序列为2.8 kb和4.8 kb,均未超出包装上限。经过同源重组包装出 的腺病毒,仍是△E1缺失型,所以必需在293细胞中才能完成增殖过程。
, 百拇医药
本实验中,以pJM17和带有目的基因的pΔE1sp1A同转入293细胞进行同源重组,获得重组腺 病毒,经过多次实验才成功,而且病毒滴度与同类研究相比较低,影响进一步应用研究及以 此方法进行其它目的基因的转基因治疗研究,最近He TC报道[5]一种新的在细菌 内进行同源重 组的腺病毒载体系统,获得重组载体质粒后再转染293细胞,包装出感染性病毒颗粒,提 高了病毒滴度,节省了实验时间,本实验室现以此方法同源重组了CD基因、人白介素12和B7 -1的cDNA的腺病毒载体质粒,包装后病毒产出率较高。参照本次实验结果,应用新的腺 病毒载体系统,将可能在下一步体内实验中得到较好抑瘤效果。
部分受国家自然基金资助,项目号 39600172
[参考文献]
[1] 高 军,朱 伟,崔 龙,等.含CD基因的腺病毒载体的构建[J].海军医 学杂志,1999,20(2):132.
, 百拇医药
[2] Graham FL,Prevec L. Methods for construction of adenovirus vector s[J]. Molecular Biotechnology,1995,3:207.
[3] McGrory J,Bautista D,Graham FL. A simple technique for the rescu e of early region I mutations into infectious human adenovirus type 5[J]. Virolo gy,1988,163:614.
[4] Bett AJ, Haddara W , Prevec L, et al. An effi cient and flexible sys tem for construction of adenovirus vectors with insertions or deletions on early regions 1 and 3[J]. Proc Natl Acad Sci USA ,1994,91:8802.
[5] He TC, Zhou S, Costa LTC, et al. A simplified system for gen erating recombinant adenoviruses[J]. Pro Natl Acad Sci USA, 1998,95:2509 .
(收稿:2000-04-10), 百拇医药