白细胞介素1受体拮抗剂对小鼠再灌注损伤的保护作用
作者:毛颖 周良辅 杨国源
单位:毛颖(200040 上海医科大学附属华山医院神经外科);周良辅(200040 上海医科大学附属华山医院神经外科);杨国源(美国密歇根大学神经外科)
关键词:脑缺血;再灌注;细胞间粘附分子1;受体;白细胞介素1
中华医学杂志000922 【摘要】 目的 探讨在小鼠线栓模型中,基因转染过度表达的IL-1ra蛋白对局灶性脑缺血再灌注损伤的保护作用。方法 成年CD-1小鼠,右侧脑室内注射腺病毒载体(编码人类重组IL-1ra或LacZ基因)或生理盐水。5 d后,单侧大脑中动脉线栓阻断1 h,再灌注23 h。采用激光多普勒血流仪(LDF)监测脑表面血流,HE染色脑切片计算脑梗死体积,内源性白蛋白免疫组织化学染色评价血脑屏障破坏程度,并采用免疫组织化学染色,计数脑内细胞间粘附分子(ICAM-1)表达阳性血管。结果 IL-1ra基因转染小鼠脑梗死面积明显小于LacZ基因转染组和生理盐水对照组(36.0 mm3±5.3 mm3 , 60.0 mm3±6.2 mm3和69.5 mm3±6.3 mm3,P<0.05)。IL-1ra基因转染组小鼠血脑屏障破坏程度也明显轻于LacZ基因转染组和生理盐水对照组(P<0.05)。同时缺血皮质区和基底节区ICAM-1阳性血管数明显少于LacZ基因转染组和生理盐水对照组(P<0.05)。结论 证实IL-1ra对脑缺血/再灌注损伤具有保护作用。转基因表达的IL-1ra能减少缺血区ICAM-1的表达。
, 百拇医药
Attenuation of reperfusion injury in the mouse transfected interleukin-1 receptor antagonist
MAO Ying
(Department of Neurosurgery, Huashan Hospital, Shanghai Medical University, Shanghai 200040, China)
ZHOU Liangfu
(Department of Neurosurgery, Huashan Hospital, Shanghai Medical University, Shanghai 200040, China)
YANG Guoyuan.
, 百拇医药
(Department of Neurosurgery, Huashan Hospital, Shanghai Medical University, Shanghai 200040, China)
【Abstract】 Objective To investigate the therapeutic effects of overexpression of interleukin-1 receptor antagonist (IL-1ra), administered by gene transfer, on the transient cerebral ischemic injury in an experimental mice suture model. Methods Adenovirus vector encoding human IL-1ra gene (Ad.RSVIL-1ra) or LacZ gene (Ad.RSVLacZ) or normal saline was administered by injection into the right lateral ventricle in adult CD-1 mice. Five days after the virus injection, the mice received 1h transient middle cerebral artery occlusion with 23 h reperfusion. Surface cerebral blood flow was measured using laser Doppler flowmetry. Brain infarct volume was evaluated on the sections with hematoxylin-eosin staining. Blood-brain barrier (BBB) permeability was determined using immunostaining of extravasated endogenous albumin. The number of intracellular adhesion molecular-1-positive vessels was determined by immunohistochemistry. Results The infarct volume in the Ad.RSVIL-1ra transfected mice was markedly reduced compared with the Ad.RSVLacZ transfected or saline mice (36.0±5.3 mm3 vs 60.0±6.2 mm3, 69.5±6.3 mm3, P<0.05). BBB disruption area was also smaller in the Ad. RSVIL-1ra transfected mice than in the Ad.RSVLacZ transfected and saline mice (P<0.05). The expression of intracellular adhesion molecular-1 (ICAM-1) positive vessels in the ischemic cortex and basal ganglia was greatly attenuated in the Ad. RSVIL-1ra transfected mice (cortex:135±23, vs 311±40 and 357±51;basal ganglia:90±21,vs 207±43 and 259±43, P<0.05). Conclusion IL-1ra has neuroprotective property during ischemia/reperfusion injury. Overexpression of IL-1ra via gene transfer can attenuate the expression of ICAM-1 in the ischemic area.
, http://www.100md.com
【Key words】 Cerebral ischemia; Reperfusion; Intracellular adhesion molecular-1; Receptors, interleukin-1
脑缺血后再灌注损伤在作用机理上不同于缺血损害,可以引起更严重的损害,迟发性缺血后低灌注、细胞肿胀、自由基损害和凋亡。但再灌注损伤的具体作用机制还不明确。通过基因转染使外源基因在脑内表达是研究脑缺血病理机制的有效手段。在大鼠和小鼠脑室中注射携带白细胞介素1受体拮抗剂(IL-1ra)基因片段的腺病毒载体,能使IL-1ra在脑组织中表达持续数天[1,2]。我们采用基因转染的方法,研究过度表达的IL-1ra蛋白对小鼠再灌注损伤的保护作用。
材料和方法
1.实验分组:雄性成年CD-1小鼠(Charles River,美国),体重30~35 g。分为3组(1)IL-1ra组:8只,局灶性脑缺血前5 d小鼠右侧脑室内注入编码人IL-1racDNA的腺病毒载体;(2)LacZ组:8只,同样条件下在小鼠右侧脑室内注入编码人LacZ基因的腺病毒载体,用于排除腺病毒本身对实验的影响;(3)Saline组:8只,同样条件下在小鼠右侧脑室内注入等量生理盐水,排除手术操作对实验的影响。
, http://www.100md.com
2.腺病毒载体构建:实验前,首先构建复制缺陷的人腺病毒血清5型来源的腺病毒载体,具体方法已有文献介绍[3]。我们构建了2种不同的重组腺病毒载体Ad.RSVIL-1ra和Ad.RSVLacZ,分别携带人类IL-1ra cDNA片段和编码E.coli LacZ基因的cDNA片段。以Rous肉瘤病毒(RSV)为启动子驱动基因转录。2种载体唯一不同的是携带的目的基因cDNA片段。
3.腺病毒注射:小鼠麻醉后被置于立体定向头架上,矢状缝右侧1 mm,冠状缝后方1 mm颅骨钻孔,33 Ga注射针穿刺右侧脑室。1 μl腺病毒悬液(浓度1×1012颗粒/ml)注入脑室,速度0.2 μl/min。完成后5 min内缓慢撤出针头,骨蜡封闭骨孔,缝合切口。为了解腺病毒载体引起脑内炎症反应的程度,各实验组另选小鼠2只,于脑室注射后1 d断头,取针道处10 μm厚脑片,作HE染色,光镜下分析炎症细胞浸润。
4.局灶性脑缺血(单侧大脑中动脉线栓阻断):脑室内病毒载体或生理盐水注射后5 d,4%异氟醚气体麻醉诱导(70%氮与30%氧混合气),面罩吸入1.5%异氟醚作麻醉维持。反馈控制电热毯,控制体温在37℃±1℃。PE-10管作左侧股动脉插管以监测血压和血气。
, http://www.100md.com
小鼠暂时性单侧大脑中动脉线栓模型(缺血1 h/再灌流23 h),已有另文介绍[4]。暴露左侧颈总动脉(CCA)和颈外动脉(ECA),于CCA分叉处用微型动脉夹临时阻断ECA,在ECA末端将其切断,自断口送入经处理后末端呈球型的5~0单股尼龙线,直视下将线头转入ICA,向上至遇阻力为止,线头顶端至CCA分叉处距离约11.0 mm±0.5 mm。缝合切口,麻醉复苏。插线后1 h,再次将小鼠麻醉,打开切口,将尼龙线自ECA断口徐徐拔出,使线头退至CCA分叉处,实现再灌流。
5.脑血流(CBF)测定:采用激光多普勒血流测定仪(LDF)测量局部脑血流。选择三点测定脑血流(小鼠颅骨菲薄,颅骨外所测局部CBF值与开颅所测值差异无显著意义),分别代表缺血中心区、缺血对照区和缺血半暗区CBF。血流变化以缺血后CBF/缺血前基值×%表示。
6.脑梗死体积测定:缺血1 h,再灌流23 h后,断头,取脑,干冰速冻,冰冻切片机上在距额极1、3、5、7 mm处切取20 μm厚冠状脑片。常规HE染色,显示梗死区域。采用计算机图像分析系统处理图像,计算梗死面积和梗死体积。水肿对梗死体积的影响采用Swanson等[5]的方法进行纠正。
, 百拇医药
7.内源性白蛋白免疫组织化学染色:在切取脑片作梗死区域分析同时,再切取10 μm厚冠状脑片。采用标准ABC染色法,切片在1∶400的兔抗小鼠白蛋白抗体中4℃下孵育过夜。漂洗后,再将玻片放入生物素化的羊抗兔二抗中孵育90 min。3,3'-diaminobenzidine tetrahydrochloride(DAB)作为过氧化物酶底物显色。对照片采用相同浓度正常兔IgG代替一抗。内源性白蛋白被染成深棕色。计算机图像分析系统计算6个冠状面(Bregma 1.34、0.86、0.38、-0.10、-0.58和-1.06)上白蛋白染色面积。水肿对血脑屏障(BBB)破坏面积的影响采用Swanson等[5]的方法进行纠正。
8.细胞间粘附分子-1(ICAM-1)免疫组织化学染色:在切取脑片作梗死区域及BBB破坏分析同时,用冰冻切片机切取位于Bregma 0.38处的20 μm厚度的冠状脑片,并直接贴于玻片,风干。常规ABC染色法,切片在1∶300的大鼠抗小鼠CD-54(ICAM-1)单抗中4℃下孵育过夜。切片在室温下与生物素化的兔抗大鼠二抗(1∶200)孵育90 min。DAB作为过氧化物酶底物显色并用苏木素复染。照片采用相同浓度的正常大鼠IgG替代一抗。光镜下,脑片上每侧半球选择皮质区和基底节区进行ICAM-1阳性血管(深棕色)计数,采用手工计数可除外ICAM-1表达阳性的炎症细胞。
, 百拇医药
9.统计学分析:采用方差分析判断3组间各项指标的差异,如差异有显著意义,再经Bonferroni校正,作组间均数两两比较。数值均以平均值±标准误表示。统计显著意义设定为P<0.05。
结果
1.脑血流改变: IL-1ra组、LacZ组和Saline组小鼠插线后5 min缺血中心区的CBF分别降至缺血前基值的12%±1%、15%±1%和13%±2%,3组间CBF变化没有明显差别。对照侧脑表面CBF线栓后分别维持在缺血前基值的100%±3%、101%±1%和99%±2%。再灌注后缺血中心区的CBF即刻恢复至缺血前基值的76%±5%、70%±4%和66%±8%,再灌注23 h后,缺血中心区的CBF仍能维持在缺血前基值的50%左右。3组间缺血和再灌注前后脑表面血流变化未见明显差异(P>0.05)。
2.脑梗死体积: IL-1ra组脑梗死体积36.0 mm3±5 mm3比对照组LacZ组60.0 mm3±6.2 mm3和Saline组69.5 mm3±6.3 mm3减小40%~48%左右(F=6.977,P<0.05)。组间两两比较显示IL-1ra组脑梗死体积与2个对照组有显著差异,但对照组间差异无显著意义。
, http://www.100md.com
3.血脑屏障破坏:采用内源性白蛋白渗出范围评价血脑屏障破坏程度,缺血对照侧染色阴性。IL-1ra组6个冠状面上血脑屏障破坏范围均明显小于LacZ组和Saline组(P<0.05)。
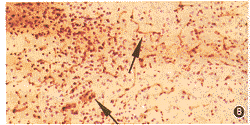
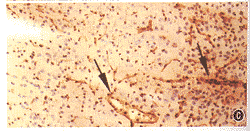
4.ICAM-1阳性血管表达:上述免疫组织化学方法能清楚显示ICAM-1阳性血管。各组对侧半球只有少量ICAM-1阳性血管表达(少于10根/层面),差异无显著意义。但缺血侧微血管内皮上ICAM-1表达明显上调,并且皮质区表达数多于基底节区,呈现自缺血核心区到缺血边缘区表达逐渐增多的趋势。IL-1ra组皮质区ICAM-1阳性血管数少于LacZ组和Saline组(135±23,比311±40,357±51,F=9.137,P<0.05,图1)。IL-1ra组缺血侧基底节区ICAM-1阳性血管数也明显少于LacZ组和Saline组(90±21比207±43,259±43,F=9.554,P<0.05)。组间两两比较,IL-1ra组缺血侧皮质区和基底节区ICAM-1阳性血管数与2个对照组差异有显著意义,而对照组间差异无显著意义。
, 百拇医药
3组间缺血前后的生理指标(血压、PO2、PCO2、pH和氧饱和度)无明显改变(P>0.05)。将腺病毒或生理盐水注入侧脑室未发现全身毒性症状或神经系统症状。HE染色显示3组小鼠针道周围都有轻微组织反应,但白细胞浸润局限于针道周围。3组间组织反应没有显著差别。
讨论
再灌注后的急性炎症反应与脑缺血后的继发性脑损害存在密切关系。粘附分子和细胞因子在缺血和再灌注早期即能产生,使缺血损伤转变为炎症损伤。缺血区炎症细胞浸润可使微血管堵塞,造成“无灌流现象”;同时炎症细胞可产生蛋白溶解酶,氧自由基以及其他损害因子,破坏血管内皮,引起血脑屏障破坏和出血。本研究证实:(1)炎症细胞在缺血区的聚集和粘附的时相与再灌注后的脑损害具有相关性。再灌注后6 h,缺血区可见明显白细胞浸润,并比永久性脑缺血出现得更快,范围更广,说明血流再灌注可使炎症反应加重。同时脑梗死体积在再灌注后6~24 h内迅速增大,到48 h达到与永久性损害相似的梗死体积,这一梗死体积发展过程与炎症细胞的浸润时相一致[6]。(2)去除血液中白细胞能改善再灌注损伤。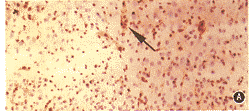
, 百拇医药
图1 ICAM-1免疫组织化学染色,显示IL-lra组(A)半暗区的ICAM-1阳性血管数明显少于LacZ组(B)和Saline组(C)的相应区 HE ×10(箭头示阳性血管)
细胞因子对炎症细胞具有趋化作用,促进炎症细胞在缺血区聚集。脑缺血后再灌注能引起细胞因子的释放。白细胞介素-1β(IL-1β)是一种炎症细胞的强烈趋化因子,能诱导和促进脑缺血后其他炎症介质的损伤作用,引起神经元死亡[8]。在白细胞介素1移化酶(ICE)基因敲除的转基因小鼠中,因抑制了白细胞介素1前体转化为白细胞介素1,脑缺血损害明显减轻[8,9]。IL-1ra是单核细胞来源的17 000多肽,在体内和体外实验中都能抑制IL-1β的作用[10]。我们在前期实验中,利用腺病毒载体编码人IL-1ra基因,通过脑室内微量注射,使IL-1ra在大鼠和小鼠的室管膜细胞中过度表达,能减少脑缺血后的梗死面积[1,2],同时也证实过度表达的IL-1ra蛋白能减轻脑缺血后的脑水肿和炎症反应[11]。但目前对IL-1在再灌注损伤中的作用机制尚不明确。研究白细胞介素1在缺血再灌注损伤中的机理,有利于找到治疗临床脑缺血病人的新途径。
, 百拇医药
脑缺血/再灌注后发生急性炎症反应的前提条件是炎症细胞粘附于血管内皮细胞,这一粘附反应依赖于粘附分子间的复杂反应。脑缺血再灌注损伤后粘附分子表达上调。Matsuo等[12]报道大鼠大脑中动脉阻断后1~3 h细胞间粘附分子-1(ICAM-1)和内皮白细胞粘附分子-1(ELAM-1)表达增高,并可维持到缺血后1周。阻断内皮细胞上ICAM-1与白细胞结合的位点,能使大鼠暂时性脑缺血后梗死范围减少45~50%[13]。说明ICAM-1在脑缺血再灌注后的损伤机制中起重要作用。
本研究发现,白细胞介素1受体拮抗剂对小鼠再灌注损伤有明显的保护作用,能改善脑缺血损伤,稳定血脑屏障,减轻炎症反应。并能抑制粘附分子的表达。说明白细胞介素1在再灌注损伤中确实起重要作用。作用途径之一可能通过减少细胞间粘附分子的表达,减少炎症细胞附壁,从而阻止炎症细胞附壁、移行,损害脑组织。但白细胞介素1究竟激活何种信息传递路径发挥作用,还需作进一步研究。
, http://www.100md.com
基金项目:美国NIH NS-35089(GYY)和NS-23870(ALB)基金资助项目
参考文献
1,Betz AL, Yang GY, Davidson BL, et al. Attenuation of stroke size in rats using an adenoviral vector to induce overexpression of interleukin-1 receptor antagonist in brain. J Cereb Blood Flow Metab, 1995, 15: 547-551.
2,Yang G, Zhao Y, Davidson BL, et al. Overexpression of interleukin-1 receptor antagonist in the mouse brain reduces ischemic brain injury. Brain Res, 1997, 751: 181-188.
, 百拇医药
3,Roessler BJ, Hartman JW, Vallance DK, et al. Inhibition of IL-1 induced effects in synoviocytes transduced with the human IL-1 receptor antagonist cDNA using an adenoviral vector. Hum Gene Ther, 1995, 6: 307-316.
4,Mao Y, Yang GY, Zhou LF, et al. Focal cerebral ischemia in the mouse: description of a model and effects of permanent and temporary occlusion. Mol Brain Res, 1999, 63:366-370.
5,Swanson RA, Morton MT, Tsao WG, et al. A semiautomated method for measuring brain infarct volume. J Cereb Blood Flow Metab, 1990, 10: 290-293.
, http://www.100md.com
6,Zhang RL, Chopp M, Chen H, et al. Temporal profile of ischemic tissue damage, neutrophil response, and vascular plugging following permanent and transient (2H) middle cerebral artery occlusion in the rat. J Neurol Sci, 1994, 125: 3-10.
7,Betz AL, Schielke GP, Yang GY. Interleukin-1 in cerebral ischemia. Keio J Med, 1996, 45:230-238.
8,Hara H, Fink K, Moskowitz MA, et al. Attenuation of transient focal cerebral ischemic injury in transgenic mice expressing a mutant ICE inhibitory protein. J Cereb Blood Flow Metab, 1997, 17: 370-375.
, 百拇医药
9,Schielke GP, Yang GY, Betz AL, et al. Reduced ischemic brain injury in interleukin-1? converting enzyme (ICE) deficient mice. J Cereb Blood Flow Metab, 1998, 18: 180-185.
10,Wang XK, Barone FC, Aiyar NV, et al. Interleukin-1 receptor and receptor antagonist gene expression after focal stroke in rats. Stroke, 1997, 28:155-162.
11,Yang GY, Liu XL,Kadoya C, et al. Attenuation of ischemic inflammatory response in mouse brain using an adenoviral vector to induce overexpression of interkin-1 receptor antagonist. J Cereb Blood Flow Metab, 1998, 18: 840-847.
, 百拇医药
12,Matsuo Y, Onodera H, Shiga Y, et al. Role of cell adhesion molecules in brain injury after transient middle cerebral artery occlusion in the rat. Brain Res, 1994, 656: 344-352.
13,Zhang RL, Chopp M, Li Y, et al. Anti-ICAM-1 antibody reduces ischemic cell damage after transient middle cerebral artery occlusion in the rat. Neurolology, 1994, 44: 1747-1751.
(收稿日期:1999-06-25), http://www.100md.com
单位:毛颖(200040 上海医科大学附属华山医院神经外科);周良辅(200040 上海医科大学附属华山医院神经外科);杨国源(美国密歇根大学神经外科)
关键词:脑缺血;再灌注;细胞间粘附分子1;受体;白细胞介素1
中华医学杂志000922 【摘要】 目的 探讨在小鼠线栓模型中,基因转染过度表达的IL-1ra蛋白对局灶性脑缺血再灌注损伤的保护作用。方法 成年CD-1小鼠,右侧脑室内注射腺病毒载体(编码人类重组IL-1ra或LacZ基因)或生理盐水。5 d后,单侧大脑中动脉线栓阻断1 h,再灌注23 h。采用激光多普勒血流仪(LDF)监测脑表面血流,HE染色脑切片计算脑梗死体积,内源性白蛋白免疫组织化学染色评价血脑屏障破坏程度,并采用免疫组织化学染色,计数脑内细胞间粘附分子(ICAM-1)表达阳性血管。结果 IL-1ra基因转染小鼠脑梗死面积明显小于LacZ基因转染组和生理盐水对照组(36.0 mm3±5.3 mm3 , 60.0 mm3±6.2 mm3和69.5 mm3±6.3 mm3,P<0.05)。IL-1ra基因转染组小鼠血脑屏障破坏程度也明显轻于LacZ基因转染组和生理盐水对照组(P<0.05)。同时缺血皮质区和基底节区ICAM-1阳性血管数明显少于LacZ基因转染组和生理盐水对照组(P<0.05)。结论 证实IL-1ra对脑缺血/再灌注损伤具有保护作用。转基因表达的IL-1ra能减少缺血区ICAM-1的表达。
, 百拇医药
Attenuation of reperfusion injury in the mouse transfected interleukin-1 receptor antagonist
MAO Ying
(Department of Neurosurgery, Huashan Hospital, Shanghai Medical University, Shanghai 200040, China)
ZHOU Liangfu
(Department of Neurosurgery, Huashan Hospital, Shanghai Medical University, Shanghai 200040, China)
YANG Guoyuan.
, 百拇医药
(Department of Neurosurgery, Huashan Hospital, Shanghai Medical University, Shanghai 200040, China)
【Abstract】 Objective To investigate the therapeutic effects of overexpression of interleukin-1 receptor antagonist (IL-1ra), administered by gene transfer, on the transient cerebral ischemic injury in an experimental mice suture model. Methods Adenovirus vector encoding human IL-1ra gene (Ad.RSVIL-1ra) or LacZ gene (Ad.RSVLacZ) or normal saline was administered by injection into the right lateral ventricle in adult CD-1 mice. Five days after the virus injection, the mice received 1h transient middle cerebral artery occlusion with 23 h reperfusion. Surface cerebral blood flow was measured using laser Doppler flowmetry. Brain infarct volume was evaluated on the sections with hematoxylin-eosin staining. Blood-brain barrier (BBB) permeability was determined using immunostaining of extravasated endogenous albumin. The number of intracellular adhesion molecular-1-positive vessels was determined by immunohistochemistry. Results The infarct volume in the Ad.RSVIL-1ra transfected mice was markedly reduced compared with the Ad.RSVLacZ transfected or saline mice (36.0±5.3 mm3 vs 60.0±6.2 mm3, 69.5±6.3 mm3, P<0.05). BBB disruption area was also smaller in the Ad. RSVIL-1ra transfected mice than in the Ad.RSVLacZ transfected and saline mice (P<0.05). The expression of intracellular adhesion molecular-1 (ICAM-1) positive vessels in the ischemic cortex and basal ganglia was greatly attenuated in the Ad. RSVIL-1ra transfected mice (cortex:135±23, vs 311±40 and 357±51;basal ganglia:90±21,vs 207±43 and 259±43, P<0.05). Conclusion IL-1ra has neuroprotective property during ischemia/reperfusion injury. Overexpression of IL-1ra via gene transfer can attenuate the expression of ICAM-1 in the ischemic area.
, http://www.100md.com
【Key words】 Cerebral ischemia; Reperfusion; Intracellular adhesion molecular-1; Receptors, interleukin-1
脑缺血后再灌注损伤在作用机理上不同于缺血损害,可以引起更严重的损害,迟发性缺血后低灌注、细胞肿胀、自由基损害和凋亡。但再灌注损伤的具体作用机制还不明确。通过基因转染使外源基因在脑内表达是研究脑缺血病理机制的有效手段。在大鼠和小鼠脑室中注射携带白细胞介素1受体拮抗剂(IL-1ra)基因片段的腺病毒载体,能使IL-1ra在脑组织中表达持续数天[1,2]。我们采用基因转染的方法,研究过度表达的IL-1ra蛋白对小鼠再灌注损伤的保护作用。
材料和方法
1.实验分组:雄性成年CD-1小鼠(Charles River,美国),体重30~35 g。分为3组(1)IL-1ra组:8只,局灶性脑缺血前5 d小鼠右侧脑室内注入编码人IL-1racDNA的腺病毒载体;(2)LacZ组:8只,同样条件下在小鼠右侧脑室内注入编码人LacZ基因的腺病毒载体,用于排除腺病毒本身对实验的影响;(3)Saline组:8只,同样条件下在小鼠右侧脑室内注入等量生理盐水,排除手术操作对实验的影响。
, http://www.100md.com
2.腺病毒载体构建:实验前,首先构建复制缺陷的人腺病毒血清5型来源的腺病毒载体,具体方法已有文献介绍[3]。我们构建了2种不同的重组腺病毒载体Ad.RSVIL-1ra和Ad.RSVLacZ,分别携带人类IL-1ra cDNA片段和编码E.coli LacZ基因的cDNA片段。以Rous肉瘤病毒(RSV)为启动子驱动基因转录。2种载体唯一不同的是携带的目的基因cDNA片段。
3.腺病毒注射:小鼠麻醉后被置于立体定向头架上,矢状缝右侧1 mm,冠状缝后方1 mm颅骨钻孔,33 Ga注射针穿刺右侧脑室。1 μl腺病毒悬液(浓度1×1012颗粒/ml)注入脑室,速度0.2 μl/min。完成后5 min内缓慢撤出针头,骨蜡封闭骨孔,缝合切口。为了解腺病毒载体引起脑内炎症反应的程度,各实验组另选小鼠2只,于脑室注射后1 d断头,取针道处10 μm厚脑片,作HE染色,光镜下分析炎症细胞浸润。
4.局灶性脑缺血(单侧大脑中动脉线栓阻断):脑室内病毒载体或生理盐水注射后5 d,4%异氟醚气体麻醉诱导(70%氮与30%氧混合气),面罩吸入1.5%异氟醚作麻醉维持。反馈控制电热毯,控制体温在37℃±1℃。PE-10管作左侧股动脉插管以监测血压和血气。
, http://www.100md.com
小鼠暂时性单侧大脑中动脉线栓模型(缺血1 h/再灌流23 h),已有另文介绍[4]。暴露左侧颈总动脉(CCA)和颈外动脉(ECA),于CCA分叉处用微型动脉夹临时阻断ECA,在ECA末端将其切断,自断口送入经处理后末端呈球型的5~0单股尼龙线,直视下将线头转入ICA,向上至遇阻力为止,线头顶端至CCA分叉处距离约11.0 mm±0.5 mm。缝合切口,麻醉复苏。插线后1 h,再次将小鼠麻醉,打开切口,将尼龙线自ECA断口徐徐拔出,使线头退至CCA分叉处,实现再灌流。
5.脑血流(CBF)测定:采用激光多普勒血流测定仪(LDF)测量局部脑血流。选择三点测定脑血流(小鼠颅骨菲薄,颅骨外所测局部CBF值与开颅所测值差异无显著意义),分别代表缺血中心区、缺血对照区和缺血半暗区CBF。血流变化以缺血后CBF/缺血前基值×%表示。
6.脑梗死体积测定:缺血1 h,再灌流23 h后,断头,取脑,干冰速冻,冰冻切片机上在距额极1、3、5、7 mm处切取20 μm厚冠状脑片。常规HE染色,显示梗死区域。采用计算机图像分析系统处理图像,计算梗死面积和梗死体积。水肿对梗死体积的影响采用Swanson等[5]的方法进行纠正。
, 百拇医药
7.内源性白蛋白免疫组织化学染色:在切取脑片作梗死区域分析同时,再切取10 μm厚冠状脑片。采用标准ABC染色法,切片在1∶400的兔抗小鼠白蛋白抗体中4℃下孵育过夜。漂洗后,再将玻片放入生物素化的羊抗兔二抗中孵育90 min。3,3'-diaminobenzidine tetrahydrochloride(DAB)作为过氧化物酶底物显色。对照片采用相同浓度正常兔IgG代替一抗。内源性白蛋白被染成深棕色。计算机图像分析系统计算6个冠状面(Bregma 1.34、0.86、0.38、-0.10、-0.58和-1.06)上白蛋白染色面积。水肿对血脑屏障(BBB)破坏面积的影响采用Swanson等[5]的方法进行纠正。
8.细胞间粘附分子-1(ICAM-1)免疫组织化学染色:在切取脑片作梗死区域及BBB破坏分析同时,用冰冻切片机切取位于Bregma 0.38处的20 μm厚度的冠状脑片,并直接贴于玻片,风干。常规ABC染色法,切片在1∶300的大鼠抗小鼠CD-54(ICAM-1)单抗中4℃下孵育过夜。切片在室温下与生物素化的兔抗大鼠二抗(1∶200)孵育90 min。DAB作为过氧化物酶底物显色并用苏木素复染。照片采用相同浓度的正常大鼠IgG替代一抗。光镜下,脑片上每侧半球选择皮质区和基底节区进行ICAM-1阳性血管(深棕色)计数,采用手工计数可除外ICAM-1表达阳性的炎症细胞。
, 百拇医药
9.统计学分析:采用方差分析判断3组间各项指标的差异,如差异有显著意义,再经Bonferroni校正,作组间均数两两比较。数值均以平均值±标准误表示。统计显著意义设定为P<0.05。
结果
1.脑血流改变: IL-1ra组、LacZ组和Saline组小鼠插线后5 min缺血中心区的CBF分别降至缺血前基值的12%±1%、15%±1%和13%±2%,3组间CBF变化没有明显差别。对照侧脑表面CBF线栓后分别维持在缺血前基值的100%±3%、101%±1%和99%±2%。再灌注后缺血中心区的CBF即刻恢复至缺血前基值的76%±5%、70%±4%和66%±8%,再灌注23 h后,缺血中心区的CBF仍能维持在缺血前基值的50%左右。3组间缺血和再灌注前后脑表面血流变化未见明显差异(P>0.05)。
2.脑梗死体积: IL-1ra组脑梗死体积36.0 mm3±5 mm3比对照组LacZ组60.0 mm3±6.2 mm3和Saline组69.5 mm3±6.3 mm3减小40%~48%左右(F=6.977,P<0.05)。组间两两比较显示IL-1ra组脑梗死体积与2个对照组有显著差异,但对照组间差异无显著意义。
, http://www.100md.com
3.血脑屏障破坏:采用内源性白蛋白渗出范围评价血脑屏障破坏程度,缺血对照侧染色阴性。IL-1ra组6个冠状面上血脑屏障破坏范围均明显小于LacZ组和Saline组(P<0.05)。
4.ICAM-1阳性血管表达:上述免疫组织化学方法能清楚显示ICAM-1阳性血管。各组对侧半球只有少量ICAM-1阳性血管表达(少于10根/层面),差异无显著意义。但缺血侧微血管内皮上ICAM-1表达明显上调,并且皮质区表达数多于基底节区,呈现自缺血核心区到缺血边缘区表达逐渐增多的趋势。IL-1ra组皮质区ICAM-1阳性血管数少于LacZ组和Saline组(135±23,比311±40,357±51,F=9.137,P<0.05,图1)。IL-1ra组缺血侧基底节区ICAM-1阳性血管数也明显少于LacZ组和Saline组(90±21比207±43,259±43,F=9.554,P<0.05)。组间两两比较,IL-1ra组缺血侧皮质区和基底节区ICAM-1阳性血管数与2个对照组差异有显著意义,而对照组间差异无显著意义。
, 百拇医药
3组间缺血前后的生理指标(血压、PO2、PCO2、pH和氧饱和度)无明显改变(P>0.05)。将腺病毒或生理盐水注入侧脑室未发现全身毒性症状或神经系统症状。HE染色显示3组小鼠针道周围都有轻微组织反应,但白细胞浸润局限于针道周围。3组间组织反应没有显著差别。
讨论
再灌注后的急性炎症反应与脑缺血后的继发性脑损害存在密切关系。粘附分子和细胞因子在缺血和再灌注早期即能产生,使缺血损伤转变为炎症损伤。缺血区炎症细胞浸润可使微血管堵塞,造成“无灌流现象”;同时炎症细胞可产生蛋白溶解酶,氧自由基以及其他损害因子,破坏血管内皮,引起血脑屏障破坏和出血。本研究证实:(1)炎症细胞在缺血区的聚集和粘附的时相与再灌注后的脑损害具有相关性。再灌注后6 h,缺血区可见明显白细胞浸润,并比永久性脑缺血出现得更快,范围更广,说明血流再灌注可使炎症反应加重。同时脑梗死体积在再灌注后6~24 h内迅速增大,到48 h达到与永久性损害相似的梗死体积,这一梗死体积发展过程与炎症细胞的浸润时相一致[6]。(2)去除血液中白细胞能改善再灌注损伤。



, 百拇医药
图1 ICAM-1免疫组织化学染色,显示IL-lra组(A)半暗区的ICAM-1阳性血管数明显少于LacZ组(B)和Saline组(C)的相应区 HE ×10(箭头示阳性血管)
细胞因子对炎症细胞具有趋化作用,促进炎症细胞在缺血区聚集。脑缺血后再灌注能引起细胞因子的释放。白细胞介素-1β(IL-1β)是一种炎症细胞的强烈趋化因子,能诱导和促进脑缺血后其他炎症介质的损伤作用,引起神经元死亡[8]。在白细胞介素1移化酶(ICE)基因敲除的转基因小鼠中,因抑制了白细胞介素1前体转化为白细胞介素1,脑缺血损害明显减轻[8,9]。IL-1ra是单核细胞来源的17 000多肽,在体内和体外实验中都能抑制IL-1β的作用[10]。我们在前期实验中,利用腺病毒载体编码人IL-1ra基因,通过脑室内微量注射,使IL-1ra在大鼠和小鼠的室管膜细胞中过度表达,能减少脑缺血后的梗死面积[1,2],同时也证实过度表达的IL-1ra蛋白能减轻脑缺血后的脑水肿和炎症反应[11]。但目前对IL-1在再灌注损伤中的作用机制尚不明确。研究白细胞介素1在缺血再灌注损伤中的机理,有利于找到治疗临床脑缺血病人的新途径。
, 百拇医药
脑缺血/再灌注后发生急性炎症反应的前提条件是炎症细胞粘附于血管内皮细胞,这一粘附反应依赖于粘附分子间的复杂反应。脑缺血再灌注损伤后粘附分子表达上调。Matsuo等[12]报道大鼠大脑中动脉阻断后1~3 h细胞间粘附分子-1(ICAM-1)和内皮白细胞粘附分子-1(ELAM-1)表达增高,并可维持到缺血后1周。阻断内皮细胞上ICAM-1与白细胞结合的位点,能使大鼠暂时性脑缺血后梗死范围减少45~50%[13]。说明ICAM-1在脑缺血再灌注后的损伤机制中起重要作用。
本研究发现,白细胞介素1受体拮抗剂对小鼠再灌注损伤有明显的保护作用,能改善脑缺血损伤,稳定血脑屏障,减轻炎症反应。并能抑制粘附分子的表达。说明白细胞介素1在再灌注损伤中确实起重要作用。作用途径之一可能通过减少细胞间粘附分子的表达,减少炎症细胞附壁,从而阻止炎症细胞附壁、移行,损害脑组织。但白细胞介素1究竟激活何种信息传递路径发挥作用,还需作进一步研究。
, http://www.100md.com
基金项目:美国NIH NS-35089(GYY)和NS-23870(ALB)基金资助项目
参考文献
1,Betz AL, Yang GY, Davidson BL, et al. Attenuation of stroke size in rats using an adenoviral vector to induce overexpression of interleukin-1 receptor antagonist in brain. J Cereb Blood Flow Metab, 1995, 15: 547-551.
2,Yang G, Zhao Y, Davidson BL, et al. Overexpression of interleukin-1 receptor antagonist in the mouse brain reduces ischemic brain injury. Brain Res, 1997, 751: 181-188.
, 百拇医药
3,Roessler BJ, Hartman JW, Vallance DK, et al. Inhibition of IL-1 induced effects in synoviocytes transduced with the human IL-1 receptor antagonist cDNA using an adenoviral vector. Hum Gene Ther, 1995, 6: 307-316.
4,Mao Y, Yang GY, Zhou LF, et al. Focal cerebral ischemia in the mouse: description of a model and effects of permanent and temporary occlusion. Mol Brain Res, 1999, 63:366-370.
5,Swanson RA, Morton MT, Tsao WG, et al. A semiautomated method for measuring brain infarct volume. J Cereb Blood Flow Metab, 1990, 10: 290-293.
, http://www.100md.com
6,Zhang RL, Chopp M, Chen H, et al. Temporal profile of ischemic tissue damage, neutrophil response, and vascular plugging following permanent and transient (2H) middle cerebral artery occlusion in the rat. J Neurol Sci, 1994, 125: 3-10.
7,Betz AL, Schielke GP, Yang GY. Interleukin-1 in cerebral ischemia. Keio J Med, 1996, 45:230-238.
8,Hara H, Fink K, Moskowitz MA, et al. Attenuation of transient focal cerebral ischemic injury in transgenic mice expressing a mutant ICE inhibitory protein. J Cereb Blood Flow Metab, 1997, 17: 370-375.
, 百拇医药
9,Schielke GP, Yang GY, Betz AL, et al. Reduced ischemic brain injury in interleukin-1? converting enzyme (ICE) deficient mice. J Cereb Blood Flow Metab, 1998, 18: 180-185.
10,Wang XK, Barone FC, Aiyar NV, et al. Interleukin-1 receptor and receptor antagonist gene expression after focal stroke in rats. Stroke, 1997, 28:155-162.
11,Yang GY, Liu XL,Kadoya C, et al. Attenuation of ischemic inflammatory response in mouse brain using an adenoviral vector to induce overexpression of interkin-1 receptor antagonist. J Cereb Blood Flow Metab, 1998, 18: 840-847.
, 百拇医药
12,Matsuo Y, Onodera H, Shiga Y, et al. Role of cell adhesion molecules in brain injury after transient middle cerebral artery occlusion in the rat. Brain Res, 1994, 656: 344-352.
13,Zhang RL, Chopp M, Li Y, et al. Anti-ICAM-1 antibody reduces ischemic cell damage after transient middle cerebral artery occlusion in the rat. Neurolology, 1994, 44: 1747-1751.
(收稿日期:1999-06-25), http://www.100md.com